高コレステロール血症、混合型脂質異常症(心臓の血中濃度の上昇)患者における冠動脈疾患(心筋に血液を供給する血管の閉塞を引き起こす病気)および心筋梗塞(心筋細胞の死滅)の一次予防(病気が始まる前)コレステロールとトリグリセリド)および高トリグリセリド血症(トリグリセリドの増加)、フレドリクソン分類(血漿リポタンパク質(血液中の脂肪)の増加につながる遺伝的に決定される疾患の分類)IIa、IIb、IV 型。
以下のような他の脂質異常症の治療:
フレドリクソン III 型および V 型。糖尿病に関連する脂質異常症、および黄色腫に関連する脂質異常症(腱、皮膚および体の他の部分におけるコレステロールに富む黄色がかった物質の蓄積)。
膵炎(膵臓の炎症)のリスクがあり、血清トリグリセリド値が高い成人患者(高脂血症 IV 型および V 型)で、それらをコントロールするための特定の食事療法に適切に反応しない患者の治療。
この薬はどのように作用するのでしょうか?
ゲムフィブロジルは、総コレステロール、LDL コレステロール (「悪玉」コレステロール)、VLDL コレステロール (「悪玉」コレステロール) およびトリグリセリドのレベルを低下させ、HDL コレステロールのレベルを増加させることによって作用する脂質 (血中脂肪) 調節剤です。 「善玉」コレステロール)。
服用後1~2時間で血中濃度が最大に達し、使用8週間目からコレステロール値が低下することが研究で示されています。
ゲムフィブロジルの禁忌 – メドレー
フォーミュラの成分に対して過敏症(アレルギー)がある場合、または肝臓、腎臓、胆嚢(胆汁を蓄える器官)に重大な問題がある場合は、この薬を使用しないでください。
ゲムフィブロジルと以下の薬剤の併用は禁忌です。
シンバスタチン、ロバスタチン、アトルバスタチン、ロスバスタチン、レパグリニド、ダサブビル。
ゲムフィブロジルの使い方 – メドレー
錠剤は、食事の 30 分前に、飲み込むのに十分な量の液体と一緒に摂取する必要があります。
本当に異常であるかどうかを確認するには、脂質レベル (血液中の脂肪) を複数回測定する必要があります。ゲムフィブロジルによる治療を開始する前に、肥満患者の適切な食事、飲酒量の削減、運動および減量、さらには糖尿病や甲状腺機能低下症(甲状腺機能の低下)などの他の医学的問題の管理により血清脂質を管理するあらゆる試みを行う必要があります。 。
この薬による治療中、患者は低コレステロール食を継続する必要があります。治療中、血漿脂質の定期的な測定を実行する必要があります。 3 か月後に患者の脂質反応が不十分であることが判明した場合は、治療を中断するか、補助治療を開始する必要があります。
投与量
推奨される1日用量は900 mg〜1,200 mg(ゲンフィブロジル 900 mg 1錠またはゲンフィブロジル 600 mg 2錠)で、1日最大用量1,500 mg(ゲンフィブロジル 600 mg 1錠とゲンフィブロジル 900 mg 1錠)を超えません。 。
900 mg を夕食の 30 分前に単回投与する必要があります。 1,200 mg を朝食と夕食の 30 分前に 1 日 2 回に分けて服用する必要があります。
小児への使用
安全性と有効性は確立されていません。

治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。医師の知識なしに治療を中止しないでください。
この薬は割ったり、開けたり、噛んだりしないでください。
この薬を使い忘れた場合はどうすればよいですか?
医師が指定した時間に薬を飲み忘れた場合は、思い出したときにすぐに飲みましょう。ただし、次の服用時間が近い場合は、忘れた服用分を飛ばして次の服用量を服用し、通常どおり医師の推奨する服用スケジュールを続けてください。この場合、飲み忘れた分を補うために2倍量の薬を服用しないでください。用量を忘れると、治療の効果が損なわれる可能性があります。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
ゲムフィブロジルの注意事項 – メドレー
胆石の形成:
ゲムフィブロジルは、胆石(胆嚢内の「石」)の形成を促進する可能性があります。胆石が見つかった場合は、この薬による治療を中止する必要があります。
血液の変化:
場合によっては、治療の開始時に、特定の血液成分(ヘモグロビンレベル、赤血球に存在するタンパク質、または白血球、白血球の数の減少など)のわずかな減少、血液検査の変化(ヘマトクリット、血液中の赤血球数の推定値を提供する検査)。ただし、これらのレベルは、ゲムフィブロジルを長期間使用すると安定します。この薬による治療開始から最初の 12 か月間は、定期的に血液検査を受けることをお勧めします。
妊孕性と妊娠中の使用:
妊婦を対象とした適切でよく管理された研究はありません。妊婦へのゲムフィブロジルの投与は、利益が患者または胎児へのリスクを明らかに上回る患者にのみ行われるべきである。
この薬は、医師または歯科外科医のアドバイスなしに妊婦が使用しないでください。
妊娠中、授乳中、または妊娠を計画している場合は、医師または歯科医に伝えてください。
授乳中(授乳中)の使用:
授乳中に医師のアドバイスなしにゲムフィブロジルを使用しないでください。ゲムフィブロジルが母乳中に排泄されるかどうかは不明であるため、授乳中である場合、またはこの薬を使用中に授乳を開始する場合は、医師または歯科医に相談してください。
機械を運転または操作する能力への影響:
この薬の使用後に、機械の運転や操作能力に影響を与える既知の影響はありません。
高齢者への使用:
高齢の患者に対しても、成人に与えられたのと同じガイドラインに従わなければなりません。
ゲムフィブロジルの副作用 – メドレー
ゲムフィブロジルの使用で発生する可能性のある最も一般的な副作用 (この薬を使用している患者の 10% 以上で発生) は次のとおりです。
胃腸反応(胃と腸の)、消化不良(消化不良)、腹痛、急性虫垂炎(虫垂の急性炎症)、心房細動(心拍リズムの変化の一種)。
その他の副作用は患者の 1% 以上によって報告されました (この薬剤を使用する患者の 1% ~ 10% の間で発生します)。ただし、ゲムフィブロジルを投与されたグループとプラセボ (患者に投与される物質) を投与されたグループとの間に有意差はありませんでした。ただし、薬の作用に関与する有効成分は含まれていません)は次のとおりです。
下痢、倦怠感(だるさ)、吐き気・嘔吐、湿疹(皮膚アレルギー反応)、発疹(発疹)、めまい、便秘(便秘)、頭痛(頭痛)。
ゲムフィブロジルによる治療に起因すると思われる追加の副作用も報告されています。
一般的な反応 (この薬を使用している患者の 1% ~ 10% に発生します):
頭痛、発疹。
まれな反応 (この薬を使用している患者の 0.01% ~ 0.1% で発生します):
胆汁うっ滞性黄疸(胆汁色素の沈着による皮膚の黄色)、膵炎(膵臓の炎症)、めまい、眠気、感覚異常(明らかな理由もなく皮膚に感じる灼熱感、チクチク感、かゆみなどの異常感覚) 、末梢神経炎(神経の炎症)、うつ病、性欲減退、かすみ目、インポテンス(陰茎の勃起を維持することが困難)、関節痛(関節痛)、滑膜炎(関節膜の炎症)、筋肉痛(筋肉痛)、ミオパシー(筋肉系の問題)、筋無力症(筋力低下)、四肢の痛み、横紋筋融解症(筋肉細胞の破壊)、剥離性皮膚炎(皮むけを伴う皮膚の変化)、皮膚炎(皮膚の炎症)、そう痒症(かゆみ)、血管浮腫(皮下または粘膜の領域の腫れ、一般にアレルギー起源)、蕁麻疹(かゆみを引き起こす皮膚の発疹)、喉頭(喉と肺の間の領域)の浮腫(腫れ)、重度の貧血(血液中のヘモグロビンの減少) )、白血球減少症(白血球の減少)、血小板減少症(白血球と血小板の数の減少)、好酸球増加症(好酸球と呼ばれる血液白血球の数の増加)、骨髄低形成症(血液白血球の産生の減少)。
さらに次のような副作用も報告されています。
光過敏症(光に対する皮膚の過敏症)、脱毛症(脱毛)、胆嚢炎(胆嚢の炎症)、胆石症(胆石の形成)。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。また、顧客サービスを通じて会社に通知してください。
ゲンフィブロジルの組成 – メドレー
プレゼンテーション:

600mgフィルムコーティング錠:
30錠入りパック。
900mgフィルムコーティング錠:
15錠入りです。
経口使用。
大人用。
構成:
各 600 mg フィルムコーティング錠には次のものが含まれます。
|
ゲムフィブロジル |
600mg |
|
賦形剤* |
1錠 |
※微結晶セルロース、二酸化ケイ素、フマル酸ステアリルナトリウム、クロスカルメロースナトリウム、ポリソルベート80、ポビドン、デンプン、ポリビニルアルコール、二酸化チタン、マクロゴール、タルク。
各 900 mg フィルムコーティング錠には次のものが含まれます。
|
ゲムフィブロジル |
900mg |
|
賦形剤* |
1錠 |
※微結晶セルロース、二酸化ケイ素、フマル酸ステアリルナトリウム、クロスカルメロースナトリウム、ポリソルベート80、ポビドン、デンプン、ポリビニルアルコール、二酸化チタン、マクロゴール、タルク。
ゲムフィブロジルの過剰摂取 – メドレー
ゲンフィブロジルを過剰摂取した場合は、直ちに医師の診察を受けてください。その症状には、腹痛、肝酵素の変化、下痢、クレアチンホスホキナーゼ(主に筋肉組織に存在する酵素)の増加、筋肉痛や関節痛、吐き気、嘔吐などがあります。過剰摂取が発生した場合は、対症療法および支持療法を提供する必要があります。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
ゲムフィブロジルの薬物相互作用 – メドレー
HMG-CoA レダクターゼ阻害剤 (肝臓によるコレステロールの生成に作用する酵素の一種) などの脂質調節剤の使用:
ゲムフィブロジルを、HMG-CoA レダクターゼ阻害剤 (シンバスタチン、ロバスタチン、アトルバスタチン、ロスバスタチンなど) などの他の脂質調節剤と同時に使用しないでください。この場合、重度のミオパチー(筋肉の病気)、横紋筋融解症(筋肉細胞の破壊)、急性腎不全(腎機能の急激な低下)を引き起こすリスクがあります。
抗凝固剤:
ゲムフィブロジルをワルファリン (血液凝固を抑制する薬) と併用する場合は注意してください。プロトロンビン時間(血液凝固因子)の望ましいレベルを維持するには、ワルファリンの用量を減らす必要があります。プロトロンビン時間を測定するために、レベルが安定するまで定期的に検査を受けることをお勧めします。

CYP2C8 基質:
CYP2C8 阻害剤であるゲムフィブロジルは、併用投与すると CYP2C8 基質の曝露を増加させる可能性があります。したがって、ゲムフィブロジルを併用する場合は、主に CYP2C8 酵素によって代謝される薬剤の用量を減らす必要があるかもしれません。
臨床検査:
臨床検査の肝機能検査に変化が生じる場合があります。これらの増加は通常、可逆的です。定期的に肝機能検査を受けることをお勧めします。異常が続く場合は、この薬による治療を中止する必要があります。
胆汁酸に関連する樹脂:
ゲムフィブロジルを樹脂顆粒の形の薬剤(コレスチポールなど)と一緒に使用しないでください。 2 つの薬を 2 時間以上間隔をあけて投与することが推奨されます。
コルヒチン:
コルヒチンとゲムフィブロジルの併用投与により、神経筋毒性 (神経組織および筋肉への損傷) および横紋筋融解症 (筋肉細胞の破壊) のリスクが増加する可能性があります。高齢者や腎機能障害または肝機能障害(腎臓または肝機能の低下)のある患者では、リスクが増加する可能性があります。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
物質ゲムフィブロジルの作用 – メドレー
効果の結果
非HDLコレステロールが200 mg/dLを超え、心臓病の病歴のない個人を対象とした広範な一次予防、プラセボ対照、無作為化、二重盲検ヘルシンキ心臓研究では、ゲムフィブロジル(活性物質)がトリグリセリド総血漿コレステロールを有意に減少させました。総コレステロールとLDLコレステロールは中程度であり、HDLコレステロールは大幅に増加しました。 5年間の研究期間中、ゲムフィブロジル(活性物質)を投与された患者グループは、CADの全体的な発生率が34%減少したことを示しました(研究の4年目と5年目では、CADの減少は50%を超えました)。非致死的MIは37%減少し、心臓死は26%減少した。冠動脈疾患の発生率における全体的な差は、プラセボを受けた患者と比較して、ゲムフィブロジル(活性物質)で治療された患者の方が有意に低かった(p < 0.02; 両側検定)。
薬理的特性
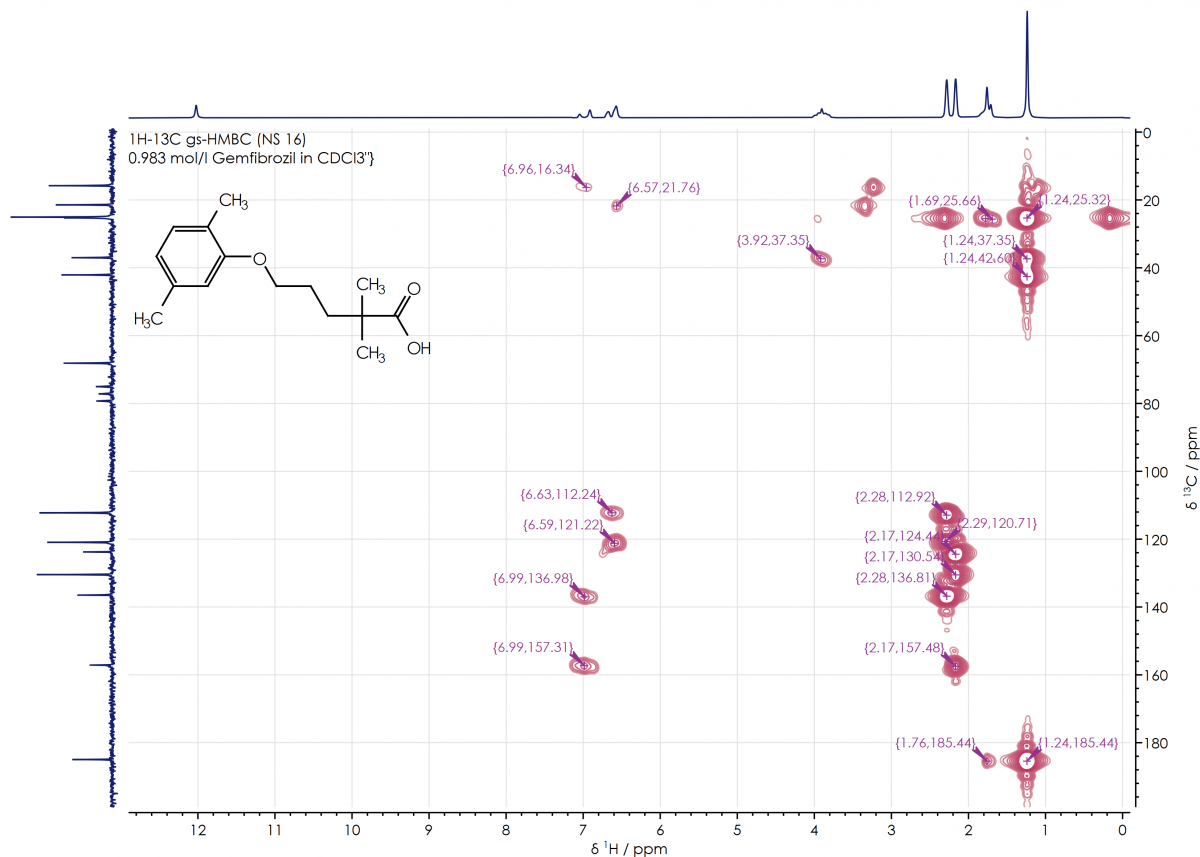
ゲムフィブロジル(活性物質)は、非ハロゲン化フェノキシペンタン酸です。化学名は5(2.5ジメチルフェノキシ)2.2ジメチルペンタン酸です。実験式は C15H22O3 です。ゲムフィブロジル(有効成分)は、融点が58~61℃の白色化合物です。その溶解度は、水と酸では 0.0019%、希塩基では 1% 以上です。ゲムフィブロジル(活性物質)は通常の条件下では安定です。
薬力学特性
作用機序:

ゲムフィブロジル(活性物質)の作用機序はまだ完全には理解されていません。ヒトでは、ゲムフィブロジル(活性物質)は末梢脂肪分解を阻害し、遊離脂肪酸の肝臓への取り込みを減少させます。また、合成を阻害し、超低密度リポタンパク質 (VLDL) のキャリアであるアポリポタンパク質 B のクリアランスを増加させ、VLDL 産生の減少につながります。ゲムフィブロジル (活性物質) は、高密度リポタンパク質 (HDL) サブフラクション、HDL2 および HDL3、およびアポリポタンパク質 AI および A-II のレベルを増加させます。動物実験では、ゲムフィブロジル(活性物質)によって肝臓からのコレステロールの代謝と除去が増加することが示唆されています。
ゲムフィブロジル (活性物質) は、総コレステロール、LDL コレステロール (低密度リポタンパク質)、VLDL コレステロールおよびトリグリセリドのレベルを低下させ、HDL コレステロールのレベルを増加させる脂質調節剤です。
薬物動態学的特性
吸収:
ゲムフィブロジル(活性物質)は、経口投与後、胃腸管からよく吸収されます。血漿ピークは 1 ~ 2 時間の間に発生し、複数回投与後の血漿半減期は 1.5 時間です。血漿レベルは用量に比例し、複数回の用量を使用しても蓄積は見られません。
ゲムフィブロジル(活性物質)の薬物動態は、投与時間と関連して食事のタイミングに影響されます。ある研究では、食事の0.5時間前に投与すると、薬物の吸収速度と範囲の両方が大幅に増加しました。ゲムフィブロジルを食事の0.5時間前に投与した場合と比較して、食後に投与した場合、平均AUCは14%から44%減少しました。その後の研究では、ゲムフィブロジル (活性物質) の最大吸収率は食事の 0.5 時間前に投与した場合に得られ、C max は食事または絶食時に投与した場合より 50% ~ 60% 高くなりました。この研究では、食事に関連した投与タイミングの AUC に対する有意な影響はありませんでした。
分布:
ゲムフィブロジル (活性物質) は血漿タンパク質と高度に結合しており、他の薬物と置換相互作用を起こす可能性があります。
代謝:
ゲムフィブロジル(活性物質)は、環に結合したメチル基の酸化を受け、ヒドロキシメチルおよびカルボキシル代謝物を連続的に形成します。
排泄:
人間に投与された用量の約 70% は、主に抱合型グルクロニドの形で尿中に排泄され、用量の 2% 未満が未変化のゲムフィブロジル (活性物質) の形で排泄され、用量の 6% は排泄されます。糞便の中で。
前臨床安全性データ
発がん、突然変異誘発、生殖能力の低下:
人間を対象とした適切でよく管理された研究はありません。ヒトの曝露量(AUC に基づく)の 0.2 倍および 1.3 倍に相当するゲムフィブロジル(活性物質)の用量を用いて、ラットで長期研究が実施されました。良性肝結節および肝癌の発生率は、高用量を投与された雄ラットで有意に高かった。高用量のゲムフィブロジル(活性物質)を投与されたラットでは、良性および悪性肝新生物の合計発生率が大幅に増加しました。
このクラスの 3 つの薬剤を比較する発がん性比較研究もラットで実施されました: フェノフィブラート (10 mg/kg および 60 mg/kg; ヒトの推奨用量の 0.3 倍および 1.6 倍)、クロフィブラート (400 mg/kg; 推奨用量の 1.6 倍)ヒトの推奨用量)およびゲムフィブロジル(活性物質)(250 mg/kg、ヒトの推奨用量の1.7倍)。膵腺房腺腫は、フェノフィブラートで治療された男性と女性で拡大しました。クロフィブラートで治療した男性では肝細胞癌と膵腺房腺腫の増加が観察され、女性では肝腫瘍性結節の増加が観察されました。ゲムフィブロジル(活性物質)で治療した男性と女性では肝腫瘍性結節の増加も観察され、3 つの薬剤を投与した男性では精巣間質細胞腫瘍の増加が観察されました。
ヒトの曝露量(AUC に基づく)の 0.1 倍および 0.7 倍に相当する用量で、マウスを対象とした長期研究が実施されました。対照と比較して肝腫瘍の発生率に統計的に有意な差はなかったが、試験された用量は他のフィブラート系薬剤で発がん性があると確認された用量よりも低かった。ヒトに推奨される用量(体表面積に基づく)の約2倍を雄ラットに10週間投与すると、用量に関連した生殖能力の低下が生じた。その後の研究では、この効果は薬を投与しなかった約8週間後には逆転し、子孫には伝わらないことが実証されました。胎児毒性の減少は、高用量で観察された出生体重の減少によって明らかになりました。
ゲムフィブロジル ストレージ ケア – メドレー
この薬は室温(15~30℃)で保管してください。湿気から守ります。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。
薬の特徴:
この薬はコーティングされた白色の長方形の錠剤の形で提供され、片面には刻み目があり、もう片面にはメドレーが刻まれています。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かない場所に保管する必要があります。
ゲンフィブロジラの法的格言 – メドレー
MS – 1.8326.0199
農場。答え:
タチアナ・デ・カンポス博士
CRF-SP番号29,482。
メドレー・ファーマシューティカ株式会社。
Rua Macedo Costa、55 – カンピナス – SP
CNPJ 10.588.595/0007-97
ブラジルの産業
医師の処方箋に基づいて販売します。


.jpg?ssl=1)







