アリクストラは、深部静脈血栓症(脚の深部静脈に血栓が形成された場合)および肺血栓塞栓症(血栓が肺の血管に詰まった場合)の治療にも使用されます。
アリクストラは、不安定狭心症(心臓の動脈が狭くなり、その結果として臓器への血液供給が減少することによって引き起こされる痛み)や急性心筋梗塞(心臓発作)の治療にも使用されます。
アリクストラはどのように機能しますか?
アリクストラは抗血栓薬です。その有効成分であるフォンダパリヌクスは、血液凝固プロセスを阻害することで作用し、血管内での血栓(血栓)の形成を防ぎます。
アリクストラの禁忌
次の場合は Arixtra を使用しないでください。
- フォンダパリヌクスナトリウムまたはその配合成分にアレルギーがある場合。
- 自然出血、出血性脳血管障害(出血性脳卒中、一般に脳卒中として知られている)、または何らかの活動性の出血が見られる。
- 心臓に細菌感染症がある(急性細菌性心内膜炎)。
- 重度の腎障害がある(クレアチニンクリアランスが 20 mL/min 未満であると定義される腎臓機能不全)。
アリクストラの使い方
溶液は投与前に目視検査して粒子状物質が存在する可能性を観察する必要があります。
アリクストラは、皮下注射(皮膚の下)または静脈内注射(静脈を介して)によって投与されます。この薬は筋肉内注射(筋肉内注射)によって投与しないでください。
皮下注射は、従来の注射器と同じ方法で投与されます。静脈内投与は、静脈内カテーテルを介して行うか、カテーテルから直接注射するか、0.9% 生理食塩水のミニバッグを使用して行う必要があります。
Arixtra プレフィルドシリンジには、注射後の針の損傷を防ぐ自動針保護システムが含まれています。
未使用の製品または廃棄物は廃棄する必要があります。
皮下投与経路:

皮下投与部位は、左右の前側腹壁と左右の後側腹壁の間で交互に行う必要があります。プレフィルドシリンジを使用する場合、薬剤の損失を避けるため、注入前にシリンジから気泡を追い出さないでください。針の全長を親指と人差し指で挟んだ皮膚のひだに垂直に挿入する必要があります。注射中は皮膚のひだを維持する必要があります。
Arixtra は医師の指示の下で使用することを目的としています。患者は、医師が適切と判断し、必要に応じて医師の監督のもとで自己注射を行う場合にのみ自己注射を行うことができます。皮下注射の技術に関する適切なトレーニングを提供する必要があります。

自己管理の手順を以下に概説します。
シリンジ部品:
- 針カバー。
- ピストン;
- 指のサポート。
- 安全装置。
使用説明書:
- 石鹸と水で手を注意深く洗い、タオルで乾かしてください。
- ダンボール箱からシリンジを取り出し、使用期限内であること、未開封または破損していないことを確認してください。
- 快適な姿勢で座ったり横になったりしてください。
下腹部(下腹部)、へそから少なくとも 5 cm 下の場所を選択してください(図 A)。
塗布するたびに、下腹部の左右を交互に塗ります。これは、注射部位の不快感を軽減するのに役立ちます。
下腹部に注射できない場合は、看護師または医師に相談してください。
図A
- 注射部分をアルコール綿で拭きます。
- まず針カバーをひねって (図 B1)、次にシリンジ本体からまっすぐ引き抜き (図 B2)、針カバーを取り外します。
図B1
図B2
針カバーを廃棄します。
重要な注意事項:
- 注射する前に針に触れたり、針を表面に触れさせたりしないでください。
- シリンジ内に小さな気泡が見られるのは正常です。注射する前にこの気泡を取り除こうとしないでください。取り除こうとすると、薬の一部が失われる可能性があります。
- きれいになった皮膚を折り目がつくまで優しくつまみます。注射を行う間、親指と人差し指の間の折り目を保持します (図 C)。
図C
- シリンジを指でしっかりと持ちます。針の全長に沿って皮膚のひだに直角に針を挿入します (図 D)。
図D
- プランジャーを最後まで押して、シリンジの内容物をすべて注入します (図 E)。
図E
- プランジャーを放すと、針は自動的に後退し、安全装置に戻り、永続的にロックされます (図 F)。
図F
使用済みの注射器は家庭ゴミとして処分しないでください。医師または薬剤師の指示に従って廃棄してください。
静脈内投与経路(ST上昇を伴う急性心筋梗塞の治療における初回投与のみ):
静脈内投与 (静脈経由) は、静脈内カテーテルを介して直接、または少量の 0.9% 生理食塩水 (25 または 50 mL) を介してのみ行う必要があります。プレフィルドシリンジを使用する場合、薬剤の損失を避けるため、注入前にシリンジから気泡を追い出さないでください。直接投与する場合、すべての薬剤が確実に投与されるように、注射後に生理食塩水をカテーテルに通す必要があります。生理食塩水を介して投与する場合、注入は 1 ~ 2 分間行わなければなりません。
アリクストラの投与量
大人:
静脈血栓塞栓性イベントの予防:
整形外科および腹部外科:
Arixtra の推奨用量は 2.5mg を 1 日 1 回、手術後に皮下注射で投与します。
最初の投与は、手術終了後少なくとも 6 時間経過し、出血が止まった後にのみ投与してください。
治療は、静脈血栓塞栓症(血栓による静脈の閉塞)のリスクが低下するまで、通常は患者が歩けるようになるまで、手術後少なくとも 5 ~ 9 日間継続する必要があります。
経験によれば、股関節骨折の手術を受けた患者では、静脈血栓塞栓症のリスクが手術後 9 日を超えても継続します。これらの患者では、さらに最大 24 日間、アリクストラによる長期の予防(予防)を考慮する必要があります。
血栓塞栓性合併症のリスクのある患者:
Arixtra の推奨用量は、1 日 1 回 2.5mg で、皮下注射によって投与されます。患者を対象に6~14日間の治療が臨床研究されています。
深部静脈血栓症(DVT)および急性肺血栓塞栓症(PTE)の治療:
1日1回皮下注射により投与されるアリクストラの推奨用量は次のとおりです。
- 体重50kg未満の場合は5mg。
- 体重50〜100kgの場合は7.5mg。
- 体重100kg以上の場合は10mg。
治療は少なくとも 5 日間、適切な経口抗凝固療法が確立されるまで継続する必要があります (国際正規化比、2 対 3)。ビタミンK拮抗薬による併用治療はできるだけ早く、通常は72時間以内に開始する必要があります。 Arixtra による通常の治療期間は 5 ~ 9 日間です。
不安定狭心症/非ST上昇型心筋梗塞の治療:
Arixtra の推奨用量は、皮下注射による 1 日 1 回 2.5 mg です。治療は診断が下されたらすぐに開始し、最長8日間、または早期に発生した場合は退院まで継続する必要があります。
非初回経皮的冠動脈インターベンション(PCI、薬剤で血栓が溶解しない場合に使用される心臓動脈の閉塞を解除する方法)を受けており、アリクストラを使用している場合は、標準的な診療に従って未分画ヘパリン(抗凝固物質の一種)を投与する必要があります。ただし、PCI 中に限ります。フォンダパリヌクスの最後の投与からの時間を考慮し、患者の潜在的な出血リスクを考慮してください。
経皮カテーテルの除去後にアリクストラの皮下投与を再開する時期は、臨床上の判断に基づく必要があります。不安定狭心症/非ST上昇型心筋梗塞の臨床研究では、経皮カテーテルを抜去してから2時間後まで治療は再開されませんでした。
心筋(心筋)の血行再建手術(例:詰まった心臓動脈の一部を置換するための伏在バイパス移植片の設置)を受けた患者では、可能であれば、手術前の24時間はアリクストラを投与すべきではありません。手術後 48 時間後に再開する必要があります。
ST 上昇心筋梗塞の治療:
Arixtra の推奨用量は 1 日 1 回 2.5 mg です。最初の用量は静脈内に投与し、次の用量は皮下注射する必要があります。治療は診断が下されたらすぐに開始し、最長8日間、または早期に発生した場合は退院まで継続する必要があります。
非初回経皮的冠動脈インターベンション(PCI、薬物療法で血栓が溶解しない場合に使用される心臓動脈の閉塞を解除する方法)を受けており、アリクストラを使用している場合は、標準的な診療に従って未分画ヘパリン(抗凝固物質の一種)を投与する必要がありますが、 PCI 時のみ。フォンダパリヌクスの最後の投与からの時間を考慮し、患者の潜在的な出血リスクを考慮してください。
経皮カテーテルを抜去した後にアリクストラの皮下投与を再開する時期は、医師の判断に基づいてください。 ST上昇心筋梗塞の臨床研究では、経皮カテーテルを抜去してから3時間後まで治療は再開されませんでした。
心筋(心筋)の血行再建手術(例:詰まった心臓動脈を置換するための伏在性バイパスグラフトの設置)を受けた患者では、可能であれば手術前の24時間はアリクストラを投与すべきではありません。手術の48時間後に再開できます。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。医師の知識なしに治療を中止しないでください。
Arixtra の使用を忘れた場合はどうすればよいですか?
飲み忘れた場合は、思い出したときにすぐに注射してください。忘れた分を補うために 2 回分を注射しないでください。何をすべきかわからない場合は、医師に相談してください。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
アリクストラの予防措置
投与経路:
Arixtra は皮下 (皮下) にのみ投与してください。急性冠症候群(心臓発作)の治療では、必要に応じて医師の監督の下、最初の投与量を静脈内に使用することができます。
アリクストラは、血栓の形成を防ぐため、またはすでに形成された血栓を治療するために処方されています。
この薬の作用により、出血しやすい十二指腸潰瘍または胃潰瘍を患っている場合、出血が問題となる可能性があります。最近脳、脊椎、目の手術を受けた場合。または血液凝固に影響を与える他の薬を服用している場合。これらのいずれかに当てはまると思われる場合は、医師に相談してください。
次のような場合は医師に伝えてください。
- 肝臓病がある。
- 75歳以上である。
- 重量は50kg未満。
- 以前のヘパリンによる治療後に、凝固の問題や血小板 (血液凝固に関与する細胞) の数の減少が発生しましたか。
クレアチニンクリアランスが 30 mL/分未満の腎臓機能不全がある場合は、医師の詳しい知識や指導がない限り、この薬を服用しないでください。
手術を受けた場合、アリクストラの初回投与は手術後約 6 時間後、切り傷からの出血が止まった後にのみ投与する必要があります。この薬は血液の凝固能力を低下させるため、それより前にアリクストラを投与すると、出血による傷が悪化する可能性があります。
Arixtra の使用中に脊椎麻酔を受けるか、脊椎周囲の空間から液体を除去する (腰椎穿刺) 場合、注射部位で脊椎の出血が起こる危険性があり、これは重篤になる可能性があります。ご質問がある場合は、まず医師にご相談ください。
Arixtra シリンジにはラテックスが含まれています。
注射針プロテクターにはラテックスが含まれています。ラテックスにアレルギーがある場合は医師に伝えてください。
車両の運転や機械の操作能力への影響:
機械を運転したり使用したりする能力への影響に関する研究は行われていない。
妊娠:
明らかに必要な場合を除き、妊娠中の女性はアリクストラを使用しないでください。
妊娠している場合、または妊娠の可能性がある場合は、医師に知らせてください。
授乳:
アリクストラによる治療中は授乳はお勧めできません。
この薬は、医師または歯科外科医のアドバイスなしに妊娠中の女性が使用すべきではありません。
アリクストラの副作用
どの薬も人によっては有害事象を引き起こす可能性があります。
アリクストラを使用した患者で報告された副作用は以下のとおりです。
一般的な反応 (この薬を使用している患者の 1% ~ 10% に発生します):
- 出血。この薬を使用している 100 人に 1 人以上で発生する可能性のある最も一般的な有害事象は出血です。出血があれば重症化する可能性があります。このような場合は、直ちに医師に連絡してください。
- あざ(体に紫色の斑点)。
- 貧血(赤血球数の減少);
- 腫れ(浮腫)。
まれな反応 (この薬を使用している患者の 0.1% ~ 1% に発生します):
- 血小板(血液凝固の原因となる血球)の数の減少または増加。
- 頭痛;
- 吐き気、嘔吐。
- 肝(肝臓)血液検査の結果の変化。
- 熱;
- 発疹(皮膚の発疹);
- そう痒症(かゆみ)、傷口からの分泌物。
まれな反応 (この薬を使用している患者の 0.01% ~ 0.1% で発生します):
- 術後の創傷感染。
- アレルギー反応(かゆみ、腫れ、発疹を含む);
- 血液中のカリウム濃度が低い。
- 不安、混乱、めまい、眠気;
- 低血圧(低血圧);
- 呼吸困難、咳。
- 胃痛、消化不良、便秘(便秘)、下痢。
- 血液中のビリルビン(肝臓によって生成される物質)の増加。
- 注射部位での反応。
- 胸の痛み、脚の痛み。
- 疲れ;
- 赤み;
- 失神。
ここに記載されていない症状であっても、新たな症状がある場合は必ず医師に知らせてください。
注意:
この製品は新薬であり、研究により許容できる有効性と安全性が示されていますが、たとえ正しく適応され使用されたとしても、予測できないまたは未知の副作用が発生する可能性があります。この場合は医師または歯科医師に知らせてください。
アリクストラの構成
プレゼンテーション:
皮下使用 (2.5 mg および 7.5 mg の投与) または静脈内 (2.5 mg の投与のみ) 用の注射可能な溶液で、シリンジ 2 個を含むパッケージで提供されます。
皮下または静脈内使用。
大人(17歳以上)ご利用いただけます。
構成:
各シリンジには次のものが含まれています。
注射用溶液0.5mL中にフォンダパリヌクスナトリウム2.5mg、または注射用溶液0.6mL中にフォンダパリヌクスナトリウム7.5mg。
賦形剤:
塩化ナトリウム、注射用水(必要に応じてpHを調整するための塩酸または水酸化ナトリウム)。
アリクストラの過剰摂取
症状と兆候:
推奨量を超えるアリクストラの用量は、出血のリスクの増加につながる可能性があります。
処理:
出血性合併症を伴う過剰摂取の場合は、治療を中止し、主な原因を調査する必要があります。外科的止血(出血を止める)、血液補充(輸血)、血漿輸血(90%が水、10%がタンパク質、抗体、酵素、ホルモン、その他の物質で構成される血液の液体部分)などの適切な治療の開始。新鮮な場合は、血漿交換(血漿交換)を考慮する必要があります。
誤ってアリクストラを推奨用量を超えて使用した場合は、出血のリスクが高まる可能性があるため、すぐに医師の診察を受けてください。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
アリクストラの薬物相互作用
アリクストラが他の薬の効果に影響を与えるのと同様に、一部の薬はアリクストラの効果に影響を与える可能性があります。処方箋なしで販売されている薬であっても、あなたが服用している、または服用する予定の他の薬については、医師または薬剤師に伝えてください。医師の処方がない限り、血液凝固に影響を与える他の薬をアリクストラと一緒に使用しないでください。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
物質アリクストラの作用
有効性の結果
ST-Tセグメントの上昇を伴わない急性冠症候群の患者において、フォンダパリナックスは9日目の虚血性イベントのリスクを軽減する点でエノキサパリンと同様であるが、大出血を大幅に減少させ、長期的な死亡率と罹患率を改善する。
Fondaparinux で治療され、非初回 PCI を受けた AI/STEMI 患者では、処置中に UFH を受けた場合、カテーテル血栓や大出血の発生率は低かった。
大規模な整形外科手術を受ける患者において、フォンダパリナックス 2.5 mg を 1 日 1 回、手術の 6 時間後に皮下投与すると、エノキサパリンよりも優れた効果が実証され、臨床的に関連する出血のリスクを増加させることなく、深部静脈血栓症の全体的なリスクを 50% 以上減少させることができました。
モニターなしで1日1回皮下投与されるフォンダパリナックスは、血行力学的に安定した肺塞栓症患者の初期治療における未分画ヘパリンの投与と少なくとも同程度に有効かつ安全である。
症候性深部静脈血栓症患者の初期治療において、1日1回皮下投与されるフォンダパリヌクスは、少なくとも1日2回のエノキサパリン(体重調整用量)投与と同等の有効性および安全性を有する。
薬理学的特徴
薬力学特性
薬物療法グループ:
抗血栓剤。
作用機序
Fondaparinux は、活性化第 X 因子 (X a ) の合成選択的阻害剤です。フォンダパリナックスの抗血栓活性は、アンチトロンビン III (ATIII) によって媒介される第 Xa 因子の選択的阻害の結果です。フォンダパリナックスは、ATIII への選択的結合を通じて、ATIII による第 Xa 因子の生理学的中和を(約 300 倍)強化します。
中和因子 Xa は血液凝固カスケードを中断し、トロンビン形成と血栓発生の両方を阻害します。
フォンダパリナックスはトロンビン (活性化第 II 因子) を不活性化せず、血小板機能に対する既知の影響はありません。
薬力学的効果
フォンダパリナックスは、2.5 mg の用量で、活性化部分トロンボプラスチン時間 (aPTT)、活性化凝固時間 (ACT) またはプロトロンビン時間 (INR) の血漿検査などの日常的な凝固検査に対して臨床的に関連した影響を及ぼしません。 )、出血時間や線溶活性についても同様です。ただし、まれに aPTT の自発的な報告が寄せられています。
2.5mgの用量で増加しました。
フォンダパリナックスは、ヘパリン誘発性血小板減少症 (HIT) II 型患者の血清とは交差反応しません。
抗 Xa 活性
フォンダパリヌクスの薬力学/薬物動態は、第 Xa 因子活性を通じて定量化されたフォンダパリヌクスの血漿濃度から得られます。抗 Xa アッセイの校正には Fondaparinux のみを使用できます。ヘパリンまたは低分子量ヘパリン (LMWH) の国際標準は、この用途には適切ではありません。その結果、フォンダパリヌックス濃度は、フォンダパリヌックスキャリブレーターのミリグラム/リットルで表されます。
薬物動態学的特性
吸収
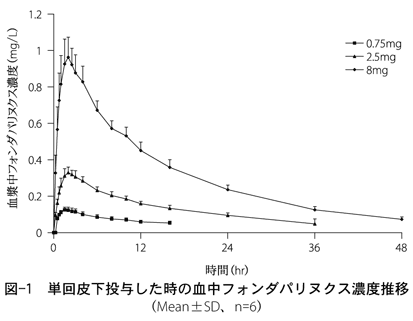
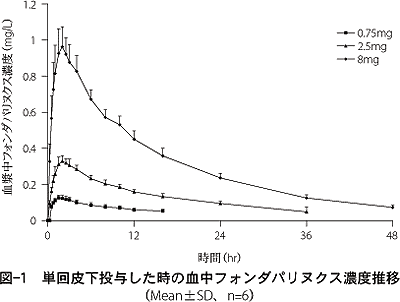
皮下投与後、フォンダパリナックスは完全かつ迅速に吸収されます (100% 絶対バイオアベイラビリティ)。若い健康な人に2.5 mgのフォンダパリヌクスナトリウム(活性物質)を1回皮下注射すると、約2時間で0.34 mg/Lのピーク血漿濃度(C max )に達します。平均Cmax値の半分に相当する血漿濃度は、投与後25分で到達します。
健康な高齢者の場合、フォンダパリヌクスの皮下投与量は 2 ~ 8 mg の範囲で薬物動態が直線的です。 1 日 1 回の皮下投与後、3 ~ 4 日後に定常状態の血漿レベルに達し、 Cmaxおよび曲線下面積 (AUC) は 1.3 倍増加します。健康な高齢者に静脈内ボーラス投与した後、フォンダパリヌクスの薬物動態は治療範囲全体にわたって直線的なままでした。
人工股関節置換手術を受ける患者に、フォンダパリヌクスナトリウム(活性物質)2.5 mgを1日1回皮下投与すると、定常状態でのピーク血漿濃度は平均して0.39~0.50 mg /mLで、投与後約3時間で到達します。これらの患者では、定常状態での最小血漿濃度は 0.14 ~ 0.19 mg/mL です。
症候性深部静脈血栓症および肺血栓塞栓症の患者で、フォンダパリヌクスナトリウム(活性型)5mg(体重50kg未満)、7.5mg(体重50~100kg)および10mg(体重100kg超)による治療を受けている場合物質)を 1 日 1 回皮下投与すると、体重に応じて用量を調整すると、すべての体重カテゴリーにわたって同様の平均ピーク定常状態および谷の血漿濃度が得られます。
定常状態での平均ピーク血漿濃度は 1.20 ~ 1.26 mg/L の範囲にあります。
これらの患者では、定常状態での平均最小血漿濃度は 0.46 ~ 0.62 mg/L の範囲にあります。
分布
健康な成人では、皮下または静脈内に投与されたフォンダパリナックスは、定常状態および非平衡状態での見かけの分布量が 7 ~ 11 リットルであることからわかるように、主に血液中に分布し、血管外液にはごく一部しか分布しません。インビトロでは、フォンダパリナックスはアンチトロンビン III (ATIII) に高度に (少なくとも 94%) 特異的に結合しますが、血小板因子 4 (PF4) や赤血球などの他の血漿タンパク質にはあまり結合しません。
代謝
正常な腎機能を持つ個人では、投与量の大部分が変化せずに尿中に排泄されるため、フォンダパリヌクスの生体内代謝は研究されていません。
排除
フォンダパリヌクスは、主に未変化の薬剤として尿中に排泄されます。健康な人では、皮下または静脈内に 1 回投与すると、64 ~ 77% が 72 時間以内に尿中に排泄されます。排出半減期は、健康な若者では約 17 時間、健康な高齢者では約 21 時間です。腎機能が正常な患者では、フォンダパリヌクスの平均クリアランスは 7.82 mL/分です。
特殊な患者集団
腎不全
フォンダパリヌクスの排泄は、主な排泄経路が未変化の形での尿中への排泄であるため、腎不全患者では長期にわたります。待機的股関節手術または股関節骨折手術後に予防を受けている患者では、軽度の腎不全患者ではフォンダパリヌクスの総クリアランスが約 25% 低くなります (クレアチニンクリアランス50 ~ 80 mL/分)。
正常な腎機能が損なわれた患者と比較して、中等度の腎不全(クレアチニンクリアランスが30~50 mL/分)の患者では約40%低く、重度の腎不全(30 mL/分未満)の患者では約55%低くなります。
関連する終末半減期値は、中等度の腎障害のある患者では 29 時間、重度の腎障害のある患者では 72 時間でした。深部静脈血栓症(DVT)の治療を受けている患者でも、フォンダパリヌックスクリアランスと腎機能障害の程度との間の同様の関係が観察されました。
静脈血栓塞栓性イベントの予防
集団薬物動態モデルは、フォンダパリナックスを投与されている下肢の大規模整形外科手術(MOSLL)を受ける患者から得られたデータを使用して開発され、クレアチニンクリアランスが23.5 mL/min と低い患者も含まれていました。
このモデルを使用した薬物動態シミュレーションでは、クレアチニンクリアランスが20 ~ 30 mL/分の患者に 1.5 mg を 1 日 1 回または 2.5 mg を隔日投与した場合の平均フォンダパリヌクス曝露量が、軽度から中等度の腎機能障害のある患者で観察されたものと同様であることが示されました(クレアチニンクリアランスは30 ~ 80 mL/min)、1 日 1 回 2.5 mg を投与します。
肝不全
フォンダパリヌクスの遊離濃度は、軽度から中等度の肝機能障害のある患者では変化しないと予想されます。したがって、薬物動態に基づいて用量を調整する必要はありません。肝機能障害のある人にフォンダパリヌクスを単回皮下投与した後、肝機能が正常な人。
フォンダパリヌクスの血漿中濃度の低下は、肝機能障害のある個人におけるATIIIの血漿中濃度の低下に続発して、ATIIIへの結合が低下し、その結果フォンダパリヌクスの腎クリアランスが増加したことに起因すると考えられた。
フォンダパリヌクスの薬物動態は、重度の肝障害患者を対象として研究されていません。
子供たち
フォンダパリヌクス ナトリウム (活性物質) の薬物動態パラメーターは、24 人の小児患者 (1 ~ 18 歳) からの希少な採血データを使用した集団薬物動態分析で特徴付けられました。
小児患者に 0.1 mg/kg を 1 日 1 回皮下投与すると、DVT または PE の治療に推奨される用量を投与した場合に成人で観察されるのと同様のフォンダパリヌクスへの曝露が生じました。
お年寄り
75 歳以上の患者ではフォンダパリヌクスの除去が長期化します。股関節骨折手術または待機的股関節手術における2.5 mgのフォンダパリヌクスナトリウム(活性物質)による予防を評価した研究では、65歳未満の患者と比較した場合、75歳以上の患者ではフォンダパリヌクスの総クリアランスが約25%低かった。フォンダパリヌクスクリアランスと年齢との同様の関係が、DVT 治療を受けている患者でも観察されました。
セックス
体重を調整した後、性別間の差は観察されませんでした。
人種
人種による薬物動態の違いは前向きに研究されていません。しかし、健康なアジア人(日本人)を対象に実施された研究では、健康な白人人と比較して異なる薬物動態プロファイルは明らかにされませんでした。同様に、整形外科手術を受けている患者で実施された集団薬物動態分析の結果に基づくと、黒人と白人の患者の間で血漿クリアランスの差異は観察されませんでした。
体重
体重が 50 kg 未満の患者の場合、フォンダパリヌクスの総クリアランスは約 30% 減少します (警告と注意事項の項目を参照)。
Arixtra ストレージ ケア
15℃~30℃の室温で保管してください。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。
物理的な側面:
Arixtra シリンジには、透明から実質的に透明な無色の液体が入っています。
粒子が存在する可能性を観察するために、投与前に溶液を目視検査する必要があります。粒子状物質が観察された場合は、薬剤を廃棄してください。
Arixtra プレフィルドシリンジには、注射後の針の損傷を防ぐ自動針保護システムが含まれています。
未使用の製品または残留物は廃棄する必要があります。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かないところに保管してください。
アリクストラの法的格言
MS 1.0107.0274。
農場。答え:
エディニルソン・ダ・シルバ・オリベイラ。
CRF-RJ番号18875。
製造元:
アスペン ノートルダム ド ボンデヴィル。
1, rue de l’Abbaye, 76960 Notre Dame de Bondeville – フランス。
登録およびインポート:
グラクソ・スミスクライン・ブラジル株式会社
エストラーダ ドス バンデイランテス、8,464。
リオデジャネイロ – RJ.
CNPJ 33.247.743/0001-10。
医師の処方箋に基づいて販売します。











