Contracep ® 150 mg は長時間作用型の注射可能な避妊薬であり、12 ~ 13 週間の間隔で投与する必要があり、最長 13 週間 (91 日) ごとに投与する必要があります。

コントラセップ® 150 mg の使用は、99.7% の症例で避妊に効果があり、失敗率は 0.3% です。
避妊薬はどのように機能しますか?
コントラセップ® 150 mg は、性腺刺激ホルモン(下垂体によって生成され、月経周期に関与するホルモン)の分泌を阻害し、排卵(卵子が卵巣から子宮に移動する過程)を妨げる合成プロゲスチン(合成プロゲステロン ホルモン)です。 、受精できる場所)、子宮内膜(子宮の内部を覆う層)の厚さを減少させます。その結果、避妊効果が得られます。
避妊具の禁忌
Contracep ® 150 mg は次の場合には禁忌です。
- 妊娠している、または妊娠していると思われる患者の妊娠を診断するための検査。
- 酢酸メドロキシプロゲステロンまたはその配合成分に対する過敏症が知られている患者。
- 原因不明の性器出血のある患者。
- 乳がんの疑いのある患者、または乳がんが証明されている患者。
- 重度の肝機能障害(肝機能の変化)のある患者。
- 活動性血栓性静脈炎、または現在または過去に血栓塞栓性障害または脳血管障害の病歴がある患者。
- 稽留流産の既往歴のある患者。
この薬は男性の使用が禁忌です。
コントラセプ® 150 mg 注射剤は初潮 (最初の月経) 前には適応されません。
この薬は、妊娠している女性、または治療中に妊娠する可能性のある女性は使用しないでください。
避妊具の使用方法
Contracep ® 150 mg のバイアルとプレフィルドシリンジは、投与する用量が均一な懸濁液になるように、使用前に激しく振盪する必要があります。
Contracep ® 150 mg を筋肉内 (筋肉内) に適用する必要があります。 Contracep ®溶液は、他の薬剤と同時に (同じ注射器内で) 投与しないでください。
避妊のための推奨用量:
12~13週間ごとに、臀部(臀部)または三角筋(上腕)の筋肉に150 mgを筋肉内投与します。申請間の最大間隔は 13 週間 (91 日) である必要があります。
Contracep ® 150 mg は妊娠中に使用しないでください。これらのリスクを排除するには、通常の月経周期の開始後最初の 5 日間に注射を行うことが重要です。または、子供に母乳を与えていない場合は、産後最初の 5 日間。授乳中の場合は、コントラセップ® 150 mg を産後 6 週目からのみ投与してください。
Contracep ® 150 mg を他の避妊法の代わりに使用する場合、その方法の作用機序に基づいて避妊効果を保証する方法で適用する必要があります。 (例: 経口避妊薬を変更する患者は、最後の有効な経口避妊薬錠剤を服用してから 7 日以内に最初の注射を受けなければなりません)。
小児への使用
コントラセップ® 150 mg は初経(最初の月経)前には適応されません。
プレフィルドシリンジの使用に関する特別な指示
激しく振って懸濁液を均質化します。シリンジプロテクターを取り外し、慎重に針を取り付けます。ニードルプロテクターを取り外して注射を行ってください。プレフィルドシリンジは単回使用のみです。
非互換性
注射剤は他の薬剤と混合してはなりません。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。医師の知識なしに治療を中止しないでください。
コントラセプの使用を忘れた場合はどうすればよいですか?
コントラセプ® 150 mg は、12 ~ 13 週間の間隔で、最大 13 週間 (91 日) ごとに筋肉内投与する必要があります。
最後の塗布から 91 日以上が経過した場合は、新たに Contracep ® 150 mg を塗布する前に、血液検査により妊娠を除外する必要があります。
13 週間が終了する前に、医師に連絡して、新しい申請の正しい日付をスケジュールしてください。
この薬は医師の指示に従って厳密に使用する限り、優れた避妊効果があります。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
避妊具の使用上の注意
一般的な
Contracep ® 150 mg による治療中に予期せぬ膣内出血が発生した場合は、診断検査が推奨されます。このような場合は医師に知らせてください。
この薬はうつ病、糖尿病、体液貯留を悪化させる可能性があります。
うつ病を患っている、またはうつ病を患っていた場合は医師に伝えてください。
糖尿病や高血圧(血圧上昇)がある場合は医師に伝えてください。
この薬は、一部の臨床検査や子宮頸部検査の結果を変える可能性があります。臨床検査を受ける場合は、コントラセップ® 150 mg で治療を受けていることを病理学者に知らせてください。
突然の完全または部分的な視力喪失、または眼球突出(眼球の異常な突出)、複視(ものが二重に見える)または片頭痛(頭痛)が突然始まった場合は、検査が完了するまで薬を再投与してはなりません。実施した。
コントラセップ® 150 mg を服用する前に、次の症状がある場合も医師に伝えてください。
- 骨疾患、定期的な飲酒または喫煙、神経性食欲不振、骨粗鬆症の強い家族歴など、弱い骨(骨粗鬆症)の危険因子。
- 月経が不規則または通常より軽い。
- 現在または過去に乳がんがある、または乳がんにかかっていると考えている。
- 乳がんの家族歴。
- 異常なマンモグラフィー (胸部 X 線)、線維嚢胞性乳房疾患、乳房のしこりまたはしこり、または乳首からの出血。
- 腎臓の問題;
- 高血圧;
- 彼は脳卒中を患った。
- 腕、脚、または肺に血栓があったことがある。片頭痛;
- 喘息;
- てんかん(けいれんまたは発作);
- その他の病状。
結合型エストロゲンをメドロキシプロゲステロンと組み合わせて使用すると、65 歳以上の閉経後の女性の認知症のリスクが高まる可能性があるため、使用すべきではありません。
エストロゲンおよびプロゲステロン療法を受けている閉経後の女性(50~79歳)では、心臓発作、脳卒中、DVT(深部静脈血栓症)、肺塞栓症、浸潤性乳がんのリスクが増加する可能性があります。疑わしい場合はすぐに中断してください。
処方薬や市販薬、ビタミン、ハーブサプリメントなど、服用しているすべての薬について医師に伝えてください。 Contracep® 150 mg は、他の薬剤と相互作用して重篤な副作用を引き起こす可能性があります。 Contracep ® 150 mg の使用中に、他の薬剤の用量を変更する必要がある場合があります。
以下のものを摂取している場合は特に医師に伝えてください。
- 鎮静薬(睡眠を引き起こす)。
- ボセンタン。
- 発作に対する薬。
- グリセオフルビン;
- 抗生物質;
- HIV (エイズ) 治療薬。
- アミノグルテチミド;
- セントジョーンズワート。
酢酸メドロキシプロゲステロンの使用中に妊娠した女性では、子宮外妊娠(子宮外妊娠)が発生する可能性があります。子宮外妊娠は、多くの場合手術が必要となる医療上の緊急事態です。子宮外妊娠は内出血、不妊、さらには死に至る可能性があります。
Contracep ® 150 mg を使用すると、以下の病状の兆候や症状が悪化(悪化)する可能性があります。
喘息、エリテマトーデス、てんかん、ポルフィリン症。
避妊方法のうち、100%効果があるのは性的禁欲だけです。避妊方法の有効性については以下を参照してください。
表 – 最低期待率と典型的な失敗率(継続的避妊薬使用の最初の1年間に誤って妊娠した女性の割合で表す)
|
方法 |
期待値が低い |
通常のレート |
|
コントラセップ® (プロゲスチン注射剤) |
0.3 |
0.3 |
|
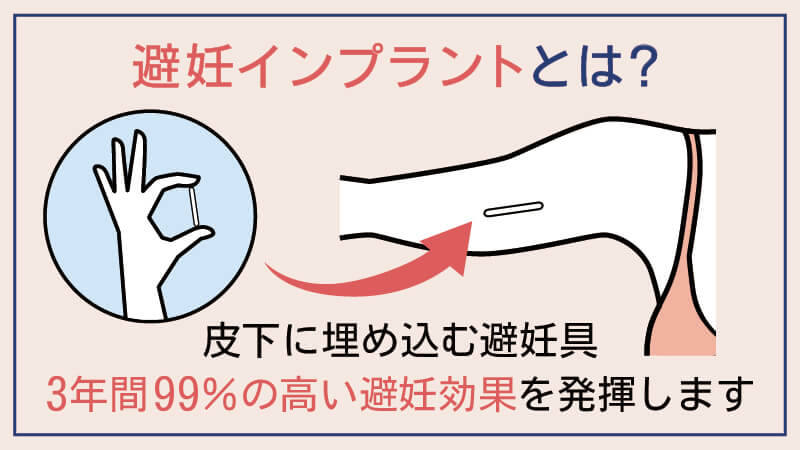
インプラント (ノープラント – 6 カプセル) |
0.2* |
0.2* |
|
女性の不妊手術 |
0.2 |
0.4 |
|
男性の不妊手術 |
0.1 |
0.15 |
|
コンビネーションピル |
0.1 |
3 |
|
プロゲスチンのみの錠剤 |
0.5 |
3 |
|
プロゲスタート IUD |
2.0 |
3 |
|
銅製 IUD T380A |
0.8 |
3 |
|
男性用コンドーム(コンドーム) |
2 |
12 |
|
ダイヤフラム |
6 |
18 |
|
ペッサリー |
6 |
18 |
|
殺精子剤 |
3 |
21 |
|
膣スポンジ – 経産婦 |
9 |
28 |
|
膣スポンジ – 未産婦 |
6 |
18 |
|
定期的な禁欲 |
1-9 |
20 |
|
性交中断 |
4 |
18 |
|
方法なし |
85 |
85 |
ソース:
トラッセルら。避妊効果研究を解釈するためのガイド。 Obstet.Gynecol。 1990年; 76:558-67。
*ノープラントのリーフレット
期待値が低い:
メソッドが指示どおりに使用された場合。
通常の料金:
推奨事項に厳密に従っていないものも含まれます。
医師は、コントラセップ® 150 mg の投与を受けて妊娠した患者、または重度の腹痛を訴えた患者における子宮外妊娠(子宮外)の可能性に注意を払う必要があります。
患者の予備的な身体検査とフォローアップには、乳房および骨盤臓器の適切な評価、およびパップスミアが含まれる必要があります。

Contracep ® 150 mg を使用すると、閉経の始まりを隠すことができます。
コントラセップ® 150 mg は、作用時間が長く、その結果として注射後の出血時間を予測することが難しいため、続発性無月経や機能性子宮出血の治療には推奨されません。このような状態では、経口治療が推奨されます。
この薬は月経を長期間中断したり、重度の月経間出血を引き起こす可能性があります。
避妊具の警告
酢酸メドロキシプロゲステロン注射剤を長期間使用する閉経前女性(最初の月経と最後の月経の間の期間)では、骨密度の低下(骨粗鬆症、骨の弱さを引き起こす病気)が発生することがあります。骨粗鬆症の危険因子を持つ女性(アルコール、タバコ、骨粗鬆症を引き起こす可能性のあるその他の薬物の慢性使用(抗けいれん薬やコルチコステロイドなど)、BMI(体重と身長の関係)が低い女性、および/または次のような症状のある患者摂食障害、骨代謝疾患(骨の生成と破壊)、および骨粗鬆症の家族歴がある場合は、医師の意見が骨粗鬆症のリスクを上回る場合を除き、コントラセプ® 150 mg の使用を避けるべきです。何らかの変化があった場合は医師に伝えてください。
すべての患者がカルシウムとビタミン D を十分に摂取することが推奨されます。
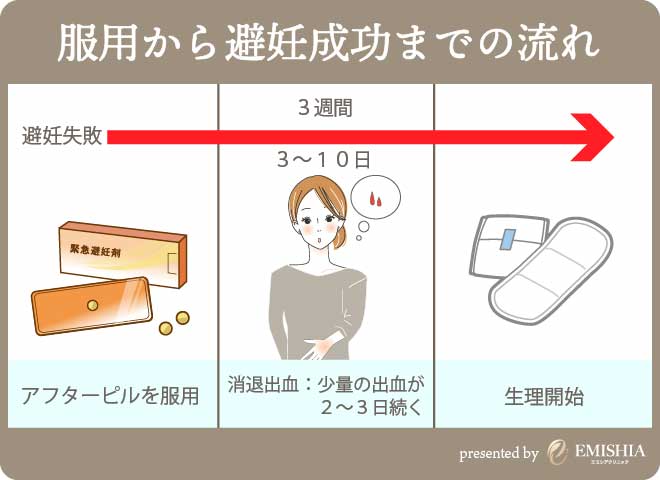
コントラセップ® 150 mg を使用しているほとんどの女性では、月経出血パターンの変化が観察されます (例: 不規則または予測不可能な出血、まれに継続的または大量の出血)。
治療の開始時には、月経と月経の間に出血や少量の出血が発生することがあります。
女性がコントラセップ® 150 mg を使用し続けると、不正出血を経験する人はほとんどいませんが、他の治療を必要とせずに、最長 18 か月またはそれ以上の期間にわたって無月経 (月経の欠如) を経験する人はほとんどいません。
持続性または大量の出血は、Contracep ® 150 mg の使用とは関係ありません。出血が続く場合や重度の場合は、すぐに医師に相談してください。
コントラセップ® 150 mg は、長期にわたる避妊効果をもたらします。薬の服用を中止してから妊娠するまでの平均期間(妊娠可能な患者の場合)は、使用期間に関係なく、10か月で、範囲は4~31か月です。 Contracep ® 150 mg による治療を受けている患者は、治療中に体重が増加する傾向を示しました。
Contracep ® 150 mg は、HIV 感染症 (AIDS) を含む性感染症 (STD) として知られる感染症を防ぐ効果はありません。
避妊法の利点とそのリスクは、女性ごとに個別に評価する必要があります。コントラセップ® 150 mg の使用は、99.7% の症例で避妊に効果があり、失敗率は 0.3% です。
機械の運転および操作能力への影響
機械の運転および操作能力に対する Contracep ® 150 mg の影響は体系的に評価されていません。
避妊薬の副作用
非常に一般的な反応 (この薬を使用している患者の 10% 以上で発生します)
緊張、頭痛、腹痛、腹部不快感、体重増加、体重減少。
一般的な反応 (この薬を使用している患者の 1% ~ 10% で発生します)
うつ病、性欲減退、めまい、吐き気(気分が悪い)、腹部膨満(体積の増加)、脱毛症(脱毛)、座瘡(にきび)、発疹(発疹)、腰痛、おりもの、乳房の圧痛、体液貯留、無力症(衰弱)。
まれな反応 (この薬を使用している患者の 0.1% ~ 1% に発生します)
薬剤に対する過敏症(アレルギー反応)、不眠症、けいれん、眠気、ほてり(体のほてり)、肝障害、多毛症(異常な毛の生え方)、蕁麻疹(かゆみを引き起こす、通常はアレルギー性の皮膚発疹)、そう痒症(かゆみ)、機能不全子宮出血(不規則、増加、減少、斑点)、乳汁漏出(乳房からの乳汁の異常分泌)、骨盤痛(腹部の下の領域の痛み)。
まれな反応(この薬を使用している患者の 0.01% ~ 0.1% で発生します)
アナフィラキシー反応(重度のアレルギー反応)、アナフィラキシー様反応(別のタイプの重篤なアレルギー反応)、血管浮腫(皮膚の深部の腫れを伴う重度の蕁麻疹)、長期無排卵(排卵の欠如)、無オルガズム(オルガスムの欠如)、塞栓症(血管の閉塞)、血栓症(血栓の形成)、黄疸(胆汁色素の蓄積による皮膚や粘膜の黄色化)、後天性脂肪異栄養症(体脂肪の減少)、関節痛(関節の痛み)、筋肉のけいれん(収縮) 、膣炎(膣内の炎症)、無月経(月経の欠如)、乳房の痛み、発熱(発熱)、倦怠感(倦怠感)、注射部位の反応、注射部位の持続性萎縮(皮膚および/または筋肉の変化)薬剤が適用された場所)、注射部位の結節/隆起、注射部位の痛み/圧痛、骨密度の低下(骨からのカルシウムの損失)、耐糖能の低下(グルコースの変化)。
市販後の経験では、コントラセップ® 150 mg を使用した患者において、骨折を含む骨粗鬆症のまれな症例が報告されています。 Contracep ® 150 mg の使用は、乳がん、腕、脚、肺、目での血栓の形成、脳卒中、視力喪失またはその他の目の問題や発作のリスク増加を引き起こす可能性があります。
骨への影響
Contracep ® 150 mg 注射剤を使用している女性は、骨密度の大幅な低下を経験する可能性があります。骨損失は使用期間が長くなるほど大きくなり、完全に元に戻らない場合があります。骨成長の重要な時期である青年期または成人初期にコントラセップ® 150 mg 注射剤を使用すると、ピーク骨量が減少し、その後の骨粗鬆症性骨折のリスクが増加するかどうかは不明です。
次のような症状がある場合は、すぐに医療従事者に連絡してください。 鋭い胸の痛み、喀血、または突然の息切れ(肺に血栓がある可能性を示します)、突然の激しい頭痛または嘔吐、めまいまたは失神、視力または言語、脱力感またはしびれ腕または脚の痛みまたは腫れ(脚の血栓の可能性を示します)、ふくらはぎの痛みまたは腫れ(脚の血栓の可能性を示します)、異常な大量の性器出血、下腹部の痛みまたは圧痛、持続的な痛み、膿または出血注射部位、目や皮膚の黄ばみ、蕁麻疹、呼吸困難など。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。
また、顧客サービスを通じて会社に通知してください。
避妊具特別集団
妊娠中の使用
コントラセップ® 150 mg は妊婦には禁忌です。無月経(月経周期がない)を経験している場合は、この薬の使用を開始する前に妊娠を除外するための検査を受けることをお勧めします。
妊娠中にコントラセップ® 150 mg を誤って使用すると、赤ちゃんの性器の発育が変化し、発育が低下する可能性があり、その結果、子どもが低出生体重児になるリスクが高まり、合併症や死亡リスクが高まる可能性があります。
この薬は妊娠中に先天異常を引き起こします。
治療中または治療終了後に妊娠している場合は医師に知らせてください。
授乳期(授乳中)に使用する
コントラセップ® 150 mg とその代謝物は母乳中に排泄されますが、これが赤ちゃんに害を及ぼすことを示唆する証拠はなく、授乳中でも使用できます。コントラセップ® 150mg の投与は、産後 6 週目からのみ行ってください。
授乳中の場合は医師に伝えてください。
避妊具の成分
Contracep ®の各 mL には以下が含まれます。
|
酢酸メドロキシプロゲステロン |
150.00mg |
|
車両* qsp |
1.00mL |
※エチルアルコール、塩化ナトリウム、メチルパラベン、プロピルパラベン、シメチコン、ポリソルベート80、マクロゴール、注射用水。
避妊具の贈呈
注射用懸濁液 150 mg/mL
1 mL のアンプルが 1 箱入っています。
投与経路:筋肉内経路。
大人用。
避妊具の過剰摂取
過剰摂取の治療は対症療法的かつ支持的なものでなければなりません。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
避妊薬と薬物の相互作用

Contracep ® 150 mg による治療を開始する前または治療中に他の薬剤を使用している場合は、医師に知らせることが非常に重要です。医師は、薬剤が相互に反応して、それらの薬剤の作用または他の薬剤の作用を変化させるかどうかを評価する必要があります。これは薬物相互作用と呼ばれるもので、コントラセップ® 150 mg をアミノグルテチミド (クッシング症候群の治療に使用される薬) と一緒に使用すると発生する可能性があり、この他の薬の効果が低下する可能性があります。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
避妊具の作用
有効性の結果
プロゲステロン剤は、稀発月経または続発性無月経の女性に消退性出血をうまく誘導するために使用されています。この目的で最もよく使用される薬剤は酢酸メドロキシプロゲステロン (有効成分) です。酢酸メドロキシプロゲステロン(活性物質)の短期間の経口治療により、無月経女性の 93% で消退出血が生じます。 1
機能不全子宮出血患者を対象に実施された前向きランダム化研究では、酢酸メドロキシプロゲステロン(有効成分)により患者の 76% で出血が止まり、平均出血時間は 3 日でした。 2あるレビュー研究では、酢酸メドロキシプロゲステロン (活性物質) を含む経口プロゲスチンは、機能不全子宮出血の 87% 減少を実証しました。 3機能不全子宮出血患者を対象とした別の研究では、酢酸メドロキシプロゲステロン (活性物質) 10 mg を 1 日 2 回に分けて使用すると、3 か月の使用後に平均 57.7% の失血の減少が実証されました。 4
子宮摘出を受けていない閉経期の女性におけるエストロゲンの子宮内膜への影響に対抗するホルモン療法において、エストロゲン療法を補完するものとして、酢酸メドロキシプロゲステロン(活性物質)の有効性がいくつかの研究で実証されています。ウッドラフアンプ;更年期障害研究グループを代表してピッカー博士は、酢酸メドロキシプロゲステロンと結合型エストロゲンを組み合わせて使用した患者は、結合型エストロゲン単独で治療した女性よりも子宮内膜増殖症の発生率が有意に低いことを実証した。 596人の閉経患者を3年間追跡した別の研究では、連続的または周期的な酢酸メドロキシプロゲステロン(活性物質)と抱合型エストロゲンの併用により、エストロゲン単独療法と比較して子宮内膜が過形成変化から保護されることが実証されました。 6
参考文献
1. Battino S、Ben-Ami M、Geslevich Y、Weiner E、Shalev E。続発性無月経の女性における経口ジドロゲステロンまたは酢酸メドロキシプロゲステロンの投与後の消退出血に関連する要因。婦人科オブステット投資。 1996;42:113–6。
2. マンローMG、他。急性子宮出血に対する経口酢酸メドロキシプロゲステロンと併用経口避妊薬: ランダム化対照試験。産科婦人科。 2006年; 108(4):924-9。
3. マッテソン KA 他大量月経出血の非外科的管理:系統的レビュー。産科婦人科。 2013:121(3):632-43。
4. クリプラニ A ら。酢酸メドロキシプロゲステロンと比較した、機能不全子宮出血の管理におけるトラネキサム酸の役割。 J Obstet Gynaecol 2006; 26(7):673-8。
5. 更年期障害研究グループのウッドラフ JD、ピッカー JH。結合型エストロゲン(プレマリン)と酢酸メドロキシプロゲステロン、または結合型エストロゲン単独を服用している閉経後の女性における子宮内膜過形成の発生率。 Am J Obstet Gynecol 1994; 170(5):1213-23。
6. PEPI 裁判の執筆グループ。閉経後女性の子宮内膜組織学に対するホルモン補充療法の影響。閉経後エストロゲン/プロゲスチン介入(PEPI)試験。自工会 1996; 275(5):370-5
出典:プロベラ薬の専門リーフレット。
薬理学的特徴
薬力学特性
酢酸メドロキシプロゲステロン(活性物質)(17a-ヒドロキシ-6a-メチルプロゲステロンアセテート)は、プロゲステロンの誘導体です。
作用機序
酢酸メドロキシプロゲステロン(活性物質)は合成プロゲスチン(内因性ホルモンのプロゲステロンと構造的に関連している)であり、内分泌系に対していくつかの薬理作用があることが示されています。
- 下垂体性腺刺激ホルモン (FSH および LH) の阻害。
- ACTHおよびヒドロコルチゾンの血中濃度の低下。
- 循環テストステロンの減少;
- 循環エストロゲンレベルの低下(FSH阻害と肝臓レダクターゼの酵素的誘導の結果、テストステロンクリアランスが増加し、その結果アンドロゲンからエストロゲンへの変換が減少します)。
これらの作用はすべて、以下に説明する多くの薬理学的効果をもたらします。
酢酸メドロキシプロゲステロン(活性物質)は、適切な内因性エストロゲンとともに推奨用量で女性に経口または非経口投与され、増殖性子宮内膜を分泌性子宮内膜に変換します。アンドロゲン作用とアナボリック作用が指摘されていますが、この薬には顕著なエストロゲン作用がないようです。入手可能なデータによると、一般的に推奨される経口用量を 1 日 1 回投与した場合には、この作用は起こらないことが示されています。
臨床研究
女性の健康イニシアチブに関する調査 – WHI
WHI結合型ウマエストロゲン(0.625mg)/酢酸メドロキシプロゲステロン(2.5mg)の研究には、ベースライン時に無傷の子宮を持つ50~79歳の閉経後女性16,608人が参加し、特定の慢性疾患の予防におけるプラセボと比較した併用療法のリスクと利点を評価しました。主な目的は冠状動脈性心疾患(非致死性心筋梗塞および致死的な冠状動脈性心疾患)の発生率であり、主な有害転帰として浸潤性乳がんが研究されました。この研究は以前、追跡調査中央値5.2年(計画では8.5年)後に中止されたが、その理由は、中止手順によれば、乳がんおよび心血管イベントのリスク増加が「インデックス・グローバル」に含まれる特定の利益を超えたためである。
結合型馬エストロゲン/酢酸メドロキシプロゲステロン(活性物質)の組み合わせによる治療により、骨粗鬆症性骨折(23%)および全骨折(24%)の有意な減少が報告されました。
100 万人の女性の調査 – (100 万人の女性の調査 – MWS)
MWSは、英国の50~64歳の女性1,084,110人を登録した前向きコホート研究で、そのうち確定閉経年齢の828,923人が、ホルモン治療に関連した乳がんリスクの主な分析に含まれていた。合計すると、研究対象集団の 50% が、ある時点でホルモン治療を使用しました。研究の開始時にホルモン治療をより頻繁に使用していた患者は、エストロゲン単独(41%)またはエストロゲン/プロゲステロンの組み合わせ(50%)を含む製剤の使用を報告しました。平均追跡期間は、がん発生率分析で2.6年、死亡率分析で4.1年でした。
心臓とエストロゲン/プロゲスチン補充研究 – HERS
HERS および HERS II 研究は、冠状動脈疾患を患う閉経後の女性を対象とした、結合型馬エストロゲン (0.625 mg) と酢酸メドロキシプロゲステロン (2.5 mg) の併用療法の継続経口投与による長期効果に関する、前向きのランダム化二次心臓予防研究の 2 つでした。平均年齢66.7歳で子宮に損傷がない2,763人の閉経後の女性がこの研究に登録された。平均追跡期間は、HERS では 4.1 年、HERS II ではさらに 2.7 年(合計 6.8 年)でした。
Women’s Health Initiative の記憶に関する研究 – WHIMS

WHI のサブ研究である WHIMS 研究には、結合型馬エストロゲン (0.625 mg)/酢酸メドロキシプロゲステロン (活性物質) (2.5 mg) または結合型馬の効果を評価するために、65 ~ 79 歳の主に健康な閉経後の女性 4,532 人が参加しました。エストロゲン (0.625 mg) 単独の場合、プラセボと比較した認知症の可能性の発生率。結合型ウマエストロゲン/酢酸メドロキシプロゲステロン(活性物質)の平均追跡期間は4.05年でした。
薬物動態学的特性
吸収
経口酢酸メドロキシプロゲステロン(活性物質)は急速に吸収され、2 ~ 4 時間で最大濃度が得られます。経口酢酸メドロキシプロゲステロン(活性物質)の半減期は約 17 時間です。 90%がタンパク質に結合しており、主に尿中に排泄されます。
食事の影響
食物と一緒に投与すると、酢酸メドロキシプロゲステロン (活性物質) の生物学的利用能が増加します。酢酸メドロキシプロゲステロン (活性物質) 10 mg を食事の直前または直後に経口投与すると、酢酸メドロキシプロゲステロン (活性物質) の最大血清濃度 (Cmax) (それぞれ 51 および 77%) および曲線下面積が増加しました。 (AUC、それぞれ 18% と 33%)。酢酸メドロキシプロゲステロン(活性物質)の半減期は、食物によって変化しませんでした。
分布
酢酸メドロキシプロゲステロン(活性物質)は約 90% がタンパク質、主にアルブミンに結合します。酢酸メドロキシプロゲステロン (活性物質) は、グロブリン結合性ホルモンと結合しません。酢酸メドロキシプロゲステロン(活性物質)が結合しないことにより、薬理学的反応が調節されます。
代謝
経口投与後、酢酸メドロキシプロゲステロン (活性物質) は肝臓で環 A を介して、および/または側鎖の水酸化により広範囲に代謝され、その後抱合されて尿中に除去されます。酢酸メドロキシプロゲステロン (活性物質) の少なくとも 16 の代謝物が同定されています。酢酸メドロキシプロゲステロン (活性物質) の代謝を評価するために計画された研究では、ヒト肝ミクロソームにおける酢酸メドロキシプロゲステロン (活性物質) の代謝全体にヒト シトクロム P450 3A4 が主に関与していることが結果から示唆されています。
排除
酢酸メドロキシプロゲステロン(活性物質)の代謝産物の大部分は抱合グルクロニドとして尿中に排泄され、硫酸塩として排泄されるのはほんの少量です。脂肪肝患者の 10 mg または 100 mg の投与後、無傷の酢酸メドロキシプロゲステロン (活性物質) として 24 時間にわたって尿中に排泄された平均用量パーセンテージは、それぞれ 7.3% と 6.4% でした。経口酢酸メドロキシプロゲステロン(活性物質)の排出半減期は 12 ~ 17 時間です。
前臨床安全性データ
発がん、突然変異誘発、生殖能力の変化
酢酸メドロキシプロゲステロン(活性物質)の長期筋肉内投与は、ビーグル犬に乳腺腫瘍を引き起こすことが示されています。ラットおよびマウスにおける酢酸メドロキシプロゲステロン (活性物質) の経口投与に関連した発がん性効果の証拠はありません。酢酸メドロキシプロゲステロン (活性物質) は、一連のin vitroまたはin vivo遺伝毒性試験において変異原性がありませんでした。高用量の酢酸メドロキシプロゲステロン(活性物質)は不妊治療薬であり、高用量では治療が中止されるまで生殖能力に変化を引き起こすことが期待できます。
出典:プロベラ薬の専門リーフレット。
避妊具の保管管理
室温(15℃~30℃)で保管してください。光や湿気から守ります。カートリッジ/アンプルのパッケージは直立した状態で保管してください。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。
薬の特徴
製品の物理的および感覚的特徴: 均一な白い懸濁液。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かないところに保管してください。

避妊具の法的声明
MS登録番号1.0583.0220。
農場。答え:
マリア・ゲイサ・ピメンテル・デ・リマ・エ・シルバ博士
CRF – SP番号8,082
登録者:
Germed Farmacêutica Ltda
ロッド、ジャーナリスト、フランシスコ・アギーレ・プロエンサ、KM 08
チャカラ アッセイ地区
CEP 13186-901
オルトランディア – SP
CNPJ: 45.992.062/0001-65
ブラジルの産業
販売者:
EMS シグマファーマ株式会社
オルトランディア – SP
製造元:
EMS S/A
オルトランディア – SP
医師の処方箋に基づいて販売します。








-1024x576.jpg?resize=1024,576&ssl=1)


