薬を投与する前に、医師は血液検査を行ってフェリンジェクトの必要用量を計算する必要があります。

フェリンジェクトはどのように機能しますか?
フェリンジェクトは、貧血の治療に使用される抗貧血製剤です。 Ferinject には、カルボキシマルトース第二鉄 (炭水化物の鉄化合物) の形で鉄が含まれています。鉄は、赤血球のヘモグロビンと筋肉組織のミオグロビンの酸素輸送機能に必須の元素です。
さらに、鉄は人体の維持に必要な他の多くの機能にも関与しています。
フェリンジェクトの禁忌
フェリンジェクトは以下の患者には使用されるべきではありません。
- カルボキシマルトース第二鉄複合体、カルボキシマルトース第二鉄溶液、または製剤中の賦形剤のいずれかに対する既知のアレルギー(過敏症)がある。
- 鉄欠乏によって引き起こされないあらゆるタイプの貧血(非鉄欠乏)、たとえば他の小球性アネミン。
- 鉄過剰症(体内の鉄過剰)または鉄の使用障害の状況。
フェリンジェクトの使い方
医師は次の 3 つの方法で Ferinject を投与できます。
希釈せずに注射(ボーラス)で、透析中に、または希釈して点滴で使用します。
注射 (ボーラス):
鉄分 1,000 mg に相当する最大 20 mL のフェリンジェクトを週に 1 回、静脈に直接投与できます。
透析を受けている場合:
血液透析セッション中に、透析装置を通じて最大 200 mg (1 日の最大 1 回投与量) のフェリンジェクトを受け取ることができます。
注入:
鉄分 1,000 mg に相当する最大 20 mL のフェリンジェクトを週に 1 回、静脈に直接投与します。点滴による塗布の場合、Ferinject は 0.9% 塩化ナトリウム溶液で希釈され、最大 250 mL の容量が得られ、外観は茶色になります。
医師は適切な用量を計算し、投与方法、頻度、治療期間を選択する責任を負います。フェリンジェクトは皮下または筋肉内に投与しないでください。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。医師の知識なしに治療を中止しないでください。
Ferinjectの使用を忘れた場合はどうすればよいですか?
まだ投与されていない場合は、できるだけ早く投与する必要があります。次回の投与は、投与間隔を考慮して、推奨投与量スケジュールに従わなければなりません。
疑問がある場合は、薬剤師または医師または歯科医師にアドバイスを求めてください。
フェリンジェクトの注意事項

感染症、喘息、湿疹(皮膚病変)、アレルギー、肝臓病がある場合は医師に伝えてください。
Ferinject には、原液 1 ミリリットルあたり 0.24 ミリモル (または 5.5 mg) のナトリウムが含まれています。減塩食を摂取している患者の場合は、これを考慮する必要があります。
Ferinject には、原液 1 ミリリットルあたり最大 75 mcg のアルミニウムが含まれています。透析を受けている患者を治療する際には、このことを考慮する必要があります。
静脈内に投与される鉄剤は、アナフィラキシー反応 (重度のアレルギー反応) を含む過敏反応を引き起こす可能性があり、致命的な場合もあります。したがって、心肺蘇生のサポートが受けられる必要があります。投与中にアレルギー反応または不耐症の兆候が生じた場合は、治療を直ちに中止する必要があります。
カルボキシマルトース第二鉄を含む非経口鉄錯体の以前の投与後に過敏症反応が報告されていますが、この種の副作用は観察されていません。Ferinject の各投与後、少なくとも 30 分間はすべての患者を観察する必要があります。
妊娠中および授乳中の使用
薬を服用する前に、妊娠中または授乳中であることを医師に伝えてください。
妊娠期間中、特に妊娠初期または授乳中に投与する前に、その使用のリスクと利益についての慎重な医学的評価が必要です。治療は通常、妊娠の最後の 6 か月に限定されるべきです。
妊娠リスクカテゴリーB
この薬は、妊娠中または授乳中の女性が医師または歯科外科医のアドバイスなしに使用しないでください。
小児への使用
Ferinject は小児では研究されていないため、小児には推奨されません。小児におけるフェリンジェクトの使用に関するデータは限られています。
高齢者への使用
高齢患者に対するフェリンジェクトの静脈内投与には特別な注意は必要ありません。ケアは他の患者と同様に行う必要があります。
血液透析依存性の慢性腎臓病患者
鉄の 1 日最大 1 回注射量は 200 mg を超えないようにしてください。このような患者が 200 mg を超える鉄を単回投与された場合の安全性データはありません。
腎機能障害のある患者さん
腎機能障害および慢性心不全の患者では、肝酵素の上昇が見られましたが、一般的な安全性の懸念は生じませんでした。
肝機能障害のある患者
肝障害のある患者を対象とした研究は行われていません。肝機能障害のある患者、特に鉄過剰が促進因子である遅発性皮膚ポルフィリン症の患者では、非経口(すなわち、経口または胃腸系以外、例えば静脈)からの鉄投与は避けるべきである。
肝不全患者への鉄の非経口投与は、リスクと利益を慎重に評価した後にのみ実行する必要があります。 Ferinject が肝臓酵素の一時的な増加を引き起こす可能性があることが知られています。
このような場合、鉄剤が処方されている場合は、肝機能を監視する必要があります。
機械を運転および操作する能力への影響
この薬の使用が機械の運転や操作能力に影響を与える可能性はほとんどありません。
他の物質との併用
フェリンジェクトは、経口鉄化合物と併用すると効果が低下する可能性があるため、併用しないでください。市販薬を含む他の薬を服用している場合、または最近服用した場合は、医師に伝えてください。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
フェリンジェクトの副作用
すべての患者が有害事象を経験するわけではありませんが、他の医薬品と同様に、フェリンジェクトも有害事象を引き起こす可能性があります。
最も一般的に報告されている副作用は吐き気で、患者の 2.9% に発生します。
一般的な反応 (この薬を使用している患者の 1% ~ 10% に発生します):
頭痛、めまい、高血圧(高血圧)、吐き気、塗布部位の反応、低リン血症(血液中のリン酸塩レベルが非常に低い)、潮紅(発赤)。
まれな反応 (この薬を使用している患者の 0.1% ~ 1% に発生します):
過敏症、感覚異常(灼熱感、チクチク感、くすぐったさ、チクチク感などの異常な感覚)、味覚障害(味覚の変化)、頻脈(心拍数の上昇)、低血圧(血圧低下)、呼吸困難(息切れ)、嘔吐、消化不良(胃のむかつき)、腹痛、便秘、下痢、紅斑(発赤)、そう痒症(かゆみ)、じんましん、発疹、筋肉痛(筋肉痛)、腰痛・関節痛、四肢の痛み、けいれん(筋肉の震え、発熱、倦怠感、胸痛、末梢浮腫(腫れ)、痛み、悪寒 血液中の酵素(アスパラギン酸アミノトランスフェラーゼ、ガンマグルタミルトランスフェラーゼ、乳酸デヒドロゲナーゼ、アルカリホスファターゼ)が増加し、肝臓内のアラニンアミノトランスフェラーゼと呼ばれる特定の酵素が増加します。
まれな反応 (この薬を使用している患者の 0.01% ~ 0.1% で発生します):
アナフィラキシー様反応(重度のアレルギー)および倦怠感。
販売開始後の自発報告による副作用
フェリンジェクトの販売開始後、以下のような副作用が認められました。
|
オルガンクラスシステム |
優先条件* |
|
神経系疾患 |
意識を失い、めまいが起こります。 |
|
精神障害 |
不安。 |
|
心血管疾患 |
失神、失神。 |
|
皮膚および皮下組織の疾患 |
血管浮腫、皮膚炎、顔面蒼白および浮腫。 |
|
呼吸器、胸部、縦隔の疾患 |
気管支けいれん。 |
|
一般的および管理部位の障害 |
インフルエンザの症状(測定可能な発熱を伴う) |
※頻度は不明。
研究室の変更:
以下の臨床検査値の変化は臨床研究中に観察され、その頻度は観察された測定値に基づいて計算されたものであり、報告された副作用ではありません。
非常に一般的 (gt; 1/10):
血中リンの一時的な減少。
一般的 (?1/100、lt;1/10):
ガンマグルタミルトランスフェラーゼの増加。
アンコモン (?1/1,000、lt;1/100):
アラニンアミノトランスフェラーゼの増加、アルカリホスファターゼの増加、アスパラギン酸アミノトランスフェラーゼの増加、血中乳酸デヒドロゲナーゼの増加。
これらの副作用のいずれかが重篤になった場合、または記載されていない副作用に気づいた場合は、医師または薬剤師に相談してください。
注意:
この製品は新薬であり、研究により許容できる有効性と安全性が示されていますが、たとえ正しく適応され使用されたとしても、予測できないまたは未知の副作用が発生する可能性があります。この場合は医師または歯科医師に知らせてください。
フェリンジェクトの構成
各 10 ml バイアルには次のものが含まれています。
カルボキシマルトース第二鉄 1800 mg (鉄 III 500 mg に相当)。
賦形剤:
注射用水、水酸化ナトリウム(pH調整用)、塩酸(pH調整用)。
フェリンジェクトの過剰摂取
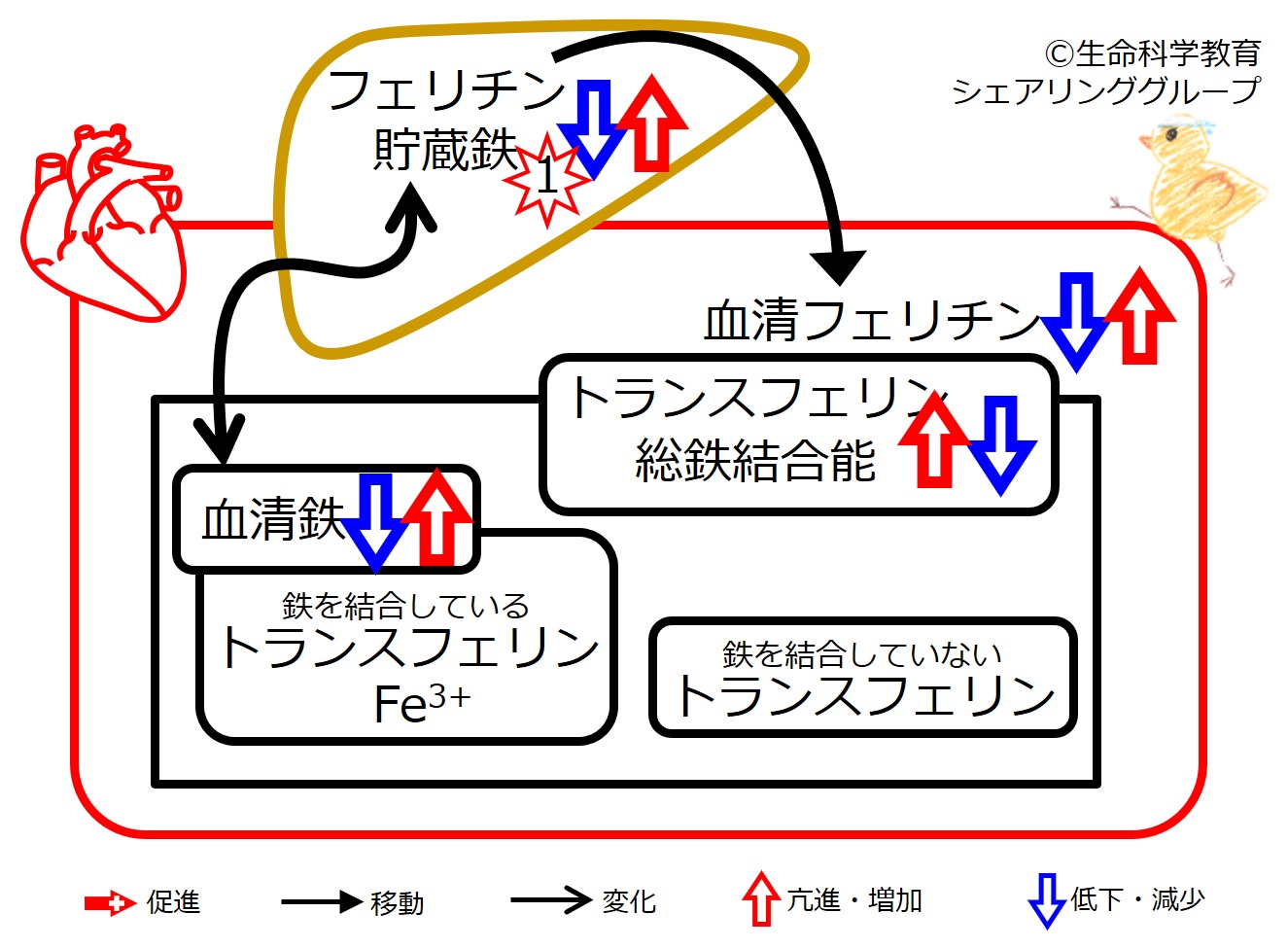
過剰な用量を使用すると、保管場所に鉄が蓄積する可能性があります。医師はフェリチンや血清トランスフェリンなどの鉄パラメータを監視する必要があります。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。
さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
フェリンジェクトの薬物相互作用
非経口使用のためのすべての鉄ベースの製剤と同様に、経口鉄吸収が低下するため、カルボキシマルトース第二鉄 (活性物質) を経口鉄化合物と同時に投与すべきではありません。したがって、必要に応じて、カルボキシマルトース第二鉄(活性物質)の最後の注射後少なくとも 5 日間は経口鉄療法を開始しないでください。
フェリンジェクト物質の作用
有効性の結果
カルボキシマルトース第二鉄(活性物質)の治療効果は、炎症性腸疾患、重度の子宮出血2、産後貧血3-5、慢性腎臓病の患者を含む鉄欠乏性貧血の成人集団を対象とした無作為多施設共同公開比較臨床研究で評価されました。透析なし6、8-10、または透析中7、9、10。ほとんどの研究では、カルボキシマルトース第二鉄(活性物質)の1,000 mg以上の鉄を15分間かけて投与した場合(その後の投与量は1週間間隔で投与)における有効性が、硫酸第一鉄の6~12週間の投与計画と比較されました。経口摂取、1 日 3 回 65 mg の鉄に相当2,4-6、または 100 mg の鉄を 1 日 2 回摂取1。
カルボキシマルトース第二鉄(活性物質)の静脈内投与は、ヘモグロビンレベルの改善に効果的であり、硫酸第一鉄を用いた場合よりも、ベースライン値と比較してヘモグロビンレベルのより迅速で統計的に有意な増加を伴いました。治療の4週間目で、カルボキシマルトース第二鉄(活性物質)で治療した患者の34.2%に対し、経口硫酸第一鉄で治療したグループの18.2%は、ヘモグロビンの増加を2 g/dL以下に達成した(plt;0.051、2.6)。両方の治療グループの網赤血球能力の最大レベルは、治療の 2 週間目に観察されました。治療の 2 週間目以降、カルボキシマルトース第二鉄 (活性物質) では、硫酸第一鉄で治療したグループと比較して、有意に高いフェリチン レベルが達成されました。
カルボキシマルトース第二鉄 (活性物質) は、硫酸第一鉄よりも有意に高い割合 (plt;0.0002) で血清フェリチン反応と関連しており、血清フェリチン レベルの急速かつ顕著な増加をもたらし、平均値 3 ~ 7 または中央値 1 は 300 ~ 600 でした。治療の最初または 2 週間目の mcg/L。これらのレベルはその後いくらかの低下を示しましたが、研究終了までベースラインレベルよりも約40~400 mcg/L高いままであり、患者は2週目または31.3~7週目に最後の鉄投与を受けました。 12週目の終わり(研究終了)に、フェリチン反応(血清レベル50~800 mcg/L3または100~800 mcg/L1として定義)を示した患者の割合は、カルボキシマルトース第二鉄で治療したグループの方が高かった。炎症性腸疾患 (26.5% 対 3.3%)1 および産後貧血 (77.7% 対 32.6%) の患者において、鉄で治療された患者よりも (活性物質) の摂取量が多かった。
トランスフェリン飽和度は、カルボキシマルトース第二鉄 (活性物質) の使用により 21.4-6 週目または 43 週目に 15-28% 増加し、硫酸第一鉄の使用により 10-17% 増加しました 1.3-6。すべての研究評価期間において、ベースラインに対するトランスフェリン飽和度の変化は、硫酸第一鉄よりもカルボキシマルトース第二鉄 (活性物質) の方が有意に高かった (plt;0.001)。
産後/手術後の貧血については、Breymann C et al.鉄欠乏性貧血を治療するためのカルボキシマルトース第二鉄と硫酸第一鉄の安全性と有効性を比較します。患者は、カルボキシマルトース第二鉄(1,000 mgを週に最大3回、15分かけて投与;n=227)または硫酸第一鉄(100 mgを1日2回、12週間、12週間)を受ける群に無作為に割り付けられた(2:1の比率)。 。
ヘモグロビンと貯蔵鉄の変化は12週目に分析されました。カルボキシマルトース第二鉄はヘモグロビンの補正において硫酸第一鉄と同じくらい効果的でしたが、治療期間ははるかに短くなりました(2週間対12週間)。フェリチンレベルが著しく高かった。したがって、非経口カルボキシマルトース第二鉄は、治療期間の短縮、アドヒアランスの向上、貯蔵鉄の迅速な正常化、胃腸障害の発生率の低下といった利点を備えた、産後/手術後の貧血に対する安全で効果的な治療選択肢です。
貧血の有無にかかわらず、うっ血性心不全(NYHAクラスIIまたはIII)および鉄欠乏症の患者459人に対するカルボキシマルトース第二鉄(活性物質)による治療は、無作為化およびプラセボと比較した多施設共同研究の結果によれば、症状と腎機能の改善を示したFAIR-HF (鉄欠乏症および慢性心不全患者におけるカルボキシマルトース第二鉄 (活性物質) の評価)。患者の総合評価によれば、カルボキシマルトース第二鉄(活性物質)を投与された患者のうち、50%が改善を記録したのに対し、プラセボを投与された患者では28%でした。 4、12、および 24 週目に、カルボキシマルトース鉄 (活性物質) と比較して、推定糸球体濾過率 (eGFR) の増加が観察されました。プラセボ群では腎機能がわずかに低下。研究終了時(24週目)、カルボキシマルトース第二鉄群(活性物質)のGFRは、ベースラインと比較して平均3.2 mL/分/1.73 m 2増加しましたが、0.6 mL/分/1減少しました。 、プラセボグループでは73 m 2 (p=0.017)。カルボキシマルトース第二鉄(活性物質)に対する反応は、研究開始時の腎機能障害のレベル、性別、年齢、心不全の重症度、または貧血の存在とは無関係でした。
エビスタティエフ R. et al.炎症性腸疾患(IBD)および鉄欠乏性貧血(ADF)の患者を対象に、カルボキシマルトース第二鉄(CMF)の新しい単回投与レジメン(毎週1,000mg)と、個別に計算した用量のスクロース第二鉄(SF)の有効性と安全性を比較した。 CMFで治療された240人の患者とDESで治療された235人の患者の結果が分析されました。 SF患者よりもCMF患者の方がヘモグロビン(Hb)反応(150人[65.8%]対118人[53.6%];差12.2%、p=0.004)またはHb正常化(166人[72.8%]対136人[61.8%])を達成した患者の方が多かった。 %]; 差は 11.0%、p=0.015)。
研究薬の忍容性は良好で、薬剤関連の有害事象は臨床経験と一致していました。この研究では、ガンツォーニ式を使用して計算されたSFの投与スケジュールと比較して、CMFのより単純な投与スケジュールでより優れた有効性と治療遵守が実証されたほか、優れた安全性プロファイルも実証されました。
Steinmetz T らによる観察研究。らは、2008年12月から2010年7月までにドイツの73の血液学/腫瘍科センターに登録された鉄欠乏性貧血のがん患者401人(18歳以上)を評価した。赤血球生成促進剤(AEE)と関連するかどうかに関係なく、カルボキシマルトース第二鉄(CMF)が投与された。 。患者の90%は固形腫瘍を患っており、細胞傷害性化学療法を受けていた(72%)。
患者当たりの平均用量はCMF 1,333 mgで、15.7%がESAを受けていました。軽度、中等度、重度の貧血患者において、効果は同等でした。平均して、ヘモグロビンは 5 週間以内に増加し、研究の終了 (12 週目) まで 11 ~ 12 g/dl の間で維持されました。 CMF は忍容性が良好でした。患者の 2.4% が吐き気と下痢を報告しました。
したがって、CMFで治療された癌および鉄欠乏性貧血患者のヘモグロビンは、ベースラインのヘモグロビンレベルまたは併用ESA療法に関係なく、11~12 g/dlで安定したままであると結論付けられ、CMFが癌患者の鉄欠乏性貧血の治療に有効であることが示唆された。
ムニョス氏のレビューでは、肥満手術を受ける患者における鉄補給の必要性が示されています。しかし、経口鉄剤治療のアドヒアランスは良好ではありません。さらに、すでに確立された鉄欠乏症では、これらの化合物の経口投与に対する抵抗性が観察されます。このような状況では、鉄の静脈内投与が鉄欠乏性貧血の治療における安全で効果的な代替手段として考えられます。貧血を改善し、貯蔵鉄を補充した後でも、モニタリングは無期限に継続し、必要に応じて鉄の補充を実行する必要があります。カルボキシマルトース第二鉄などの静脈内投与用の新しい鉄剤は安全で使いやすく、1,000 mg の単回投与が可能なため、この患者集団における鉄欠乏症の治療または予防に優れたツールとなります。
要約すると、より迅速かつ高用量で投与できるカルボキシマルトース第二鉄の導入は、静脈内鉄療法に新たな次元をもたらします。慢性腎臓病、産科疾患、化学療法を受けているがん患者、月経過多の女性、炎症性腸疾患(IBD)患者など、さまざまな臨床状況における貧血の病態生理学的メカニズムを理解することで、静脈内鉄剤による治療アプローチが可能になり、貧血の数を減らし、貧血の数を減らすことができます。輸血の量。
薬理学的特徴
薬力学的特性:
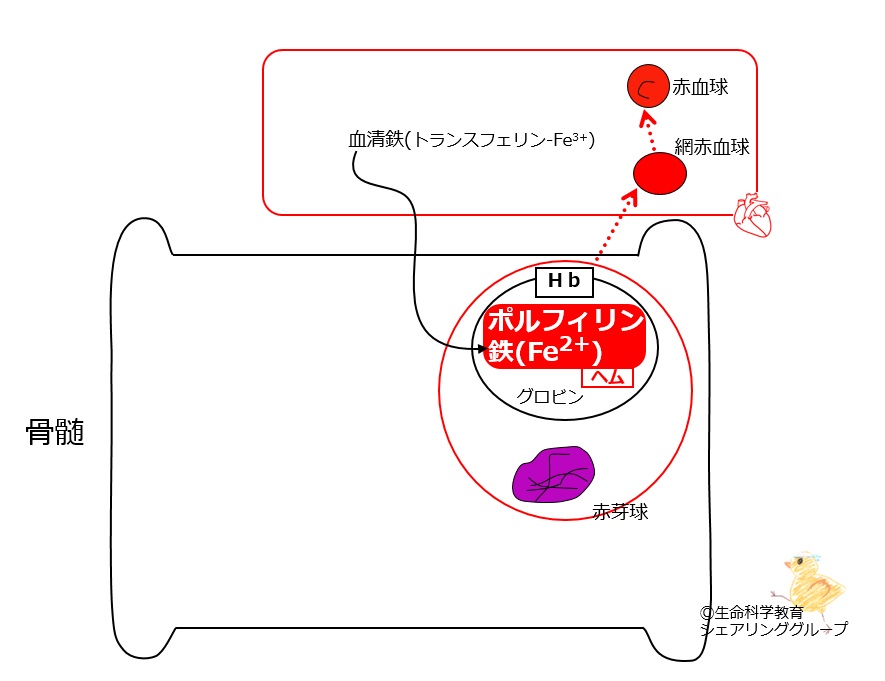
注射・輸液用カルボキシマルトース第二鉄(有効成分)溶液は、炭水化物配位子を有する多核水酸化第二鉄コアを有する非デキストラン鉄錯体の形態で安定な鉄を含むカルボキシマルトース第二鉄のコロイド溶液です。錯体の安定性が高いため、弱く結合した鉄 (不安定鉄または遊離鉄とも呼ばれる) はごく少量しか存在しません。カルボキシマルトース第二鉄のコア構造は、生理学的鉄貯蔵タンパク質であるフェリチンのコア構造に似ています。この複合体は、体内の鉄の輸送とタンパク質の貯蔵(それぞれトランスフェリンとフェリチン)のために、制御された方法で利用可能な鉄を提供することを目的としています。
赤血球による放射性標識カルボキシマルトース第二鉄からの 59Fe 利用率は、投与後 24 日で、鉄欠乏患者では 91% ~ 99%、腎性貧血患者では 61% ~ 84% の範囲でした。鉄欠乏性貧血患者におけるカルボキシマルトース第二鉄(活性物質)による治療は、鉄が利用可能になるにつれて赤血球前駆細胞の成熟が増加したことを示す網赤血球数の明らかな増加を引き起こしました。
血清フェリチンレベルが正常範囲まで上昇すると、貯蔵鉄が補充されたことが確認されます。
臨床研究では、カルボキシマルトース第二鉄 (活性物質) の静脈内投与後の方が、他の薬剤の経口投与よりも速い血液学的反応と貯蔵鉄の置換が実証されています。
薬物動態学的特性
分布:
貧血患者に100~1,000mgの鉄を含むカルボキシマルトース第二鉄を単回投与した後のピーク血清鉄濃度は37~333mcg/mlでした。
中央区画の分布容積は血漿の容積(約 3L)に相当します。
鉄欠乏または鉄欠乏性貧血の患者にボーラス注射として投与されるカルボキシマルトース第二鉄(10%鉄)の静脈内投与の安全性、忍容性、薬物動態および薬力学を評価するために、第1/2相試験も実施されました。患者(n=31)は、10%の鉄を含むカルボキシマルトース第二鉄の製剤(10%カルボキシマルトース第二鉄)を、鉄200〜1,000mgの範囲の用量で、鉄100mg/秒で投与された。分布の平均体積は、血漿の体積に対応して、2.3 ~ 3.2 L の間で変化しました。最終排出半減期は 7.2 ~ 10.5 時間の範囲で、5% 鉄を含むカルボキシマルトース第二鉄製剤 (7 ~ 12 時間) と同様でした。
陽電子放出断層撮影法 (TEP) により、52Fe/59Fe 標識カルボキシマルトース第二鉄からの 52Fe が肝臓、脾臓、骨髄に急速に分布することが実証されました。肝臓と脾臓では約 25 分間の分布段階が観察され、骨髄では最初の 10 分間に急速な吸収が観察され、その後、より遅いが一定の速度でのさらなる流入が観察されました。 52Fe は血液から急速に除去され、観察期間の終了時 (約 8 時間) には、注入された量のほとんどが骨髄に分布しました。赤血球による 59Fe の使用は 61% から 99% の範囲でした。
24 日後、鉄欠乏性貧血患者の 59Fe 利用率は 91% から 99% に上昇し、腎性貧血患者の 59Fe 利用率は 61% から 84% に上昇しました。
代謝:
カルボキシマルトース第二鉄は、主に骨髄、肝臓、脾臓の細網内皮系に保持されます。
消去:
カルボキシマルトース第二鉄に含まれる鉄は血漿から急速に除去されます。ある研究では、終末半減期は 7 ~ 12 時間、平均滞留時間は 11 ~ 17 時間でした。腎鉄除去は有意ではなかった。
前臨床安全性データ:

安全性薬理学、反復投与毒性、生殖毒性および遺伝毒性に関する従来の研究に基づく前臨床データでは、人体に対する特別な危険性は明らかにされていません。前臨床研究では、カルボキシマルトース第二鉄 (活性物質) から放出される鉄が胎盤関門を通過し、限定され制御された量で乳中に排泄されることが示されています。鉄分が豊富な動物を用いた生殖毒性研究では、カルボキシマルトース第二鉄(活性物質)は胎児の軽度の骨格異常と関連していましたが、それは母体毒性を引き起こす用量でのみでした。ラットの生殖能力に関する研究では、生殖能力や交尾能力に影響はありませんでした。カルボキシマルトース第二鉄 (活性物質) の発がん性の可能性を評価するための動物での長期研究は行われていません。
動物データは、カルボキシマルトース第二鉄 (活性物質) が抗デキストラン抗体と交差反応せず、感作の可能性がないことを示しています。カルボキシマルトース第二鉄(活性物質)は、遺伝子変異アッセイ(細菌細胞およびラットリンパ腫細胞のインビトロアッセイ)および染色体損傷(ヒトリンパ球のインビトロアッセイおよびラット小核のインビボアッセイ)において遺伝毒性を示さなかった。
フェリンジェクトのストレージケア
製品は室温(15℃~30℃)で保管してください。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かない場所に保管する必要があります。
Ferinject は開封後、すぐに使用してください。塩化ナトリウム溶液で希釈した後は、直ちに使用してください。
身体的特徴
Ferinject は、静脈内注射/点滴用の溶液として提供され、色は濃い茶色で、透明ではありません。
フェリンジェクトの法律上の格言
MS – 1.0639。 0262
農場。答え:
カーラ・A・インポシナート – CRF-SP番号 38,535
製造元:
ビプソGmbH
ジンゲン – ドイツ
輸入者:
武田薬品工業株式会社
ハイウェイ SP 340 S/N km 133.5 – ジャグアリウナ – SP
CNPJ 60.397.775/0008-40

ブラジルの産業
スイスの Vifor (International), Inc. からのライセンスに基づいて販売されています
医師の処方箋に基づいて販売します。








-1024x576.jpg?resize=1024,576&ssl=1)


