リバビリンはどのように作用しますか?
リバビリン® は、新しいウイルスの形成を防ぐウイルス戦術であると最もよく説明できます。ウイルスの複製を阻害すると、ウイルス感染と戦うための免疫応答が自然に発達します。

リバビリンの禁忌
リバビリン® は以下の場合には禁忌です。
- リバビリンまたはその成分に対するアレルギー(過敏症)。
- 妊娠中の女性。リバビリン®による治療は、治療開始直前に行われた妊娠検査で陰性結果が得られた後にのみ開始してください。
- 授乳中。
- 過去6か月以内の不安定または制御不能な心疾患を含む重篤な心疾患の既往歴。
- 重度の肝機能障害または非代償性肝硬変。
- 重度の腎不全。
- ヘモグロビン症(サラセミア、鎌状赤血球症など)。
- HCV と HIV が重複感染し、肝硬変を患い、Child-Pugh スコアを持つ患者はいますか? 6.
この薬は、妊娠している女性、または治療中に妊娠する可能性のある女性は使用しないでください。
この薬は妊娠中に先天異常を引き起こします。
この薬は重度の腎不全患者への使用は禁忌です。
リバビリンの使い方
大人
C型肝炎の治療で推奨される経口用量は、体重が75kg未満の患者には1日あたり1000mgを2回に分けて、体重が75kgを超える患者には1日あたり1200mgを2回に分けて投与します。治療を中止した後に病気が再発した。
子供たち
1 日の平均用量も分割すると、体重 1 kg あたり 10 mg になります。小児におけるリバビリンの使用については十分な研究が行われていないため、3 歳未満の小児の治療ではリスク/ベネフィット比を考慮する必要があります。これらの子供たちの場合、小児の 1 日あたりの投与量は確立されていませんが、研究によると、体重 1 kg あたり 12 mg に達する可能性があります。
この薬は割ったり、開けたり、噛んだりしないでください。
治療の時間、用量、期間を常に尊重し、医師のアドバイスに従ってください。
医師のアドバイスなしに治療を中止しないでください。
リバビリンの使用を忘れた場合はどうすればよいですか?
決して同時に2回分を服用しないでください。投与を忘れた場合は、医師が決めた間隔を守り、できるだけ早く服用する必要があります。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
リバビリンの注意事項
リバビリン®を服用しないでください。
- リバビリンまたはリバビリン®の他の成分に対してアレルギー (過敏症) がある場合。
- 妊娠中または授乳中の場合。
- 心臓に問題がある場合、または過去 6 か月以内に他の重篤な心臓病にかかっていた場合。
- 重度の肝疾患がある場合(例、皮膚が黄色くなり、過剰な体液が蓄積している)。
- 貧血型の血液疾患(鎌状赤血球やサラセミアなど)がある。
- HIV にも感染しており、重度の肝疾患を患っている場合は、リバビリン®とペグ化インターフェロン アルファ-2a の併用による治療を開始すべきでない場合があります。医師は評価のために通知を受ける必要があります。
詳細については、ペグ化インターフェロン アルファ-2a またはインターフェロン アルファ-2a のリーフレットも参照してください。
医師に次のように伝えてください。
- あなたが出産適齢期の女性の場合。
- あなたが男性患者で、パートナーが出産適齢期の場合。
- 心臓に問題がある場合。この場合は、注意深く監視する必要があります。治療前および治療中に心電図検査を受けることをお勧めします。
- 極度の疲労を伴う心臓の問題がある場合。これは薬の使用によって引き起こされる貧血が原因である可能性があります。
- これまでに貧血を患ったことがある(一般に、貧血を発症するリスクは男性よりも女性の方が高い)。
- C型肝炎以外の肝臓疾患がある場合。
- 腎臓に問題がある場合。リバビリン®の用量を減らすか、治療を一時停止する必要がある場合もあります。
- 呼吸困難、息切れ、皮膚や粘膜の突然の腫れ、かゆみ、発疹などのアレルギー反応の症状が現れた場合は、リバビリン®による治療を直ちに中止し、直ちに医師の診察を受けてください。
- リバビリン®による治療中にうつ病を患ったことがある、またはうつ病に関連する症状(悲しみ、失望など)を発症したことがある。
- HIV にも感染しており、エイズの治療を受けている場合。
- 貧血または血球数の低下により、以前のC型肝炎治療を中止した場合。
治療を開始する前に、すべての患者は腎機能検査を受けなければなりません。医師は、リバビリン®による治療を開始する前に血液検査を行います。血液検査は、治療の 2 週間後と 4 週間の間、さらにその後は医師が必要と判断したときに繰り返し行う必要があります。
あなたが出産可能年齢の女性の場合は、治療を開始する前に妊娠検査を受けてください。検査は治療中は毎月、治療終了後は 4 か月間繰り返す必要があります。
リバビリン®およびペグ化インターフェロン アルファ-2a による治療を受けた患者では、歯の喪失を引き起こす可能性がある歯と歯肉の疾患が報告されています。さらに、リバビリン®とペグ化αインターフェロン-2a の組み合わせによる長期治療では、口渇により歯や口の中の皮膚 (口腔粘膜) が損傷する可能性があります。 1日2回徹底的に歯を磨き、定期的に歯科検診を受ける必要があります。
患者によっては、嘔吐が起こることもあります。この反応が起こった場合は、嘔吐した後は必ず口をよく洗ってください。
この薬には乳糖が含まれています。
リバビリンの副作用

すべての薬と同様に、リバビリン® も副作用を引き起こす可能性がありますが、すべての人が副作用を経験するわけではありません。
一部の患者は、リバビリン®治療とインターフェロン アルファの併用によりうつ病になり、場合によっては、自殺願望や攻撃的行動 (時には他の人に対して) を起こします。自殺した患者もいた。うつ病になりやすい、自殺願望がある、または行動が変化していることに気付いた場合は、緊急治療を受けてください。
家族や親しい友人に、うつ病の初期の兆候や行動の変化に注意を払うよう手伝ってもらいましょう。
治療中、医師は定期的に血液検査を実施して、白血球(感染症と戦う細胞)、赤血球(酸素を運ぶ細胞)、血小板(感染症を引き起こす細胞)に変化がないかどうかを確認するように指示します。血液凝固)、肝機能、または他の検査値の変化。
以下の副作用に気づいた場合は、すぐに医師に相談してください。
激しい胸痛;持続的な咳、不規則な心拍、呼吸困難。混乱、憂鬱、重度の腹痛、血便(または黒色のタール便)、重度の鼻血、発熱または悪寒。視力の問題。これらの事象は、ペグ化インターフェロン アルファ-2a またはインターフェロン アルファ-2a に関連するリバビリン®を投与した場合に発生する可能性があります。これらの有害事象は重篤であり、患者は緊急の医療援助を必要とする場合があります。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。また、顧客サービスを通じて会社に通知してください。
リバビリンの組成
各カプセルには次のものが含まれています。
|
リバビリン |
250mg |
|
適量の賦形剤 |
1カプセル |
賦形剤:
ポビドン、デンプングリコール酸ナトリウム、乳糖、ステアリン酸マグネシウム。
リバビリンの紹介
250mgのリバビリンを含むカプセル。 60カプセル入りのボトルが入ったパッケージ。
投与経路: 経口使用。
成人および小児用。
リバビリンの過剰摂取
ヒトにおけるリバビリンの過剰摂取は報告されていません。ラットの経口 LD50 は 2 g で、活動低下および胃腸症状と関連しています (推定ヒト等価用量は体表面積に基づいて 0.17 g/kg です)。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
リバビリンの薬物相互作用
HIV 重複感染のある患者: HIV の治療を受けているかどうかを医師に伝えてください。
乳酸アシドーシス(体内に乳酸が蓄積し、血液が酸性になること)と肝機能の悪化は、HIV治療法であるHAART(効果の高い抗レトロウイルス療法)に伴う副作用です。リバビリン®とペグ化インターフェロン アルファ-2a またはインターフェロン アルファ 2a の組み合わせである HAART を受けている場合、乳酸アシドーシスおよび肝機能障害のリスクが増加する可能性があります。医師はこれらの副作用の兆候や症状を監視します。
HIV 感染またはエイズを患っているためにジドブジンまたはスタブジンを服用している場合、リバビリン® がこれらの薬剤の効果を低下させる可能性があります。したがって、HIV 感染が悪化しないように定期的に血液検査を実施してください。このようなことが起こった場合、医師はリバビリン®による治療を中止することを決定する場合があります。さらに、ジドブジンをリバビリン® およびインターフェロン アルファと組み合わせて投与されている患者は、貧血を発症するリスクが高くなる可能性があります。
リバビリン®とジダノシン (エイズ治療薬) の同時投与は推奨されません。
ジダノシンの一部の副作用(肝臓の問題、腕や足の痛みやうずき、膵炎など)がより頻繁に発生する可能性があります。

リバビリンは体内に 2 か月間残留する可能性があるため、この説明書に記載されている他の薬による治療を開始する前に医師または薬剤師に知らせてください。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
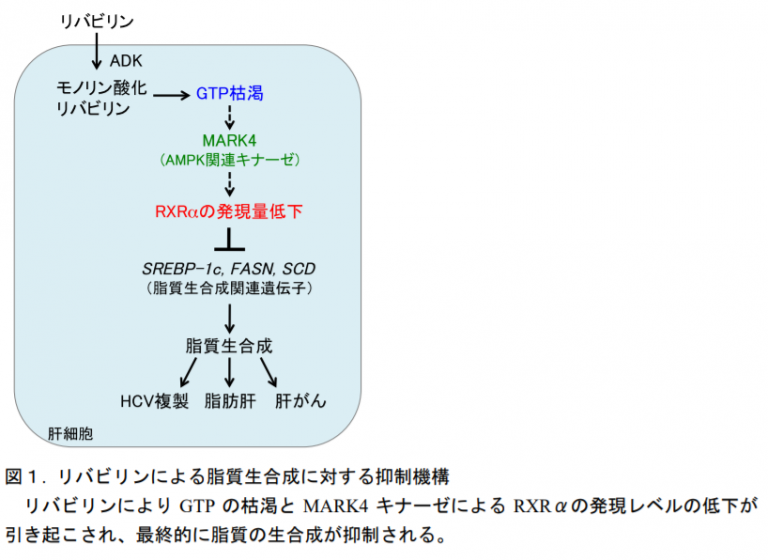
リバビリンという物質の作用
効果の結果
1998年に、1744人の患者を対象とした2件の臨床試験が発表され、αインターフェロン1単独療法よりもαインターフェロンとリバビリンの併用療法の最大の利点が示され、遺伝子型1および遺伝子型非遺伝子型の患者の48週間の治療でより大きな利点が示された。 1 回 24 週間。この行為は後に 1999 年に開催されたパリ国際合意によって承認されました。
別の研究は、ペグ化インターフェロン アルファと関連するリバビリンの最適な用量と、最も適切な治療時間を確立することを目的として実施されました。 4つのグループが治療を受け、1つのグループはペグ化インターフェロン アルファとリバビリン 800 mgを24週間組み合わせ、1つのグループはペグ化インターフェロン アルファとリバビリン 1000~1200 mgを24週間組み合わせ、別のグループはペグ化インターフェロン アルファとリバビリン 800 mgを48週間使用し、4番目のグループはペグ化インターフェロン アルファとリバビリン 800 mgを24週間組み合わせました。ペグ化インターフェロンとリバビリン 1000 ~ 1200 mg を 48 週間投与したグループ。この研究では、1型遺伝子型の患者については、48週間の治療を行ったグループが24週間の治療よりも統計的に優れており、標準用量のリバビリンが低用量のリバビリンよりも統計的に優れていることが示された。 2 型および 3 型の遺伝子型を持つ患者では、治療グループ 4 のウイルス反応の割合は統計的に有意な差を示さなかった。したがって、ペグ化インターフェロン アルファおよびリバビリンによる治療は遺伝子型によって個別化されます。遺伝子型 1 の HCV 患者は 48 週間の治療と標準用量のリバビリンが必要です。遺伝子型2型および3型の患者は、ペグ化インターフェロンアルファと低用量のリバビリンを24週間投与することで十分に治療できます。
薬理的特性
リバビリンは急速に吸収され、組織内に広く分布し、主に代謝されて主に尿中に排泄されます。
リバビリンを用いたヒト臨床試験では、一般的なウイルス感染症の制御におけるその有効性と安全性が証明されています。リバビリンは経口投与によって急速に吸収され、薬物の血漿中濃度のピークは投与後 1 ~ 2 時間以内に生じ、主に尿中に排泄されます。腎機能が正常な健康な成人では、単回経口投与量の約 53% が 72 ~ 80 時間以内に尿中に排泄され、約 33% が最初の 24 時間以内に排泄されます。 1 回の経口投与量の約 15% が 72 時間以内に糞便中に排泄されます。
男性、ラット、アカゲザルでは、赤血球におけるリバビリンおよび/またはその代謝産物の蓄積が認められています。男性では赤血球のプラトーが 4 日以内に観察され、見かけの半減期 40 日 (赤血球の半減期) で徐々に減少します。
リバビリンの保管管理
室温15℃~30℃で保管してください。湿気から保護されています。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。
薬の特徴
リバビリン® は、白色の結晶性粉末を含む薄緑色/濃緑色のカプセルの形で提供されます。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かないところに保管してください。
リバビリンの法的声明
登録MS。 1.1637.0030
農場。答え:
イライザ 斉藤幸恵
CRF-SP No.10,878
製造元:
ブラウ ファーマセウティカ SA
CNPJ 58.430.828/0002-40
Av. イヴォ・マリオ・アイザック・ピレス、7602
CEP 06720-480 – コチア – SP
ブラジルの産業
登録者:
ブラウ ファーマセウティカ SA
CNPJ No.58.430.828/0001-60
ロッド・ラポソ・タバレス 30.5 km no.
CEP 06705-030 – コチア – SP
ブラジルの産業
医師の処方箋に基づいて販売します。
処方箋が必要な場合のみ販売可能です。








-1024x576.jpg?resize=1024,576&ssl=1)


