ファーマゴンはどのように機能しますか?
Firmagon ® には、前立腺がんの治療に使用されるテストステロン生成をブロックする合成ホルモンであるデガレリクスが含まれています。デガレリクスは、天然ホルモン (ゴナドトロピン放出ホルモン、GnRH) を模倣し、その効果を直接ブロックします。その結果、デガレリクスは前立腺がんを刺激する男性ホルモンのテストステロンのレベルを即座に低下させます。

Firmagon ®の作用が始まるまでの平均時間は 2 ~ 4 時間ですが、この期間中にすでにテストステロン レベルが低下しているためです。テストステロン濃度が最低になるのは、Firmagon ®投与後約 24 ~ 36 時間です。
フィルマゴンの禁忌

次の質問の答えが「はい」の場合は、Firmagon ®を使用しないでください。
フォーミュラの成分に対して過敏症 (アレルギー反応) があることがわかっていますか?

この薬は小児による使用は禁忌です。
この薬は女性の使用は禁忌です。

この薬は、妊娠している女性、または治療中に妊娠する可能性のある女性は使用しないでください。
フィルマゴンの使い方

この薬は通常、薬剤師、看護師、または医師によって投与されます。
Firmagon ® は皮膚の下にのみ注射する必要があります (皮下投与)。 Firmagon ® は静脈から投与してはなりません (静脈内投与)。静脈への誤った注射を避けるために予防措置を講じる必要があります。注射部位は腹部内で変える必要があります。
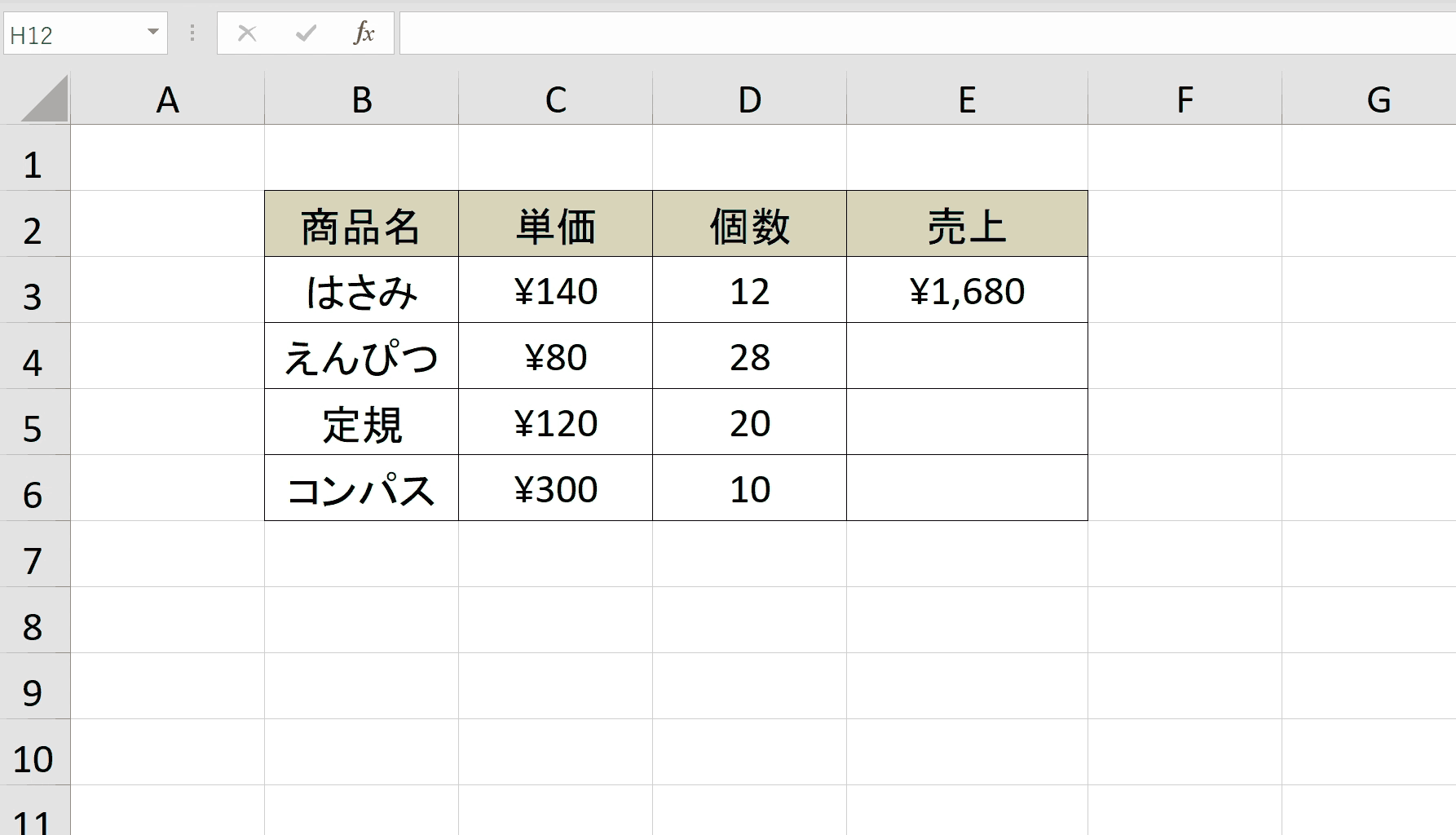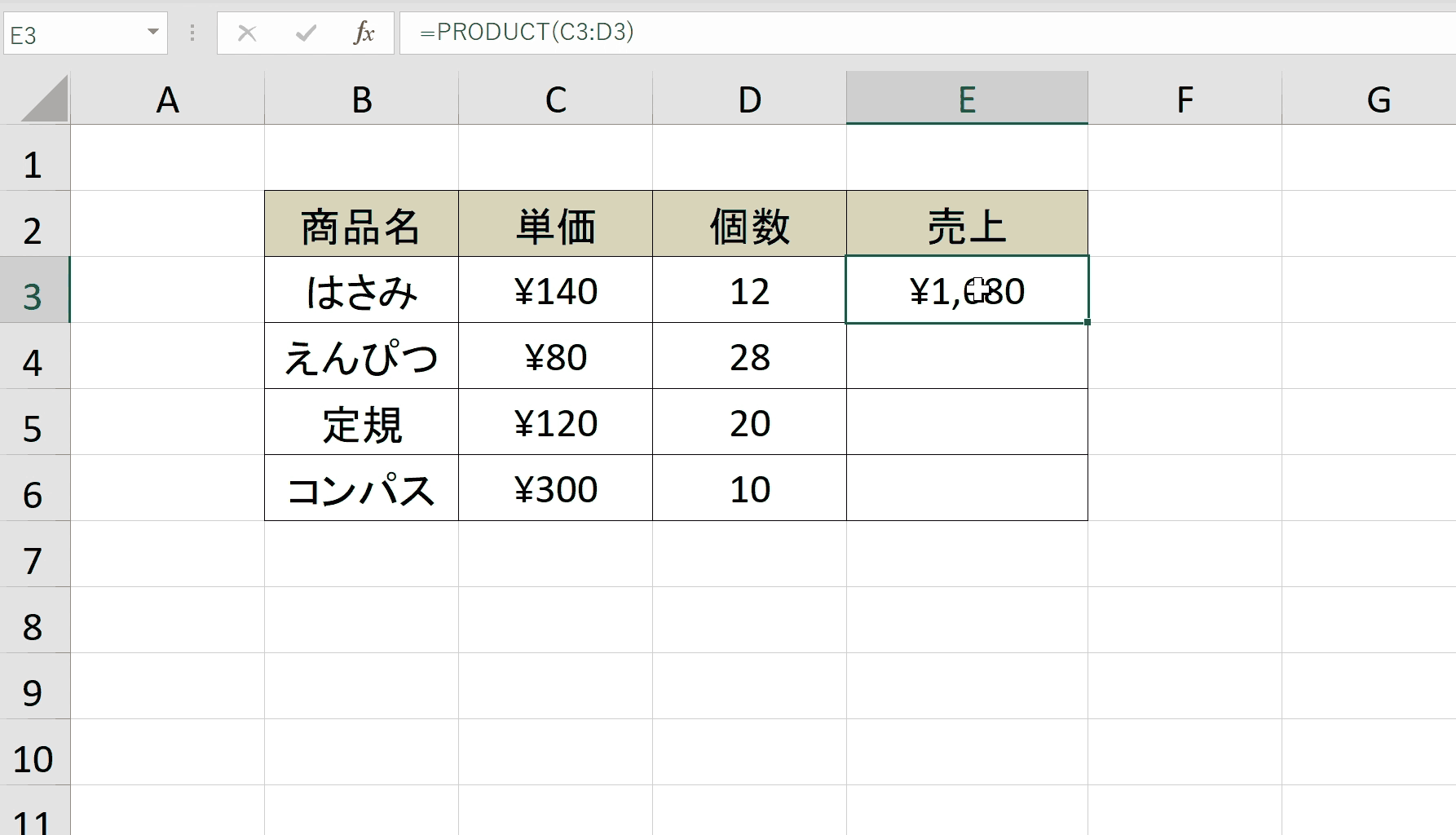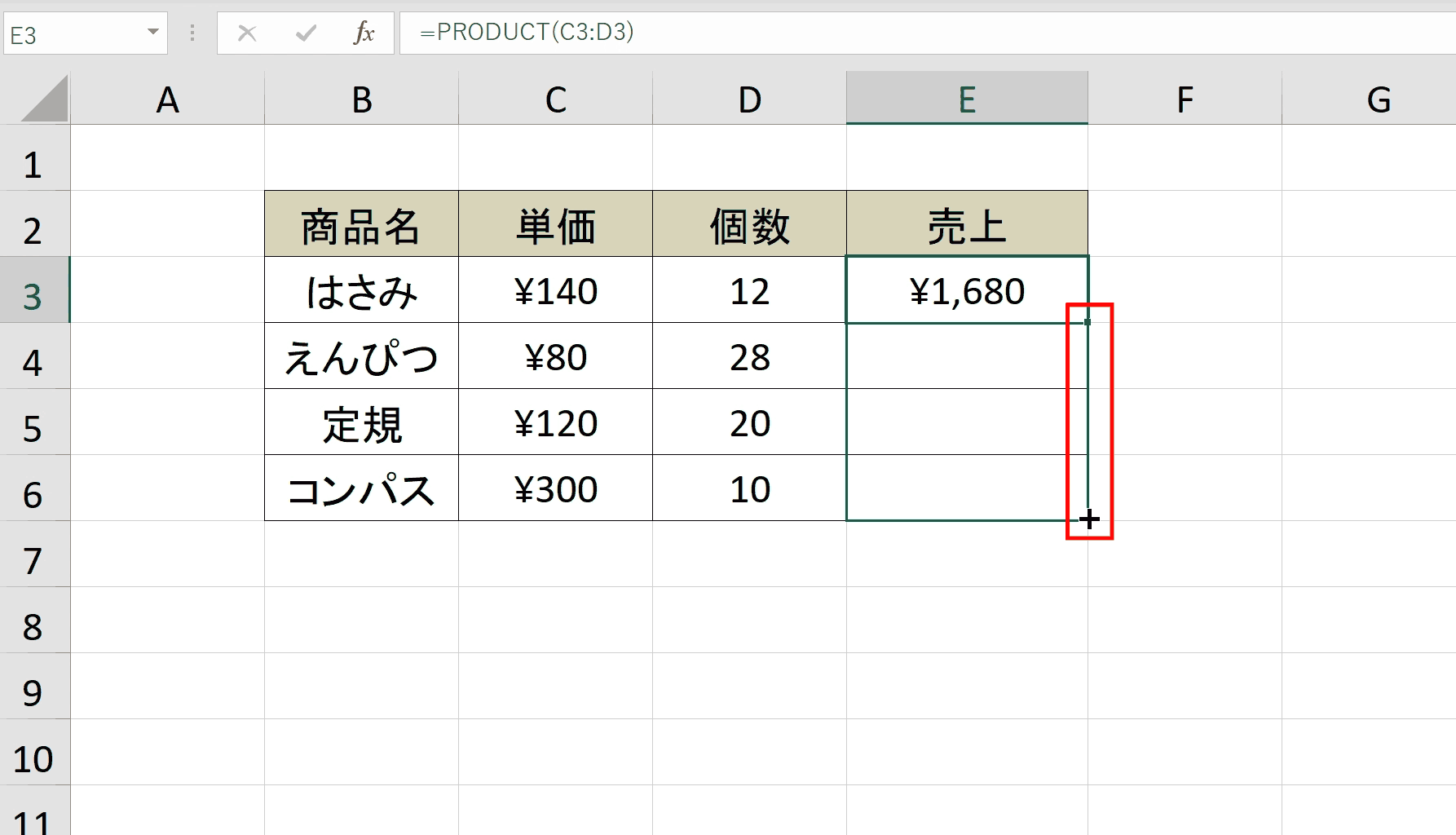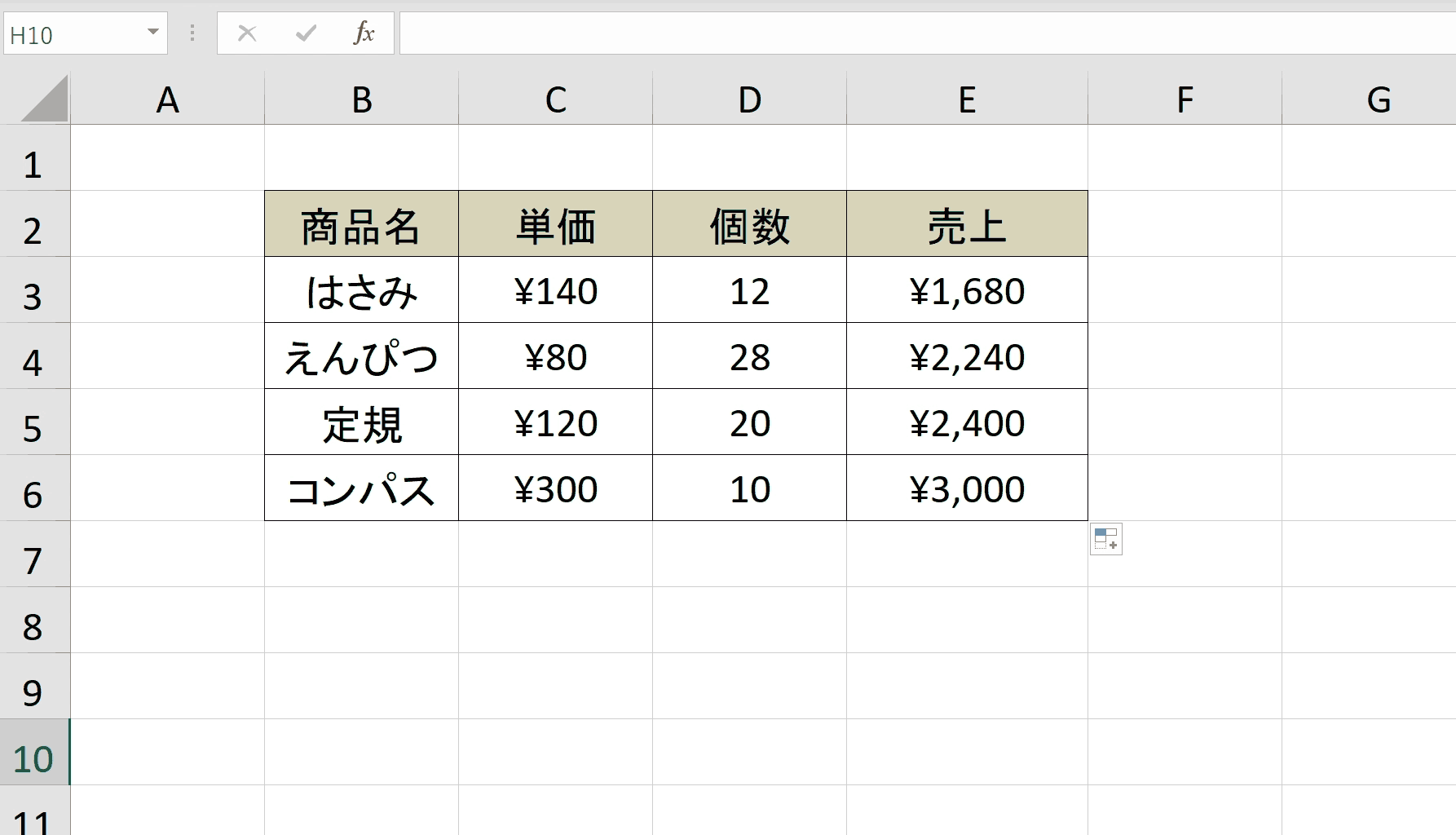
注射は、患者が圧力にさらされない領域に投与する必要があります。つまり、ベルトが使用されている領域、ズボンのボタンが留められている領域、または肋骨に近い領域には投与しないでください。
準備方法

再構成の指示には注意深く従う必要があります。
観察:

ボトルを振ってはいけません。
溶解後は直ちに使用してください。
Firmagon ® 120 mg パッケージには、皮下注射用に別々に調製する必要がある粉末と希釈剤の 2 セットが含まれています。したがって、以下の手順をもう一度繰り返す必要があります。
- バイアルアダプターからパッケージを取り外します。ゴム栓が壊れてアダプターが固定されるまでアダプターを下に押して、アダプターを粉末バイアルに挿入します。
- プランジャーを挿入して希釈剤シリンジを準備します。
- シリンジのキャップを取り外します。シリンジを粉末バイアルアダプターに接続し、ひねります。すべての希釈液を粉末ボトルに移します。
- シリンジをアダプターに接続した状態で、液体が透明になり、粉末や未溶解の粒子がなくなるまで穏やかに旋回させます。粉末が液面より上のボトルに付着している場合は、ボトルをわずかに傾けることができます。泡の形成を防ぐため、振盪を避けてください。
液体の表面に小さな気泡の輪があっても許容されます。再構成手順には通常数分かかりますが、最大 15 分かかる場合もあります。
- ボトルを逆さまにし、注射器の線の位置まで溶液を抜きます。
フィルマゴン® 120mg用
注射器で溶液 3.0 mL を抜き取ります。
フィルマゴン® 80mg用
注射器で溶液 4.0 mL を抜き取ります。
常に正確な量が取り出されていることを確認し、気泡の存在に注意してください。
- 皮下深く投与する場合は、バイアルアダプターからシリンジを取り外し、安全針を接続します。
溶解後は直ちに製品を投与してください。
- この製品は皮下深部注射によって投与する必要があります。腹部の皮膚を引き締め、皮下組織を持ち上げます。針は45度までの角度で深く刺してください。
ファーマゴン® 120 mg の場合:
溶液を 3.0 mL 注入します。
ファーマゴン® 80 mg の場合:
溶液を 4.0 mL 注入します。
- Firmagon 120 mg: 2 回目の用量でも再溶解手順を繰り返します。別の注射部位を選択し、3.0 mL を注射します。
再溶解は、パッケージに同梱されている希釈液を使用して行う必要があります。
Firmagon® 120 mg とともに投与される再構成溶液の最終容量は 3.0 mL で、再構成後、各 mL には 40 mg のデガレリクスが含まれます。
Firmagon® 80 mg とともに投与される再構成溶液の最終容量は 4.0 mL で、再構成後、各 mL には 20 mg のデガレリクスが含まれます。
フィルマゴンの投与量
Firmagon ® は皮下投与する必要があります。
|
開始用量 |
維持用量 – 毎月の投与 |
|
240 mgを各120 mgの皮下注射2回として投与 |
80mgを皮下注射として投与 |
最初の維持用量は、初回投与から 1 か月後に投与する必要があります。
液体を注射すると体内でゲルが形成され、1 か月間継続的にデガレリクスが放出されます。
医師は、臨床パラメータと前立腺特異抗原(PSA)の血中濃度をモニタリングすることにより、デガレリクスの治療効果を評価します。臨床研究では、初回用量の投与直後にテストステロン (T) の抑制が起こり、3 日後には患者の 96% が医学的去勢 (T ≧ 0.5 ng/mL) に相当するテストステロン レベルを示し、1 か月後には 100% になることが実証されています。維持用量で最長1年間の長期治療により、患者の97%が抑制されたテストステロンレベル(T≧0.5ng/mL)を維持していることが実証されています。
患者の臨床反応が最適ではないように見える場合は、血清テストステロンレベルが十分に抑制されたままであるかどうかを確認する必要があります。
デガレリクスはテストステロンの増加を誘導しないため、治療開始時に増加に対する保護として抗アンドロゲン剤を追加する必要はありません。
Firmagon ® は毎月投与する必要がある薬です。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。医師の知識なしに治療を中止しないでください。
Firmagon の使用を忘れた場合はどうすればよいですか?
投与を忘れた場合は医師に相談してください。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
ファーマゴンの注意事項
以下の問題がある場合は、医師に相談してください。
- 心臓のリズムに問題がある(不整脈)、またはこの症状に対して薬で治療を受けている。 Firmagon ®の使用により、心拍リズムの問題のリスクが増加する可能性があります。
- 糖尿病。糖尿病は悪化または再発する可能性があるため、糖尿病がある場合は、血糖値をより頻繁に監視する必要があります。
Firmagon ®の使用により、次の状態が発生する可能性があります。
過敏症
Firmagon ® は、未治療の重度の喘息、アナフィラキシー反応(重度のアレルギー反応)、または重度の蕁麻疹または血管浮腫(主に唇と目の領域の皮下の腫れ)の病歴のある患者を対象とした研究は行われていません。
骨密度の変化
医学文献では、睾丸摘出術(睾丸の外科的除去)を受けた男性、またはGnRH(ゴナドトロピン放出ホルモン)アゴニストによる治療を受けた男性の骨密度が低下した症例が報告されています。男性のテストステロン抑制剤による長期治療は骨密度に影響を与えると言えます。デガレリクスによる治療中に骨密度は評価されませんでした。研究が不足しているため、デガレリクスによる治療中の骨折のリスクは不明です。
QT間隔(心電図検査で観察される特定の間隔)の延長
長期のアンドロゲン抑制療法により、QT 間隔が延長される可能性があります。 Firmagon ® は、QT 間隔が 450 ミリ秒を超える修正歴のある患者、 「トルサード ド ポワント」 (QT または QTU 間隔の延長を伴う心室心拍数の加速)の既往歴がある、またはその危険因子を示す患者では研究されていません。 QT間隔を延長する可能性のある他の薬剤による治療を受けている患者。したがって、これらの患者では、医師はFirmagon ®による治療のリスク/ベネフィット比を評価します。
耐糖能: 耐糖能の低下は、精巣摘出術 (睾丸の外科的除去) を受けた男性、または GnRH (ゴナドトロピン放出ホルモン) アゴニストによる治療を受けた男性で観察されています。糖尿病の発症または悪化が起こる可能性があります。したがって、糖尿病患者はアンドロゲン除去療法を受ける場合、より頻繁な血糖モニタリングが必要になる可能性があります。インスリンおよび血糖値に対するデガレリクスの影響は研究されていません。
特殊な人々に対する注意と警告
研究によると、軽度から中等度の腎障害のある患者では、体がデガレリクスを排出する速度が約 20 ~ 30% 低下することが示されています。したがって、これらの患者における用量調整は推奨されません。重度の腎障害のある患者に関するデータは不足しているため、この患者集団については注意することが賢明です。重度の肝機能障害のある患者は研究されていないため、医師はこのグループには注意する必要があります。
車両の運転や機械の操作能力への影響
Firmagon ®については、車両の運転や機械の操作能力に影響があるかどうかを評価する研究は行われていません。ただし、倦怠感やめまいは治療に伴う、または病気に起因する一般的な副作用であるため、車両の運転や機械の操作能力に影響を与える可能性があります。
フィルマゴンの副作用
デガレリクス治療中に最も一般的に観察された副作用は、顔面紅潮や体重増加(1年間治療を受けた患者のそれぞれ25%と7%で報告)などのテストステロン抑制による予想される生理学的影響、または治療期間中の有害事象によるものでした。注射部位。
報告された注射部位の有害事象は主に痛みと紅斑で、それぞれ患者の28%と17%で報告され、頻度は低いが腫れ(6%)、硬結(4%)、結節(3%)であった。これらの事象は主に初回用量で発生しましたが、80 mg の用量での維持療法中、注射 100 回あたりのこれらの事象の発生率は、痛みが 3 件、紅斑、腫れ、結節、硬直が 1 件でした。報告されたイベントはほとんどが一時的なもので、軽度から中等度の強度であり、中止に至ったケースはほとんどありませんでした (<1%)。注射部位での感染、膿瘍、壊死など、外科的処置やドレナージを必要とする重篤な反応は、ほとんど報告されていません。
以下にリストされる望ましくない影響の頻度は、次の規則を使用して定義されます。
非常に一般的 (? 1/10)。共通 (?1/100 ~ lt;1/10);非一般的 (?1/1,000 ~ lt; 1/100)。各周波数グループ内で、望ましくない影響が深刻度の低い順に示されます。
|
非常に一般的 (? 1/10) |
一般的 (?1/100 および <1/10) |
非コモンズ (?1/1,000 ~ lt; 1/100) |
|
リンパ系および血液系の疾患 |
||
| – | – |
ヘモグロビンを減らす |
|
免疫系疾患 |
||
| – | – |
過敏症 |
|
精神障害 |
||
| – | 不眠症 |
性欲の喪失 |
|
神経系疾患 |
||
| – |
めまい、頭痛 |
– |
|
血管障害 |
||
|
赤面 |
– |
高血圧 |
|
胃腸疾患 |
||
| – | 吐き気、便秘 |
下痢 |
|
肝胆道疾患 |
||
| – | 肝臓のトランスアミナーゼの増加 | – |
|
皮膚および皮下の疾患 |
||
| – | 寝汗 |
蕁麻疹、多汗症、皮膚の色素沈着過剰 |
|
生殖器系と乳房の疾患 |
||
| – | – |
勃起不全、精巣萎縮、女性化乳房 |
|
投与部位の一般的な障害および症状 |
||
|
投与現場での有害事象 |
悪寒、発熱、無力症、倦怠感 |
「インフルエンザのような」症状 |
|
調査 |
||
| – | 体重増加* |
– |
注意: この製品は新薬であり、研究により許容できる有効性と安全性が示されていますが、たとえ正しく指示され使用されたとしても、予測できないまたは未知の有害事象が発生する可能性があります。この場合は医師または歯科医師に知らせてください。
フィルマゴン特別集団
肝臓や腎臓に障害のある高齢患者
高齢者や軽度または中等度の肝臓(肝臓)機能または腎臓(腎臓)機能障害のある患者の場合は、用量を調整する必要はありません。重度の肝障害または腎障害のある患者は研究されていないため、製品を使用する場合は注意が必要です。
肝障害が疑われる、または確認された患者は、デガレリクスの研究には含まれていませんでした。医師は、Firmagon ®による治療中にこれらの患者の肝機能を監視することをお勧めします。
フィルマゴンの構成
120 mg 凍結乾燥粉末の各バイアルには次のものが含まれています。
デガレリクス128mg*。
賦形剤:
マンニトール
*製品の調製および投与中の損失を考慮して、正しい量を確実に投与するために過剰な有効成分が添加されています。
80 mg 凍結乾燥粉末の各バイアルには次のものが含まれています。
デガレリクス88.2mg*。
賦形剤:
マンニトール
*製品の調製および投与中の損失を考慮して、正しい量を確実に投与するために過剰な有効成分が添加されています。
希釈液が入った各シリンジには次のものが含まれています。
注射用水
フィルマゴンのプレゼンテーション
フィルマゴン® 120mg
デガレリックス酢酸塩 120 mg の注射用溶液は、凍結乾燥粉末のバイアル 2 本、希釈剤 3.0 mL を含むシリンジ 2 本、バイアルアダプター 2 個、注射針 2 本、およびプランジャー 2 個が入ったパックで入手可能です。
フィルマゴン® 80mg
酢酸デガレリックス 80 mg の注射用溶液は、凍結乾燥粉末のバイアル 1 個、希釈剤 4.2 mL を含むシリンジ 1 個、バイアルアダプター 1 個、注射針 1 個およびプランジャー 1 個を含むパッケージで入手可能です。
皮下使用。
大人用。
フィルマゴンの過剰摂取
他の濃度での投与は、ゲル沈着物(「デポー」製剤)が形成されるため推奨されません。
医師が処方した量を超える量を投与した場合は、すぐに医師に連絡してください。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
フィルマゴンの薬物相互作用
Firmagon ® は、心拍リズムの問題の治療に使用される一部の薬剤 (例: キニジン、プロカインアミド、アミオダロン、ソタロール) または心拍リズムに影響を与えるその他の薬剤 (例: メサドン、シサプリド、モキシフロキサシン、抗精神病薬) を妨げる可能性があります。
食べ物とアルコールとの相互作用
現在までのところ、Firmagon ®と食物およびアルコールの干渉に関するデータはありません。
臨床検査および非臨床検査の変化
Firmagon ®による治療は、下垂体性腺系 (下垂体および睾丸) を抑制します。 Firmagon ®による治療中および治療後に、下垂体 (下垂体) および生殖腺 (睾丸) 機能検査の結果が変化する可能性があります。
治療前に正常値だった患者では、次のような変化が観察されます。
- 肝酵素(肝トランスアミナーゼ – ALT、AST、GGT)の著しく異常な値。
- 血液学的値、ヘマトクリットおよびヘモグロビン(血液検査結果)の顕著な減少。
- カリウム、クレアチニン、尿素(尿検査に含まれる物質)の値が著しく異常。
- 心電図測定値の変化 (QT 間隔の延長 – 心臓検査で観察される特定の間隔)。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
フィルマゴンのフードインタラクション
現在までのところ、酢酸デガレリックス (活性物質) と食品およびアルコールの干渉に関するデータはありません。
物質フィルマゴンの作用
効果の結果
デガレリクスの有効性と安全性は、非盲検、多施設共同、無作為化、実薬対照、並行群間試験で評価されました。この研究では、デガレリクスの初回用量 240 mg (40 mg/mL) に続いて毎月 160 mg (40 mg/mL) または 80 mg (20 mg/mL) の用量を皮下投与する 2 つの月次投与計画の有効性と安全性が調査されました。 ) mL)、アンドロゲン枯渇の適応がある前立腺がん患者におけるリュープロレリン 7.5 mg の筋肉内投与と比較。合計 620 人の患者が 3 つの治療グループのいずれかに無作為に割り付けられ、そのうち 504 人 (81%) の患者が研究を完了しました。
デガレリクス 240/80 治療群では 41 人(20%)の患者が研究を中止したが、リュープロレリン群では 32 人(16%)の患者が研究を中止した。治療を受けた患者のうち:
- 31%は限局性前立腺がんを患っていた。
- 29%は局所進行性前立腺がんを患っていた。
- 20%は転移性前立腺がんを患っていた。
- 7%は未知の転移性疾患を持っていました。
- 13%は以前に治癒目的の手術または放射線治療を受けており、PSAが上昇していた。
ベースラインの人口統計は研究群間で同様でした。主な目的は、デガレリクスが 12 か月の治療期間中にテストステロン抑制を 0.5 ng/mL 以下に達成および維持するのに効果的であることを実証することでした。
最低有効維持用量のデガレリクス 80 mg が選択されました。
血清テストステロン(T)の抑制? 0.5ng/mL
デガレリックス酢酸塩(有効成分)は、テストステロンを迅速に抑制するのに効果的です。
T?を獲得した患者の割合治療開始後0.5ng/mL:
|
時間 |
デガレリクス 240/80mg |
リュープロレリン7.5mg |
|
1日目 |
52% |
0% |
|
3日目 |
99% |
0% |
|
7日目 |
99% |
0% |
|
14日目 |
100% |
18% |
|
28日目 |
100% |
100% |
テストステロンの増加を防ぐ
デガレリックス酢酸塩 (活性物質) で治療された患者の中で、テストステロンの増加を経験した患者はいませんでした。 3日目にはテストステロン値が平均94%減少しました。
リュープロレリンで治療された患者の大部分は、テストステロンの増加を経験しました。 3 日目にはテストステロンが平均 65% 増加しました。テストステロンの増加は、最初の 2 週間以内にベースラインのテストステロン レベルを 15% 以上上回るものとして定義されました。この差は統計的に有意でした (p lt; 0.001)
0日目から28日目までのテストステロンの変化の割合。
図 1: 治療グループごとのベースラインから 28 日目までのテストステロンの変化率 (四分位間の範囲の平均):
テストステロンの可逆性
局所療法(主に前立腺切除術と放射線)後にPSAが増加した患者を対象とした研究では、酢酸デガレリックス(活性物質)が7か月間投与され、その後7か月間モニタリングされました。治療中止後のテストステロン回復期間の中央値(gt;0.5 ng/mL、去勢レベル以上)は112日でした(モニタリング期間の開始日、つまり最後の注射投与後28日から数えます)。濃度が 1.5 ng/mL (正常なテストステロン濃度の下限値を超える) を超えるまでの平均時間は 168 日でした。
長期的な効果
この研究における奏効は、28日目に医学的去勢を達成し、364日目まで維持し、テストステロン濃度が0.5ng/mlを超えないことと定義された。
28 日目から 364 日目までのテストステロンの累積確率 -0.5 ng/mL:
|
デガレリックス酢酸塩(有効成分) 240/80 mg N=207 |
リュープロレリン 7.5 mg N=201 |
|
|
反応のある患者の数 |
202 | 194 |
|
応答率 (信頼区間)* |
97.2% (93.5; 98.8%) |
96.4% |
※カプラン・マイヤーはグループ内で推定。
前立腺特異抗原(PSA)の減少
臨床研究プログラム中に腫瘍サイズは直接測定されませんでしたが、酢酸デガレリックスの 12 か月後の平均 PSA の 95% 減少によって実証されるように、間接的な有益な腫瘍反応が存在しました。
この研究における平均ベースライン PSA は次のとおりです。
- デガレリクス 240/80 mg 治療群の場合、19.8 ng/mL (四分位範囲: P25 9.4 ng/mL、P75 46.4 ng/mL)。
- リュープロレリン 7.5 mg 治療グループの場合、17.4 ng/mL (四分位範囲: P25 8.4 ng/mL、P75 56.5 ng/mL)。
図 2: 治療グループごとのベースラインから 56 日目までの PSA の変化率 (四分位間の範囲の平均):
この差は、14 日目と 28 日目の事前に指定された分析では統計的に有意でした (plt;0.001)。
前立腺特異抗原(PSA)レベルは、デガレリクス投与後 2 週間で 64%、1 か月後に 85%、3 か月後に 95% 減少し、1 年間の治療を通じて抑制されたまま(約 97%)に維持されました。
56 日目から 364 日目まで、ベースラインからの変化率において、酢酸デガレリックス (活性物質) と比較対照薬との間に有意差はありませんでした。
前立腺の容積に対する影響
3ヶ月間のデガレリクス療法(240/80mg用量レジメン)により、放射線療法前にホルモン療法を必要とした患者、または薬理学的去勢の候補である患者において、経直腸的超音波(TRUS)で測定した前立腺容積が37%減少した。前立腺容積の減少は、抗アンドロゲン保護を備えたゴセレリンで得られたものと同様でした。
QT/QTc間隔への影響
デガレリックス酢酸塩(活性物質)とリュープロレリンを比較する確認研究では、定期的な心電図が実施されました。どちらの治療法でも、患者の約 20% で QT/QTc 間隔が 450 ミリ秒を超えました。ベースラインから研究終了まで、酢酸デガレリックス(活性物質)の平均変化は 12.3 ミリ秒(3.2%)、リュープロレリンの場合は 16.7 ミリ秒(3.5%)でした。
QT間隔の詳細な研究により、QT/QTc間隔に対するデガレリクスの本質的な影響はないことが実証されました。心臓再分極 (QTcF)、心拍数、房室伝導、心臓脱分極、T 波または U 波に対するデガレリクスの本質的な効果の欠如が、デガレリクスの 60 分間の静脈内注入を受けた健康な男性 (N=80) で確認され、平均C maxは222 ng/mLで、前立腺がん治療中に得られるC max の約3~4倍です。
抗デガレリクス抗体
抗デガレリックス抗体の発現は、酢酸デガレリックス(活性物質)による 1 年間の治療後に患者の 10% で観察され、酢酸デガレリックス(活性物質)による 5.5 年間の治療後には患者の 29% で観察されました。デガレリックス酢酸塩 (活性物質) による治療の有効性または安全性が、5.5 年間の治療後の抗体形成によって影響を受けるという兆候はありません。
薬理学的特徴
薬物療法グループ:
内分泌療法、他の拮抗ホルモンおよび関連薬剤。
薬力学特性
作用機序
デガレリクスは、下垂体 GnRH 受容体に競合的かつ可逆的に結合する選択的 GnRH 受容体アンタゴニスト (ブロッカー) で、ゴナドトロピン、そしてその結果としてテストステロン (T) の放出を急速に減少させます。前立腺がんは、ホルモン感受性前立腺がんの治療における基本原則であるテストステロン欠乏に敏感です。 GnRH アゴニストとは異なり、GnRH 受容体拮抗薬は、黄体形成ホルモン (LH) 濃度の上昇を誘発せず、その後、治療開始後にテストステロン/腫瘍刺激が増加し、潜在的な症状発現 (再燃) が起こります。
デガレリックス酢酸塩 (活性物質) 240 mg を個別に投与し、続いて維持用量 80 mg を投与すると、LH、卵胞刺激ホルモン (FSH)、続いてテストステロンの濃度が急速に低下します。ジヒドロテストテロン (DHT) の血漿濃度は、テストステロンと同様に低下します。
デガレリックス酢酸塩 (有効成分) は、医療去勢レベル 0.5 ng/mL を十分に下回るテストステロン抑制を達成および維持するのに効果的です。毎月80mgを維持すると、97%の患者で少なくとも1年間、持続的なテストステロン抑制が得られました。 1 年間の治療後のテストステロン レベルの中央値は 0.087 ng/mL (四分位範囲 0.06 ~ 0.15) N=167 でした。)
薬物動態学的特性
注射された溶液の濃度は薬物動態挙動に大きな影響を与えます。したがって、推奨される濃度以外の用量あたりの濃度を使用すべきではありません。
吸収
デガレリクス酢酸塩(活性物質)は、皮下投与後に沈着物(「デポ」)を形成し、デガレリクスを血液循環中に放出します。前立腺がん患者を対象に実施された研究の薬物動態学的結果を以下の表に示します。
維持期におけるデガレリクスの平均濃度は、20 mg/mL の濃度で 80 mg で 10.9 ng/mL でした。
|
薬物動態パラメータ |
デガレリックス酢酸塩(主成分) 240mg |
| C max (ng/mL) |
53.4 |
| T max (日) |
1.4 |
| T 1/2 (日) |
43 |
|
AUC (直径ng/mL) |
1240 |
前立腺がん患者に濃度 40 mg/mL のデガレリクス 240 mg を皮下投与すると、デガレリクスは初回用量 240 mg(40 mg/mL)の平均半減期が約 43 日で二相的に消失します。 )および28日間の維持用量80mg(20mg/mL)。皮下投与後の長い半減期は、注射部位に形成されたデポーからのデガレリクスの放出が非常に遅いためです。薬物の薬物動態学的挙動は、注射懸濁液中の薬物の濃度に影響されます。
分布
高齢男性の分布量は約1L/kgです。血漿タンパク質の結合率は約 90% であると推定されています。
代謝
デガレリクスは、肝胆道系からの通過中に一般的なペプチド分解を受け、主にペプチド断片として糞便中に排泄されます。皮下投与後の血漿サンプルでは有意な代謝物は検出されませんでした。 in vitro研究では、デガレリクスがヒト CYP450 システムの基質ではないことが実証されました。
排泄
健康な男性では、静脈内投与された単回投与量の約 20 ~ 30% が尿中に排泄され、70 ~ 80% が肝胆道系を介して排泄されることが示唆されます。健康な高齢男性におけるデガレリクスのクリアランスは35 ~ 50 mL/h/kg と測定されています。
薬の治療作用が始まるまでの推定平均時間
臨床研究では、初回用量の投与直後にテストステロン(T)抑制が起こり、3日後には患者の96%が医学的去勢(T≧0.5ng/ml)に相当する血漿テストステロンレベルを有し、1ヵ月後には100%となることが実証されている。
特別な集団
腎機能障害のある患者さん
腎障害患者における薬物動態研究は行われていない。所定の用量のデガレリクスのうち、変化せずに腎臓から排泄されるのはわずか約 20 ~ 30% だけです。
確認的な第 III 相試験データの集団薬物動態解析により、軽度から中等度の腎障害を持つ患者におけるデガレリクスのクリアランスが約 20 ~ 30% 減少することが実証されました。したがって、軽度から中等度の腎障害のある患者の用量調整は推奨されません。重度の腎障害のある患者に関するデータは不足しているため、デガレリクスを使用する場合はこの患者集団に注意することが賢明です。
肝障害のある患者さん
デガレリクスは、軽度から中等度の肝障害のある患者を対象とした薬物動態研究で研究されました。健常者と比較して、肝障害のある被験者では曝露増加の兆候は観察されませんでした。肝障害患者では、投与後24時間でベースライン値と比較して肝機能検査に変化は観察されなかった。軽度から中等度の肝障害のある患者には用量調整は必要ありません。
重度の肝機能障害のある患者は研究されていないため、このグループには注意することをお勧めします。
お年寄り
臨床プログラムで検査された患者は、典型的な前立腺がんの対象集団でした。患者の平均年齢は74歳(範囲は47~98歳)であった。
フィルマゴン ストレージ ケア
Firmagon ® は、室温 (15 ~ 30 °C) で乾燥した場所に保管する必要があります。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。
外見
凍結乾燥粉末および希釈剤(注射用溶液)。
官能特性
フリーズドライパウダー
タブレット、白またはほぼ白。
注射可能な溶液
無色透明の液体。
再構成された溶液は透明で、未溶解物質が含まれていない必要があります。
溶解後は直ちに使用してください。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かないところに保管してください。
フィルマゴンの法的格言
MS – 1.2876.0017
農場。答え:
シルビア・タカハシ・ヴィアナ
CRF/SP 38.932
メーカー(粉末):
フェリング社
ウィットランド 11 – D-24109 –
キール、ドイツ。
製造元(希釈剤):
フェリング社
ウィットランド 11 – D-24109
キール、ドイツ。
梱包業者:
フェリング インターナショナル センター SA
FICSA Chemin de la Vergognausaz、1162
サン・プレックス、スイス。
以下の者が輸入、販売、登録しています。
フェリング株式会社の研究所
サンマルコス広場、624 05455-050
サンパウロ – SP
CNPJ: 74.232.034/0001-48
SAC:
0800 772 4656
医師の処方箋に基づいて販売します。








-1024x576.jpg?resize=1024,576&ssl=1)


