塩酸ブロムヘキシンの禁忌 – Pharlab

塩酸ブロムヘキシン(活性物質)は、ブロムヘキシンまたは配合成分の他の成分に対して過敏症のある患者には禁忌です。フルクトース不耐症の患者には、大人用と子供用のシロップは禁忌です。
塩酸ブロムヘキシンの使用方法 – Pharlab
計量カップのマークを使用して、正しい用量を取得します。
用量は、経口使用の場合、体重1kgあたり塩酸ブロムヘキシン(活性物質)0.1mgを1日3回繰り返す割合で計算できます。
塩酸ブロムヘキシン(有効成分)小児用シロップ
1mL中に塩酸ブロムヘキシン(有効成分)0.8mgを含有します。
2歳から? 6年
2.5mL、(2mg)を1日3回。
6歳から12歳までの子供
5mL、(4mg)を1日3回。
大人および12歳以上の青少年
10mL(8mg)を1日3回。
塩酸ブロムヘキシン(原体)成人用シロップ
1mL中に塩酸ブロムヘキシン(有効成分)1.6mgを含有します。
大人および12歳以上の青少年
5mL、(8mg)を1日3回。
塩酸ブロムヘキシン(原体)シロップの1日総摂取量目安
2歳から? 6年
6mg/日。
6歳以上のお子様から? 12年
12mg/日。
大人および12歳以上の青少年
24mg/日。
塩酸ブロムヘキシンに関する注意事項 – Pharlab
ブロムヘキシンなどの去痰薬の投与に一時的に関連して、スティーブンス・ジョンソン症候群や中毒性表皮壊死融解症(TEN)を伴う重度の皮膚病変が発生した症例はほとんど報告されていません。これらの多くは、患者の基礎疾患や併用薬によって説明できる可能性があります。さらに、スティーブンス・ジョンソン症候群または TEN の初期段階では、患者は発熱、体の痛み、鼻炎、咳、喉の痛みなどの非特異的なインフルエンザのような症状を経験することがあります。これらの非特異的なインフルエンザのような症状に混乱して、咳止め薬や風邪薬の使用による対症療法が開始される場合があります。
このため、皮膚や粘膜に新たな病変が現れた場合は、予防措置としてブロムヘキシンによる治療を中止し、直ちに医師の診察を受ける必要があります。
塩酸ブロムヘキシン(活性物質)で治療を受けている患者は、分泌量の増加が予想されることに注意する必要があります。
急性呼吸器疾患の場合、症状が 4 ~ 5 日経っても改善しない場合、または治療期間中に悪化する場合は、医師に相談する必要があります。
塩酸ブロムヘキシン(有効成分)シロップには砂糖が含まれていないため、糖尿病患者でも使用できます。
成人用の塩酸ブロムヘキシン(活性物質)シロップには、成人および12歳以上の青少年の最大推奨1日量(30mL)あたり、成人用の塩酸ブロムヘキシン(活性物質)シロップには4.8gのソルビトールが含まれ、子供用の塩酸ブロムヘキシン(活性物質)シロップには9.6gのソルビトールが含まれています。フルクトース不耐症の患者はこの薬を使用しないでください。この薬は軽度の下剤効果を引き起こす可能性があります。
この薬は2歳未満の小児には使用しないでください。
受胎能力、妊娠、授乳
妊婦におけるブロムヘキシンの使用に関するデータは限られています。動物実験では、生殖毒性に関して直接的または間接的な有害な影響は示されていません。
予防策として、妊娠中は塩酸ブロムヘキシン(有効成分)の使用を避けることが望ましいです。
塩酸ブロムヘキシン(有効成分)は、妊娠中のリスクカテゴリーBに分類されています。
この薬は医師のアドバイスなしに妊婦が使用しないでください。

ブロムヘキシンとその代謝物が母乳中に排泄されるかどうかは不明です。
動物で入手可能な薬理学的/毒物学的データは、母乳中にブロムヘキシンとその代謝産物が排泄されることを実証しました。授乳中の乳児に対するリスクを排除することはできません。塩酸ブロムヘキシン(有効成分)は授乳中に使用しないでください。
塩酸ブロムヘキシン(活性物質)がヒトの生殖能力に及ぼす影響については研究が行われていません。利用可能な前臨床経験に基づくと、塩酸ブロムヘキシン (活性物質) の使用が生殖能力に及ぼす影響の可能性は示されていません。
塩酸ブロムヘキシンの副作用 – Pharlab
異常な反応
上腹部の痛み、吐き気(気分が悪くなる)、嘔吐、下痢。
まれな反応
過敏症(アレルギー)、発疹(皮膚の赤い斑点、通常はかゆみと皮むけ)。
頻度が不明な反応
アナフィラキシー反応(重度のアレルギー反応)、アナフィラキシーショック(ショックを伴う重度のアレルギー反応)、気管支けいれん(肺に空気を運ぶ経路の収縮)、血管神経性浮腫(唇、舌、喉の腫れ)、蕁麻疹(皮膚の発赤反応)プラークの出現)、そう痒症(かゆみ)。
有害事象が発生した場合は、健康監視通知システム (NOTIVISA) または州または地方自治体の健康監視機関に通知してください。
塩酸ブロムヘキシンの薬物相互作用 – Pharlab
アンピシリン、エリスロマイシン、オキシテトラサイクリンなどの他の薬剤との関連する好ましくない相互作用は報告されていません。
経口抗凝固薬またはジゴキシンとの相互作用研究は行われていません。
塩酸ブロムヘキシンの食品との相互作用 – Pharlab
塩酸ブロムヘキシン(活性物質)は食事の有無にかかわらず摂取できます。
塩酸ブロムヘキシンという物質の作用 – Pharlab
効果の結果
軽度から重度の慢性気管支炎の成人患者61人を対象とした6か月の研究では、毎日24mgのブロムヘキシンを投与された30人の患者グループの83%(患者25人、うち重度に分類された8人)が主観的な改善を達成した(良くなったと感じた) )、対してプラセボを投与されたボランティア 31 人のうち 19% (患者 6 人)。
ブロムヘキシン 16 mg を 1 日 3 回、11 日間、プラセボとの二重盲検比較で慢性気管支炎患者の粘液粘度の低下を評価した研究では、塩酸ブロムヘキシン (活性物質) は粘度を 39 % 低下させました (研究開始時との関係で)、プラセボ群では粘液粘度が 7% 悪化しました。
薬理的特性
ブロムヘキシンは、植物有効成分バシシンの合成誘導体です。前臨床研究では、気管支漿液分泌の割合の増加が実証されました。ブロムヘキシンは粘液の粘度を低下させ、毛様体上皮を活性化して (粘液線毛クリアランス)、粘液の輸送と排出を促進します。
臨床研究では、気管支領域におけるブロムヘキシンの分泌分解作用および分泌促進作用が実証されており、これにより喀痰が促進され、咳が軽減されます。
ブロムヘキシンの投与後、痰および気管支肺分泌物中の抗生物質(アモキシシリン、エリスロマイシン、オキシテトラサイクリン)の濃度が増加します。
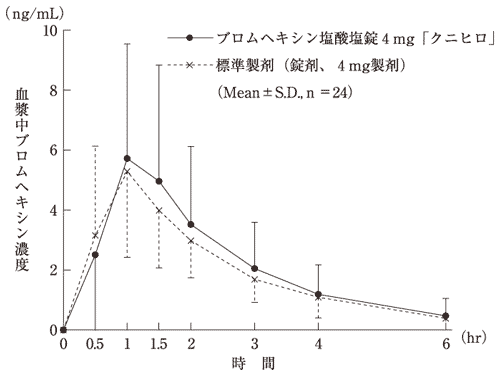
ブロムヘキシンの薬物動態は、アンピシリンまたはオキシテトラサイクリンとの同時投与によって有意な影響を受けませんでした。また、比較履歴によると、ブロムヘキシンとエリスロマイシンの間に関連する相互作用はありません。
長期間の販売期間中に関連する相互作用の報告がないことは、これらの薬剤との実質的な相互作用の可能性がないことを示唆しています。
薬物動態学的特性
吸収
ブロムヘキシンは胃腸管から迅速かつ完全に吸収されます。
塩酸ブロムヘキシン (活性物質) の絶対バイオアベイラビリティは、塩酸ブロムヘキシン (活性物質) 溶液の場合、約 26.8 ± 13.1% です。薬物の約 75 ~ 80% が初回通過代謝を受けます。
食事中に塩酸ブロムヘキシン(活性物質)を投与すると、おそらく初回通過効果が部分的に阻害されるため、ブロムヘキシンの血漿濃度が上昇します。
経口投与から約5時間後に作用が現れます。
分布
静脈内投与後、ブロムヘキシンは体全体に急速かつ広範囲に分布し、平均定常状態分布量は最大 1209 ± 206 L (19 L/kg) でした。ブロムヘキシン 32 mg および 64 mg を経口投与した後、肺組織 (気管支および実質) における分布を調査しました。
ブロムヘキシン投与の 2 時間後、肺組織の濃度は、血漿濃度と比較して、細気管支気管支組織では 1.5 ~ 4.5 倍、肺実質では 2.4 ~ 5.9 倍高くなりました。
ブロムヘキシン 8mg および 16mg の静脈内使用用製剤の投与後に、肺組織内の分布を調査しました。投与2時間後、肺組織中の濃度は、血漿中濃度と比較して、気管支および気管支組織では4.2〜4.3倍、肺実質では3.0〜4.3倍高かった。
未変化のブロムヘキシンの 95% が血漿タンパク質に結合します (非制限結合)。
代謝
ブロムヘキシンは、ほぼ完全に代謝されて、さまざまなヒドロキシル化代謝産物とジブロマントラニル酸になります。すべての代謝産物とブロムヘキシン自体は、N-グルクロニドおよび O-グルクロニドの形で結合している可能性が最も高くなります。スルホンアミド、オキシテトラサイクリン、エリスロマイシンによる代謝パターンの変化を示す証拠はありません。したがって、CYP 450 2C9 または 3A4 の基質との関連する相互作用は考えられません。
排除
ブロムヘキシンは、抽出率(肝血流範囲 843 ~ 1073 mL/min での静脈内投与後のクリアランス)が高い薬剤であり、その結果、個体内および個体間のばらつきが大きくなります(CV gt; 30%)。放射性標識ブロムヘキシンの投与後、用量の約 97.4 ± 1.9% が尿中の放射能として回収され、未変化の化合物としては 1% 未満でした。
ブロムヘキシンの血漿濃度は、複数の指数関数的に減少します。 8~32 mgの単回用量を経口投与した後、最終排出半減期は6.6~31.4時間の間で変化しました。 15~100mgの静脈内投与後の最終排出半減期は7.1~15.4時間の範囲でした。複数回投与の薬物動態の予測に関連する半減期は約 1 時間です。したがって、複数回投与しても蓄積は観察されなかった(蓄積係数:1.1)。
直線性/非直線性
ブロムヘキシンは、経口投与後、8 ~ 32 mg の範囲で用量比例薬物動態を示します。
静脈内投与後、ブロムヘキシンは 15 ~ 100 mg の範囲で用量に比例した薬物動態を示します。
特殊な集団
高齢者や腎不全、肝不全患者におけるブロムヘキシンに関する薬物動態データはない。
広範な臨床経験では、これらの集団における安全性研究の必要性は証明されていません。











