臨床研究により、菌血症および敗血症(新生児敗血症を含む)における硫酸アミカシン(活性物質)の臨床効果が明らかになりました。気道、骨および関節、中枢神経系(髄膜炎を含む)、皮膚および軟部組織の重度の感染症。腹腔内感染症(腹膜炎を含む)。火傷および術後感染症(血管手術後を含む)。

研究では、これらの細菌によって引き起こされる複雑かつ重度の再発性尿路感染症に対する硫酸アミカシン(活性物質)の有効性も明らかになりました。
アミカシン(活性物質)を含むアミノグリコシドは、原因物質が毒性の低い他の抗生物質に対して感受性がない限り、尿路感染症の初期および単純な症状には適応されません。
合併症のない尿路感染症の治療にアミカシン(活性物質)の使用の適応がある場合は、より少ない用量を処方する必要があります。
原因物質とアミカシン(活性物質)に対するその感受性を特定するには、細菌学的検査を実施する必要があります。
グラム陰性感染が疑われる場合には、アンチバイオグラムの結果が得られる前であっても、初期治療としてアミカシン(活性物質)を導入することができます。
ゲンタマイシンおよび/またはトブラマイシンに耐性のあるグラム陰性菌株、特にプロテウス・レットゲリ、プロビデンシア・スチュアルティ、セラチア・マルセッセンスおよび緑膿菌に対する硫酸アミカシン(活性物質)の有効性は、臨床研究を通じて証明されています。薬剤による治療を継続するかどうかの決定は、感受性検査の結果、感染症の重症度、患者の反応、および警告に含まれる追加の考慮事項に基づいて行う必要があります。
アミカシン(活性物質)は、ブドウ球菌感染症の治療に効果があることが示されており、ブドウ球菌が原因であると疑われる、またはそのことが知られている疾患、たとえばブドウ球菌が原因の重度の感染症の治療における初期療法として使用できます。グラム陰性菌またはブドウ球菌による感染症、他の抗生物質にアレルギーのある患者における感受性ブドウ球菌によって引き起こされる感染症、およびブドウ球菌とグラム陰性菌によって引き起こされる混合感染症。
新生児敗血症などの重篤な感染症の場合、連鎖球菌などのグラム陽性微生物による感染の可能性があるため、別のペニシリン系抗生物質の併用治療が必要となる場合があります。
硫酸アミカシンの禁忌 – Hipolabor
アミカシン (活性物質) は、アミカシン (活性物質) または製剤の他の成分に対する過敏症の病歴のある患者には禁忌です。
アミカシン (活性物質) は、このクラスの薬物に対する患者の交差感受性が知られているため、重度の毒性反応または他のアミノグリコシドに対する過敏症の病歴のある患者には禁忌となる場合があります。
硫酸アミカシンの使用方法 – Hipolabor
- アンプルを約 45 °の角度に傾けて持ちます。
- 親指の先をボトルの首に置きます。
- 人差し指でアンプルの上部を包み、開くまで押し戻します。
静脈内投与
溶液の調製
静脈内使用用の溶液は、生理食塩水、5% ブドウ糖血清、または別の適合性溶液などの滅菌溶液 100 または 200 mL に所望の用量を加えることによって調製されます。
成人の場合、投与は30〜60分間かけて行われます。 1日の総用量は15mg/kg/日を超えてはなりません。
小児患者の場合、注入される液体の量は患者が許容できる量によって異なります。アミカシン (活性物質) を 30 ~ 60 分間注入するのに十分な量である必要があります。
乳児の場合、点滴は 1 ~ 2 時間継続する必要があります。アミカシン (活性物質) は他の薬剤と事前に混合してはならず、推奨される投与量と投与経路に従って個別に投与する必要があります。
非経口使用の薬剤は、ボトルや溶液が許す限り、投与前に色の変化や粒子の存在を検出する必要があります。
アミノグリコシド系抗生物質は、投与経路を問わず、他の薬剤と事前に混合してはならず、別々に投与する必要があります。
アミノグリコシドには毒性のリスクがあるため、治療には固定用量が推奨されず、体重に基づいた用量が推奨されます。
投与量の計算は各患者のニーズに合わせて行うことが重要です。
溶液は最終的に淡黄色に変わることがありますが、これは効能の低下を示すものではありません。
投与量
正しい投与量を計算するには、治療前に患者の体重を測定する必要があります。腎機能は、血清クレアチニンを測定するか、内因性クレアチニンクリアランスを計算することによって評価する必要があります。
血清尿素の測定はそれほど信頼できません。これらの検査は治療中に定期的に繰り返す必要があります。
可能な限り、アミカシン (活性物質) の血清濃度を測定して、過剰ではなく適切な薬物レベルを確保する必要があります。
可能であれば、最小濃度と血清ピークの測定は治療中に断続的に行われ、ピーク濃度(注射後 30 ~ 90 分)が 35μg/mL を超えることや最小濃度(次の投与直前)が 10μg/mL を超えることを避けるべきです。 mL。
投与量は指示に従って調整する必要があります。
腎機能が正常な患者では、1 日 1 回の用量を使用できます。このような場合、最大濃度は 35μg/mL を超える可能性があります。
腎機能が正常な患者に対する筋肉内および静脈内投与
腎機能が正常な成人および小児に推奨される筋肉内または静脈内投与量は、15 mg/kg/日を一定の間隔で 2 回または 3 回に分けて投与する、つまり 12 時間ごとに 7.5 mg/kg、または 8 時間ごとに 5 mg/kg です。
太りすぎの患者の投与量は 1.5g/日を超えてはなりません。
未熟児の場合、推奨用量は 12 時間ごとに 7.5mg/kg です。新生児には、10mg/kgの負荷用量を投与し、その後12時間ごとに7.5mg/kgを投与する必要があります。
生後2週間を超える小児および乳児には、12時間ごとに7.5mg/kg、または8時間ごとに5mg/kgを投与する必要があります。
1日1回の投与量
あるいは、クレアチニンクリアランスに反映される腎機能を有する患者では?菌血症、敗血症、気道感染症、複雑性尿路感染症、腹腔内感染症の場合には、50mL/分、成人では15mg/kg、小児(生後1か月以上)では20mg/kgを1日1回静脈内投与することができます。感染症、および経験的には発熱性好中球減少症。
他の臓器障害のある患者における 1 日 1 回投与の使用に関するデータは限られています。
線量を計算するときは注意が必要です。
50mg/mL の溶液が入ったバイアルをさらに希釈して、低出生体重児の未熟児に正確な用量を提供することができます。
通常の治療期間は 7 ~ 10 日間で、投与経路に関係なく、薬物の 1 日の総用量は 15 ~ 20 mg/kg/日を超えてはなりません。
治療が10日を超える可能性がある耐性感染症または複雑な感染症の場合、硫酸アミカシン(活性物質)の使用を再評価する必要があり、継続する場合は、腎臓、前庭だけでなくアミカシン(活性物質)の血清レベルも監視する必要があります。そして聴覚機能。
推奨用量を使用すると、アミカシン (活性物質) に感受性のある微生物によって引き起こされる単純な感染症の場合は、通常 24 ~ 48 時間後に反応します。 3 ~ 5 日以内に臨床的改善が見られない場合は、治療を中止し、抗生物質感受性検査を繰り返す必要があります。
治療の失敗は微生物の抵抗性または敗血症病巣の存在が原因である可能性があり、この場合には外科的ドレナージが必要です。硫酸アミカシン(活性物質)の使用が必要な合併症のない尿路感染症の場合、1日の総用量は500mgを2回に分けて(250mgを1日2回)、または1回に7〜10日間投与できます。
腎機能障害患者への投与
クレアチニンクリアランスltに代表される腎不全患者の場合。 50mL/分、アミカシン (活性物質) の 1 日総用量を 1 日 1 回の投与で投与することは、これらの患者が長期間にわたってより高い最低濃度に曝露されることになるため、推奨されません。
腎機能障害のある患者の用量調整については以下を参照してください。
通常の用量(1日2~3回)を守っている腎不全患者の場合は、可能な限り、適切な方法を使用してアミカシン(活性物質)の血清濃度を監視する必要があります。
腎機能障害のある患者の用量は、通常の用量を長期間投与するか、一定の間隔で減量して投与することによって調整できます。
どちらの方法も、腎機能が低下した患者におけるアミノグリコシドの半減期に関連するため、患者のクレアチニンクリアランスまたは血清クレアチニン値に基づいています。
これらの投与スケジュールは、患者の臨床検査および臨床検査に従って使用する必要があり、必要に応じて変更する必要があります。患者が透析を受けている場合は、どちらの方法も使用しないでください。
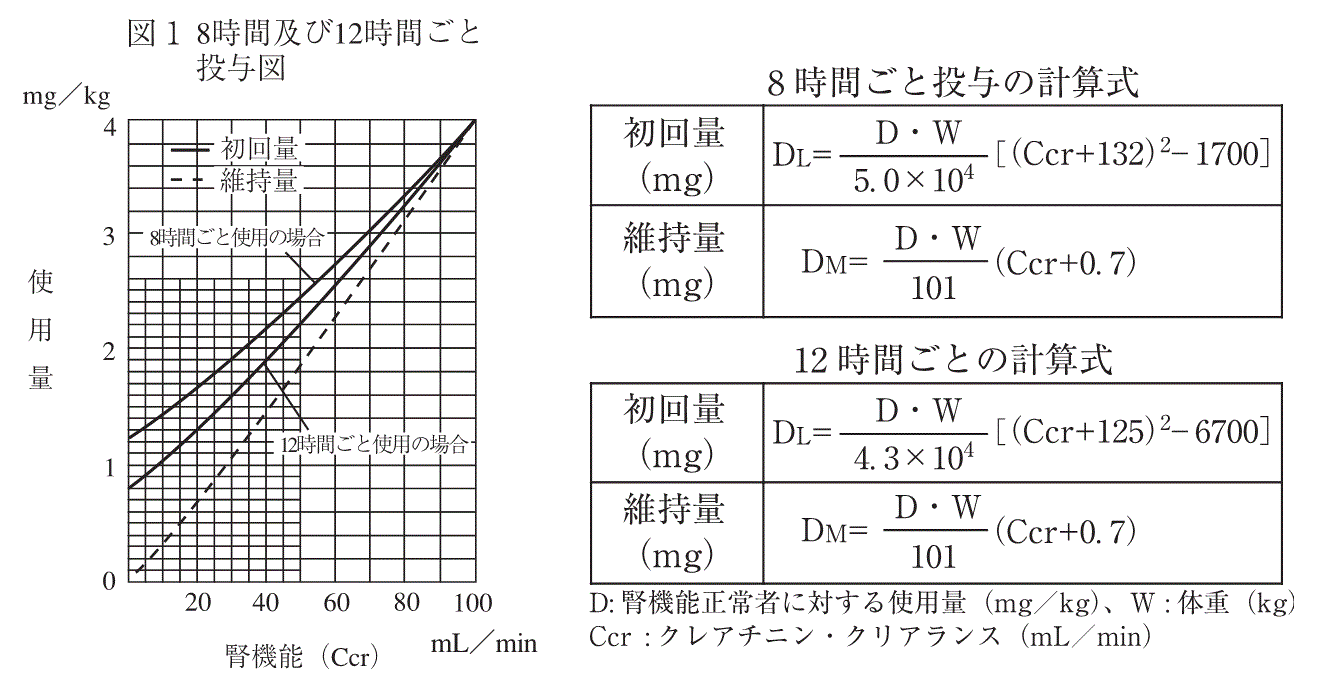
延長された間隔での通常の投与量
クレアチニンクリアランスを得ることができないが、患者が安定している場合、通常の用量(すなわち、正常な腎機能を有する患者の場合、1日2回の投与スケジュールで7.5mg/kg)の投与間隔が時間単位で得られる。したがって、血清クレアチニン値が 2mg/100mL の患者は、18 時間ごとに 7.5mg/kg の推奨単回投与を受けることになります。
投与間隔を固定して投与量を減らす
機能が変化し、硫酸アミカシン(有効成分)を一定間隔で投与したい場合には、用量を減量する必要があります。
正確な投与を確保し、過剰な濃度を避けるために、これらの患者の硫酸アミカシン (活性物質) の血清濃度を測定する必要があります。
患者の状態が安定しており、血清測定値が利用できない場合、血清クレアチニンおよびクレアチニンクリアランス値が、用量ガイドとして使用するための最も容易に利用可能な腎機能評価パラメーターとして使用されます。
負荷用量として 7.5mg/kg の用量で治療を開始します。これは、上で計算した正常な腎機能を持つ患者に推奨される用量と同じです。
12 時間ごとに投与される維持用量を決定するには、患者のクレアチニンクリアランスの減少に比例して負荷用量を減らす必要があります。
12時間ごとの維持量:
(CC = クレアチニンクリアランス)
?通常の CC (mL/分)
(CC = クレアチニンクリアランス)。
(定常状態の血清クレアチニン値が既知の患者の場合) 12 時間間隔で減量用量を決定する別のより大雑把な代替方法は、通常推奨される用量を患者の血清クレアチニンで割ることです。
上記のスキームは厳密な推奨事項ではなく、アミカシン (活性物質) の血清レベルが得られない場合に用量を調整するための実用的なガイドです。
硫酸アミカシンの予防措置 – Hipolabor
アミノグリコシド系抗生物質による非経口治療を受けている患者は、耳毒性および腎毒性のリスクがあるため、頻繁に検査を受ける必要があります。
14 日を超える治療の安全性は確立されていません。
永続的な両側の前庭および聴覚の聴器毒性によって現れる神経毒性は、既存の腎病変のある患者や、高用量および/または推奨より長期間にわたって薬剤を投与された正常な腎機能を持つ患者に発生する可能性があります。
腎機能障害のある患者では、アミノグリコシド誘発性聴器毒性のリスクがより高くなります。通常、高周波に対する難聴が最初に発生し、聴力検査によってのみ検出できます。
前庭損傷の症状としてめまいが発生する場合があります。神経毒性のその他の症状には、眠気、うずき、筋肉のけいれん、けいれんなどが含まれる場合があります。
アミノグリコシドによる聴器毒性のリスクは、血清濃度の持続的な高いピークと、血清濃度/時間曲線の減衰期間の高い血清濃度の両方への曝露の程度とともに増加します。
多くの場合、蝸牛または前庭病変を発症している患者は、治療中に8番目のペアの毒性を警告するような症状を示さず、薬の中止後に不可逆的な部分的または完全な両側性難聴を示します。
アミノグリコシドの使用によって引き起こされる聴器毒性は、一般に不可逆的です。
アミノグリコシドには腎毒性がある可能性があり、腎機能障害のある患者や、高用量または長期の治療を受けている患者ではリスクが高くなります。
神経筋遮断および呼吸麻痺は、アミノグリコシドの非経口投与、局所点滴(腹部および整形外科の洗浄、蓄膿症の局所治療)後、および経口使用後に報告されています。
薬物の投与経路に関係なく、特に麻酔薬、ツボクラリン、サクシニルコリン、デカメトニウムなどの神経筋遮断薬を使用している患者、および抗凝固剤を投与されたクエン酸血を大量に投与されている患者では、これらの現象が発生する可能性があることに留意する必要があります。 。

閉塞が発生した場合、カルシウム塩によって閉塞を解消することができますが、機械的換気措置も必要になる場合があります。
腎機能および第 8 神経機能は、特に治療前に腎機能不全の疑いまたは証拠がある患者や、当初は腎機能が正常であったが治療中に機能不全の兆候が現れた患者では、頻繁に評価する必要があります。
可能であれば、アミカシン (活性物質) の血清レベルを監視し、適切なレベルを提供し、毒性レベルを回避してください。
尿検査は、尿密度のレベルの低下、タンパク質排泄の増加、および円柱または細胞の存在を調べるために実行する必要があります。
血清尿素およびクレアチニンの測定またはクレアチニンクリアランスを定期的に実行する必要があります。患者が検査を受けるのに十分な年齢である場合、特にリスクの高い患者には連続聴力検査を実施する必要があります。
腎毒性または聴器毒性の兆候(めまい、めまい、耳鳴り、耳鳴り、難聴)が発生した場合は、薬剤の投与を中止するか、投与量を変更する必要があります。
他の神経毒性薬または腎毒性薬、特にバシトラシン、シスプラチン、アムホテリシン b、セファロリジン、パロモマイシン、ビオマイシン、ポリミキシン b、コリスチン、バンコマイシンおよび他のアミノグリコシドの同時またはその後の経口、局所、または全身使用は避けるべきです。
高齢や脱水症状も毒性のリスクを高める要因となります。
硫酸アミカシン (活性物質) と強力な利尿薬 (エタクリン酸またはフロセミド) の併用は避けるべきです。これらの薬剤は聴器毒性も引き起こす可能性があります。
利尿薬を静脈内投与すると、血清および組織中の抗生物質の濃度が増加し、アミノグリコシドの毒性が増加します。
硫酸アミカシン (活性物質) には、敏感な人の生命を脅かすアナフィラキシー症状やそれほど重度ではない喘息エピソードなど、アレルギー型反応を引き起こす可能性がある亜硫酸水素ナトリウムが含まれています。
一般集団における亜硫酸塩過敏症の罹患率は一般的ではなく、おそらく低いと考えられます。亜硫酸塩感受性は、喘息患者では非喘息患者よりも頻繁に観察されます。
アミノグリコシドは、外科的処置に伴う膀胱を除いて、局所的に適用するとほぼ完全かつ迅速に吸収されます。
アミノグリコシド系抗生物質を含む製剤で大小の手術野を洗浄した後に、神経筋遮断による不可逆的な難聴、腎不全、死亡例が報告されています。
腎毒性
患者は治療中十分に水分補給しなければならず、治療開始前および治療期間中は毎日、通常の方法を使用して腎機能を評価する必要があります。
腎刺激の兆候(円柱尿、白血球尿、血尿またはアルブミン尿)や、クレアチニンクリアランスの低下、尿比重の低下、尿素、クレアチニンまたは乏尿の増加などの腎機能障害の兆候が現れた場合は、用量の減量が必要になる場合があります。
高窒素血症の増加または利尿の進行性の減少がある場合は、治療を中断する必要があります。
高齢患者では、血清尿素やクレアチニンの測定などの日常的な検査では証明されない腎機能の低下が見られる場合があります。
このような場合、クレアチニンクリアランスを測定することがより有用である可能性があります。これらの患者では、アミノグリコシド系抗生物質による治療中に腎機能を定期的に評価することが特に重要です。
神経毒性
高用量のアミカシン(活性物質)を投与された実験動物では、神経筋遮断および筋肉麻痺が発生することが実証されています。
アミカシン(活性物質)を麻酔薬または神経筋遮断薬と同時に投与する場合は、神経筋遮断および呼吸停止の可能性を考慮する必要があります。閉塞が発生した場合は、カルシウム塩によって回復することができます。
アミノグリコシドは、神経筋接合部に対する潜在的なクラーレ様作用により筋力低下を悪化させる可能性があるため、重症筋無力症やパーキンソニズムなどの筋障害のある患者には注意して使用する必要があります。
その他

他の抗生物質と同様、アミカシン (活性物質) を使用すると、非感受性微生物が異常増殖する可能性があります。このような場合は、適切な治療を開始する必要があります。
アミノグリコシドとベータラクタム系抗生物質 (ペニシリンまたはセファロスポリン) のin vitro会合は、重大な相互不活化を引き起こす可能性があります。アミノグリコシドとペニシリン系薬剤が異なる経路で投与されると、血清活性の低下が発生する可能性があります。
アミノグリコシドの不活化は、腎機能に重度の変化がある患者においてのみ臨床的に重要です。この不活化は、検査のために採取された体液検体中で継続する可能性があり、その結果、アミノグリコシドの測定値が不正確になる可能性があります。
これらの検体は正しく取り扱う必要があります(速やかに検査するか、凍結するか、β-ラクタマーゼで処理するか)。
特別な集団
妊娠中および授乳中の使用
アミノグリコシドは、妊婦に投与すると胎児に害を及ぼす可能性があります。アミノグリコシドは胎盤を通過し、母親が妊娠中にストレプトマイシンを投与された子供における完全かつ不可逆的な先天性両側性難聴がいくつか報告されています。
妊婦を他のアミノグリコシドで治療した場合、胎児や新生児に対する重篤な副作用は報告されていませんが、その可能性は存在します。
アミカシン (活性物質) を使用したラットおよびマウスでの生殖研究では、アミカシン (活性物質) の使用による生殖能力の変化または胎児への危険性の証拠は示されませんでした。
妊婦を対象とした十分に管理された研究はありませんが、実験的研究には胎児への副作用に関する明確な証拠は含まれていません。
治療中に患者が妊娠した場合、または妊娠中にこの薬を投与した場合、胎児に対する潜在的なリスクについて患者に警告する必要があります。
この薬物が母乳中に排泄されるかどうかは不明です。多くの薬は母乳中に排泄されるため、患者が薬を服用している間は原則として授乳は行わないでください。
妊娠リスクカテゴリー:カテゴリーD。
この薬は医師のアドバイスなしに妊婦が使用しないでください。妊娠が疑われる場合は、すぐに医師に知らせてください。
お年寄り
高齢患者に対する特別な推奨事項はありません。
子供たち
未熟児および新生児に対するアミノグリコシドの使用は、これらの患者の腎臓が未熟であるため、注意して行う必要があり、その結果、これらの薬物の血清半減期が増加します。
発がん、突然変異誘発、生殖能力へのダメージ
アミカシン(活性物質)の発がん性を評価するための動物での長期研究は開発されていません。
硫酸アミカシン(活性物質)をヒトの一日用量の最大10倍の用量でラットに投与しても、どちらの性別の生殖能力にも影響はありませんでした。
硫酸アミカシンの副作用 – Hipolabor
すべてのアミノグリコシドは、耳毒性、腎毒性、前庭毒性、神経筋遮断を引き起こす可能性があります。
これらの毒性作用は、現在または過去に腎機能障害の病歴がある患者、他の腎毒性薬または聴器毒性薬ですでに治療されている患者、および推奨される期間および/または用量を超える治療を受けた患者でより頻繁に発生します。
神経毒性/聴器毒性

第 8 脳神経に対する毒性の影響により、難聴、平衡感覚の喪失、またはその両方が生じる可能性があります。アミカシン(活性物質)は主に聴覚機能に影響を与えます。
蝸牛損傷には、聴力検査で難聴が検出される前に起こることが多い高周波難聴が含まれます。
神経毒性/神経筋遮断
アミノグリコシドによる治療は、急性の筋肉麻痺や無呼吸を引き起こす可能性があります。
腎毒性
以下のことが説明されていました。
血清クレアチニンの上昇、アルブミン尿、尿中の白血球、赤血球または円柱の存在、高窒素血症および乏尿。腎機能の変化は通常、薬の中止により回復します。
他のアミノグリコシドの場合と同様に、市販後に中毒性腎症や急性腎不全が報告されています。
その他
まれに観察されるその他の反応としては、皮膚発疹、薬熱、頭痛、知覚異常、振戦、悪心および嘔吐、好酸球増加症、関節痛、貧血、低血圧および低マグネシウム血症があります。アミカシン(活性物質)の硝子体内投与(眼内注射)後に、場合によっては永久的な視力喪失を引き起こす黄斑梗塞が報告されています。
有害事象が発生した場合は、健康監視通知システム – NOTIVISA (www.anvisa.gov.br/hotsite/notivisa/index.htm で利用可能)、または州または地方自治体の健康監視に通知してください。
硫酸アミカシンの薬物相互作用 – Hipolabor
局所的または全身的な神経毒性または腎毒性抗生物質の同時使用および/または連続使用は避けるべきです。主にカナマイシン、ゲンタマイシン、ネチルマイシン、トブラマイシン、ネオマイシン、シソマイシン、ストレプトマイシン、セファロリジン、パロモマイシン、ビオマイシン、ポリミキシン B、コリスチンおよびバンコマイシンです。フロセミド、エタクリン酸、水銀剤、マンニトールなどの強力な利尿薬の使用も含まれます。
一部の利尿薬はそれ自体が聴器毒性を引き起こし、静脈内に投与される利尿薬はアミノグリコシドの毒性を高め、血清および組織中の濃度を変化させます。
アミカシン(活性物質)を麻酔薬または神経筋遮断を引き起こす薬剤と同時に投与する場合は、神経筋遮断および呼吸麻痺の可能性を考慮する必要があります。
閉塞が発生した場合、カルシウム塩がこの現象を逆転させることができます。
硫酸アミカシンという物質の作用 – Hipolabor
有効性の結果
グラム陰性菌:
アミカシン (活性物質)は、シュードモナス属、大腸菌、プロテウス属に対してin vitro で活性を示します。 (インドール陽性およびインドール陰性)、プロビデンシア種、クレブシエラ・エンテロバクター・セラチア種、アシネトバクター種。 (以前のMima-Herellea ) およびCitrobacter freundii 。ゲンタマイシン、トブラマイシン、カナマイシンなどの他のアミノグリコシドに耐性のあるこれらの細菌の多くの菌株は、インビトロでアミカシン(活性物質)に感受性があります。
in vitro研究では、β-ラクタム系抗生物質と結合した硫酸アミカシン (活性物質) が、臨床的に重要ないくつかのグラム陰性菌に対して相乗的に作用することが実証されました。アミカシン (活性物質) へのin vitro曝露後、多くのグラム陰性菌の細菌増殖が持続的に抑制されます (抗生物質後効果)。アミカシン (活性物質) は、ゲンタマイシン、トブラマイシン、カナマイシンに影響を与えるほとんどのアミノグリコシド不活化酵素による分解に耐性があります。
グラム陽性:
アミカシン (活性物質) は、メチシリン耐性株を含む、ペニシリナーゼを産生するブドウ球菌、または産生しないブドウ球菌に対してin vitro で活性を示します。しかし、アミノグリコシドは一般に、他のグラム陽性菌、すなわち化膿連鎖球菌、腸球菌、肺炎連鎖球菌に対しては活性が低いことが示されています。
薬理学的特徴
薬の作用:
アミカシン(活性物質)は、カナマイシンに由来する半合成アミノグリコシド系抗生物質です。
筋肉内投与:
アミカシン (活性物質) は筋肉内投与後、局所的に急速に吸収され、良好な耐容性を示します。
正常な成人ボランティアでは、250mg (3.7mg/kg)、375mg (5mg/kg)、および 500mg (7.5mg/kg) を筋肉内投与した 1 時間後の平均ピーク血清濃度は、約 12、16、および 21μg/mL です。それぞれ単回投与。
投与後10時間の時点で、血清レベルはそれぞれ約0.3μg/mL、1.2μg/mL、および2.1μg/mLである。
推奨用量に従って投与した場合、10日間にわたる反復投与では薬物蓄積の証拠は観察されませんでした。
腎機能が正常な人では、筋肉内投与量の約 91.9% が最初の 8 時間以内に変化せずに尿中に排泄され、24 時間以内に 98.2% が尿中に排泄されます。 6時間の平均尿中濃度は、250mg投与後563μg/mL、375mg投与後697μg/mL、500mg投与後832μg/mLであった。
さまざまな体重(1.5kg未満、1.5kgから2.0kg、2.0kg以上)の新生児に7.5mg/kgの用量を筋肉内投与した研究では、他のアミノグリコシドと同様に、血清半減期値が逆相関していることが明らかになりました。出生後の年齢とアミカシン(活性物質)の腎クリアランスを伴います。
分布量は、アミカシン (活性物質) が他のアミノグリコシドと同様に、主に新生児の細胞外液に残留していることを示しています。どちらのグループも、12時間ごとに反復投与した5日後には蓄積を示さなかった。
静脈内投与:
正常な成人では、500mg (7.5mg/kg) を 30 分間かけて静脈内点滴により単回投与すると、点滴終了時の平均ピーク血清濃度は 38μg/mL、レベルは 24μg/mL となりました。注入後30分、1時間、10時間でそれぞれmL、18?g/mL、0.75?g/mL。
投与量の 84% が 9 時間以内に尿中に排泄され、94% が 24 時間以内に排泄されました。
正常な成人では、12 時間ごとに 7.5 mg/kg を繰り返し注入しても薬物の蓄積はなく、忍容性は良好でした。
腎機能が正常な成人ボランティアにアミカシン(活性物質)15mg/kgを30分間単回静脈内投与すると、平均ピーク血清濃度は77μg/mL、レベルは47μg/mLとなった。注入後1時間および12時間でそれぞれ1μg/mLおよび1μg/mLであった。
高齢患者(平均クレアチニンクリアランス64mL/分)では、15mg/kgを30分間注入した後の平均ピーク濃度55μg/mLが観察され、血清濃度は12時間で5.4μg/mL、1.3μg/mLであった。 g/mL 注入後 24 時間。
複数回投与の研究では、15~20 mg/kg の 1 日 1 回投与を受けた正常な腎機能を持つ患者には蓄積はありませんでした。
一般的な:
正常な成人を対象に行われた薬物動態研究により、平均血清半減期は 2 時間をわずかに超え、平均見かけの総分布容積は 24 リットル、つまり体重の約 28% であることが明らかになりました。
血清タンパク質結合率は 0 ~ 11% の範囲です。腎機能が正常な人の平均血清クリアランス速度は約 100mL/分、腎クリアランスは 94mL/分です。
アミカシン(活性物質)は主に糸球体濾過によって排泄されます。腎機能が変化している患者や糸球体濾過圧が低下している患者では、薬物の排泄が非常に遅くなります(血清半減期が効果的に延長されます)。
したがって、患者の腎機能を注意深く評価し、それに応じて投与量を調整する必要があります。
推奨用量の薬剤を投与した後、尿、胆汁、喀痰、気管支分泌物、間質液、胸水、滑液にも有意な濃度が見られることに加えて、骨、心臓、膀胱、肺実質でも治療レベルが認められます。
アミカシン (活性物質) は胎盤関門を通過し、羊水中でかなりの濃度に達します。
胎児血清濃度のピークは母体血清濃度のピークの約 16% であり、母体血清半減期値と胎児血清半減期値はそれぞれ約 2 時間と 3.7 時間です。








-1024x576.jpg?resize=1024,576&ssl=1)


