エボテカンとシスプラチンの併用は、ステージ IV-B が確認され、再発または持続性の子宮頸がんを患っており、手術および/または放射線療法による治療が受けられない患者の治療に適応されます。

エボテカンはどのように機能しますか?
エボテカンの主な化合物であるトポテカンは、細胞増殖に重要なトポイソメラーゼ I と呼ばれる酵素の作用をブロックすることで腫瘍に対して作用します。トポテカンはこの酵素を阻害することでがん細胞に損傷を与え、腫瘍の増殖を防ぎます。
エボテカンの禁忌
エボテカンは、トポテカンまたはその成分に対する重度の過敏反応(アレルギー)の病歴のある患者には禁忌です。エボテカンは、妊娠中または授乳中の患者、あるいは治療開始前に重度の骨髄抑制(血球産生の減少)のある患者には使用すべきではありません。あなたのケースを評価するには医師に相談してください。
この薬は医師のアドバイスなしに妊婦が使用しないでください。妊娠が疑われる場合は、すぐに医師に知らせてください。
エボテカンの使い方
静脈内使用。
エボテカンの投与量
エボテカンは細胞毒性のある注射可能な薬剤であるため、医療専門家のリーフレットに記載されている推奨事項に従って、資格のある専門家が投与する必要があります。医師は、あなたの症状に最適な薬の投与方法と最適な投与量を知っています。
エボテカンは通常、30 分間かけて患者の静脈に注入されます。エボテカンの推奨用量は、
卵巣癌または小細胞肺癌の場合
エボテカンの 1 日あたりの推奨用量は、連続 5 日間で 1.5 mg/m² です。
子宮頸がんの場合
エボテカンの推奨用量は、3 日間で 0.75 mg/m² です。
通常、この治療パターンは 3 週間ごとに繰り返されます。血液検査の結果によって治療法が異なる場合があります。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
Evotecan の使用を忘れた場合はどうすればよいですか?
疑問がある場合は、薬剤師または医師または歯科医師にアドバイスを求めてください。
エボテカンの予防措置
エボテカンによる治療は、がんに対する化学療法薬の使用に経験のある医師の監督の下で開始する必要があります。
次の場合は、Evotecan を使用する前に医師によく相談してください。
- あなたは肝臓に問題を抱えています。
- 呼吸器または肺に何らかの問題がある。
- 妊娠中、妊娠を計画している、または授乳中である。
治療中、医師は血小板数などの定期的な血液検査を指示して、摂取した用量の効果を監視し、必要に応じて量を調整する必要があります。
エボテカンを毒性の可能性のある他の薬剤と一緒に投与する場合は、用量の調整が必要になる場合があります(薬物相互作用のサブ項目を参照)。
詳細については医師にご相談ください。

小児への使用に関する十分な科学的情報はまだありません。
授乳中
エボテカンは授乳中も禁忌です。
車両の運転や機械の操作能力への影響
疲労感や脱力感が続く場合は、運転や機械の操作には注意してください。
エボテカンの副作用
すべての薬と同様に、エボテカンは望ましくない影響を引き起こす可能性があります。
以下の副作用はエボテカンの使用に関連しています。
非常に一般的な反応 (この薬を使用している患者の 10% で発生します)
- 感染;
- 貧血;
- 好中球減少症および発熱性好中球減少症(血液中に存在する白血球の一種である好中球の数の減少)。
- 白血球減少症(血液中に存在する白い防御細胞である白血球の数の減少);
- 血小板減少症(血液凝固に関与する細胞である血小板の数の減少);
- 食欲不振;
- 下痢;
- 吐き気と嘔吐。
- 腹痛;
- 便秘;
- 口内炎(胃の炎症);
- 脱毛;
- 弱さ;
- 疲れ;
- 発熱(発熱状態)。
一般的な反応 (この薬を使用している患者の 1% ~ 10% で発生します)
- 全身感染症。
- 汎血球減少症(血球数の全体的な減少)。
- 皮膚過敏症(発疹を含む);
- 高ビリルビン血症;
- 倦怠感と体調不良。
まれな反応(この薬を使用している患者の 0.01% 未満で発生します)
間質性肺疾患。
非常にまれな反応(この薬を使用している患者の 0.001% 未満で発生します)
血管外漏出。
未知の反応
重度の出血(血小板減少症を伴う)。
頻度不明(自発的な症例報告からのイベント)
- 重度の腹痛、吐き気、吐血、黒色便または血便(胃腸穿孔の症状の可能性あり)。
- 口内炎、嚥下困難、腹痛、吐き気、嘔吐、下痢、血便。これらは、口、胃、腸の内層の炎症(粘膜炎症)の兆候や症状である可能性があります。
これらの症状が 1 つ以上発生した場合は、すぐに医師に相談してください。症状が悪化した場合、またはここに記載されていない症状に気づいた場合は、医師に相談してください。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。また、顧客サービスを通じて会社に通知してください。
エボテカンの特別集団
妊娠
エボテカンは前臨床研究で胚と胎児に有害な影響を与えることが示されています。
他の細胞毒性(つまり細胞に有害な)化学療法薬と同様、エボテカンも妊婦に投与すると胎児に害を及ぼす可能性があります。エボテカン服用中は妊娠を避け、妊娠した場合は直ちに医師に知らせてください。
この薬は医師のアドバイスなしに妊婦が使用しないでください。妊娠が疑われる場合は、すぐに医師に知らせてください。

エボテカンの成分
注射可能な Evotecan の各バイアルには次のものが含まれています。
|
トポテカン(塩酸塩の形) |
4.0mg |
|
賦形剤* |
1バイアル |
※マンニトール、酒石酸、塩酸または水酸化ナトリウム(pH調整用)。
エボテカンのプレゼンテーション
注射可能な凍結乾燥粉末。 4 mg の有効成分を含む 1 つのバイアルを包装。
投与経路: 静脈内使用。
18歳以上の成人向けご利用となります。
参照医薬品と同等の類似医薬品。
エボテカンの過剰摂取
兆候と症状
エボテカンの静脈内投与を受けた患者では、過剰摂取(処方量の最大 10 倍)が報告されています。過剰摂取の主な合併症は、骨髄における血球の産生の減少(骨髄抑制)です。過剰摂取で観察される兆候と症状は、エボテカンに関連する既知の副作用と一致しています。さらに、過剰摂取後の肝臓酵素の上昇と粘膜炎が報告されています。
処理
エボテカンの過剰摂取に対する既知の解毒剤はありません。患者のケアは、臨床上の適応症または国立毒物センターからの推奨事項があれば、それに従う必要があります。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
エボテカンの薬物相互作用
特定の医薬品や食品はエボテカンと相互作用し、その作用を妨げます。
エボテカンを服用している間は、これらを使用したくない場合があります。彼らです:
- 他の細胞傷害性薬剤(パクリタキセルやエトポシドなど)。
- 白金含有薬剤(シスプラチンまたはカルボプラチンなど)。
- ABCB1 および ABCG2 阻害剤 (エラクリダールなど)。
したがって、他の薬を服用している場合、または最近服用した場合は、医師に知らせてください。処方箋なしで使用しているものについても話してください。医師はあなたの薬を見直して、エボテカンの服用中に使用できないものが使用されていないことを確認します。これらの薬のいずれかが必要で、代替品がない場合は、医師に相談してください。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
エボテカンという物質の作用
有効性の結果
臨床研究
小細胞肺がん
第一選択治療に感受性があった再発小細胞肺癌におけるIVトポテカンとCAV治療レジメン(シクロホスファミド、ドキソルビシン、ビンクリスチン)に関する比較研究(SKamp;F 104864/090)では、数値的により高い奏効率が得られたトポテカン使用時 (22%; 95% CI: 15; 30) と CAV (15%; 95% CI: 8; 22) の比較。すべての放射線学的反応は独立して検証されました。
感受性は、治療を行わない 3 か月の間隔として定義されました。採用を促進するために、この定義は治療を行わない 60 日間の間隔に変更されました。奏効期間の中央値(トポテカンで14週間、CAVで15週間)、増悪までの時間(トポテカンで13週間、CAVで12週間)、生存期間(トポテカンで25週間、CAVで22週間)はどちらも同様であった。治療法。肺がん患者症状評価スケールによると、トポテカンで治療を受けた患者は、呼吸困難、咳、胸痛、食欲不振、睡眠障害、嗄れ声、疲労感、日常生活活動の妨害などの症状のCAVのより大きな軽減を報告しており、次のような重大な結果が得られました。呼吸困難、嗄れ声、疲労、日常生活の妨害との関係。
CAV で治療された患者では、統計的に有意ではありませんが、喀血が大幅に軽減されました。以下に挙げる症状が悪化するまでの時間は、トポテカンで治療された患者のほうがCAVを受けた患者よりも数値的に長かった(つまり、悪化が遅れた):呼吸困難、食欲不振、睡眠障害、日常活動の障害、声がれ、疲労感が顕著であったが、呼吸困難や食欲不振などの症状を引き起こします。胸痛が悪化するまでの時間は、IV トポテカン治療と CAV 治療では同様でしたが、喀血との関係では数値的には長かったです。
CAVを伴う(臨床中止日1997年5月30日)。
研究 SKamp;F 104864/090 の有効性データは、1998 年 3 月 20 日の 2 回目の臨床中止日に基づいて更新されました。定性的には、有効性データは変更されず、応答率 (トポテカン 24.3% 対 18.3%) のわずかな数値更新のみでした。 CAV の場合)および生存期間中央値(トポテカンの場合は 25 週間、CAV の場合は 24.77 週間)。
卵巣癌
再発卵巣癌におけるIVトポテカン(n=112)とIVパクリタキセル(n=114)の比較研究(SKamp;F 104864/039)では、トポテカンのほうが数値的に高い奏効率(20.5%、CIは95%)でした。 : 13.1-28.0)、パクリタキセル (14%; 95% CI: 7.7-20.4) と比較した。治療間の差は 6.5% (95% CI: -3.3-16.3) でした。
すべての放射線学的反応は独立して検証されました。反応期間の中央値はトポテカンで25.9週間、パクリタキセルで21.6週間でした。進行までの期間の中央値は、トポテカン群で18.9週間(95% CI: 12.1-23.6)、パクリタキセル群で14.7週間(95% CI: 11.9-18.3)でした。生存期間の中央値は、トポテカン群で63.0週間(95% CI: 46.6-71.9)、パクリタキセル群で53週間(95% CI: 42.3-68.7)でした。
知らせ:
すべてのデータは、治療意図 (ITT) 集団分析値を示しています。
子宮頸がん
婦人科腫瘍グループ (GOG 0179) が実施したランダム化比較第 III 相研究では、子宮頸癌ステージ IV の治療において、トポテカンとシスプラチンの併用療法 (n=147) とシスプラチン単独療法 (n=146) が比較されました。 B、再発性または持続性の子宮で、手術および/または放射線による治癒療法が適切ではないと考えられています。シスプラチンまたは他の細胞傷害性薬剤による一次化学療法を受けた患者はいなかった。トポテカンとシスプラチンの併用治療を受けたグループの全体的な奏効率は 24% で、シスプラチン単独療法を受けたグループで達成された 12% よりも有意に高かった (p=0.0073)。
トポテカンとシスプラチンの併用療法群、またはシスプラチン単独療法群の完全奏効率は、それぞれ10%と3%でした。この観察は、2.9か月[(範囲:2.6~3.5); p=0.026] および全生存期間 [9.4 か月 (範囲: 7.9 ~ 11.9) 対 6.5 [(範囲: 5.8 ~ 8.8); p=0.033]トポテカンとシスプラチンの併用治療群では、シスプラチン単独投与群と比較した。トポテカンとシスプラチンの併用治療を受けたグループの1年生存率は40.4%(95% CI: 32.2-48.5)であったのに対し、シスプラチンのみを投与されたグループでは28%(95% CI: 20.6-35.4)でした。 。 2年生存率は、両方の患者集団でそれぞれ11.9%(95% CI: 5.5-18.3)および7.1%(95% CI: 2.0-12.2)でした。健康関連の生活の質(HrQoL)の二次評価項目は、次に従って分析されました。
がん治療における簡単な痛みのインベントリの機能評価 – 子宮頸がんおよびUNISCALE。
HrQoL 評価は、無作為化前、治療サイクル 2 および 5 の前、および無作為化の 9 か月後に実施されました。シスプラチン単独療法と比較して、トポテカンとシスプラチンの併用で観察された血液毒性の増加は、患者の HrQoL 転帰を有意に低下させませんでした。
統合された安全性データ
安全性データは、5,583 サイクルのトポテカンを受けた再発肺がん患者 631 人と再発卵巣がん患者 523 人の統合データセットとして示されています。
血液学的データ
好中球減少症
サイクル 1 中の重度 (好中球数 0.5×109/リットル未満) は患者の 55% で観察され、患者の 21% で 7 日以上持続し、全体の患者の 76% (サイクルの 39%) で観察されました。 。重度の好中球減少症に関連して、発熱または感染症がサイクル 1 中に患者の 11% で発生し、全体では患者の 18% (サイクルの 5%) で発生しました。重度の好中球減少症が発症するまでの平均期間は9日、中央値は7日でした。重度の好中球減少症は、サイクルの 11% で合計 7 日以上続きました。臨床研究で治療を受けた全患者(重度の好中球減少症患者と重度の好中球減少症がない患者を含む)のうち、11%(コースの4%)が発熱し、26%(コースの9%)が感染症を発症した。さらに、治療を受けた全患者の 5% (サイクルの 1%) が敗血症を発症しました。
血小板減少症
患者の25%(サイクルの8%)で重度(CTC基準のv1で定義されている血小板数が25×109/リットル未満)。中等度、患者の 25% (サイクルの 15%) における血小板数が 25.0 ~ 50.0×109/リットルの間であると定義されます。重度の血小板減少症が出現するまでの平均期間は 15 日、中央値は 5 日でした。
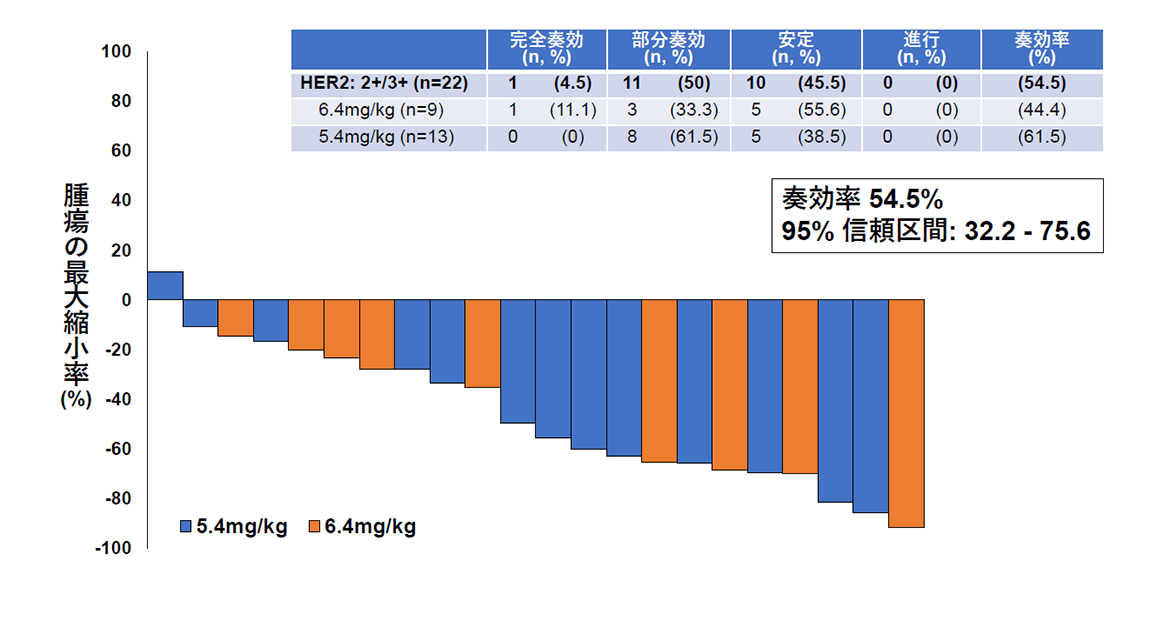
血小板輸血はサイクルの 4% で行われました。腫瘍出血による死亡例を含む、血小板減少症に関連する重大な後遺症の報告はまれでした。
貧血: 患者の 37% (サイクルの 14%) が中等度から重度 (Hb 8.0 g/dL 未満)。赤血球輸血は患者の 52% (サイクルの 21%) で実施されました。
非血液学的データ
頻繁に報告される非血液学的影響は、吐き気 (52%)、嘔吐 (32%)、下痢 (19%)、便秘 (9%)、口内炎 (15%) などの胃腸管に関連したものでした。重度の吐き気、嘔吐、下痢、口内炎(グレード3または4)の発生率は、それぞれ4%、3%、2%、1%でした。
軽度の腹痛も患者の 4% で報告されました。
トポテカンによる治療中に、患者の約 25% で疲労が観察され、16% で無力症が観察されました。重度の疲労の発生率は 3% で、重度の無力症 (グレード 3 または 4) の発生率も同様でした。
完全または顕著な脱毛症が患者の 30% で観察され、部分的脱毛症が 15% で観察されました。
患者に発生し、トポテカンによる治療に関連する、または関連する可能性があるとして記録されたその他の事象は、食欲不振 (13%)、倦怠感 (4%)、および高ビリルビン血症 (1%) でした。
発疹、蕁麻疹、血管浮腫、アナフィラキシー反応などの過敏反応の報告はまれでした。臨床研究では、患者の 4% で発疹、1.5% でそう痒症が報告されました。
薬理学的特徴
薬力学特性
作用機序
トポテカンの抗腫瘍活性には、複製運動が始まる前にねじれ張力を弱めるため、DNA 複製に密接に関与する酵素であるトポイソメラーゼ I の阻害が含まれます。トポテカンはトポイソメラーゼ I を阻害し、酵素の共有結合複合体と触媒機構の中間体である DNA 鎖の切断を安定化します。トポテカンによるトポイソメラーゼ I の阻害によって引き起こされる細胞損傷は、一本鎖 DNA 切断に関連するタンパク質の誘導です。
薬物動態学的特性
吸収
注射剤には適用されません。
分布
トポテカンは、体内水分の約 3 倍に相当する大量の分布量(約 132 L)を持ち、半減期は 2 ~ 3 時間と短い。薬物動態パラメーター間の比較により、5 日後の薬物動態に変化がないことが示唆されました。
トポテカンの血漿タンパク質への結合は低く (35%)、血球と血漿間の分布は均一でした。
血漿クリアランスと分布量は、女性よりも男性の方がわずかに高いことが報告されています。ただし、その違いの大きさは体表面積の違いほどではありませんでした。
代謝
トポテカンの不活化の主な経路は、不活性なカルボン酸形態への pH 依存性の可逆的な開環です。
代謝によるトポテカンの除去は 10% 未満です。細胞ベースのアッセイで親化合物と同等またはそれより低い活性を示した N-デスメチル代謝物が、尿、血漿、および糞便中に見つかりました。 IV投与後、親化合物の代謝産物の平均AUC割合は、総トポテカンおよびトポテカンラクトンについて10%未満であった。トポテカンの O-グルクロニドと N-デスメチル トポテカンが尿中に同定されました。

インビトロでは、トポテカンはシトクロム P450 酵素 CYP1A2、CYP2A6、CYP2C8/9、CYP2C19、CYP2D6、CYP2E、CYP3A または CYP4A もヒト細胞質酵素のジヒドロピリミジンデヒドロゲナーゼまたはキサンチンオキシダーゼも阻害しませんでした。
排除
トポテカン塩酸塩の IV 投与後、血漿濃度は二指数関数的に減少しました。 IV トポテカンの薬物動態は用量に比例します。毎日の反復投与による各トポテカン製剤の蓄積はほとんどまたはまったくなく、複数回投与による薬物動態の変化の証拠はありません。
トポテカンを毎日 30 分間の点滴として 0.5 ~ 1.5 mg/m2 の用量で 5 日間 IV 投与した後、トポテカンは肝臓の血流の約 2/3 に相当する高いクリアランス (64 リットル/時間) を示しました。
トポテカンを 1 日 5 回投与した後の薬物関連物質の総回収量は、投与量の 71% ~ 76% (IV) でした。約 51% が総トポテカンとして、2.5% が N-デスメチル トポテカンとして尿中に除去されました。
トポテカンの糞便排泄は投与量の 18% に寄与しましたが、N-デスメチル トポテカンの糞便排泄は約 1.5% でした。全体として、N-デスメチル代謝物は、尿および糞便中に回収された薬物関連物質全体の平均 7% 未満 (範囲: 4% ~ 9%) に寄与していました。尿中に検出されたトポテカン O-グルクロニドおよびトポテカン N-デスメチル O-グルクロニドの濃度は、用量の 2% 以下でした。
トポテカンをシスプラチンと組み合わせて投与した場合(1日目にシスプラチン、1~5日目にトポテカン)、トポテカンクリアランスは1日目と比較して5日目に減少しました:21.3リットル/h/m2に対して19.1リットル/h/m2。集団研究では、グラニセトロン、オンダンセトロン、モルヒネ、またはコルチコステロイドの同時投与は、トポテカンの薬物動態に重大な影響を与えていないようです。
特殊な集団
集団研究では、年齢、体重、腹水などのいくつかの要因がトポテカンクリアランスに有意な影響を示さなかった。
子供たち
小児集団におけるトポテカンの薬物動態は、2~7.5 mg/m²/日の用量で24時間連続点滴を受ける小児、または0.75~1.95 mg/m²/日の用量で72時間連続点滴を受けた小児で研究されました。どちらの研究でも、クリアランスは同じ用量を使用した成人で観察されたクリアランスと同様でした。
腎不全
腎不全患者における IV トポテカンの血漿クリアランス (クレアチニン クリアランス 40 ~ 60 mL/min) は、対照患者と比較して約 67% に減少しました。分布量はわずかに減少したため、半減期は 14% しか増加しませんでした。中等度の腎障害のある患者では、トポテカン血漿クリアランスが対照患者で記録された値の 34% に減少しました。分布量も約 25% 減少し、その結果、平均半減期が 1.9 時間から 4.9 時間に延長されました。
肝不全
肝障害患者(血清ビリルビン1.5~10mg/mL)におけるIV投与後のトポテカンラクトンの血漿クリアランスは、対照患者群と比較して約67%に減少した。トポテカンの半減期は約 30% 増加しましたが、分布量に明らかな変化は観察されませんでした。肝障害のある患者における総トポテカンの血漿クリアランスは、対照群の患者と比較してわずか 10% 増加しました。
Evotecan ストレージ ケア
Evotecan の未開封のバイアルは、元のパッケージに入れて光から保護し、10°C ~ 25°C の温度で保管した場合、製造日から 24 か月間安定です。
注射用水での再構成の準備後、エボテカン溶液は 25°C の温度で 24 時間物理化学的に安定であり、光から保護されます。示されているように 5% 生理食塩水またはグルコース溶液で希釈した後、エボテカン溶液は、光から保護しなくても 25°C の温度で 24 時間物理的および化学的に安定です。微生物学的観点から、輸液製剤は直ちに使用する必要があります。この製剤をすぐに使用しない場合、使用前の保管時間と条件はユーザーの責任であり、通常は再構成から室温で 24 時間を超えてはならず、検証および管理された無菌条件下で行われます。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた薬は使用しないでください。
元のパッケージに入れて保管してください。

薬の特徴
バイアルには、淡黄色から緑がかった黄色の間の色の粉末が入っています。再構成後の溶液の色は、無色からわずかに黄色がかった色まで変化します。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かない場所に保管する必要があります。
Evotecan の法的声明
MS – 1.2110.0344
担当薬剤師:
エディナSM中村
CRF-SP No.9,258
登録者:
Wyeth Indústria Farmacêutica Ltda.
アレクサンドル デュマ通り、1,860
CEP 04717-904
サンパウロ – SP
CNPJ番号 61.072.393/0001-33
製造元:
ファルマコ ウルグアヨ SA
Avenida Dámaso Antonio Larrañaga, 4479
モンテビデオ、ウルグアイ
輸入者:
Wyeth Indústria Farmacêutica Ltda.
プレジデンテ カステロ ブランコ ハイウェイ、番号 32,501、km 32.5
CEP 06696-000
イタペビ/SP
使用は病院に限定されます。
医師の処方箋に基づいて販売されています。








-1024x576.jpg?resize=1024,576&ssl=1)


