ノボミックスはどのように機能しますか?
糖尿病は、血糖値を制御するために体が十分なインスリンを生成しない病気です。 NovoMix 30 は血糖濃度を低下させます。 NovoMix 30 は、30/70 の比率で即効性と持続性の両方を備えた最新のインスリン (インスリン類似体) です。現代のインスリンはヒトインスリンの改良版です。
この薬は塗布後 10 ~ 20 分で血糖値が下がり始め、塗布後 1 ~ 4 時間で最大効果に達し、最長 24 時間持続します。
NovoMix 30 は、経口抗糖尿病薬と組み合わせて使用できます。
ノボミックス 30 の禁忌
NovoMix 30 は使用しないでください。
- インスリン アスパルトまたは製品の成分のいずれかに対してアレルギー (過敏症) がある場合。
- 低血糖の症状(低血糖の症状)がある場合。
- インスリン注入ポンプにおいて。
- カートリッジまたはカートリッジを含むアプリケーションシステムが落下、損傷、または粉砕された場合。
- 正しく保管されていなかった場合、または冷凍されていた場合。
- 再懸濁後、インスリンが均一に白く乳状でない場合。
- 再懸濁後に材料の顆粒が存在する場合、または固体の白い粒子がカートリッジの底または壁に付着している場合。
この薬は10歳未満の子供には禁忌です。
ノボミックス30の使い方
インスリンの必要性について医師や看護師に相談してください。
NovoMix 30 Penfill は常に医師の処方に従って使用し、医師の指示に従ってください。
NovoMix 30 を経口糖尿病治療薬と組み合わせて使用する場合は、用量を調整する必要があります。
医師がインスリンの種類またはブランドを別のものに変更した場合、投与量の調整が必要になる場合があります。医師のアドバイスなしにインスリンの投与量を変更しないでください。
低血糖を避けるため、注射後10分以内に炭水化物を含む食事または軽食を摂取してください。
通常、NovoMix 30 は食事前に投与されます。必要に応じて、食後すぐにご使用いただけます。
特別な集団
腎臓や肝臓の機能が低下している場合、または 65 歳以上の場合は、より定期的に血糖値を測定し、インスリン投与量の変更について医師と相談する必要があります。
- NovoMix 30 を使用する前に:
- ラベルをチェックして、正しい種類のインスリンであることを確認してください。
- ゴムプランジャーを含むカートリッジを常に確認してください。目に見える損傷がある場合、またはゴム製プランジャーとラベルの白いストリップの間に隙間がある場合は、カートリッジを使用しないでください。これはインスリン漏れの結果である可能性があります。カートリッジが破損していると思われる場合は、販売元に返品してください。詳細については、アプリケーション システムの取扱説明書を参照してください。
- 汚染を避けるため、注射のたびに必ず新しい針を使用してください。
- ニードルと NovoMix 30 Penfill は共有しないでください。
このインスリンをどこでどのように使用するか:
NovoMix 30 は皮膚の下 (皮下) に塗布する必要があります。インスリンを静脈や筋肉に直接注射しないでください。
注射のたびに同じ領域内の注射部位を常に交互に行うことで、しこりや皮膚病変が発生するリスクが軽減されます。
注射を受けるのに最適な場所は次のとおりです。
腰の前(腹部)、お尻、太ももの前、または腕の上部。インスリンを腰の前部に注射すると、より早く効きます。
血糖値を定期的に測定する必要があります。
使用説明書
インスリンの再懸濁:
再懸濁できるように、カートリッジ内に少なくとも 12 単位のインスリンが残っていることを確認します。 12 個未満の場合は、新しいカートリッジを使用してください。
新しいカートリッジを使用するたびに (アプリケーション システム内にカートリッジを配置する前に):
使用前にインスリンを室温に戻してください。これにより、再懸濁が容易になります。
- カートリッジを手のひらで10回転がします。カートリッジを水平に保つことが重要です (図 A を参照)。
- カートリッジを「a」と「b」の位置の間で 10 回上下に動かします (図 B を参照)。ガラス球がカートリッジの一方の端からもう一方の端に移動します。
- 液体が均一に白く乳白色になるまで、回転と移動の手順を繰り返します (図 A および B を参照)。再懸濁後に液体が均一に白く乳白色にならない場合は、インスリンを使用しないでください。
- 他の申請手順をすぐに完了してください。
各注射について:
カートリッジを中に入れた状態で、塗布システムを「a」と「b」の位置の間で上下に動かします (図 B を参照)。液体が均一に白く乳白色になるまで、少なくとも 10 回動かします。
他の申請手順をすぐに完了してください。
このインスリンの注射方法は次のとおりです。
- インスリンを皮下に注射します。医師または看護師のアドバイスを受け、注入システムのマニュアルに記載されている注入技術を使用してください。
- 針を皮膚の下に少なくとも 6 秒間押し続けます。針が皮膚から外されるまで、注射ボタンを完全に押したままにしてください。これにより、正しく適用され、血液が針やインスリンカートリッジに入るのを防ぎます。
- 注射後は必ず針を取り外して廃棄し、NovoMix 30 は針を付けずに保管してください。
- そうしないと、液体が漏れて不正確な投与量が発生する可能性があります。
カートリッジを再充填しないでください。
NovoMix 30 Penfill は、ノボ ノルディスクのインスリン送達システムおよび針と併用するように設計されています。 NovoMix 30 Penfill と別のインスリン カートリッジを使用して治療を受ける場合は、インスリンの種類ごとに 1 つの送達システムを使用する必要があります。
予防措置として、カートリッジの紛失または破損に備えて、予備の Penfill カートリッジを常に携帯してください。
投与量
NovoMix 30 の投与量は個別であり、患者のニーズに応じて決定されます。
2 型糖尿病患者において、経口糖尿病薬単独では血糖コントロールが不十分な場合、ノボミックス 30 を単独療法として、または経口抗糖尿病薬と併用して投与できます。 2 型糖尿病患者の場合、NovoMix 30 の投与量を開始する推奨量は、朝食時に 6 単位、夕食 (夕食) 時に 6 単位です。 NovoMix 30 は、1 日 1 回、夕食時に 12 U を摂取して開始することもできます。 NovoMix 30 を 1 日 1 回使用する場合、通常、30 単位に達したら 1 日 2 回に切り替え、朝食と夕食に等量に分けて使用することをお勧めします。
NovoMix 30 による 1 日 3 回の投与計画は、朝の用量を午前と昼食の用量に分割することで、1 日 2 回の投与計画から安全に開始できます。
用量調整には次の滴定ガイドが推奨されます。
|
食前の血糖値 |
用量調整 |
|
|
lt; 4.4ミリモル/L |
lt; 80mg/dL |
– 2U |
|
4.4~6.1ミリモル/L |
80 – 110 mg/dL |
0 |
|
6.2~7.8ミリモル/L |
111 – 140 mg/dL |
+2U |
|
7.9~10mmol/L |
141 – 180 mg/dL |
+4U |
|
gt; 10ミリモル/L |
gt; 180mg/dL |
+6U |
過去 3 日間の最も低い食前レベルを使用する必要があります。この 3 日間の間に低血糖が起こった場合は、用量を増量すべきではありません。 HbA1C 目標に達するまで、用量調整は週に 1 回行うことができます。食前血糖値は、前回の投与量が適切であるかを評価するために使用する必要があります。
1 型糖尿病患者の場合、個人のインスリン必要量は通常 0.5 ~ 1.0 単位/kg/日であり、この必要量は NovoMix 30 によって部分的または完全に満たされます。
1日の必要量は、インスリン抵抗性のある患者(肥満などによる)では高く、内因性インスリンが残存している患者では低くなります。
別のインスリンからの移行:
治療をヒトインスリンプレミックスから NovoMix 30 に移行する場合は、同じ投与計画から開始してください。次に、個々のニーズに応じて用量を調整します (上の表の滴定ガイドラインを参照)。
お年寄り:
NovoMix 30 は高齢の患者でも使用できます。ただし、75 歳以上の患者において OAD と NovoMix 30 を併用した経験は限られています。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。医師の知識なしに治療を中止しないでください。
NovoMix 30 を使用するのを忘れた場合はどうすればよいですか?
NovoMix 30 の塗布を忘れると、血糖値が高くなりすぎる可能性があります (これを高血糖といいます)。
高血糖の危険信号は徐々に現れます。
これらには次のものが含まれます。
排尿量の増加、喉の渇き、食欲不振、気分の悪さ(吐き気または嘔吐)、眠気または疲労感、皮膚の乾燥および紅潮、口渇、果物のような口臭(ケトン体)。
これらは、糖尿病性ケトアシドーシス(体が糖の代わりに脂肪を使用するため、血液中に酸が蓄積すること)と呼ばれる非常に重篤な状態の兆候である可能性があります。この状態が治療されないと、糖尿病性昏睡や死に至る可能性があります。上記の兆候のいずれかを経験した場合は、血糖値を測定し、可能であれば尿のケトン体検査を行って、すぐに医師の診察を受けてください。
高血糖は次の場合にも発生する可能性があります。
- 十分なインスリンを注射していない。
- 必要以上に少ないインスリンを繰り返し注射する。
- 感染症または発熱がある。
- いつもよりたくさん食べる。
- いつもより運動量を減らしてください。
インスリンの使用を中止した場合:
これは重度の高血糖やケトアシドーシスを引き起こす可能性があります。医師に相談せずにインスリンの使用をやめないでください。医師は何をする必要があるかを教えてくれます。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
ノボミックス30の注意事項
インスリンの使用を開始する前に、リーフレット全体をよく読んでください。
このリーフレットは大切に保管してください。さらに質問がある場合は、もう一度読んで、医師、看護師、または薬剤師に問い合わせてください。
この薬はあなた専用に処方されています。自分と同じ症状であっても害を及ぼす可能性がありますので、他の人に渡さないでください。

このリーフレットに記載されていない副作用であっても、何らかの副作用が発生した場合は、医師、看護師、または薬剤師に相談してください。
以下の場合は、NovoMix 30 に特に注意してください。
- 腎臓、肝臓、副腎、下垂体、甲状腺に問題がある。
- 通常よりも運動量が多い場合、または血糖値に影響を与える可能性があるため、通常の食事を変更する場合。
- 病気の場合は、インスリンの使用を継続し、医師に相談してください。
- 海外旅行の際、タイムゾーンの異なる場所に移動すると、インスリンの必要性や注射時間に影響が出る可能性があります。旅行を計画している場合は医師に相談してください。
妊娠と授乳
妊娠中または妊娠を計画している場合は、医師にご相談ください。妊娠中の NovoMix 30 の臨床経験は限られています。妊娠中および出産後には、インスリン投与量の調整が必要になる場合があります。糖尿病の慎重な管理、特に低血糖の予防は、赤ちゃんの健康にとって重要です。
授乳中のノボミックス 30 による治療には制限はありません。
妊娠している場合は、インスリンの使用を中止せず、医師の診断または歯科医のアドバイスを受けてください。
この薬は、医師または歯科外科医のアドバイスなしに妊娠中の女性が使用すべきではありません。
運転と機械の使用
血糖値が高いか低い場合、集中力や反応力が低下する可能性があり、その結果、機械の運転や操作能力が低下する可能性があります。あなたや他の人に危険をもたらす可能性があるすべての状況において、このことを念頭に置いてください。運転または機械の操作ができる場合は、医師に相談してください。
- 低血糖が頻繁に起こる場合。
- 低血糖を認識することが難しい場合。
小児人口
NovoMix 30 は、インスリンの事前混合が必要な 10 歳以上の小児および青少年に使用できます。 6 歳から 9 歳の小児については、臨床研究によるデータが限られています。
この薬はドーピングを引き起こす可能性があります。
主な薬物相互作用
多くの薬は血糖値に影響を与えるため、インスリンの投与量を変更する必要がある可能性があります。処方されていない薬であっても、ノボミックス 30 以外の薬を服用している場合、または最近服用した場合は、医師または薬剤師に相談してください。インスリン治療に影響を与える可能性のある最も一般的な薬剤を以下に示します。
以下の薬のいずれかを使用すると、血糖値が低下する(低血糖)可能性があります。
- 糖尿病の治療のためのその他の薬。
- モノアミンオキシダーゼ阻害剤(MAOI)(うつ病の治療に使用)。
- ベータ遮断薬(高血圧の治療に使用されます)。
- アンジオテンシン変換酵素 (ACE) 阻害剤 (特定の心臓病または高血圧の治療に使用されます)。
- サリチル酸塩(痛みを和らげ、熱を下げるために使用されます)。
- アナボリックステロイド(テストステロンなど)。
- スルホンアミド(感染症の治療に使用されます)。
以下の薬を使用すると、血糖値が上昇する(高血糖)可能性があります。
- 経口避妊薬(避妊用)。
- チアジド類(高血圧および体液貯留の治療に使用されます)。
- 糖質コルチコイド(炎症の治療に使用される「コルチゾン」など)。
- 甲状腺ホルモン(甲状腺疾患の治療に使用されます)。
- 交感神経興奮薬(喘息の治療に使用されるエピネフリン [アドレナリン]、またはサルブタモール、テルブタリンなど)。
- 成長ホルモン (成長を刺激し、体の代謝プロセスに大きな影響を与える薬)。
- ダナゾール(排卵に作用する薬)。
- オクトレオチドとランレオチド(先端巨大症、通常は中年の成人に発生し、下垂体による成長ホルモンの過剰産生によって引き起こされる稀なホルモン疾患の治療に使用されます)は、血糖値を上昇または低下させる可能性があります。
- ベータ遮断薬(高血圧の治療に使用されます)は、低血糖を認識するのに役立つ早期警告症状を軽減または完全に排除できます。
- チアゾリジンジオン (2 型糖尿病の治療に使用される経口抗糖尿病薬の一種)。長年の 2 型糖尿病、心臓病、または以前の脳卒中を患い、インスリンと組み合わせてチアゾリジンジオンで治療されている一部の患者は、心不全を発症する可能性があります。息切れ、体重の急激な増加、局所的な腫れ(浮腫)などの心不全の兆候がある場合は、できるだけ早く医師に伝えてください。
NovoMix 30 をアルコールと併用する場合:
アルコールを飲むと、血糖値が上昇または下降するため、インスリンの必要性が変化する可能性があります。注意深く監視することをお勧めします。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
ノボミックス 30 に対する副作用
他の薬と同様に、NovoMix 30 は副作用を引き起こす可能性がありますが、すべての患者がこれらの影響を経験するわけではありません。
非常に一般的な反応 (この薬を使用している患者の 10% 以上で発生します):
低血糖(低血糖)。
まれな反応 (この薬を使用している患者の 0.1% ~ 1% に発生):
アレルギーの兆候:
塗布部位に反応(痛み、発赤、蕁麻疹、腫れ、かゆみ、炎症)が起こる場合があります(局所アレルギー反応)。これらの反応は通常、インスリンを使用してから数週間後に消失します。消えない場合は医師の診察を受けてください。
すぐに医師の診察を受けてください。
- アレルギーの兆候が体の他の部分に広がった場合。または
- 突然気分が悪くなり、汗をかき始め、気分が悪くなり(嘔吐)、呼吸困難になり、心拍が速くなり、めまいを感じる場合があります。
- 視覚障害: インスリン治療を初めて開始するときは、視覚障害を経験することがありますが、通常は反応が消えます。
注射部位の変化 (リポジストロフィー):
適用部位の皮膚の下の脂肪(脂肪)組織は、減少(脂肪萎縮)または増加(脂肪肥大)します。
塗布するたびに注射部位を変えることで、こうした皮膚の変化が起こるリスクを軽減できます。注射部位の皮膚の跡や肥厚に気づいた場合は、医師または看護師に知らせてください。その部位に注射すると、これらの反応が悪化したり、インスリンの吸収が変化したりする可能性があります。
関節の腫れ:

インスリンの使用を開始すると、体液貯留により足首やその他の関節の周囲に浮腫(腫れ)が生じることがあります。通常、この状況はすぐに消えます。
糖尿病性網膜症(視力喪失を引き起こす可能性のある糖尿病に関連した眼疾患):
糖尿病性網膜症で血糖値の改善が早すぎると、網膜症が悪化する可能性があります。
この件については医師に相談してください。
まれな反応 (この薬を使用している患者の 0.01% ~ 0.1% で発生):
痛みを伴う神経障害(糖尿病に伴う神経損傷による痛み):
血糖値の改善が早すぎると、痛みが生じることがあります。これは急性疼痛性神経障害と呼ばれ、通常は一時的なものです。
非常にまれな反応 (この薬を使用している患者の 0.01% 未満で発生します):
NovoMix 30 またはその成分の 1 つに対する重度のアレルギー反応 (全身性アレルギー反応と呼ばれます)。
副作用が悪化した場合、またはこの説明書に記載されていない副作用に気付いた場合は、医師、看護師、または薬剤師に相談してください。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。
また、顧客サービスを通じて会社に通知してください。
ノボミックス 30 の構成
注射可能な懸濁液の各 mL には次のものが含まれます。
組換え DNA 技術によって生成された 100 U のインスリン アスパルト (30% 可溶性インスリン アスパルトおよび 70% のプロタミン化インスリン アスパルト)。
賦形剤:
グリセリン、フェノール、メタクレゾール、塩化亜鉛、塩化ナトリウム、第二リン酸ナトリウム二水和物、硫酸プロタミン、水酸化ナトリウム、塩酸および注射用水。 1 つのカートリッジには 300 U に相当する 3 mL が含まれています。
ノボミックス30の過剰摂取
大量のインスリンを投与すると、血糖値が低くなりすぎることがあります(これを低血糖といいます)。これは次の場合にも発生する可能性があります。
- 食べる量が少なすぎる場合、または食事を逃した場合。
- いつもより運動量が多い場合。
- アルコールを飲む場合。
低血糖の警告サインは突然現れる場合があり、次のようなものがあります。
冷や汗、冷たくて青白い肌、頭痛、心拍数の上昇、倦怠感、過度の空腹感、視力の一時的な変化、眠気、異常な疲労感や脱力感、神経過敏や震え、不安感、見当識障害の感覚、集中力の低下。
低血糖の症状が現れた場合は、砂糖を多く含む食べ物を食べて血糖値を測定してください。
血糖値が非常に低い場合は、ブドウ糖の錠剤やその他の糖分の多い食品(お菓子、クッキー、フルーツジュース)を食べて休息してください。
必要に応じて、ブドウ糖の錠剤、お菓子、ビスケット、またはフルーツジュースを常に携帯してください。
低血糖の症状が消えたり、血糖値が安定したら、インスリン治療を続けます。
家族や友人に、自分が糖尿病であること、および低血糖時の失神(意識不明)のリスクを含め、その影響について伝えてください。失神した場合は、側に回って直ちに医師の診察を受けるように伝えてください。窒息する可能性があるため、食べ物や飲み物を与えてはいけません。
訓練を受けた人がグルカゴンというホルモンを注射すると、意識不明からより早く回復することができます。グルカゴン注射を受けた場合は、意識が戻ったらすぐにブドウ糖または甘い食べ物が必要になります。グルカゴン治療に反応しない場合は、病院で治療を受ける必要があります。
- 重度の低血糖が治療されない場合、脳損傷(一時的または永久的)を引き起こし、場合によっては死に至る可能性があります。
- 失神を引き起こす低血糖症のエピソードがある場合、またはグルカゴン注射が必要な場合、または低血糖症のエピソードが数回ある場合は、医師に相談してください。インスリンの投与量や投与回数、食事、運動などを調整する必要がある場合があります。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。
さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
ノボミックス 30 の薬物相互作用
いくつかの薬剤がグルコース代謝と相互作用することが知られています。
以下の物質は患者のインスリン必要量を減らす可能性があります
- 経口抗糖尿病薬;
- モノアミンオキシダーゼ阻害剤 (MAOI);
- ベータブロッカー;
- アンジオテンシン変換酵素 (ACE) 阻害剤。
- サリチル酸塩;
- アナボリックステロイド;
- スルホンアミド。
以下の物質は患者のインスリン必要量を増加させる可能性があります
- 経口避妊薬;
- チアジド類;
- グルココルチコイド;
- 甲状腺ホルモン;
- 交感神経興奮薬;
- 成長ホルモン;
- ダナゾール。
ベータ遮断薬は低血糖の症状を隠す可能性があります。
オクトレオチド/ランレオチドは、インスリン必要量を増減させる可能性があります。
ノボミックス 30 フードインタラクション
アルコールはインスリンの血糖降下作用を強化または低下させる可能性があります。
ノボミックス 30 物質の作用
有効性の結果
大人
成人 1 型糖尿病患者におけるインスリン アスパルト (活性物質) とノボリン R ®の安全性と有効性を比較するために、2 件の非盲検、実薬コンパレーター管理による 6 か月間の安全性と有効性の研究が実施されました。
研究デザインと結果は非常に類似していたので、示されたデータは 1 つの研究のみからのものです (表 1 を参照)。
インスリンアスパルト(活性物質)は食事の直前に皮下投与され、通常のヒトインスリンは食事の30分前に皮下投与された。
NPH ヒトインスリンは、基礎インスリンとして 1 日 1 回または分割用量で投与されました。
HbA 1cの変化と重度の低血糖の発生率(第三者の介入を必要とする事象の数によって決定される)は、この研究(表 1)および前述の他の臨床研究における 2 つの治療法間で同等でした。
糖尿病性ケトアシドーシスは、成人研究および治療グループのいずれにおいても報告されていません。
表 1: 1 型糖尿病患者におけるインスリン アスパルト (活性物質) の皮下投与 (24 週間; n=882) 2
|
インスリン アスパルト(原体) + NPH インスリン |
ノボリン R + NPH インスリン |
|
|
N |
596 | 286 |
|
初期 HbA 1c (%)* |
7.9±1.1 | 8.0±1.2 |
|
初期 HbA 1cからの変化 (%) |
-0.1±0.8 | 0.0±0.8 |
|
平均 HbA 1cにおける治療間の差異 (95% 信頼区間) |
-0.2 (-0.3、-0.1) | |
|
初回インスリン投与量 (IU/Kg/24 時間)* |
0.7±0.2 | 0.7±0.2 |
|
研究終了時のインスリン投与量 (IU/Kg/24 時間)* |
0.7±0.2 | 0.7±0.2 |
|
重度の低血糖症患者 (n, %)* * |
104 (17%) | 54 (19%) |
|
初期体重(kg)* |
75.3±14.5 | 75.9±13.1 |
|
初期重量変化量(Kg)* |
0.5±3.3 | 0.9±2.9 |
※数値は平均値±SDです。
**重度の低血糖症とは、中枢神経系の症状を伴い、他の人の介入や入院が必要となる低血糖症を指します。
2 型糖尿病患者におけるインスリン アスパルト (活性物質) と通常のヒト インスリンの安全性と有効性を比較するために、非盲検、実薬コンパレーター管理の 6 か月間の安全性と有効性の研究が実施されました (表 2)。
インスリンアスパルト(活性物質)は食事の直前に皮下投与され、通常のヒトインスリンは食事の30分前に皮下投与された。
NPH ヒトインスリンは、基礎インスリンとして 1 日 1 回または分割用量で投与されました。
HbA 1cの変化と重度の低血糖の発生率(第三者の介入を必要とする事象の数によって決定される)は、両方の治療法で同等でした。
表 2: 2 型糖尿病患者におけるインスリン アスパルト (活性物質) の皮下投与 (6 か月; n=176) 3
|
インスリンアスパルト(有効成分)+NPHインスリン |
ノボリン R + NPH インスリン |
|
|
N |
90 | 86 |
|
初期 HbA 1c (%)* |
8.1±1.2 | 7.8±1.1 |
|
初期 HbA 1cからの変化 (%) |
-0.3±1.0 | -0.1±0.8 |
|
平均 HbA 1cにおける治療間の差異 (95% 信頼区間) |
-0.1 (-0.4、-0.1) | |
|
初回インスリン投与量 (IU/Kg/24 時間)* |
0.6±0.3 | 0.6±0.3 |
|
研究終了時のインスリン投与量 (IU/Kg/24 時間)* |
0.7±0.3 | 0.7±0.3 |
|
重度の低血糖症患者 (n, %)** |
9 (10%) | 5 (8%) |
|
初期体重(kg)* |
88.4±13.3 | 85.8±14.8 |
|
初期重量変化量(Kg)* |
1.2±3.0 | 0.4±3.1 |
※数値は平均値±SDです。
** 重度の低血糖とは、中枢神経系の症状を伴い、他の人の介入または入院が必要となる低血糖を指します。
小児人口
6歳から18歳までの1型糖尿病の小児および青少年(n = 283)を対象とした24週間の並行群間安全性および有効性研究では、1日複数回の皮下投与による2つの治療計画を比較しました:インスリンアスパルト(活性物質)(n = 187) または通常のヒトインスリン (n = 96)。
NPH インスリンを基礎インスリンとして投与しました。
インスリン アスパルト (活性物質) は、HbA 1cの変化によって測定されるように (表 3)、通常のヒト インスリンと同等の血糖コントロールを示し、両治療グループの低血糖発生率は同等でした。
インスリン アスパルト (活性物質) と通常のヒト インスリンの皮下投与は、2 ~ 6 歳の 1 型糖尿病の小児 (n = 26) を対象とした安全性と有効性の研究でも比較され、HbA 1cと低血糖に対して同様の効果が見られました。
表 3: 1 型糖尿病の小児におけるインスリン アスパルト (活性物質) の皮下投与 (24 週間; n=283) 4
|
インスリンアスパルト(有効成分)+NPHインスリン |
ノボリン R + NPH インスリン |
|
|
N |
187 | 96 |
|
初期 HbA 1c (%)* |
8.3±1.2 | 8.3±1.3 |
|
初期 HbA 1cからの変化 (%) |
0.1±1.0 | 0.1±1.1 |
|
平均 HbA 1cにおける治療間の差異 (95% 信頼区間) |
0.1 (-0.5、-0.1) | |
|
初回インスリン投与量 (IU/Kg/24 時間)* |
0.4±0.2 | 0.6±0.2 |
|
研究終了時のインスリン投与量 (IU/Kg/24 時間)* |
0.4±0.2 | 0.7±0.2 |
|
重度の低血糖症患者 (n, %)** |
11 (6%) | 9 (9%) |
|
糖尿病性ケトアシドーシス (n, %) |
10 (5%) | 2 (2%) |
|
初期体重(kg)* |
50.6±19.6 | 48.7±15.8 |
|
初期重量変化量(Kg)* |
2.7±3.5 | 2.4±2.6 |
妊娠
非盲検の無作為化安全性および有効性研究では、1 型糖尿病の妊婦 322 名を対象に、インスリン アスパルト (活性物質) (n = 157)と通常のヒト インスリン (n = 165) を比較しました。
対象となった患者の3分の2は、研究に参加した時点ですでに妊娠していた。
先天奇形の割合は、インスリン アスパルト (有効成分) では 5.7% でしたが、ヒト インスリンでは 7.3%でした。この差は統計的に有意ではありませんでした。
両グループの患者の 80% は妊娠中に平均 HbA 1cが 6.5% 未満に達し、母体の低血糖の発生率に有意差はありませんでした。
インスリン アスパルト (活性物質) は、夜間の低血糖現象を減らし、血糖値と血糖変動を効率的に軽減します。
約 2,000 人の患者を対象に対照臨床研究が実施され、インスリン アスパルト (活性物質) および (インスリン アスパルト (活性物質)) とヒト インスリンが比較されました。
インスリン アスパルト (活性物質) による強化療法は、6 か月の治療後に HbA 1cを評価した場合、1 型糖尿病患者においてヒト インスリンと比較して優れた代謝制御をもたらしました。
薬理学的特性
薬力学特性
作用機序
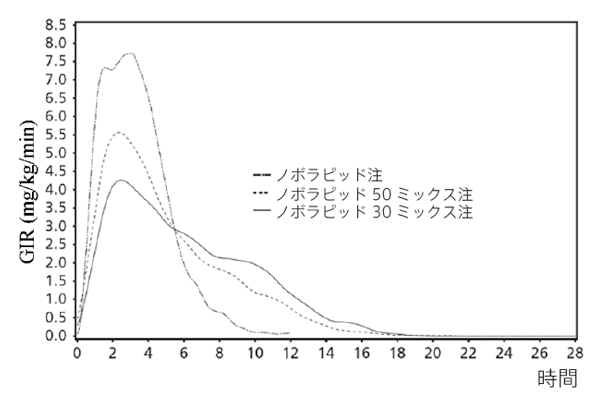
インスリン アスパルト (活性物質) は、食後 4 時間以内に評価した場合、通常のヒト インスリンと比較して作用の発現が速く、グルコース濃度も低下します。
インスリン アスパルト(活性物質)は、皮下注射後の通常のヒト インスリンと比較して作用時間が短くなります。
インスリン アスパルト(活性物質)を皮下注射すると、注射後 10 ~ 20 分で作用が現れます。
最大の効果は注射後1~3時間で発揮されます。
作用持続時間は3~5時間です。
インスリン アスパルト (活性物質) は、モル基準で通常のヒト インスリンと同等の効力があります。
大人
1 型糖尿病患者を対象とした臨床研究では、通常のヒト インスリンと比較した場合、インスリン アスパルト (活性物質) を使用すると食後血糖値が低いことが実証されました。
1 型糖尿病患者を対象とした 2 つの長期公開研究 (それぞれ 1,070 名と 884 名の患者からなる) では、インスリン アスパルト (活性物質) は糖化ヘモグロビンを 0.12 パーセント ポイント [95% CI 0.03;0.22] および 0.15 パーセント ポイント [95%] 減少させました。通常のヒトインスリンと比較した場合、CI 0.05;0.26]。大きな違いはありません。
お年寄り
インスリン アスパルト (活性物質) と通常のヒト インスリンを比較する二重盲検ランダム化クロスオーバー薬物動態学/薬力学研究が、2 型糖尿病の高齢患者 (65 ~ 83 歳の患者 19 名、平均年齢 70 歳) を対象に実施されました。
高齢者におけるインスリン アスパルト (活性物質) と通常のヒト インスリンの間の薬力学的特性 (最大GIR、AUCGIR、0 ~ 120 分) の相対的な差異は、健康なボランティアや若い糖尿病患者で観察されたものと同様でした。
子供と青少年
インスリン アスパルト (活性物質) を子供に投与すると、通常のヒト インスリンと比較して、同様の長期血糖制御が実証されました。
食前の通常のヒトインスリンとインスリンアスパルト(活性物質)および食後を比較する臨床研究が幼児(2歳から6歳の患者26名)を対象に実施され、単回投与の薬物動態学/薬力学研究が小児(6歳から12歳)を対象に実施されました。高齢者)およびティーンエイジャー(13 ~ 17 歳)。
小児におけるインスリン アスパルト (活性物質) の薬力学的プロファイルは、成人で観察されたものと同様でした。
1 型糖尿病患者を対象とした臨床研究では、通常のヒトインスリンと比較して、インスリン アスパルト (活性物質) を使用すると夜間低血糖のリスクが低下することが実証されました。

日中の低血糖のリスクは有意に増加しませんでした。
妊娠
1型糖尿病の妊婦の治療におけるインスリン アスパルト (活性物質)と通常のヒト インスリンの安全性と有効性を比較した臨床研究 (曝露された妊婦 322 名 (インスリン アスパルト (活性物質): 157 名、通常のヒト インスリン: 165 名)) ) は、インスリン アスパルト (活性物質) が妊娠または胎児/新生児の健康に及ぼす悪影響を示さなかった。
さらに、インスリン治療のアスパルト(活性物質)とヒトインスリン(インスリンアスパルト(活性物質):14名、通常のヒトインスリン:13名)に無作為に割り付けられた妊娠糖尿病の女性27名を含む臨床研究のデータは、以下の治療法と同様の安全性プロファイルを実証しました。また、インスリンアスパルテ(活性物質)で治療したグループでは、食後血糖値の制御が大幅に増加しました。
薬物動態学的特性
インスリン分子アスパルト (活性物質) では、通常のヒトインスリンで観察されるように、B28 位のプロリンアミノ酸がアスパラギン酸に置換されると、六量体形成の傾向が減少します。
したがって、インスリン アスパルテ (活性物質) は、通常のヒト インスリンと比較して皮下層からより速く吸収されます。
最大濃度に達するまでの時間は、平均して通常のヒトインスリンの半分です。
0.15 の皮下投与後、40 分以内に平均最大血漿濃度 492 pmol/L に達しました。








-1024x576.jpg?resize=1024,576&ssl=1)


