塩酸セフェピム(活性物質)は、成人において、セフェピムに感受性のある細菌によって引き起こされる以下に挙げる感染症の治療に適応されます。
- 肺炎 I および気管支炎IIを含む下気道感染症。
- 腎盂腎炎IIIおよび単純性尿路感染症IVを含む複雑性尿路感染症。
- 皮膚および皮膚構造の感染症V ;
- 腹膜炎VIおよび胆道感染症VIIを含む腹腔内感染症。
- 婦人科感染症VIII ;
- 敗血症IX 。
発熱性好中球減少症患者における実証的治療

セフェピム単独療法は、発熱性好中球減少症患者の経験的治療に適応されます。重篤な感染症のリスクが高い患者(例、最近の骨髄移植の既往がある患者、経過観察開始時から低血圧のある患者、潜在的な血液悪性腫瘍のある患者、または重度または長期の好中球減少症のある患者)では、抗菌薬の単独療法は使用できない場合があります。適切な。これらの患者に対するセフェピム単独療法の有効性を証明するにはデータが不十分です。塩酸セフェピム(活性物質)は、結腸および直腸の手術を受ける患者の外科的予防にも適応されます。
小児科への適応
塩酸セフェピム(活性物質)は、小児患者において、セフェピムに感受性のある細菌によって引き起こされる以下の感染症の治療に適応されます。
- 肺炎I;
- 腎盂腎炎 III および単純性尿路感染症IVを含む複雑性尿路感染症。
- 皮膚および皮膚構造の感染症V ;
- 敗血症IX;
- 細菌性髄膜炎XI 。
発熱性好中球減少症患者における実証的治療
セフェピム単独療法は、発熱性好中球減少症患者の経験的治療に適応されます。重篤な感染症のリスクが高い患者(例、最近の骨髄移植の既往がある患者、経過観察開始時から低血圧のある患者、潜在的な血液悪性腫瘍のある患者、または重度または長期の好中球減少症のある患者)では、抗菌薬の単独療法は使用できない場合があります。適切な。これらの患者に対するセフェピム単独療法の有効性を証明するにはデータが不十分です。
I CID J15.9 不特定の細菌性肺炎。
II ICD J40 急性または慢性として特定されていない気管支炎。
III ICD N10 急性尿細管間質性腎炎、急性腎盂腎炎。
III ICD N11 慢性尿細管間質性腎炎、慢性腎盂腎炎。
IV CID N39.0 不特定の場所の尿路感染症。
V CID L00-L08 – 皮膚および皮下組織の感染症。
VI CID K65.0 – 急性腹膜炎。
VII ICD K81 – 胆嚢炎。
VIII ICD N70-N74 – 女性の骨盤臓器の炎症性疾患。
IX CID A41.9 – 原因不明の敗血症。
X CID D70 – 無顆粒球症、好中球減少症。
XI CID G00.9 – 特定できない細菌性髄膜炎。
セフェピムに対する病原体の感受性を判断するために、適切な場合には培養および感受性試験を実施する必要があります。塩酸セフェピム(活性物質)による経験的治療は、感受性試験の結果が判明する前に開始できます。ただし、抗生物質による治療は、結果が得られ次第、その結果に応じて調整する必要があります。
グラム陽性菌およびグラム陰性菌に対する広範囲の殺菌活性により、塩酸セフェピム (活性物質) は、病原体を特定する前の単独療法として使用できます。好気性と嫌気性の混合感染のリスクがある患者では、特にセフェピムに感受性のない細菌が存在する場合、病原体が判明する前に抗嫌気性薬剤による最初の併用療法が推奨されます。
これらの結果が得られたら、微生物の感受性に応じて、塩酸セフェピム(活性物質)と他の抗感染症薬による併用療法が必要な場合もあれば、必要でない場合もあります。
塩酸セフェピムの禁忌 – Aurobindo Pharma
塩酸セフェピム(活性物質)は、製剤のいずれかの成分、セファロスポリン系の抗生物質、ペニシリン、または他のベータラクタム系抗生物質に対して過去に過敏症反応を示したことのある患者による使用は禁忌です。
塩酸セフェピムの使い方 – Aurobindo Pharma
塩酸セフェピム(活性物質)は筋肉内または静脈内に投与できます。
準備方法
塩酸セフェピム (活性物質) 粉末は、医療専門家が表 1 に記載されている希釈剤の量を使用して再構成する必要があります。使用する希釈剤は表の後に記載されています。

表 1: セフェピム塩酸塩溶液 (活性物質) の調製:
筋肉内投与 (IM) – 塩酸セフェピム (有効成分) 1g
希釈剤
注射用滅菌水、注射用0.9%塩化ナトリウム溶液、または注射用5%ブドウ糖溶液。
音量
3mL。
溶液の安定性
室温(15~30℃)で12時間、または冷蔵(2~8℃)で3日間。
推奨事項
臀部の上部外側四分円などの大きな筋肉塊への深部筋肉注射による投与。塩酸セフェピム(有効成分)を各臀部に1gを超えて注入しないでください。
静脈内投与 (IV) – 塩酸セフェピム (有効成分) 1 および 2g
直接静脈内投与
これは、重篤または生命を脅かす感染症を患っている患者、特にショックの可能性がある場合に推奨される投与経路です。
直接静脈内投与用希釈剤

注射用滅菌水、注射用5%ブドウ糖溶液、または注射用0.9%塩化ナトリウム溶液。
直接静脈内投与量
10mL。
直接静脈内投与のための溶液の安定性
室温(15~30℃)で12時間、または冷蔵(2~8℃)で3日間。
直接静脈内投与の推奨事項
得られた溶液は、3 ~ 5 分間静脈に直接注射するか、患者が適合する静脈内輸液を受けている間に投与セット チューブに注射する必要があります。
点滴静注
点滴静注用希釈剤
0.9%塩化ナトリウム、注射用5%ブドウ糖液、注射用5%塩化ナトリウム+ブドウ糖液、注射用乳酸リンゲル液。
点滴量
100mL。
点滴静注液の安定性
室温(15~30℃)で12時間、または冷蔵(2~8℃)で3日間。
点滴静注の推奨事項
直接 IV 投与について前述したように 1 g または 2 g の用量を再構成し、得られた溶液の適量を適合する静脈内輸液の 1 つを含む適切な容器に加えます。
得られた溶液は約 30 分間かけて投与する必要があります。
非経口薬は投与前に異物がないか目視検査する必要があり、異物が存在する場合は使用しないでください。
微生物学的観点から、薬剤の開封、再構成、希釈の方法によって汚染のリスクが排除できない場合、その製品は直ちに使用しなければなりません。
他のセファロスポリンと同様、塩酸セフェピム (有効成分) 粉末および再構成溶液は保管中に色が濃くなる場合がありますが、製品の効力は変わりません。
閉鎖系での塩酸セフェピム(活性物質)の調製

塩酸セフェピム (活性物質) は、以下に説明するように、静脈内注入による適用の場合にのみ、バッグに入っている 0.9% NaCl 溶液で希釈する必要があります。
組み立て
- 上方に円を描くように動かすか、親指で後方に押して、Ar Plus コネクタから黄色のカバーを取り外します。
- 希釈液バッグをバイアルに接続します。
- チューブの基部を持ってコネクタを半分に折り、Ar Plus コネクタのシールを剥がします。
移行
- 粉末が完全に希釈されるまで、液体の一部を袋からアンプル瓶に移します。
- 溶液をバイアルから希釈剤バッグに移し、バッグを締めたり緩めたりして、形成された真空により液体がバッグの内側に戻ります。
- システムが開いてしまうため、バイアルをバッグから外さないでください。
- バタフライ (1) のイージーオフ ボタンを回して輸液セットを接続し、セット チップ (2) でチューブの内膜を破ります。
知らせ:
希釈後は薬剤を追加しないでください。
- 約 30 分間製品を投与します。
- 再構成後、塩酸セフェピム (活性物質) 密閉系は室温 (15 ~ 30 ℃) で 12 時間、または冷蔵下 (2 ~ 8 ℃) で 3 日間安定です。
互換性
塩酸セフェピム溶液 (活性物質) およびほとんどのベータラクタム系抗生物質は、物理的および化学的不適合性のため、メトロニダゾール、バンコマイシン、ゲンタマイシン、硫酸トブラマイシンまたは硫酸ネチルマイシンの溶液と併用すべきではありません。
ただし、塩酸セフェピム(活性物質)との併用療法が必要な場合は、これらの抗生物質をそれぞれ個別に投与できます。
投与量
塩酸セフェピム(活性物質)は静脈内または筋肉内に投与できます。投与量と投与経路は、感染症の重症度、腎機能、患者の全身状態によって異なります。
体重40kgを超える成人および小児患者
腎機能が正常で体重 40kg 以上の成人および小児患者における塩酸セフェピム (活性物質) の用量ガイドを表 8 に示します。
表 7: 正常な腎機能を持つ体重 40kg を超える成人および小児患者に対する推奨用量計画*:
|
感染の重症度 |
用量と投与経路 |
用量範囲 |
| 軽度から中等度の尿路感染症 | 500mg~1g IVまたはIM |
12時間ごと |
| 尿路感染症以外の軽度から中等度の感染症 | 1g IVまたはIM |
12時間ごと |
| 重篤な感染症 | 2g Ⅳ |
12時間ごと |
| 非常に重篤な感染症または生命を脅かす感染症 | 2g Ⅳ |
12時間ごと |
*通常の治療期間は7〜10日間です。ただし、より重篤な感染症の場合は、より長い治療が必要になる場合があります。
発熱性好中球減少症の経験的治療の場合、通常の治療期間は少なくとも 7 日間、または好中球減少症が解消するまでである必要があります。
外科的予防法(成人)
結腸および直腸の手術を受ける患者の感染予防に推奨される用量は以下のとおりです。
最初の外科的切開の 60 分前に塩酸セフェピム (活性物質) 2g IV の単回投与を開始します。メトロニダゾール 500 mg IV を 1 回、塩酸セフェピム (活性物質) の注入終了直後に投与する必要があります。
メトロニダゾールは、製品の公式リーフレットに従って調製および投与する必要があります。
相溶性がないため、塩酸セフェピム (有効成分) とメトロニダゾールを同じ容器内で混合しないでください。メトロニダゾールを注入する前に、静脈内投与セットを互換性のある液体ですすぐことをお勧めします。
初回の予防投与後 12 時間以上外科手術が続く場合は、初回の予防投与の 12 時間後に 2 回目の塩酸セフェピム (活性物質) を投与し、続いてメトロニダゾールを投与する必要があります。
腎機能が正常な小児患者に一般的に推奨される用量
肺炎、尿路感染症、皮膚および皮膚構造の感染症
生後2か月以上で体重40kg以下の小児患者には、12時間ごとに50mg/kgを10日間投与することが推奨されます。
より重篤な感染症の場合は、投与間隔を 8 時間空けることもできます。
敗血症、細菌性髄膜炎および発熱性好中球減少症の経験的治療
生後 2 か月以上で体重 40kg 以下の小児患者には、8 時間ごとに 50mg/kg を 7 ~ 10 日間投与することが推奨されます。
生後 2 か月未満の小児患者に対する塩酸セフェピム (有効成分) の使用経験は限られています。
この経験は 50mg/kg の用量を使用して達成されましたが、生後 2 か月を超える患者で得られた薬物動態データは、生後 1 ~ 2 か月の患者には 8 時間または 12 時間ごとに 30mg/kg の用量を考慮してもよいことを示唆しています。
生後 2 か月を超える患者の場合は 50mg/kg、生後 1 か月から 2 か月までの患者の場合は 30mg/kg の用量は、成人の 2g の用量に相当します。
これらの患者に対する塩酸セフェピム(活性物質)の投与は注意深く監視する必要があります。
体重が40kgを超える小児患者には、成人の推奨用量が適用されます。
小児患者に対する推奨用量は、成人に対する最大推奨用量(8時間ごとに2g)を超えてはなりません。小児患者への筋肉内投与の経験は限られています。
腎機能障害のある患者に対する一般的に推奨される用量
腎機能障害のある患者では、腎排泄率の低下を補うためにセフェピムの用量を調整する必要があります。
軽度から中等度の腎障害のある患者に対するセフェピムの推奨初回用量は、正常な腎機能を持つ患者と同じである必要があります。
成人腎不全患者におけるセフェピムの推奨維持量を表 8 に示します。
血清クレアチニン測定のみが利用可能な場合、次の式 (Cockcroft-Gault 方程式) を使用してクレアチニンクリアランスを推定できます。血清クレアチニンは腎機能の正常な状態を表します。
腎機能障害のある男性
クレアチニンクリアランス(mL/分) = 体重 (kg) x (140 歳) / 72 x 血清クレアチニン (mg/dL)。
腎機能障害のある女性
0.85 × 男性の計算式を使用して計算された値。
表 8 腎機能障害のある成人患者における推奨維持用量スケジュール*:
*薬物動態モデルは、これらの患者には用量の減量が必要であることを示しています。
血液透析を受けており、セフェピムを併用している患者の場合、セフェピムの投与量は次のとおりです。
治療初日は負荷用量としてセフェピム1g、発熱性好中球減少症を除くすべての感染症に対して2日目以降は1日あたり500mgを投与し、その用量は1日あたり1gである。透析日には透析後にセフェピムを投与する必要があります。
可能な限り、セフェピムは毎日同じ時間に投与する必要があります。
透析を受けている患者さん
血液透析を受けている患者では、透析開始時に体内に存在するセフェピムの総量の約 68% が、3 時間の透析中に除去されます。
外来で持続腹膜透析を受けている患者には、正常な腎機能を持つ患者に推奨されているのと同じ用量、つまり感染症の重症度に応じてセフェピムを500mg、1g、または2gで投与できますが、投与間隔をあけます。 48時間。
腎機能障害のある小児患者
小児患者におけるセフェピムの主な排泄経路は尿中排泄であるため、この集団では塩酸セフェピム(活性物質)の用量の調整を考慮する必要があります。
表 8 で以前に推奨したように、同じように投与間隔を増やしたり、投与量を減らしたりする必要があります。血清クレアチニン値のみが利用可能な場合は、次のいずれかの方法を使用してクレアチニンクリアランスを推定できます。
クレアチニンクリアランス(mL/分/1.73m²) =
または
クレアチニンクリアランス(mL/分/1.73m²) =
肝機能障害のある患者に対する一般的に推奨される用量
肝機能に変化がある患者には用量調整は必要ありません。
このプレゼンテーションの安全性と有効性を確保するため、注射用塩酸セフェピム (活性物質) は推奨されない経路で投与すべきではありません。投与は静脈内または筋肉内にのみ行う必要があります。
塩酸セフェピムの予防措置 – Aurobindo Pharma
腎不全(クレアチニンクリアランス≧50mL/分)による尿量の減少、または腎機能を損なう可能性のあるその他の状態などの腎機能障害のある患者では、尿量の低下を補うために塩酸セフェピム(活性物質)の用量を調整する必要があります。腎臓の除去。
腎機能障害や腎機能を損なう可能性のあるその他の症状のある患者では、通常の用量で抗生物質の血清中濃度が高濃度かつ長期間に渡って上昇する可能性があるため、そのような患者にセフェピムを投与する場合は維持用量を減量する必要があります。
継続用量は、腎機能障害の程度、感染症の重症度、病原体の感受性によって決定する必要があります。
市販後の経験では、以下の重篤な有害事象が報告されています。
可逆性脳症(混乱、幻覚、眠気、昏睡などの意識障害)、ミオクローヌス、発作(非けいれん性てんかん重積状態を含む)、および/または腎不全。
ほとんどの症例は、推奨量を超える用量の塩酸セフェピム(活性物質)を投与された腎機能障害患者で発生しました。
一般に、神経毒性症状はセフェピムの中止後および/または血液透析後に解消されましたが、これらの症例の一部は致命的でした。
何らかのアレルギー、特に薬物に対してアレルギーを示した患者には、抗生物質を慎重に投与する必要があります。
塩酸セフェピム(有効成分)によりアレルギー反応が発生した場合は、投薬を中止し、適切な治療を行ってください。
重度の過敏反応の場合は、エピネフリンまたはその他の支持療法の投与が必要になる場合があります。
他の抗生物質と同様、塩酸セフェピム (活性物質) を使用すると、非感受性微生物が異常増殖する可能性があります。
治療中に重複感染が発生した場合は、適切な措置を講じる必要があります。クロストリジウム・ディフィシル(DACD)に関連する下痢は、塩酸セフェピム(活性物質)を含む実質的にすべての抗菌剤の使用で報告されており、軽度の下痢から致死的な大腸炎まで重症度はさまざまです。
抗生物質の使用後に下痢を呈するすべての患者において DACD を考慮する必要があります。
CDAD は抗菌薬投与後 2 か月以内に発症することが報告されているため、病歴には注意が必要です。
CDAD が疑われるか確認された場合は、 C. ディフィシルに対して直接作用しない抗生物質の継続使用を中止する必要がある場合があります。
アミノグリコシドや強力な利尿薬など、腎毒性の可能性がある薬剤を塩酸セフェピム(活性物質)と同時に投与する場合は、腎機能を注意深く監視する必要があります。
塩酸セフェピム(活性物質)による治療を開始する前に、患者が以前にセフェピム、セファロスポリン、ペニシリン、または他の薬剤に対して即時型過敏反応を起こしたことがあるかどうかを判断するために、慎重な分析を実施する必要があります。
ペニシリンに過敏な患者にこの製品を処方する場合は、β-ラクタム系抗生物質との交差過敏症が報告されており、ペニシリンアレルギーの病歴を持つ患者の最大10%で発生する可能性があるため、慎重に投与する必要があります。
塩酸セフェピム(有効成分)に対するアレルギー反応が生じた場合は、この薬による治療を中止する必要があります。
重篤な急性過敏症反応には、エピネフリンによる治療や、臨床的に適応のある酸素、コルチコステロイド、静脈内輸液、静脈内抗ヒスタミン薬、アミノプレッサー、気道モニタリングなどの緊急措置が必要となる場合があります。
車両の運転や機械の操作能力への影響
車両を運転したり機械を操作したりする患者に対する塩酸セフェピム(活性物質)の影響は研究されていません。
ただし、意識状態の変化、めまい、混乱、幻覚などの副作用が発生し、機械の運転や操作に影響を与える可能性があります。
発がん、突然変異誘発、生殖能力障害
発がん性の可能性を評価するための長期にわたる動物実験は行われていません。
遺伝毒性に関するin vitroおよびin vivo試験により、セフェピムには遺伝毒性がないことが示されました。
ラットでは生殖能力の障害は観察されませんでした。
妊娠
マウス、ラット、ウサギでの生殖研究では、胎児への害の証拠は示されていません。しかし、妊婦を対象とした適切でよく管理された研究はありません。
動物の生殖研究は常に人間の反応を予測できるわけではないため、この薬は明らかに必要な場合にのみ妊娠中に使用する必要があります。
妊娠リスクカテゴリー:B.
この薬は、医師または歯科外科医のアドバイスなしに妊娠中の女性が使用すべきではありません。
授乳中
セフェピムは非常に低濃度で母乳中に排泄されます。
セフェピムは授乳中の女性には細心の注意を払って投与する必要があります。
小児用
塩酸セフェピム (有効成分) の乳児および小児における安全性は、成人で観察される安全性と同様です。
高齢者向けの使用
臨床研究で塩酸セフェピム(有効成分)による治療を受けた6,400人以上の成人のうち、35%が65歳以上、16%が75歳以上でした。
臨床研究では、一般に推奨される成人用量を投与された高齢者患者は、腎不全でない限り、非高齢成人患者の臨床有効性と安全性と同等の臨床有効性と安全性を示しました。
若い人と比較すると、排泄半減期がわずかに長くなり、腎クリアランス値が低くなりました。
腎機能が損なわれている場合は、用量の調整が推奨されます。
セフェピムは腎臓から実質的に排泄されることが知られており、腎機能に障害のある患者ではこの薬剤に対する毒性反応のリスクがより高くなる可能性があります。
高齢患者は腎機能が低下している可能性が高いため、用量の選択には注意が必要であり、腎機能を監視する必要があります。
可逆性脳症(錯乱、幻覚、眠気、昏睡などの意識障害)、ミオクローヌス、発作(非けいれん性てんかん重積状態を含む)、腎不全などの重篤な有害事象が、腎機能障害のある高齢者患者において通常用量で発生しています。セフェピム。
塩酸セフェピムの副作用 – Aurobindo Pharma
セファロスポリン系抗生物質については、次の有害事象と臨床検査の変化が報告されています。
スティーブンス・ジョンソン症候群、多形紅斑、中毒性表皮壊死融解症、中毒性腎症、再生不良性貧血、溶血性貧血、出血、および偽陽性の尿糖検査。
臨床経験
臨床研究 (=5598) では、最も一般的な有害事象は胃腸症状と過敏反応でした。
塩酸セフェピム(原体)に関する有害事象は以下のとおりです。
一般的な副作用 (この薬を使用している患者の 1% ~ 10% で発生します)
- IV 注入部位での反応は患者の 5.2% で発生しました。これらの反応には静脈炎 (2.9%) が含まれていました。
- 塩酸セフェピム (活性物質) の筋肉内投与は非常に良好な忍容性を示しました。適用部位に痛みや炎症があった患者はわずか 2.6% でした。
- 皮膚の発疹 (1.8%);
- 下痢 (1.2%)。
まれな副作用 (この薬を使用している患者の 0.1% ~ 1% で発生)
- そう痒症と蕁麻疹は過敏反応でした。
- 吐き気、嘔吐、口腔カンジダ症、大腸炎(偽膜性大腸炎を含む)は胃腸反応でした。
- 発熱、膣炎、紅斑も他の反応でした。
- 頭痛は中枢神経系の反応でした。
まれな副作用 (この薬を使用している患者の 0.01% ~ 0.1% で発生します)
- 腹痛;
- 便秘;
- 血管拡張;
- 呼吸困難;
- めまい;
- IV 注入部位の炎症 (0.1%);
- 感覚異常;
- 性器のかゆみ;
- 味の変化。
- 寒気;
- 非特異的カンジダ症。
非常にまれな発生率 (0.05% 未満) で発生する臨床的に重要な事象には、アナフィラキシーや発作が含まれます。
小児および乳児における塩酸セフェピム (有効成分) の安全性プロファイルは成人の場合と同様です。
臨床検査
正常なベースライン値を持つ患者の臨床研究中に発生した臨床検査異常は一時的なものでした。 1% ~ 2% の頻度で発生したものは次のとおりです。
- アラニンアミノトランスフェラーゼの上昇 (3.6%);
- アスパラギン酸アミノトランスフェラーゼ (2.5%);
- アルカリホスファターゼ、総ビリルビン、貧血、好酸球増加症、プロトロンビン時間の延長、部分トロンボプラスチン時間(2.8%)、および溶血を伴わないクームス試験陽性(18.7%)。
- 血漿尿素窒素および/または血清クレアチニンの一過性の上昇と一過性の血小板減少症が患者の 0.5% ~ 1% で観察されました。
- 一過性の白血球減少症および好中球減少症も見つかりました (<0.5%)。
市販後の経験 – ファーマコビジランス
セフェピムを用いた北米臨床研究中に報告された事象に加えて、世界規模のマーケティング経験中に以下の有害事象が報告されています。
このクラスの他の薬剤と同様に、脳症(錯乱、幻覚、眠気、昏睡などの意識障害からなる重篤な副作用)、けいれん、ミオクローヌス、および/または腎不全が報告されています。
ほとんどの症例は、推奨量を超える用量の塩酸セフェピム(活性物質)を投与された腎機能障害患者で発生しました。他のセファロスポリンと同様に、アナフィラキシーショック、一過性白血球減少症、好中球減少症、無顆粒球症、血小板減少症などのアナフィラキシー反応が報告されています。
有害事象が発生した場合は、健康監視通知システム (NOTIVISA) または州または地方自治体の健康監視機関に通知してください。
塩酸セフェピムの薬物相互作用 – Aurobindo Pharma
アミノグリコシド系抗生物質の腎毒性および聴器毒性の可能性が増加するため、高用量のアミノグリコシド(アミカシンやゲンタマイシンなど)を塩酸セフェピム(活性物質)とともに投与する場合は、腎機能を注意深く監視する必要があります。
他のセファロスポリンとフロセミドなどの強力な利尿薬を併用した場合、腎毒性が報告されています。
臨床検査における相互作用
尿中のブドウ糖に対する偽陽性反応は、銅還元検査 (ベネディクト、フェーリング液、またはクリニテスト* 錠剤) では発生する可能性がありますが、糖尿の酵素検査 (クリニスティックス* など) では発生しません。
*FDA (アメリカ合衆国食品医薬品局) に登録された商標所有者: Bayer Healthcare llc.
塩酸セフェピムという物質の作用 – Aurobindo Pharma
有効性の結果
発熱性好中球減少症患者
発熱性好中球減少症患者に対するセフェピムによる経験的単独療法の安全性と有効性は、セフェピムによる単独療法(8時間ごとに2gの投与、IV)とセフタジジムによる単独療法(8時間ごとに2gの投与、 IV)。これらの研究は317人の患者を対象に実施されました。
表 1 は、評価可能な患者集団の特徴を示しています。
表 1: 評価可能な患者の人口統計 (最初のエピソードのみ):
|
セフェピム (n=164) |
セフタジジム (n=153) |
|
|
平均年齢(歳) |
56 (範囲 18 ~ 82) | 55 (範囲 16 ~ 84) |
| 男性 | 86 (52%) | 85 (56%) |
| 女性 | 78 (48%) | 68 (44%) |
| 白血病 | 65 (40%) | 52 (34%) |
| その他の血液悪性腫瘍 | 43 (26%) | 36 (24%) |
| 固形腫瘍 | 54 (33%) | 56 (37%) |
| CAN は最下位を意味します (セル/?L) | 20.0 (0 ~ 500 の範囲) | 20.0 (0 ~ 500 の範囲) |
| 好中球減少症の平均持続期間 (日) | 6.0 (範囲 0 ~ 39) | 6.0 (範囲 0 ~ 32) |
| 留置静脈カテーテル | 97 (59%) | 86 (56%) |
| 抗生物質による予防 | 62 (38%) | 64 (42%) |
| 骨髄の腐敗 | 9 (5%) | 7 (5%) |
| パスlt;入口で90mmHg | 7 (4%) | 2 (1%) |
できる =
好中球の絶対数。
SBP = 最高血圧。
表 2 は、観察された臨床反応率を示しています。
測定されたすべての結果について、セフェピムはセフタジジムと治療上同等でした。
表 2: 発熱性好中球減少症患者における経験的治療に対するプールされた奏効率:
|
測定結果 |
セフェピメ |
セフタジジム |
| 最初のエピソードは治療を変更することなく解決し、新たな発熱エピソードや感染症はなく、治療を補完するために経口抗生物質の使用が許可されました。 | 51 | 55 |
| 最初のエピソードは治療を変更することなく解決し、新たな発熱エピソードや感染症はなく、治療後に経口抗生物質は使用されませんでした。 | 34 | 39 |
| 治療の変更の許可を得て生存 | 93 | 97 |
| 初期症状は治療を変更することなく解決し、治療を補うために経口抗生物質の使用が許可されました | 62 | 67 |
| 最初のエピソードは治療を変更することなく解決し、治療後に経口抗生物質は使用されませんでした | 46 | 51 |
重篤な感染症のリスクが高い患者(最近骨髄移植の既往歴がある患者、経過観察開始時から低血圧のある患者、潜在的な血液悪性腫瘍のある患者、または重篤な感染症のある患者を含む)におけるセフェピム単独療法の有効性を裏付けるにはデータが不十分である。または長期の好中球減少症)。
敗血症性ショック患者に関するデータはない。
外科的予防
この適応症は、結腸直腸手術を受ける19歳以上(平均年齢66歳)の患者を対象とした無作為化非盲検多施設臨床試験に基づいており、手術前にセフェピム2gを単回IV投与する。塩酸塩(活性物質)に続いてメトロニダゾール500mgを単回IV投与した場合(N=307)と、セフトリアキソン2gに続いてメトロニダゾールを単回IV投与した場合(N=308)を比較した。
用量投与は、最初の外科的切開の0時間から3時間前まで変化した。
臨床成功率(手術後 6 週間の腹腔内および手術部位の感染の不在)は、各治療グループで 75% でした。
薬理学的特徴
注射用溶液用塩酸セフェピム (活性物質) 粉末は、筋肉内 (IM) または静脈内 (IV) 投与用の広範囲のセファロスポ性抗生物質です。塩酸セフェピム(有効成分)は、塩酸セフェピム(有効成分)とL-アルギニンの無菌混合物です。
ワルギニンは、およそ 725mg/g セフェピマの濃度で添加され、再構成溶液の pH を 4.0 ~ 6.0 に制御します。
薬物動態学的特性
健康な成人男性において、500mg、1g、および2gの30分間の個別の静脈内注入または筋肉内注射後のさまざまな時点で観察されたセフェピムの中程度の血漿濃度を表3にまとめます。
表 3 健康な成人男性患者における平均セフェピム濃度 (μg/mL):
吸収
筋肉内投与後、セフェピマは完全に吸収されます。
分布
組織および特定の体分泌物中のセフェピマ濃度を表 4 に示します。
セフェピマと血清タンパク質の関係は平均 16.4% であり、ホエイ濃度には依存しません。
表 4 健康な成人男性患者における身体変動 (μg/ml) および組織中のセフェピムの平均濃度 (μg/g):
代謝
セフェピムは代謝されて n-メチルピロリジンとなり、すぐに n-オキシドに変換されます。未変化セフェピマの尿中回収率は、投与量の約 85% に相当します。尿中には未変化のセフェピマ濃度が高く検出されます。
投与量の 1% 未満が n-メチルピロリジンとして尿から回収され、6.8% が n-オキシドとして、2.5% がセフェピムのエピマーとして回収されます。
排除
セフェピマ除去の平均半減期は約 2 時間で、250 mg ~ 2 g の用量では変化しません。
9日間、8時間ごとに最大2gのIV投与を受けた健康な人には蓄積は見られませんでした。
総身体クリアランスは 120ml/分です。
セフェピマの平均腎臓クリアランスは 110ml/分であり、セフェピマがほぼ排他的に腎臓機構、主に糸球体濾過によって除去されることを示唆しています。
特別な集団
嚢胞性線維症患者の急性肺感染症の悪化の治療において、セフェピム塩酸塩(活性物質)を使用して臨床的改善が実証されました(n = 24、平均年齢15歳、5〜47歳)。
抗菌療法は、この患者集団で細菌学的根絶を達成しない可能性があります。
嚢胞性線維症患者のセフェピム薬物動態では、臨床的に関連する変化は観察されませんでした。
腎不全
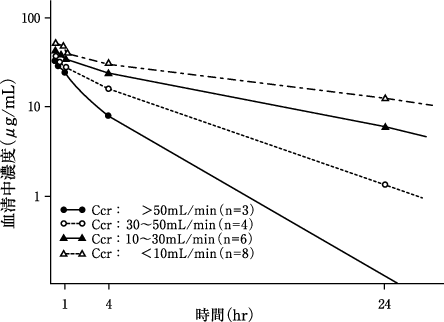
腎不全の程度がさまざまな患者では、除去の半減期が延長され、総肉体クリアランスとクレアチニンクリアランスの間に線形関係があります。
これは、この患者グループの用量調整の推奨の基礎として機能します。
透析が必要な重度の機能障害のある患者の平均半減期は、血液透析で13時間、継続的な外来腹膜透析で19時間です。
肝不全
セフェピマの薬物動態は、1Gの単回投与を受けた肝機能障害のある患者では変わらないままでした。
この患者集団では、セフェピム塩酸塩(活性物質)の用量を変更する必要はありません。
高齢の患者さん
若い患者と比較した場合、1g IVの1g IVのセフェピマ塩酸塩(活性物質)を1回投与したヘルシーボランティアは、セフェピマ塩酸塩(活性物質)を1回投与し、より大きな曲線(AUC)値と小腎クリアランス値を持っていたことがわかった。
腎機能が損なわれている場合は、高齢患者の用量調整が推奨されます。
子供と青少年
複数の用量でのセフェピマの薬物動態と単回投与量の薬物動態は、IV注入またはIM注射によって投与された50mg/kgの用量を投与された2.1ヶ月から11.2歳の患者で評価されました。少なくとも48時間、8時間または12時間ごとに複数回投与されました。
1回のIV用量の後、平均肉体クリアランスは3.3ml/min/kgで、平均分布量は0.3 L/kgでした。
平均排除の半減期は1.7時間でした。変更されていないセフェピマの平均尿回回収は、投与された用量の60.4%であり、腎クリアランスは平均2.0ml/min/kgの主要な除去ルートでした。
複数回投与量IV後、平衡状態のセフェピムの培地血漿濃度は、最初の用量後の濃度と類似しており、繰り返し用量後の離散蓄積がありました。
乳児と子供の他の薬物動態パラメーターは、用量間の間隔(8時間または12時間)に関係なく、最初の用量とバランスの決定の間で違いはありませんでした。
また、異なる年齢の患者または男性と女性の患者の間に薬物動態の違いはありませんでした。
平衡状態でのIM注射後、平均血漿濃度は0.75時間後に得られました。
平衡状態でのIM注入後の平均最小濃度は6.0でしたか?
IM注射後の平均バイオアベイラビリティは82%でした。脳脊髄液および血漿中のセフェピムの濃度を表5に示します。
表5脳脊髄液(CSF)および血漿(PL)の濃度の平均(標準偏差-DP)、および乳児と子供のセフェピマLCR/PL指数*::
*3.1ヶ月から12歳、平均年齢(PD)2.6(3.0)年の患者。中枢神経系(CNS)感染の疑いがある患者は、8時間ごとに5〜20分のIV注入により投与されたセフェピム、50mg/kgで治療されました。セフェピマによる治療の2日目または3日目の注入の終了後、約0.5、1、2、4、8時間後に、選択された患者から血液およびLCRサンプルを収集しました。
その他
セフェピマの薬物動態は、嚢胞性線維症の患者の臨床的に有意な程度に変化していません。
この患者集団では、セフェピム塩酸塩(活性物質)の用量を調整する必要はありません。
薬力学特性
微生物学
セフェピマは、細菌細胞壁合成の阻害によって作用する細菌性剤です。
Cefepimaは、アミノグリコシドまたは第3世代のセファロスポリンに耐性があるほとんどの株を含む、多種多様なグラム陽性およびグラム陰性の細菌に対して幅広い活性を持っています。
Cefepimaは、ほとんどのベタラクタマによって高加水分解耐性があり、染色体化されたベタラクタマに対する親和性が低く、グラム陰性細菌細胞の急速な浸透を示しています。
大腸菌および腸骨炭積を使用した研究では、セフェピマはペニシリン結合タンパク質(PLP)3の最大親和性を示し、その後PLP 2、次にPLPの1aと1bが続きました。
PLP 2接続は、他の非経口セファロスポリンよりも有意に高い親和性で発生し、抗菌活性を増加させる可能性があります。
PLPの1Aおよび1Bによるセフェピマの中程度の親和性は、おそらくその総殺菌活性にも寄与しています。
セフェピマは、時間阻害関係(阻害曲線)の分析と、多種多様な細菌の最小細菌濃度(CBM)を決定することにより、殺菌性であった。
CBM / CIMインデックス(最小菌類濃度 /最小阻害濃度)は、分析されたすべてのグラム陽性およびグラム陰性種からの分離株の過半数(80%以上)で2以下でした。
相乗作用は、特に緑膿菌の分離株で、 in vitroアミノグリコシドで実証されています。セフェピマは、次の微生物のほとんどの株に対して活性でした。
微生物学 – グラム陽性の好気性
- 黄色ブドウ球菌(ベタラクタマーゼ産生株を含む);
- ブドウ球菌(ベタラクタマーゼ産生株を含む); </li








-1024x576.jpg?resize=1024,576&ssl=1)


