Euvax B はどのように機能しますか?
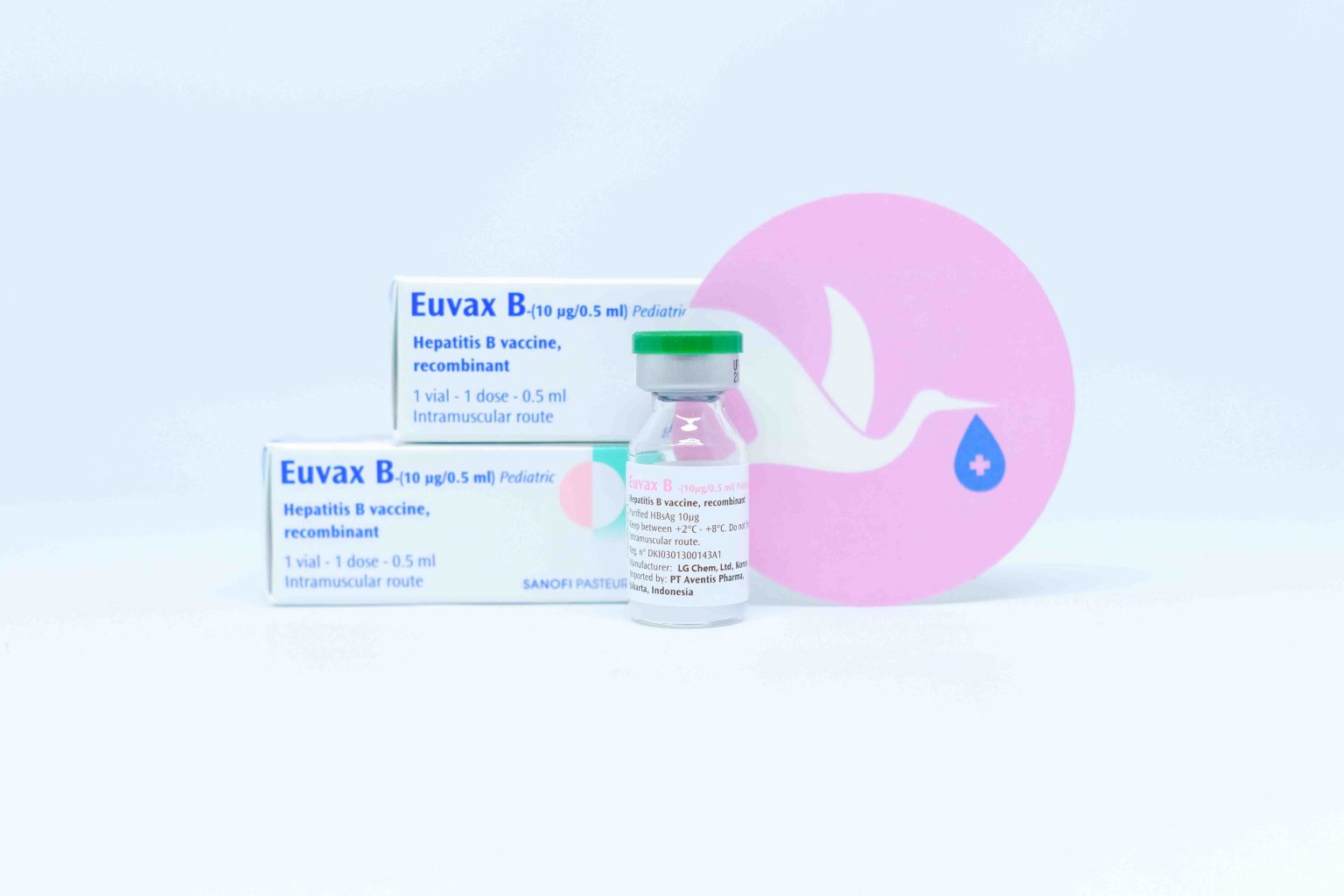
Euvax B は、酵母細胞 ( Saccharomyces cerevisiae ) 内の組換え DNA によって生成され、アジュバントとしてアルミニウム塩に吸着された高度に精製された非感染性 B 型肝炎表面抗原 (HBsAg) 粒子で構成されています。
ワクチンは、体を刺激してこの微生物に対する独自の防御(抗体)を生成することによって機能します。
B 型肝炎は、B 型肝炎ウイルスによって引き起こされる病気であり、有効な治療法がなく、長期的には肝硬変(細胞の機能が変化する肝臓疾患)の発症などの深刻な結果を引き起こす可能性があります。肝臓の癌腫(腫瘍)。
Euvax B の禁忌
ワクチンのあらゆる成分に対する過敏症。
このワクチンの使用には年齢に関連した禁忌はありません。
ユーバックスBの使い方
小児用量(新生児、乳児および15歳までの小児)は0.5mLで、10μgのHBsAgが含まれています。
成人(16歳以上)の用量は1.0mLで、20μgのHBs抗原が含まれています。
予防接種スケジュールは、次のように 3 回のワクチン接種で構成されます。
-
1回目の投与量:
選択した日に;
-
2回目の投与:
最初の投与から1か月後。
-
3回目の投与:
初回投与から6か月後。
一部の集団(すなわち、HBs抗原陽性の母親の新生児、ウイルスに曝露された、または曝露された可能性のある個人、または長期間旅行する個人)では、0、1、および2か月の代替スケジュールと12か月後の追加投与が使用される場合があります。高リスク地域)。
免疫不全患者または血液透析を受けている患者では、初回の一連の予防接種後に防御抗体力価(gt; 10IU/L)が達成されていない可能性があるため、ワクチンの追加用量が必要になる場合があります。
B 型肝炎ウイルスへの曝露が既知または疑われる場合(つまり、感染した母親から生まれた新生児、その他の経皮的経験、または経粘膜曝露)、Euvax B の初回用量は、適切な用量の免疫グロブリンとともに投与される場合があります。
初回シリーズのワクチンを 3 回接種するか、現在のワクチン接種スケジュールに従って接種することが推奨されます。いずれかの用量が適用されない場合、適切かつ長期にわたる防御反応の誘導が満足に達成されない可能性があります。
保管中に無色透明の上清とともに細かい白い沈殿物が形成される可能性があるため、使用前にワクチンの入ったバイアルを振ってください。
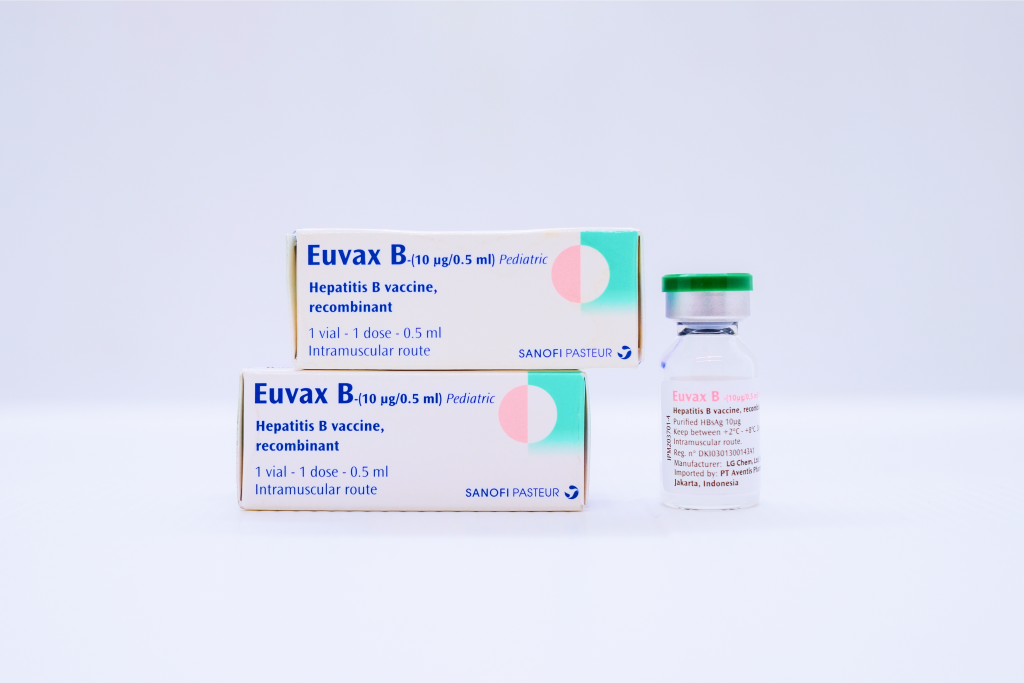
Euvax B は筋肉内にのみ投与する必要があります。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
Euvax B を使い忘れた場合はどうすればよいですか?
医師にお知らせください。
疑問がある場合は、薬剤師または医師に相談してください。
ユーバックスBの注意事項
一部の病気は、Euvax B の使用に影響を与える可能性があります。病気の症状がワクチンによる有害事象の可能性と混同される可能性があるため、あなたまたはお子様が急性の病気または高熱に罹患している場合は、医師に伝えてください。小児に頻繁に起こる風邪などのそれほど重篤ではない病気は、ワクチンの使用を禁忌としません。
多発性硬化症(脳に影響を及ぼす慢性疾患)の患者では、免疫系(防御システム)に対する何らかの刺激が症状の増加を引き起こす可能性があります。したがって、このような場合には、B型肝炎ワクチン接種の利点と多発性硬化症の悪化のリスクを比較検討する必要があります。
未熟児(体重 2,000 グラム未満)の場合は、追加接種の必要性を評価するために 3 回目の接種から 1 か月後に抗体価をチェックすることをお勧めします。
すべての注射可能なワクチンと同様に、ワクチン投与後にまれにアナフィラキシー反応が発生した場合には、常に適切かつ迅速な治療を受けられなければなりません。
ワクチンは静脈内、皮内、または臀部に投与しないでください。
他の薬を服用している場合は医師に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
Euvax B の副作用
他の薬と同様に、Euvax B もいくつかの副作用を引き起こす可能性があります。
以下の有害事象が対照臨床研究で報告されています。
非常に一般的な反応 (この薬を使用している患者の 10% で発生します)
- 適用部位の痛み。
一般的な反応 (この薬を使用している患者の 1% ~ 10% で発生)
- 炎症、硬結、浮腫(腫れ)、発熱、過敏症。
- 血腫(紫色の斑点)。
- 腹痛、下痢、嘔吐、食欲不振。
- 神経質、不眠症、過敏症;
- 異常な泣き声、眠気;
- 皮膚に赤い斑点。
異常な反応 (この薬を使用している患者の 0.1% ~ 1% の間で発生します)
- 新生児黄疸(体内のビリルビンの蓄積により、皮膚や粘膜が黄色くなることを特徴とする症候群)。
- モニリア症(真菌による皮膚および粘膜の感染症);
- 鼻炎(鼻粘膜の慢性または急性の刺激および炎症);
- 皮膚の発疹(発疹)、皮膚上の小さな赤みを帯びた隆起を伴う斑点(斑状丘疹性発疹)、皮膚の色素沈着の変化(バラ色粃糠疹)。
まれな反応(この薬を使用している患者の 0.01% ~ 0.1% で発生します)
- 頭痛、めまい;
- 吐き気;
- 筋肉痛、関節の炎症。
- 倦怠感、疲労感。
- トランスアミナーゼの一時的な増加。
非常にまれな反応(単独の報告を含む、この薬を使用する患者の 0.01% 未満で発生します)
- 視神経の炎症、顔の動きの喪失、ギラン・バレー症候群(動きの喪失を引き起こす神経疾患)、播種性硬化症の悪化。
- 好中球(体の防御細胞)の減少。
薬の使用により望ましくない反応が現れた場合は、医師または薬剤師に知らせてください。また、顧客サービスを通じて会社に通知してください。
Euvax B 特別集団
妊娠中および授乳中の使用
胎児の発育に対する HBs 抗原の影響はまだ評価されていません。しかし、すべての不活化ウイルスワクチンと同様に、胎児へのリスクは無視できると考えられています。 Euvax B は、リスクと利点を比較検討し、明らかに必要な場合にのみ妊娠中に使用する必要があります。
このワクチンは医師のアドバイスなしに妊婦には使用しないでください。
授乳中の女性に Euvax B を投与した場合の効果は、まだ臨床研究で評価されていません。これらの状況では禁忌は確立されていません。
Euvax Bの構成
0.5mL用量(小児)
| 精製B型肝炎表面抗原 | 10mcg |
| 水酸化アルミニウムゲル(アルミニウムのようなもの) | 0.25mg |
| リン酸二水素カリウム | qs |
| 第二リン酸ナトリウム | qs |
| 塩化ナトリウム | 4.25mg |
| 注射用水 | 適量0.5mL |
1.0mLの場合(成人)
| 精製B型肝炎表面抗原 | 20mcg |
| 水酸化アルミニウムゲル(アルミニウムのようなもの) | 0.5mg |
| リン酸二水素カリウム | qs |
| 第二リン酸ナトリウム | qs |
| 塩化ナトリウム | 8.5mg |
| 注射用水 | 適量 1.0mL |
ユーバックスBの過剰摂取
このテーマに関する具体的な研究はありません。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
Euvax B の薬物相互作用
B 型肝炎ワクチン (組換え) (活性物質) と標準用量の HBIg を同時に投与しても、両方が別々の場所に投与される限り、抗 HBs 抗体力価は低下しません。
B 型肝炎ワクチン (組換え) (有効成分) は、国の保健当局が推奨する予防接種スケジュールに都合よく適合する場合、BCG、DTP、DT、および/またはポリオ ワクチンと同時に投与できます。
B型肝炎ワクチン(組換え)(活性物質)は、麻疹・おたふく風邪・風疹に対するワクチン、インフルエンザ菌b型に対するワクチン、およびA型肝炎に対するワクチンと一緒に投与できます。
B型肝炎ワクチン(組換え)(活性物質)は、ヒトパピローマウイルス(HPV)ワクチン[ヒトパピローマウイルス16型および18型ワクチン(組換え型)]と同時に投与できます。
B 型肝炎ワクチン (組換え) (活性物質) を発がん性 HPV ワクチン (16 および 18、AS04 アジュバントと組換え) (HPV ワクチン) と同時に投与しても、B 型肝炎抗原に対する抗体反応における臨床的に関連した干渉は示されませんでした。 .HPV。幾何平均抗HBs抗体濃度は共投与により低下したが、血清防御率は影響を受けなかったため、この観察の臨床的意義は不明である。抗HBs効果を達成した個人の割合は? 10 mIU/mL は、同時ワクチン接種では 97.9%、B 型肝炎ワクチン (組換え) (活性物質) 単独投与では 100% でした。
異なる注射可能なワクチンは、常に異なる注射部位に投与する必要があります。
B型肝炎ワクチンの互換性
B 型肝炎ワクチン (組換え) (活性物質) は、血漿由来 B 型肝炎ワクチンまたはその他の遺伝子組み換え B 型肝炎ワクチンで開始される一次予防接種のコースを完了するために使用できます。あるいは、以前に B 型肝炎ワクチンの接種を受けた人に追加免疫として投与することもできます。血漿由来または遺伝子操作された B 型肝炎ワクチンの一次シリーズ。
出典: Engerix B Medication Professional からの挿入。
物質Euvax Bの作用
有効性の結果
リスクグループにおける予防効果
実地調査では、この病気にかかるリスクのある新生児、小児、成人に対して95%から100%の予防効果が実証されました。
B型肝炎免疫グロブリンを併用せずに、0、1、2、12か月または0、1、6か月のスケジュールに従って免疫したB型肝炎抗原E(HBeAg)陽性の母親の新生児では、95%の防御効果が実証されました( HBIg) 出生時。しかし、出生時にHBIgとワクチンを同時に投与すると、予防効果が98%に増加します。
小児期の最初のワクチン接種から 20 年後、B 型肝炎を持つ母親から生まれた人は、B 型肝炎 (組換え) ワクチンの攻撃用量を受けました。 1 か月後、これらの個人 (N=75) の少なくとも 93% が既往反応を達成し、免疫学的記憶を示しました。
健康な人および腎不全患者における予防効果

以下の表は、用量項目に記載されているさまざまなレジメンを用いた臨床研究で得られた血清防御率(例:抗HBs抗体濃度が10UI/lの被験者の割合)をまとめたものです。
|
人口 |
スキーム |
血清防御率 |
|
健康な人 |
0、1、6ヶ月 |
7ヶ月目: ? 96% |
|
1か月目: 15% |
||
|
0、1、2 – 12 か月 |
3 か月目: 89% |
|
|
13 か月目: 95.8% |
||
|
20歳以上の健康な方 |
0、7、21日 – 12か月 |
28日目: 65.2% |
|
2 か月目: 76% |
||
|
13 か月目: 98.6% |
11歳から15歳の患者に登録された2つの異なる用量とスケジュールで得られた血清防御率(SP)は、一次ワクチン接種の最初の投与後66か月まで評価され、以下の表に示されています。
|
ワクチングループ |
血清防御率 |
||||||
|
2ヶ月目 |
6ヶ月目 |
7ヶ月目 |
月30 |
42ヶ月目 |
54 ヶ月目 |
66ヶ月目 |
|
|
B型肝炎ワクチン(組換え)(有効成分) 10μg(0、1、6ヶ月スケジュール) |
55.8% | 87.6% | 98.2% | 96.9% | 92.5% | 94.7% |
91.4% |
|
B型肝炎ワクチン(組換え)(有効成分) 20μg(0.6ヶ月予定) |
11.3% | 26.4% | 96.7% | 87.1% | 83.7% | 84.4% |
79.5% |
これらのデータは、B 型肝炎ワクチン (組換え) (活性物質) による初回ワクチン接種が、少なくとも 66 か月間持続する循環抗 HBs 抗体を誘導することを示しています。一次ワクチン接種サイクルの完了後、2 つのワクチン群を比較した場合、どの時点でも血清防御率に臨床的に有意な差はありません。実際、両方のワクチン群のすべての患者(抗HBs抗体濃度が10 IU/L未満の患者を含む)は、初回ワクチン接種から72~78か月後に攻撃用量を受けた。攻撃用量の1か月後、すべての患者は攻撃用量に対して既往反応を示し、血清防御を示しました(すなわち、抗HBs抗体濃度が10 IU/L以下)。これらのデータは、一次ワクチン接種には反応したが、抗HBs抗体による血清防御レベルを失ったすべての患者において、免疫記憶を通じてB型肝炎に対する防御が依然として付与され得ることを示している。
健康な人の課題
小児期にB型肝炎ワクチン(組換え)を3回接種した12歳および13歳の個体(N=284)に、攻撃用量を投与した。 1 か月後、これらの個人の 98.9% が血清防御されていることが証明されました。
血液透析を受けている患者を含む腎不全患者
|
年齢(歳) |
スキーム |
7ヵ月目の血清防御率 |
|
16歳以上 |
0、1、2、6 か月 (2 x 20 mcg) |
3 か月目: 55.4% |
|
7 か月目: 87.1% |
II型糖尿病患者
|
年齢(歳) |
スキーム |
7か月目の血清防御率 |
|
20-39 |
0、1、6ヶ月 (20μg) |
88.5% |
|
40-49 |
81.2% |
|
|
50-59 |
83.2% |
|
|
? 60 |
58.2% |
小児における肝細胞がんの発生率の減少
台湾でB型肝炎に対する全国的なワクチン接種キャンペーンが実施された後、6歳から14歳の小児で肝細胞がんの発生率が大幅に減少したことが観察されました。 B 型肝炎抗原の有病率は大幅に減少しました。B 型肝炎抗原の持続は肝細胞癌の発症に不可欠な要素です。
出典: Engerix B Medication Professional からの挿入。
薬理学的特徴
B型肝炎ワクチン(組換え)(有効成分)は、HBs抗原に対する特異的抗体(抗HBs抗体)を誘導します。抗 HBs 抗体濃度が 10 IU/L 以上であれば、HBV 感染に対する防御と相関します。
出典: Engerix B Medication Professional からの挿入。
Euvax B ストレージ ケア
Euvax B は、+2°C ~ +8°C の間で保管および輸送する必要があります。ワクチンは凍結させてはいけません。
有効期限
+2°C ~ +8C の冷蔵保存に限り、Euvax B の保存期間はパッケージに記載されている製造日から 36 か月です。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。

ワクチンは開封したらすぐに使用しなければなりません。
プレゼンテーション
このワクチンは、わずかに不透明な白色の注射可能な懸濁液です。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
Euvax B アラート メッセージ
すべての薬は子供の手の届かないところに保管してください。
Euvax B 法的声明
MS登録番号 1.1300.1107
担当薬剤師:
シルビア・レジーナ・ブロロ
CRF-SP番号9,815
予防接種情報サービス:0800 14 84 80
製造元:
LGライフサイエンス株式会社
全北道、韓国
輸入者:
サノフィ・アベンティス・ファーマセウティカ株式会社。
Rua Conde Domingos Papaiz、413 スザノ – SP
CEP 08613-010
CNPJ 02.685.377/0008-23








-1024x576.jpg?resize=1024,576&ssl=1)


