- 有毛細胞白血病。
- 多発性骨髄腫;
- 非ホジキンリンパ腫。
- 慢性骨髄性白血病。
- 慢性B型肝炎;
- 急性および慢性C型肝炎。
- 尖圭コンジローマ。
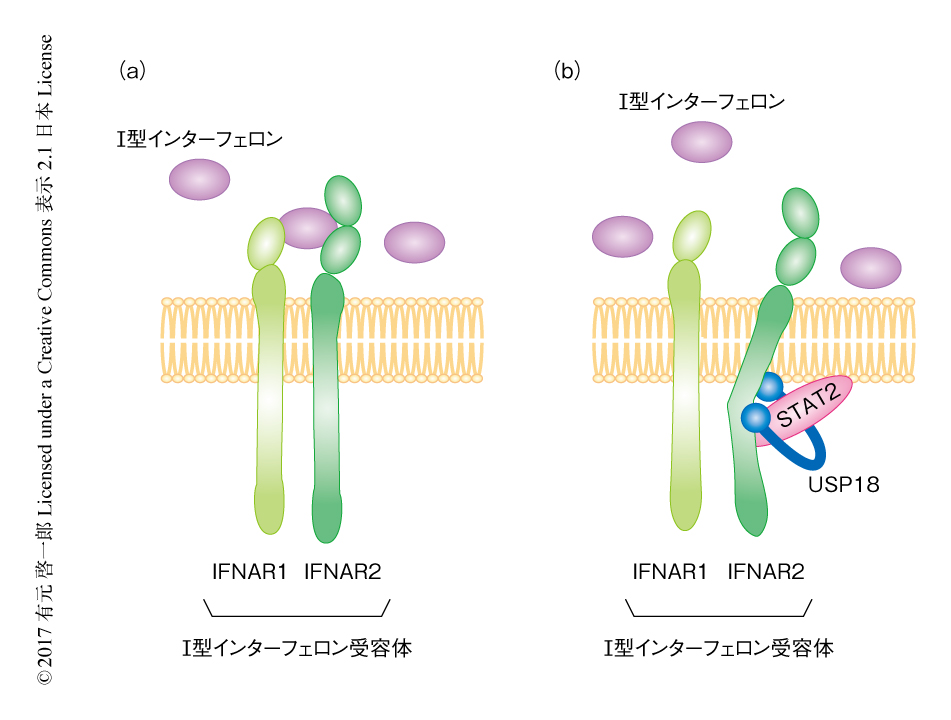
組換えヒトインターフェロンα 2A はどのように作用しますか?
組換えヒトインターフェロンα 2A および他のタイプのインターフェロンが抗腫瘍および抗ウイルス活性を発揮するメカニズムは完全にはわかっていません。しかし、腫瘍細胞に対する直接的な抗増殖作用、ウイルス複製の阻害、宿主の免疫応答の調節が、抗腫瘍および抗ウイルス活性において重要な役割を果たすと考えられています。

組換えヒトインターフェロンα 2A の禁忌
この薬は、インターフェロン アルファ Aa またはその他の配合成分に対する過敏症の場合には使用しないでください。
重度の心臓病または心臓病の病歴のある人は、この薬を使用しないでください。組換えヒトインターフェロンα 2A の使用に伴う有毒な性質の急性反応(発熱、風邪など)は、既存の症状を悪化させる可能性があるためです。心臓病がある。
重度の腎臓病または肝臓病、中枢神経系機能障害、肝硬変および/または肝臓代償不全、免疫力を低下させる治療を受けている慢性肝炎、または異種移植後に免疫力が低下した慢性骨髄性白血病のある人は、この薬を使用しないでください。臓器や組織が人から人へ)。
妊娠と授乳
胎児期の初期から中期にかけて組換えヒトインターフェロンα 2A で治療された妊娠サルを対象とした研究では胎児奇形の刺激は示されなかったが、妊婦を対象とした適切かつ対照的な研究は存在しない。
組換えヒトインターフェロンアルファ 2A は、ヒトに使用されるものと比べて非常に高い用量を投与した場合、オナガザル科 ( Macaca Mullata ) の霊長類の流産活性が大幅に増加することが実証されています。
この薬が母乳中に排泄されるかどうかは不明であるため、医師は母親にとっての薬の重要性を考慮して、授乳を中止するか治療を中止するかを決定する必要があります。
組換えヒトインターフェロンα2Aの使い方
組換えヒトインターフェロンα 2A は白色の粉末で、溶解すると無色透明の溶液になります。白い粉末のみを再構成し、目に見える粒子のない無色透明の溶液を注入する必要があります。

注射用水 1mL は、バイアルを注意深く保持してゆっくりと導入する必要があります。軽く振って、フリーズドライパウダーを水に溶かします。
使用前に、再構成インターフェロン アルファ 2A 溶液を分析して、目に見える粒子の存在を確認する必要があります。注入前に、溶液を室温に戻す必要があります。注射部位の不快感を避けるため、注射はゆっくりと行う必要があります。
組換えヒトインターフェロンα 2A の投与量
有毛細胞白血病
組換えヒトインターフェロンアルファ 2A の推奨 1 日量は 3MUI で 16 ~ 20 週間、筋肉内または皮下注射として投与されます。
最大耐用量を決定するには、注射の用量または頻度を減らすことが必要な場合があります。
推奨される維持用量は 3MUI、週 3 回です。重篤な副作用が観察された場合には、用量を半分に減らす必要がある場合があります。医師は、6 か月の治療後に組換えヒトインターフェロン アルファ 2A による治療を継続するかどうかを決定する必要があります。
多発性骨髄腫
組換えヒトインターフェロンアルファ 2A の推奨用量は 3MUI、週 3 回、筋肉内または皮下注射として投与されます。患者の耐性に基づいて、用量は週に 3 回、9MUI まで徐々に増量できます。
非ホジキンリンパ腫
組換えヒトインターフェロンアルファ 2A は、化学療法後 4 ~ 6 週間後に投与でき、推奨用量は 3MUI で、週に 3 回、少なくとも 12 週間皮下投与されます。
化学療法(シクロホスファミド、プレドニゾン、ビンクリスチン、アドリアマイシン)と組み合わせて投与する場合、推奨用量は 6MUI/m2 で、化学療法の 22 ~ 26 日目に皮下または筋肉内に投与されます。
慢性骨髄性白血病
組換えヒトインターフェロンα 2A の用量は、3 日間 1 日あたり 3MUI、3 日間にわたって 1 日あたり 6MUI、治療期間の終わりまでに 1 日あたり 9MUI の目標用量まで徐々に増量できます。
8~12週間の治療後、血液学的反応を示した患者は、完全な反応が得られるまで、または治療開始後18か月~2年経過するまで治療を続けることができます。最適な治療期間はまだ決定されていません。
慢性B型肝炎
成人の推奨用量は 5MUI、週 3 回、6 か月間皮下投与されます。
1か月の治療後に組換えヒトインターフェロンアルファ2Aに反応しない患者には、用量の増加が提案される場合があります。
3か月の治療後に反応が見られない患者は、治療の中止を考慮する必要があります。
急性および慢性C型肝炎
治療における組換えヒトインターフェロンα 2A の推奨用量は、3 ~ 5MUI を週 3 回、3 か月間皮下または筋肉内投与します。
推奨される維持用量は 3MUI で、週に 3 回、3 か月間服用します。
尖圭コンジローマ
1MUI ~ 3MUI を週 3 回、1 ~ 2 か月間皮下または筋肉内に塗布するか、1MUI を隔日で患部の基部に 3 週間連続塗布します。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
組換えヒトインターフェロンα 2A の使用を忘れた場合はどうすればよいですか?
服用を忘れた場合は、通常どおり服用を再開する必要があります。飲み忘れた分を補充する必要はありません。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
組換えヒトインターフェロンα 2A に関する注意事項
インターフェロン アルファ 2A は医師の監督下で使用する必要があります。
腎臓、肝臓、骨髄の機能に異常がある人は、注意深く監視する必要があります。

骨髄抑制(骨髄の血球生成機能の抑制)のある人に組換えヒトインターフェロン アルファ 2A を使用する場合、組換えヒトインターフェロン アルファ 2A は白血球の減少を引き起こす可能性があるため注意が必要です。このパラメータは、インターフェロン アルファ 2A による治療を開始する前、および治療中の特定の期間に注意深く監視する必要があります。完全な血液検査を定期的に実施する必要があります。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
組換えヒトインターフェロンα 2A の副作用
頻繁な副作用
疲労、発熱、悪寒、筋肉痛、頭痛、関節痛、発汗などのインフルエンザのような症状。
胃腸
- 拒食症;
- 吐き気;
- 嘔吐;
- 味の変化。
- 体重減少。
- 下痢;
- 腹痛;
- 便秘;
- 鼓腸。
肝機能
一部の患者は、アルカリホスファターゼ、乳酸、デヒドロゲナーゼ、ビリルビンのレベルの上昇を示しました。通常、そのような反応が起こった場合には、組換えヒトインターフェロンα 2A の用量を調整すべきではありません。
中枢神経系
- めまい;
- 視覚障害;
- 記憶喪失。
- うつ;
- 眠気;
- 不安;
- 神経質;
- まれに不眠症が観察されることがあります。
末梢神経系
- 感覚異常;
- 昏睡状態。
- 弱さ。
心臓血管系および呼吸器系
このような症状は、がん患者の5分の1に観察され、一過性の低血圧、高血圧、浮腫、リズム障害、動悸、胸痛などでした。咳や呼吸困難はまれに発生しました。

B 型肝炎患者ではこのような反応はまれです。
肌
- ヘルペス;
- 発疹;
- かゆみや皮膚の乾燥が時々報告されます。
- 組換えヒトインターフェロンα 2A を投与されている患者の 5 分の 1 に脱毛が観察されています。
泌尿器系
腎不全はほとんど観察されません。食欲不振や脱水症状に関連して、電解質障害が発生することがあります。
造血系
一過性の白血球減少症は、組換えヒトインターフェロンアルファ 2A の投与を受けた患者の 3 分の 1 から 2 分の 1 に発生しています。
一部の骨髄抑制患者では、血小板減少症とヘモグロビンの減少が観察されています。
造血系の重度の異常は、組換えヒトインターフェロンアルファ 2A による治療を中止してから 7 ~ 10 日後に回復する可能性があります。
その他
高血糖および注射部位の反応が少数の患者で観察されました。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。
また、顧客サービスを通じて会社に通知してください。
組換えヒトインターフェロンα 2A の組成
プレゼンテーション
注射可能な親液性粉末
|
投与量 |
|
|
1,000,000 IU |
注射可能な親液性粉末を含む 1、6、10、20 アンプルバイアルを含むパッケージ |
|
3,000,000 IU |
注射可能な親液性粉末を含む 1、6、10、20 アンプルバイアルを含むパッケージ |
|
5,000,000 IU |
注射可能な親液性粉末を含む 1、6、10、20 アンプルバイアルを含むパッケージ |
|
9,000,000IU |
注射可能な親液性粉末を含む1、6、10、20アンプルを含むパッケージ |
筋肉内または皮下経路。
大人用。
構成
組換えヒトインターフェロンα 2A の過剰摂取
過剰摂取に関する報告はまだありませんが、眠気、無力症、ふらつき、昏睡などの症状は、組換えヒトインターフェロンα 2A の大量反復投与に関連している可能性があります。このタイプの患者は病院で監視され、適切な支持療法を受ける必要があります。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。
さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
組換えヒトインターフェロンα 2A の薬物相互作用
臨床的関連性は不明ですが、αインターフェロンベースの製品は、P450系の肝臓ミクロソームシトクロミック酵素の活性を低下させることにより、酸化代謝プロセスに影響を与える可能性があります。この経路を介して代謝される他の薬剤との併用療法を処方する場合は、この事実を考慮する必要があります。インターフェロン アルファの併用投与後にテオフィリンクリアランスの減少が報告されています。
インターフェロン アルファ 2a (活性物質) は中枢神経系の機能に影響を与える可能性があるため、中枢作用のある薬剤との併用投与後に相互作用が発生する可能性があります。以前または同時に投与された薬剤の神経毒性、血液毒性、または心臓毒性の影響は、インターフェロン アルファによって悪化する可能性があります。
リバビリンと併用した治療:
慢性 C 型肝炎患者にインターフェロン アルファ 2a をリバビリンと組み合わせて投与する場合は、リバビリンの添付文書も参照してください。
対照臨床研究の結果は、αインターフェロン 2a の薬物動態に対するベバシズマブの有意ではない干渉を実証しました。
組換えヒトインターフェロンα2A物質の作用
有効性の結果
白血病: アルファ インターフェロン 2a は、白血病の治療において有効性が実証された最初の薬剤です。 31ヶ月時点で88.9%の全奏効と83%の無病生存率が実証された。現在、治療には他の薬剤との併用が含まれています。表 1 は三白血病の反応評価基準を示し、表 2 は治療結果を示します。
表 1 – 三白血病の反応を評価するための基準
|
完全な回答 |
部分的な回答 |
| 器官巨大症から正常への退行 |
器官巨大症 gt の減少。 50% |
|
循環トリコセルなし |
lt; 5% 循環トリコセル |
|
骨髄にトリコセルが存在しない |
骨髄中のトリコセルが約50%減少 |
|
ヘモグロビン? 120g/L |
ヘモグロビン? 120g/L |
|
絶対好中球 gt; 1.5× 109 /L |
絶対好中球 gt; 1.5× 109 /L |
|
血小板GT; 100× 109 /L |
血小板GT; 100× 109 /L |
表 2 – 三白血病患者におけるインターフェロン療法の結果
N: 研究に参加した患者の数。 RC: 完全な回答。 RP: 部分応答。 TRG: 世界的な応答率。 PFS: 無増悪生存期間。 SLF: 失敗のない生存。 rIFN-?: 組換えαインターフェロン。 MU: 数百万単位。 NS: 指定されていません。
皮膚T細胞リンパ腫
インターフェロン アルファ 2a の使用により、全体的な反応 gt が示されました。 50%、完全解答の場合は 20%。難治性または従来の治療に適さない進行性皮膚 T 細胞リンパ腫の患者に効果がある可能性があります。
警告
皮膚 T 細胞リンパ腫患者の約 40% では客観的な腫瘍反応は観察されていません。部分反応は通常 3 か月以内に見られ、完全な反応は 6 か月以内に見られますが、最良の反応が得られるまでに 1 年以上かかる場合もあります。答え。
慢性骨髄性白血病(CML)
αインターフェロン 2a の使用により、62.3% の細胞遺伝学的反応が実証されました。インターフェロン アルファ 2a (活性物質) は、フィラデルフィア染色体陽性の慢性骨髄性白血病の慢性期の患者の治療に有効です。インターフェロン アルファ 2a (活性物質) がこの適応症において治癒の可能性のある治療法とみなせるかどうかはまだ決定されていません。インターフェロン アルファ 2a (活性物質) は、以前の治療に関係なく、慢性期の CML 患者の 60% で血液学的寛解を促進します。
これらの患者の 3 分の 2 は、治療開始から 18 か月以内に完全な血液学的反応を示します。さらに、細胞傷害性化学療法で起こるものとは異なり、α インターフェロン 2a は 40 か月間にわたって継続的に持続的な細胞遺伝学的反応を引き起こすことができます。間欠的化学療法で補充されたインターフェロン アルファ 2a (活性物質) は、化学療法のみで治療された患者と比較して、全生存期間を延長し、疾患の進行を遅らせることが示されています。
骨髄増殖性疾患に伴う血小板増加症
インターフェロン アルファ 2a の使用により、75% の全体的な反応と 70% の完全な反応が実証されました。アルファ インターフェロン 2a (活性物質) は、CML およびその他の骨髄増殖性疾患における過剰な血小板増加症の治療に効果的です。血小板増加症を発症した CML 患者において、アルファ インターフェロン 2a (活性物質) は、その頻度で血小板数を減少させます。血栓塞栓性関連出血性疾患の影響をほとんど受けず、白血病の可能性はありません。
低悪性度の非ホジキンリンパ腫
インターフェロン アルファは他の薬と組み合わせて使用できます。リツキシマブと関連した研究では、インターフェロン アルファ 2a (活性物質) を補助療法として使用した場合、全奏効率は 45%、完全奏効は 34%、部分奏効は 11% でした。低悪性度の非ホジキンリンパ腫患者に対する化学療法(放射線療法の有無にかかわらず)。
エイズ関連カポジ肉腫:αインターフェロン2a(有効成分)
日和見感染症の病歴のないエイズに関連するカポジ肉腫患者の治療に適応されます。理想的な投与量はまだ十分に確立されていません。エイズ関連カポジ肉腫の患者は、日和見感染の既往がなく、B型症状(10%を超える体重減少、感染源が特定できない場合の38℃以上の発熱、寝汗)がなければ治療によく反応します。 T4 リンパ球の基礎数が 200 細胞/mm 3を超える。
腎細胞がん
インターフェロン アルファは 11% の完全奏効をもたらし、生存期間中央値は 67 か月でした。
進行性腎細胞癌患者では、高用量のインターフェロン アルファ 2a (1 日あたり 3,600 万 IU) の単独療法または中用量のインターフェロン アルファ 2a (活性物質) を使用した転移性または再発性疾患の患者で最も高い腫瘍反応率が観察されました。 (1,800万IUを週3回)ビンブラスチンと併用した場合と、週3回投与される単独療法における中用量のインターフェロンアルファ2a(活性物質)と比較。
低用量のインターフェロン アルファ 2a (活性物質) の単独療法 (毎日身体面積1平方メートルあたり 200 万 IU 投与) で治療された患者は、治療に反応しませんでした。インターフェロン アルファ 2a (活性物質) とビンブラスチンの併用に関する安全性データは、単独療法と比較して、軽度から中等度の白血球減少症および顆粒球減少症の頻度のわずかな増加のみを示しました。疾患に対する反応期間と生存期間は、αインターフェロン 2a (活性物質) の単独療法で治療された患者と、α インターフェロン 2a (活性物質) とビンブラスチンの併用療法で治療された患者で同様です。
ビンブラスチンと併用したαインターフェロン 2a (活性物質) による治療は、進行性腎細胞癌患者の全奏効率を約 20% 誘導し、疾患の進行を遅らせ、全生存期間を延長します。インターフェロン アルファ 2a (活性物質) をビンブラスチンと組み合わせると、化学療法単独よりも生存率が向上します。
第一選択治療としてインターフェロン アルファ 2a (活性物質) とアバスチンの併用の有効性と安全性を評価する対照臨床研究では、進行性および/または転移性腎がんの患者に多大な利益をもたらすことが示されました。アバスチン + アルファ インターフェロン 2a (活性型) では、臨床的に有意で統計的に有意な無増悪生存期間の増加 (中央値 10.2 か月対 5.4 か月、ハザード比 0.63、p <0.0001) と奏効者の割合の統計的に有意な増加が観察されました。物質) 群 (31%)、プラセボ群 + アルファ インターフェロン 2a (活性物質) (13%) と比較。 p<0.0001。しかし、観察された全生存期間の 2 か月の増加は有意ではありませんでした (中央値 23.3 か月対 21.3 か月; ハザード比 0.91; p = 0.3360)。
インターフェロン アルファ 2a 群の患者 97 名 (97 名) とアバスチン群の患者 131 名は、プロトコールで事前に定められたとおり、インターフェロン アルファ 2a の用量を週 3 回、900 万 IU から 600 万 IU または 300 万 IU に減量しました。 。サブグループ分析で示されるように、期間中の無イベント無増悪生存率に基づくと、インターフェロン アルファ 2a の用量減量は、アバスチンとインターフェロン アルファ 2a の併用の有効性には明らかに影響しなかった。
研究中にインターフェロン アルファ 2a の用量を 600 万 IU または 300 万 IU に減量したアバスチン + インターフェロン アルファ 2a 群の患者 131 人は、6、12、および 18 か月後の無増悪生存率が 73、52、および 21 % でした。 、それぞれ、アバスチン + インターフェロン アルファ 2a を投与されている全患者集団の 61、43、および 17% と比較して。
悪性黒色腫
進行性悪性黒色腫患者は、インターフェロン アルファ 2a (活性物質) による治療で皮膚腫瘍および内臓腫瘍の客観的縮小を示しました。
インターフェロン アルファ 2a (活性物質) は、外科的に切除された悪性黒色腫 (腫瘍の厚さ > 1.5 mm) を患っており、治療開始前にリンパ節転移や遠隔転移を示さない患者の無病生存期間を延長するという利点もあります。
進行性悪性黒色腫患者の 10% ~ 25% が、インターフェロン アルファ 2a 療法 (活性物質) により皮膚および内臓腫瘍の客観的縮小を示しました。週に3回、1,800万IU未満の用量を使用すると、より低い反応率が観察されました。反応した患者は、反応しなかった患者よりも長く生存しました。
C型肝炎
インターフェロン アルファ 2a とリバビリンを併用すると、リバビリンと併用した場合、29% ~ 43.1% の持続的な反応が達成されました。
薬理学的特徴
薬力学特性
アルファ インターフェロン 2a (活性物質) は、ヒト アルファ インターフェロンのいわゆる天然製剤の多くの活性を有することが示されています。
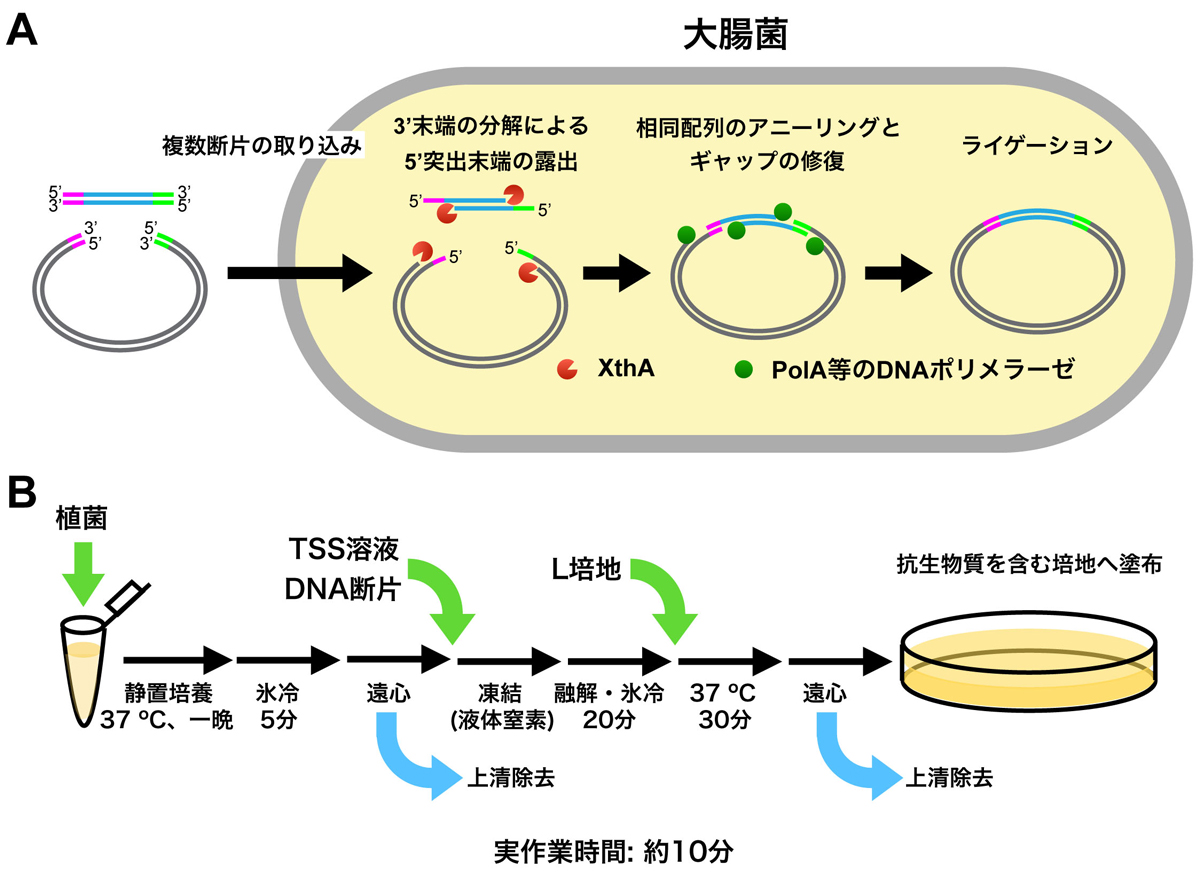
α インターフェロン 2a は、組換え DNA 技術によって生合成的に生成され、大腸菌内に挿入され発現されたクローン化ヒト白血球インターフェロン遺伝子の産物です。
インターフェロン アルファ 2a (活性物質) は、細胞内でウイルス感染に対する耐性状態を誘導し、免疫系のエフェクター部分を調節してウイルスを中和するかウイルスに感染した細胞を排除することによって、抗ウイルス効果を発揮します。
インターフェロン アルファ 2a (活性物質) の抗腫瘍作用に関与する本質的なメカニズムはまだ不明です。しかし、αインターフェロン 2a (活性物質) で処理されたヒト腫瘍細胞にはいくつかの変化が報告されています。HT 29 細胞は、DNA、RNA、およびタンパク質の合成の大幅な減少を示します。
インターフェロン アルファ 2a (活性物質) は、インビトロでいくつかのヒト腫瘍に対して抗増殖活性を発揮し、マウスにおける一部のヒト腫瘍異種移植片の増殖を阻害します。免疫不全マウスにおいてインビボで培養された限られた数のヒト腫瘍細胞株を、インターフェロンα 2a (活性物質) に対する感受性について試験した。 αインターフェロン 2a (活性物質) のin vivo抗増殖活性は、粘液性乳癌、盲腸の腺癌、結腸癌および前立腺癌を含む腫瘍において研究されています。
抗増殖活性の程度はさまざまです。
他のヒトタンパク質とは異なり、他の動物種で研究すると、αインターフェロン 2a の効果の多くは部分的または完全に抑制されます。しかし、ワクシニアウイルスに対する顕著な活性は、インターフェロンアルファ2aで事前に治療したアカゲザルでは誘導された。
薬物動態学的特性
動物(サル、イヌおよびマウス)におけるαインターフェロン 2a(活性物質)の薬物動態は、ヒトで観察されたものと同様でした。
吸収
筋肉内または皮下注射後に吸収される用量の見かけの割合は 80% を超えます。 3,600万IUの筋肉内投与後、最大血清濃度は1,500~2,580 pg/mL(平均2,020 pg/mL)の範囲であり、最大濃度に達するまでの平均時間は3.8時間でした。 3,600万IUの皮下投与後、最大血清濃度は1,250~2,320 pg/mL(平均1,730 pg/mL)の範囲であり、最大濃度に達するまでの平均時間は7.3時間でした。
分布
ヒトにおけるインターフェロン アルファ 2a (活性物質) の薬物動態は、3 ~ 1 億 9,800 万 IU の投与スケジュールに対して直線的でした。健康なボランティアに 3,600 万 IU を静脈内注入した後、定常状態での分布量は 0.22 ~ 0.75 L/kg (平均: 0.40 L/kg) の範囲でした。健康なボランティアも播種性がん患者も、αインターフェロン 2a の血清濃度には大きな個人差があります。
代謝と排泄
腎臓の異化作用は、インターフェロン アルファ 2a (活性物質) の主な除去経路です。肝臓代謝と胆汁排泄は、インターフェロン アルファ 2a (活性物質) の主要な除去経路と考えられています。健康な人では、インターフェロン アルファ 2a の排出半減期は 3.7 ~ 8.5 時間 (平均: 5.1 時間)、体内総クリアランスは 2.14 ~ 3.62 mL/min/kg (平均: 2.79 mL/min/kg) でした。 3,600万IUの注入後。
特殊な臨床状況における薬物動態
播種性がん患者および活動性慢性B型肝炎患者におけるインターフェロンアルファ2aの単回筋肉内投与後の薬物動態は、健常者で観察されたものと同様でした。最大1億9,800万IUの単回投与後に、用量に比例した血清濃度の上昇が観察されています。 1日2回(0.5~3,600万IU)、1日1回(1~5,400万IU)、または週3回(1~1億3,600万IU)の投与スケジュールでのインターフェロンアルファ2aの分布または排除に変化はありませんでした。最長28日間の投与。
一部の播種性がん患者にインターフェロンアルファ2a(活性物質)を1日1~2回、最長28日間筋肉内投与したところ、最大血漿濃度は単回投与の2~4倍となった。しかし、複数回の投与は、研究されたさまざまな投与計画中に分布または除去パラメーターに変化を引き起こしませんでした。
小児および高齢者に対する特定の臨床研究がないため、これらの人々への使用は推奨されません。
リバビリンの薬物動態学的特性の詳細については、医薬品リーフレットを参照してください。
インターフェロン アルファ 2a (活性物質) を小児に使用することは、この年齢層における安全性と有効性がまだ確立されていないため、推奨されません。
組換えヒトインターフェロンα 2A の保管管理
組換えヒトインターフェロン アルファ 2A は冷蔵保存する必要があります (2 ~ 8°C)。凍結させてはいけません。光から保護する必要があります。
この薬は調製したらすぐに使用しなければなりません。
インターフェロン アルファ 2A は、製造日から 36 か月間有効です。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かないところに保管してください。
組換えヒトインターフェロンα 2A の法律上の言い伝え
MS 登録: 1.5625.0001
担当薬剤師:
エルナニ・ラモス・ドス・サントス
CRF-RJ No.13,688
製造元:
瀋陽陽光製薬株式会社
瀋陽、中国
輸入者:
Chron Epigen Indústria e Comércio LTDA。
Av. カルロス シャガス フィリョ、791 – シダーデ大学
郵便番号: 21941-904
リオデジャネイロ – RJ – ブラジル
CNPJ: 04.415.365/0001-38
電話/ファックス:
55 21 2290-7359
SAC
(21) 2260-9660
www.chronepigen.com.br
[メールで保護されています]
医師の処方箋に基づいて販売します。







-1024x576.jpg?resize=1024,576&ssl=1)


