デスベンラファクシン コハク酸塩 – Eurofarma はどのように機能しますか?
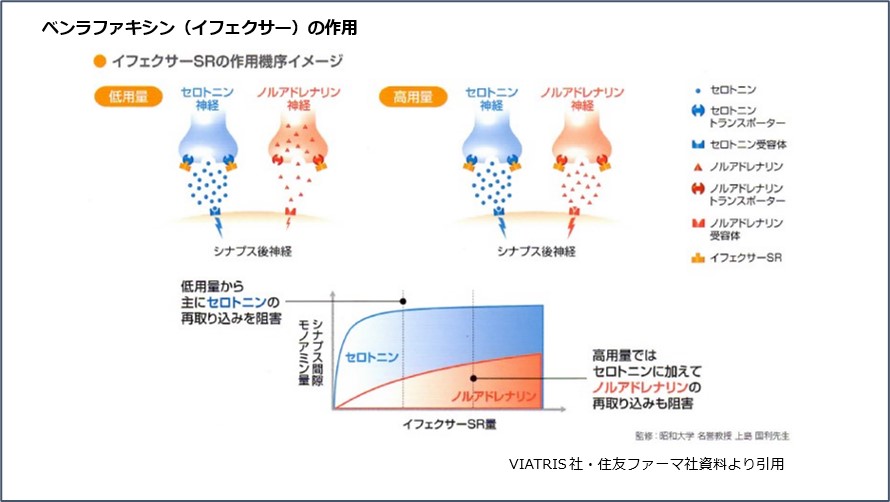
コハク酸デスベンラファクシンは、2 つの神経伝達物質 (脳内に存在する物質であるセロトニンとノルアドレナリン) の利用可能性を高めることによって作用します。これらの物質が不足するとうつ病を引き起こす可能性があります。コハク酸デスベンラファクシンの使用は、うつ病の生化学的原因である脳内のセロトニンとノルアドレナリンの化学的不均衡を修正するのに役立ちます。薬が効果を発揮し始めるまでの推定時間は最大 7 日です。
コハク酸デスベンラファクシンの禁忌 – Eurofarma
この薬は、デスベンラファクシンコハク酸塩一水和物、ベンラファクシン塩酸塩、またはその配合成分に対する過敏症(アレルギー)がある場合には使用しないでください。
この薬は、モノアミンオキシダーゼ阻害薬(別のクラスの抗うつ薬)や、ベンラファクシンおよび/またはデスベンラファクシンを含む他の薬と同時に使用しないでください。モノアミンオキシダーゼ阻害剤を使用している場合、このクラスの薬剤の中止と開始の間の推奨間隔は少なくとも 14 日である必要があります。
デスベンラファキシンコハク酸塩の使用方法 – Eurofarma
コハク酸デスベンラファキシンは経口的にのみ使用してください。デスベンラファクシンコハク酸塩錠剤をそのまま液体と一緒に直接飲み込みます。必ず医師の指示に従って正確に薬を服用してください。医師のみが治療期間を決定する必要があります。
コハク酸デスベンラファクシンの投与量 – Eurofarma
コハク酸デスベンラファクシンの推奨用量は、食事の有無にかかわらず、1 日 1 回 50 mg です。患者によっては、医師が 7 日間隔で徐々に投与量を増やすよう指示する場合があります。最大用量は 200 mg/日を超えることはできません。
腎不全(腎機能障害)の患者さん
重度の腎不全または末期腎疾患(ESRD)の患者における推奨開始用量は、1日おきに50 mgです。
肝不全(肝機能低下)の患者さん
100 mg/日を超える用量の使用は推奨されません。
高齢の患者さん
年齢のみに基づいて用量を調整する必要はありません。
デスベンラファキシンコハク酸塩の中止
常に医師の監督の下、徐々に行うことをお勧めします。突然の中断は、次の症状を伴う可能性があるため、可能な限り避けるべきです。多幸感や悲しみへの気分の変化、イライラ、興奮、めまい、不安、混乱、頭痛、無気力(だるい感じ)、情緒不安定(感情のコントロールの欠如) )、不眠症、耳鳴り(存在しないきしみ音が聞こえる)、けいれん。これらの現象は通常自然に治りますが、重篤な中止症状が報告されています。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。医師の知識なしに治療を中止しないでください。この薬は割ったり噛んだりしないでください。
Desvenlafaxine Succinate – Eurofarma を使用するのを忘れた場合はどうすればよいですか?
用量を忘れると、治療の効果が損なわれる可能性があります。思い出したらすぐに服用してください。次の服用時間が近い場合は、忘れた服用分を飛ばして次の服用量を服用し、医師の指示に従って次の服用スケジュールを続けてください。飲み忘れた分を補うために薬を 2 回服用しないでください。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
コハク酸デスベンラファキシンの予防措置 – Eurofarma
-箱.jpg)
コハク酸デスベンラファキシンは、以下の患者には注意して使用する必要があります。
- 躁病または軽躁病(出来事に対して不釣り合いな多幸感反応が起こる気分変化状態)の既往歴または家族歴がある。
- 閉塞隅角緑内障(眼内の圧力の上昇)の患者。
- 以前に動脈性高血圧症(血圧上昇)があり、頻繁なモニタリングが推奨されている患者。
- 出血しやすい傾向がある(たとえば、非ステロイド性抗炎症薬や、アセチルサリチル酸などの血小板(凝固の開始に関与する血球)の凝集を阻害する薬剤を使用している人、および/またはワルファリンなどの抗凝固薬を使用している人)。
抗うつ薬は(通常、治療の開始時と用量変更時)行動の変化、うつ病の悪化、自殺念慮を引き起こす可能性があります。あなた、患者、そしてあなたの家族が、不安、動揺、不眠症、過敏症、敵意、衝動性、アカシジア(精神運動性の興奮、つまり思考や運動)、躁病、軽躁病(症状の悪化)の出現に注意を払うことが重要です。気分、多幸感)およびその他の行動の変化。
これらの症状が現れた場合は、直ちに医師の診察を受ける必要があります。コハク酸デスベンラファキシンは、既往歴のない患者に動脈性高血圧の出現を誘発する可能性があるため、治療中は血圧を継続的にモニタリングすることが推奨されます。いくつかの研究では、血中のコレステロール量の増加が観察されており、血中コレステロール値を監視するために定期的な検査も推奨されています。不安定狭心症の患者は評価されませんでした。
この薬はドーピングを引き起こす可能性があります。
コハク酸デスベンラファクシンの副作用 – Eurofarma
非常に一般的な反応 (この薬を使用している患者の 10% 以上で発生します)
不眠症、頭痛、めまい、眠気、吐き気、口渇、多汗症(過剰な発汗)。
一般的な反応 (この薬を使用している患者の 1% ~ 10% で発生します)
食欲減退、離脱症候群、不安、神経過敏、異常な夢、イライラ、性欲減退、無オルガズム(性的快感やオーガズムの欠如)、振戦、感覚異常(しびれやうずき)、注意障害、味覚障害(味覚の変化)、かすみ目、散瞳(瞳孔の散大)、めまい(めまい)、耳鳴り(耳鳴り)、頻脈(心拍の速まり)、動悸、血圧上昇、ほてり、あくび、下痢、嘔吐、便秘、発疹、筋骨格系のこわばり、勃起不全、遅漏、疲労感、無力症(脱力感)、悪寒、緊張感、肝機能検査異常、体重増加、体重減少。
まれな反応 (この薬を使用している患者の 0.1% ~ 1% で発生)
過敏症(アレルギー)、離人症、異常なオーガズム、失神(失神)、ジスキネジア(主に口、舌、顔の筋肉の不随意運動で、舌が外に出て口の端から端への動きを伴う)、起立性低血圧(立つと血圧が下がる)、四肢冷え、鼻出血(鼻血)、脱毛症(脱毛)、尿閉、排尿躊躇、蛋白尿(尿蛋白増加・尿蛋白消失)、射精障害、射精不全、性機能障害、血中コレステロールの増加、血中トリグリセリドの増加、血中プロラクチンの増加。
まれな反応(この薬を使用している患者の 0.01% ~ 0.1% で発生します)
低ナトリウム血症(血液中のナトリウム濃度の低下)、躁状態、軽躁状態、幻覚、セロトニン症候群(精神状態、運動などの変化)、発作、ジストニア(不随意でゆっくりとした反復的な筋収縮)、膵炎(膵臓の炎症) )急性、スティーブンス・ジョンソン症候群(皮膚や粘膜に水疱を伴う重度のアレルギー反応)、血管浮腫(皮膚や粘膜の深部の腫れ、通常はアレルギー起源)、光線過敏症反応(光に対する皮膚の過剰な感受性) )。デスベンラファクシンコハク酸塩を摂取した後、便中に錠剤の残留物質 (効果なし) が見つかる場合があります。本剤の有効成分はすでに吸収されておりますので、効果には影響ありません。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。また、顧客サービスを通じて会社に通知してください。
デスベンラファクシン コハク酸塩の特別集団 – Eurofarma
妊娠と授乳
この薬は、医師または歯科外科医のアドバイスなしに妊婦が使用しないでください。
この薬への曝露による胎児の安全性を保証する研究はありません。利益がこのリスクを上回る場合にのみ、それを示す必要があります。したがって、妊娠から出産までの間、医師または歯科外科医のアドバイスなしにこの薬を使用すべきではありません。妊娠の場合はその旨を伝えてください。
授乳中または授乳する予定がある場合は、デスベンラファキシンコハク酸塩一水和物は乳中に排泄され、女性や子供に対するこの薬の安全性は不明であるため、使用することはお勧めできません。
機械を運転して操作する能力
この薬は判断力、推論力、または運動能力を損なう可能性があります。コハク酸デスベンラファクシンがどのような影響を与えるかを理解するまでは、車の運転や機械の操作など、集中力が必要な活動を行う場合には注意してください。
コハク酸デスベンラファクシンの組成 – Eurofarma
プレゼンテーション
コーティングされた徐放性錠剤。
50 mg または 100 mg のコハク酸デスベンラファキシン一水和物を含む徐放性コーティング錠を 30 錠パックします。
経口使用。
大人用。
構成
各 50 mg 徐放性フィルムコーティング錠剤には次のものが含まれます。
| デスベンラファキシンコハク酸塩一水和物 |
75.87mg* |
| 賦形剤** | 1錠 |
*デスベンラファクシンコハク酸塩一水和物 75.87 mg はそれぞれ、デスベンラファクシン 50 mg に相当します。
**ヒプロメロース、微結晶セルロース、ステアリン酸マグネシウム、タルク、ポリビニルアルコール、マクロゴール、二酸化チタン、黄色酸化鉄および赤色酸化鉄。
各 100 mg 徐放性フィルムコーティング錠剤には次のものが含まれます。
| デスベンラファキシンコハク酸塩一水和物 |
151.77mg* |
| 賦形剤** | 1錠 |
*デスベンラファクシンコハク酸塩一水和物 151.77 mg はそれぞれ、デスベンラファクシン 100 mg に相当します。
**ヒプロメロース、微結晶セルロース、ステアリン酸マグネシウム、タルク、ポリビニルアルコール、マクロゴール、二酸化チタン、キノリンイエローアルミニウムレーキ、ベンガラ。
デスベンラファクシンコハク酸塩の過剰摂取 – Eurofarma
一度に大量のコハク酸デスベンラファクシンを摂取した場合は、直ちに医師に連絡してください。デスベンラファクシンに対する特異的な解毒剤(作用を妨げる物質)は知られていません。嘔吐を誘発することはお勧めできません。
治療は次の内容で構成されます。
- 気道をきれいにし、呼吸を正常に保ちます。
- 口から胃まで設置したプローブによる胃洗浄。
- 活性炭の使用。
コハク酸デスベンラファキシンの薬物相互作用 – Eurofarma
デスベンラファクシンコハク酸塩と出血の素因を高める薬剤を併用(同じ期間)すると、自然出血のリスクが高まる可能性があります。体内のセロトニン量を増加させる可能性のある他の薬剤(他の抗うつ薬、抗精神病薬、アンフェタミン、ドーパミン拮抗薬、病院用麻酔薬)とコハク酸デスベンラファクシンを併用すると、セロトニン症候群(過剰なセロトニンに対する体の反応)の発症リスクが高まる可能性があります。これは、落ち着きのなさ、行動の変化、筋肉の硬直、体温の上昇、反射速度の上昇、致命的な可能性のある震えを引き起こします)。
この薬は中枢神経系に作用するため、アルコールとの併用は推奨されません。コハク酸デスベンラファクシンの使用により、フェンシクリジンとアンフェタミン、血清トランスアミナーゼ (肝酵素)、脂質、タンパク尿 (尿中のタンパク質の増加/尿中のタンパク質の除去) に関する尿検査など、一部の臨床検査の結果が変化する可能性があります。
他の薬を服用している場合は、医師または歯科医に伝えてください。医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
コハク酸デスベンラファクシンの食品相互作用 – Eurofarma
これまでのところ報告はありません。
コハク酸デスベンラファクシンという物質の作用 – Eurofarma
効果の結果
うつ病の治療法としてのデスベンラファクシンの有効性は、大うつ病性障害の診断基準を満たした成人外来患者を対象とした4件の固定用量プラセボ対照二重盲検無作為化8週間研究と2件の再発予防研究で確立されている。および精神障害の統計 (DSM-IV)。最初の研究では、患者はデスベンラファクシン 100 mg (n = 114)、200 mg (n = 116)、または 400 mg (n = 113) を 1 日 1 回、またはプラセボ (n = 118) の投与を受けました。 2 番目の研究では、患者は 1 日 1 回デスベンラファクシン 200 mg (n = 121) または 400 mg (n = 124) またはプラセボ (n = 124) を投与されました。他の2つの研究では、患者は1日1回デスベンラファクシン50 mg (n = 150およびn = 164)または100 mg (n = 147およびn = 158)またはプラセボ(n = 150およびn = 161)を投与されました。
デスベンラファクシンは、4つの研究で17項目のハミルトンうつ病評価尺度(HAM-D 17 )の合計スコアの改善によって測定され、そのうちの3つの研究では臨床全体印象尺度 – 改善(CGI-I)に基づいて測定されたプラセボよりも優れていることを示しました。 4つの研究。
長期研究では、DSM-IVの大うつ病性障害基準を満たす、デスベンラファクシン50mg/日による8週間の非盲検急性治療に反応し、その後デスベンラファクシンによる12週間安定状態を維持した成人外来患者を、二重のグループに無作為に割り付けた。再発について最大26週間観察し、積極的な治療を続けるかプラセボに切り替えるかを盲目的に選択します。開放相中の反応は、HAM-D 17の合計スコアとして定義されました。 11 で CGI-I ですか? 56日目の評価では2位。安定性は、HAM-D 17でフルスコアを持たないものとして定義されました。オフィス訪問の場合は 16 回。二重盲検段階での再発は次のように定義されました。
- HAM-D 17の合計スコア ?オフィス訪問の場合は 16 回。
- 有効性反応が不十分であるため中止。
- うつ病のため入院。
- 自殺未遂。
- 自殺。
継続的なデスベンラファクシン治療を受けた患者は、プラセボと比較して統計的に有意に再発までの時間が長かった。 26週時点でのカプラン・マイヤー推定再発確率は、デスベンラファクシン治療では14%、プラセボでは30%でした。
2番目の長期研究では、DSM-IVの大うつ病性障害基準を満たし、デスベンラファキシンによる12週間の急性治療に反応した成人外来患者が、急性治療中に投与された患者と同じ用量(200または400mg/日)に無作為に割り付けられた。または再発についてはプラセボを最長 26 週間観察します。開放相中の反応は、HAM-D 17 lt の合計スコアとして定義されました。二重盲検段階での再発は、84 日目の評価で次のように定義されました。
- HAM-D 17の合計スコア ?オフィス訪問の場合は 16 回。
- CGI-I スコア?オフィス訪問の場合は 6 (84 日目と比較)。
- 反応が不十分なため研究を中止。
デスベンラファクシンによる継続治療を受けた患者は、プラセボを受けた患者と比較して、その後の 26 週間の再発率が有意に低かった。
治療結果と年齢および性別との関係を分析したところ、これらの患者の特徴に基づく反応性の差異は示唆されませんでした。これらの研究では、人種が転帰に与える影響を判断するのに十分な情報がありませんでした。
薬理学的特徴
前臨床研究では、デスベンラファクシンが選択的セロトニンおよびノルエピネフリン再取り込み阻害剤 (SNRI) であることが実証されています。デスベンラファクシンの臨床効果は、中枢神経系におけるこれらの神経伝達物質の作用の増加に関連しています。
デスベンラファクシンは、インビトロでムスカリン性コリン作動性受容体、H1-ヒスタミン作動性受容体、またはβ1-アドレナリン作動性受容体を含むいくつかの受容体に対して有意な親和性を持たない。これらの受容体における薬理学的活性は、他の向精神薬で見られるいくつかの抗コリン作用、鎮静作用、および心臓血管作用と関連していることが示唆されています。同じ包括的な結合プロファイリングアッセイにおいて、デスベンラファクシンは、カルシウム、塩化物、カリウム、ナトリウムイオンチャネルを含むいくつかのイオンチャネルに対して有意な親和性を示さなかった。また、モノアミンオキシダーゼ (MAO) に対する阻害活性も示されませんでした。デスベンラファクシンは、インビトロ心臓カリウムチャネル (hERG) 研究では有意な活性を示さなかった。
前臨床げっ歯類モデルにおいて、デスベンラファクシンは、抗うつ作用、抗不安作用、体温調節作用、および疼痛抑制作用の予測活性を実証しました。
薬物動態学的特性
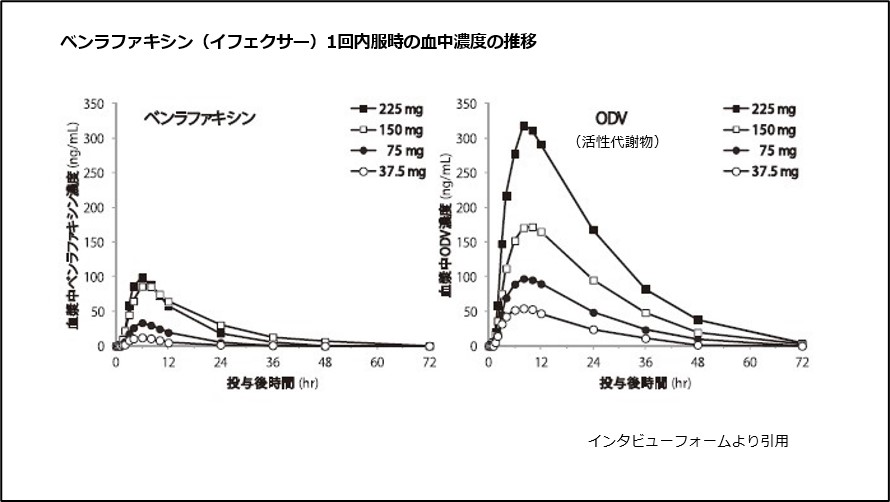
デスベンラファクシンの単回用量の薬物動態は直線的であり、50 ~ 600 mg/日の用量範囲にわたって用量に比例します。平均終末半減期 (t 1/2 ) は約 11 時間です。 1 日 1 回の投与では、約 4 ~ 5 日で定常状態の血漿濃度に達します。定常状態では、デスベンラファクシンの複数回投与の蓄積は直線的であり、単回投与の薬物動態プロファイルから予測可能です。
デスベンラファクシンの薬物動態は、女性と男性で十分に評価されています。性別による違いは最小限でした。全個人のデータを以下に示します。
吸収と分配
デスベンラファキシンコハク酸塩一水和物はよく吸収され、絶対経口バイオアベイラビリティは 80% です。最大血漿濃度までの平均時間(T max )は、経口投与後約7.5時間である。 100 mg の複数回投与後に、それぞれ 6,747 ng.h/mL および 376 ng/mL の AUC およびCmaxが観察されます。
食事の影響
健康な対象者への絶食時および食物存在下(高脂肪食)でのデスベンラファクシンの投与を含む食物存在研究では、食物存在下でCmaxが約 16% 増加する一方、AUC は同等であることが示されました。この違いは臨床的には重要ではありません。したがって、デスベンラファキシンは食事に関係なく摂取できます。

デスベンラファクシンの血漿タンパク質結合は低く (30%)、薬物濃度には依存しません。静脈内投与後の定常状態におけるデスベンラファクシンの分布量は 3.4 L/kg であり、非血管区画への分布を示しています。
代謝と排出
デスベンラファクシンの約 45% は変化せずに尿中に排泄されます。デスベンラファクシンは主に抱合(UGT1A1、UGT1A3、UGT2B4、UGT2B15、UGT2B17 などの UGT アイソフォームによって媒介される)によって代謝され、程度は低いですが酸化代謝によって代謝されます。
投与量の約 19% がグルクロニド代謝産物として排泄されます。尿中の酸化代謝物 (N,O-ジデスメチルベンラファキシン) として 5%。 CYP3A4 は、デスベンラファクシンの酸化代謝 (N-脱メチル化) を媒介する主要なシトクロム P450 アイソザイムです。
高齢者向けの使用
最大300 mgの用量を受けた健康な被験者を対象に実施された研究では、年齢に応じてデスベンラファクシンクリアランスが減少し、300歳以上の被験者ではCmaxが32%増加し、AUC値が55%増加しました。 mg. 18〜45歳の個人と比較して75歳。高齢患者(65歳以上)と若年患者の間で安全性や有効性に関して差は観察されなかったが、一部の高齢患者の感受性が高いことは無視できない。年齢のみに基づいて用量を調整する必要はありませんでした。ただし、使用量を決定する際には、デスベンラファクシンの腎クリアランスの低下の可能性を考慮する必要があります。
小児への使用
18 歳未満の患者に対する安全性と有効性は確立されていません。
腎不全患者
デスベンラファキシンコハク酸塩一水和物 100 mg の薬物動態は、軽度 (n = 9)、中等度 (n = 8)、および重度 (n = 7) の腎不全および透析を必要とする末期腎疾患 (ESRD) を有する被験者 (n = 7) を対象に研究されました。 9)および年齢が一致した健康な対照被験者(n = 8)。クリアランスはクレアチニンクリアランスと有意に相関していた。総体内クリアランスは、健康な被験者と比較して、軽度では29%、中等度では39%、重度では51%、ESRDでは58%減少しました。このクリアランスの減少により、軽度の腎障害のある個人 (24 時間 CrCl = 50 ~ 80 mL/分) では AUC が 42%、中等度の腎障害のある個人 (24 時間 CrCl = 30 ~ 50 mL/分) では 56% 増加しました。108重症者(24 時間の CrCl lt; 30 mL/min)では %、ESRD 患者では 116% でした。
平均終末半減期 (t1/2) は、健康な被験者の 11.1 時間から 13.5 時間に延長されました。 15.5;軽度、中等度、重度の腎不全とESRDのある人ではそれぞれ17.6時間と22.8時間。
標準的な 4 時間の血液透析手順中に除去される体内の薬物は 5% 未満でした。したがって、透析後の患者に追加用量を投与すべきではありません。重度の腎障害のある患者には用量調整が推奨されます。
肝不全患者
デスベンラファキシンコハク酸塩一水和物 100 mg の薬物動態は、軽度 (チャイルド ピュー A、n = 8)、中等度 (チャイルド ピュー B、n = 8)、重度 (チャイルド ピュー C、n = 8) の肝障害のある被験者で研究されました。 )および健康な人(n = 12)。
平均 AUC は、健常者と比較して、中等度および重度の肝障害患者ではそれぞれ約 31% および 35% 増加しました。平均AUC値は、軽度の肝障害のある被験者と健康な被験者で同等でした(差<5%)。
全身クリアランス(CL/F) は、健常者と比較して、中等度および重度の肝障害患者ではそれぞれ約 20% および 36% 減少しました。 CL/F値は、軽度の肝障害のある被験者と健康な被験者で同等でした(差<5%)。
平均t 1/2 は、健康な被験者および軽度の肝障害のある被験者の約10時間から、中等度および重度の肝障害のある被験者ではそれぞれ13時間および14時間に変化した。
QTc間隔の詳細な研究
健康な女性を対象に前向きに決定された基準を使用した QTc 間隔の徹底的な研究では、デスベンラファクシンは QT 間隔の延長を引き起こしませんでした。さらに、QRS 間隔への影響は観察されませんでした。
前臨床安全性データ
発がん性
デスベンラファクシンコハク酸塩一水和物をマウスおよびラットに2年間強制経口投与しても、どの研究でも腫瘍の発生率は増加しませんでした。
マウスには、最大500/300 mg/kg/日の用量でデスベンラファクシンを投与した(投与45週間後に減量)。 300 mg/kg/日の用量は、ヒトの最大推奨用量 (MRHD) 200 mg/日の 90 倍 (mg/kg) であり、MRHD の 7 倍 (mg/m 2 ) です。
ラットには、最大 300 mg/kg/日 (雄) または 500 mg/kg/日 (雌) の用量でデスベンラファクシンが投与されました。最高用量は、MRHD 200 mg/日の 90 (男性) または 150 (女性) 倍 (mg/kg)、DHMR 200 の 15 (男性) または 24 (女性) 倍 (mg/m 2 ) でした。 mg/日。
変異原性
デスベンラファクシンは、 in vitro細菌突然変異アッセイ (Ames 試験) では変異原性がなく、CHO 細胞培養におけるin vitro染色体異常アッセイ、 in vivoマウス小核アッセイ、またはマウスにおける in vivoマウス小核異常アッセイでも染色体異常誘発性ではありませんでした。 。さらに、デスベンラファクシンは、 in vitro哺乳類 CHO 細胞進行突然変異アッセイでは遺伝毒性がなく、BALB/c-3T3 マウス胚のin vitro細胞形質転換アッセイでは陰性でした。
生殖能力の低下
生殖能力の低下は、ラットとコハク酸デスベンラファキシン一水和物を投与された前臨床研究で観察されました。
この効果は、ヒトへの最大用量 (MRDH) 200 mg/日の約 30 倍 (mg/kg) および 5 倍 (mg/m 2 ) の経口用量で認められました。2 経口用量では生殖能力に影響はありませんでした。 DHMR の約 9 倍 (mg/kg 単位) および 1.5 倍 (mg/m 単位) です。この発見とヒトにおける関連性は不明です。
催奇形性
デスベンラファクシンを器官形成期の妊娠ラットおよびウサギに経口投与した場合、試験したどの用量でも、最大 30 倍(mg/kg 単位)および最大 5 倍(mg/m 2単位)でラットに催奇形性の証拠はありませんでした。 ) ラットにおけるヒトへの最大推奨用量 (MRHD) は 200 mg/日です。ウサギでは、200 mg/日の MRHD の 23 倍 (mg/kg 単位)、または MRHD の 7 倍 (mg/m 2単位) までの用量では催奇形性の証拠はありませんでした。しかしながら、胎児体重は、MRHDの30倍(mg/kg)および5倍(mg/m 2 )の無影響用量でラットにおいて減少した。
妊娠中および授乳中の妊娠ラットにコハク酸デスベンラファキシン一水和物を経口投与すると、授乳開始から最初の 4 日間で子の体重が減少し、死亡する子の数が増加しました。これらの死因は不明です。子犬の死亡率に対する無影響用量は、MRHD 200 mg/日の 30 倍 (mg/kg 単位) および 5 倍 (mg/m 2単位) でした。子の離乳後の成長と生殖能力は、MRHD の 90 倍 (mg/kg) および 15 倍 (mg/m 2 ) の用量でのデスベンラファクシンによる母親の治療によって影響を受けませんでした。
コハク酸デスベンラファクシンの治療効果が発現するまでの推定平均時間は最大 7 日です。
コハク酸デスベンラファクシンの保管ケア – Eurofarma
室温(15℃~30℃)で保管してください。湿気から守ります。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。
身体的特徴
デスベンラファキシンコハク酸塩 50 mg は、折り目のない円形、両凸、ピンク色のコーティング錠剤として提供されます。デスベンラファクシンコハク酸塩 100 mg は、折り目のない円形、両凸、アースレッドのコーティング錠剤として提供されます。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。すべての薬は子供の手の届かない場所に保管する必要があります。
デスベンラファクシンコハク酸塩の法的声明 – Eurofarma
登録 MS – 1.0043.1208
農場。返事。名詞:
イバネテ・A・ディアス・アッシ博士
CRF-SP 41.116
製造元:
ユーロファーム ラボラトリオス SA
ロッドプレス。カステッロ ブランコ、Km 35.6 イタペヴィ – SP
登録者:
ユーロファーム ラボラトリオス SA
Av. 市議会議員ホセ・ディニス、3,465 サンパウロ – SP
CNPJ: 61.190.096/0001-92
ブラジルの産業
医師の処方箋に基づいて販売します。処方箋が必要な場合のみ販売可能です。

-成分.jpg?resize=1200,491&ssl=1)






-1024x576.jpg?resize=1024,576&ssl=1)


