- スタチン(高コレステロール値の治療に一般的に使用される薬剤)の最大耐用量をスタチンまたはスタチン関連スタチンと併用しても、低密度リポタンパク質(LDL-C)(悪玉コレステロール)の事前に設定された目標レベルを達成できない患者他の脂質低下療法と併用。
- 単独療法として、または他の脂質低下(コレステロール低下)療法と組み合わせて、スタチンに不耐症の患者。
心血管疾患の罹患率と死亡率に対するプラルエントの影響はまだ確認されていません。

プラルエントはどのように機能しますか?
プラルエントは、LDL コレステロール (「悪玉コレステロール」として知られる) レベルの低下を促進します。
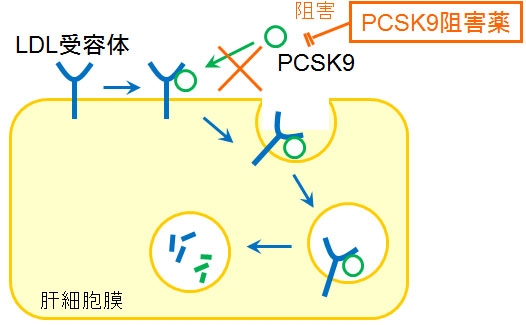
プラルエントの有効成分であるアリロクマブは、肝細胞によって分泌される PCSK9 (プロタンパク質転換酵素ズブチリシン クエキシン タイプ 9) として知られるタンパク質をブロックする完全ヒトモノクローナル抗体です。悪玉コレステロールは通常、肝臓の特定の受容体に結合することによって体から除去されます。 PCSK9はこれらの受容体の数を減少させ、悪玉コレステロールの増加を引き起こします。
PCSK9 をブロックすることにより、プラルエントは悪玉コレステロールの除去に役立つ受容体の数を増やし、血中の悪玉コレステロールの減少を促進します。

アクションを開始するまでの平均時間
臨床研究では、アリロクマブの脂質低下効果は初回投与後 15 日以内に観察され、約 4 週間で最大効果に達しました。
プラルエントの禁忌
プラルエントは、アリロクマブまたはその他の成分にアレルギーのある患者には禁忌です。
プラルエントの使い方
Praluent を投与する前に、使用説明書リーフレットを必ずお読みください。

プラルエントは、単回使用の充填済みペンを使用して、大腿、腹部、上腕に皮下注射として投与する必要があります。
注射部位をローテーションすることをお勧めします。
プラルエントは、日焼け、発疹(皮膚の発赤)、炎症、皮膚感染症などの活動性の皮膚病変や疾患のある領域には注射しないでください。
プラルエントは、同じ注射部位に他の注射薬と同時に注射しないでください。
プラルエントは、自己投与することも、皮下注射の適切な技術について医療専門家から指導を受けた後に他の人が投与することもできます。
投与後は、現在の法律で定められ、医師、看護師、または薬剤師の指示に従って、適切な耐穿刺性の容器にペンを廃棄してください。容器はリサイクルしてはなりません。容器は常に子供の手の届かないところに保管してください。

充填済みの Praluent ペンは再利用しないでください。
無菌技術や充填済みペンの正しい使用方法など、皮下注射の適切な技術について医師に指導を受けてください。
使用説明書

プラルエント ペンの部品はこの図に示されています。
75mg/mL
150mg/mL

重要な情報:
- このデバイスは 1 回限りの使い捨てペンです。 1 mL 中に 75 mg のプラルエント (アリロクマブ) が含まれています。
- プラルエント ペンには医師が処方した薬が含まれています。
- 薬は皮膚の下(皮下)に注射され、自分自身または他の人(介護者)が投与できます。
- このペンは 1 回の注射にのみ使用でき、使用後は廃棄する必要があります。
絶対です:
- Praluent ペンは子供の手の届かないところに保管してください。
- Praluent ペンを使用する前に、すべての指示をよくお読みください。
- Praluent ペンを使用するときは、必ず次の指示に従ってください。
- 未使用のペンは冷蔵庫 (2°C ~ 8°C) に保管してください。保管条件の詳細については、Praluent のリーフレットをご覧ください。
次のことを行ってはなりません:
- 黄色の安全カバーに触れてください。
- ペンを落としたり破損したりした場合は、ペンを使用してください。
- 青いキャップがないか、しっかりと取り付けられていない場合は、ペンを使用してください。
- ペンは再利用してください。
- ペンを振ってください。
- ペンをフリーズします。
- ペンを極度の熱(熱源の近く)にさらす。冷蔵室外に置く時間は 30°C で 24 時間を超えてはなりません。
- ペンを直射日光にさらしてください。
使用説明書が記載されたこのリーフレットを保管しておいてください。ご不明な点がございましたら、医師にご相談いただくか、0800-703-0014 に電話するか、 [email protected]まで電子メールを送信してください。
ステップ A – 注射の準備
始める前に、次のものが必要です。
- プラルエントのペンより。
- ティッシュをアルコールに浸したもの。
- 綿球またはガーゼ。
- 穴が開きにくい容器です。
1. ペンのラベルを確認します。
- 正しい製品を正しい用量で使用していることを確認してください。
- 有効期限を確認してください。有効期限が過ぎた場合は、ペンを使用しないでください。
2. ウィンドウを見てください。
- 液体が透明で、無色から淡黄色で、粒子状物質が含まれていないことを確認してください。そうでない場合は、製品を使用しないでください。
- 気泡が見られる場合がございます。これは正常です。
- 黄色が点灯している場合は、ペンを使用しないでください。
3. ペンを 30 ~ 40 分間室温に戻します。
- ペンを加熱しないでください。自然に室温に達するまで放置します。
- ペンは室温に戻ったらできるだけ早く使用してください。
- ペンを冷蔵庫に戻さないでください。
4. 注射部位を準備します。
- 石鹸と水で手を洗い、タオルで乾かしてください。
- 以下の場所に注射できます。 o 大腿部 o 腹部(へそ周囲 5 cm の領域を除く) o 腕の上部。
- 立っても座っても注射できます。
- アルコールに浸したティッシュで注射部位の皮膚を拭きます。
- 皮膚が敏感、硬くなっている、赤くなっている、または熱い箇所には貼らないでください。
- 目に見える静脈の近くには使用しないでください。
ステップ B – 注射方法
- 青いキャップを外します。
- 注射の準備ができるまでは青いキャップを取り外さないでください。
- 青いキャップは元に戻さないでください。
- Praluent ペンを図のように持ちます。
- 黄色の安全カバーには触れないでください。
- 窓が見えることを確認してください。
- 黄色の安全キャップが見えなくなるまで、ペンをしっかりと押し続けます。黄色の安全キャップが完全に押し込まれていないとペンは機能しません。
- 必要に応じて、皮膚を押して注射部位がしっかりしていることを確認します。
- 緑色のボタンを親指で押してすぐに放します。カチッという音が聞こえます。注射が始まりました。窓が黄色くなり始めます。
- ボタンを放した後もペンを肌に当て続けてください。
- 注入には最大 20 秒かかる場合があります。
- ペンを取り外す前に、ウィンドウが黄色くなっていないか確認してください。ウィンドウが完全に黄色になるまでペンを取り外さないでください。
- ウィンドウが完全に黄色に変わったら、注入は完了です。2 回目のクリック音が聞こえる場合があります。窓が完全に黄色にならない場合は、0800-703-0014 までお電話ください。医師に相談せずに 2 回目の投与を行わないでください。
- 皮膚からペンを引き抜きます。注射後は皮膚をこすらないでください。
- 出血が見られる場合は、出血が止まるまで綿球またはガーゼパッドをその領域に押し当ててください。
- ペンとキャップは捨ててください。青いキャップは元に戻さないでください。
- 地域の規制に従い、医師、看護師、または薬剤師の指示に従い、穴が開きにくい容器に入れて廃棄してください。容器は常に子供の手の届かないところに保管してください。
プラルエントの投与量
プラルエントの推奨開始用量は 75 mg を 2 週間に 1 回皮下投与することで、ほとんどの患者はこの用量で LDL-C レベルの適切な低下を達成しています。反応が不十分な場合は、2週間に1回の皮下投与で最大150mgまで増量することがあります。
医師は、ベースラインの LDL-C (悪玉コレステロール) レベル、治療目的、治療に対する反応 (75 mg または 150 mg) などの患者の特性に基づいて用量を個別に決定します。脂質レベルは、治療開始から 4 週間後に評価するか、滴定してそれに応じて用量を調整できます。
プラルエントは皮下にのみ投与してください。
小児患者
小児患者における安全性と有効性は確立されていません。
高齢の患者さん
高齢の患者には用量調整は必要ありません。
肝不全(肝機能の低下)
軽度から中等度の肝障害のある患者には用量調整は必要ありません。
重度の肝障害のある患者に関する利用可能なデータはない。
腎不全(腎機能の低下)
軽度から中等度の腎障害のある患者には用量調整は必要ありません。
重度の腎不全患者に関する利用可能なデータはない。
体重
患者の体重に基づいて用量を調整する必要はありません。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
プラルエントを使い忘れた場合はどうすればよいですか?
飲み忘れた場合は、できるだけ早く注射し、飲み忘れた日から 2 週間に 1 回のペースで治療を再開してください。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
プラルエントの予防措置
そう痒症(かゆみ)を含む一般的なアレルギー反応のほか、過敏症、貨幣状湿疹(皮膚上の楕円形の赤みを帯びた斑点)、蕁麻疹(かゆみを引き起こす、アレルギー性の皮膚上の盛り上がった赤みを帯びた斑点など)などの稀で時には重篤なアレルギー反応)および過敏性血管炎(血管の炎症)が臨床研究で報告されています。
重度のアレルギー反応が発生した場合は、プラルエントの使用を中止し、直ちに医師に相談してください。
糖尿病患者への注意: プラルエントには砂糖 (100 mg/mL スクロース) が含まれています。
薬物相互作用
他の薬剤に対するアリロクマブの影響
アリロクマブは生物学的製剤であるため、他の薬物に対するアリロクマブの薬物動態学的影響は予想されません。
アリロクマブをアトルバスタチンまたはロスバスタチンと組み合わせて投与した臨床研究では、アリロクマブの反復投与中にスタチン濃度の関連する変化は観察されず、これはシトクロム P450 酵素、主に CYP3A4 および CYP2C9 (肝臓に位置し、代謝に関与するシステム) が正常に機能していないことを示しています。いくつかの薬剤の影響を受けず、P-gp や OATP などの輸送タンパク質はアリロクマブの影響を受けませんでした。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
プラルエントの副作用
副作用の頻度は、次の規則に従って以下にリストされます。
- 非常に一般的な反応 (? 10%)。
- 一般的な反応 (? 1 および lt; 10%);
- 異常な反応 (? 0.1 かつ < 1%);
- まれな反応 (?0.01 および <0.1%);
- 非常にまれな反応 (lt;0.01%);
- 未知の反応 (入手可能なデータから推定できない)。
以下に記載する安全性データは、75 mg または 150 mg の用量で 2 週間に 1 回皮下投与されるアリロクマブで治療された 3,340 人の患者 (曝露期間 3,451 患者年年) におけるアリロクマブへの曝露を反映しています。治療期間は最長18か月(アリロクマブに少なくとも52週間曝露された患者2,408人、アリロクマブに少なくとも76週間曝露された患者639人を含む)。安全性データは、9件のプラセボ対照試験(4件の第2相研究と5件の第3相研究、いずれも基礎スタチン投与患者を対象)と5件のエゼチミブ対照第3相研究(3件は基礎スタチン投与患者を対象)の結果の統合分析に基づいている。スタチン)。
最も一般的な副作用(プラルエントで治療された患者の約 1%)は、注射部位反応、上気道の兆候と症状、およびそう痒症(かゆみ)でした。
プラルエントで治療された患者において治療中止につながる最も一般的な副作用は、注射部位反応でした。
臨床相試験プログラムで使用された 2 つの用量 (75 mg と 150 mg を 2 週間に 1 回) の間で安全性プロフィールに差は観察されませんでした。
対照研究では、プラルエントによる治療を受けた患者 1,158 人(34.7%)は 65 歳以上、患者 241 人(7.2%)は 75 歳以上でした。年齢の増加による安全性と有効性の有意差は観察されませんでした。
有害事象のリスト
以下の副作用は、臨床研究においてプラルエントで治療された患者において報告されました。
免疫系の障害
レア:
- 過敏症(アレルギー);
- 過敏性血管炎。
呼吸器、胸部、縦隔の疾患
一般:
上気道の兆候と症状*。
※主に中咽頭痛、鼻水、くしゃみが含まれます。
皮膚および皮下組織の疾患
一般:
かゆみ。
レア:
- 蕁麻疹;
- 貨幣状湿疹。
管理現場における一般的な混乱と状況
一般:
注射部位での反応*。
※紅斑・発赤、かゆみ、浮腫(腫れ)、痛み・圧痛を含む
一連の対照研究における、対照と比較した、プラルエントの使用で報告された一般的な副作用の頻度:
|
副作用 |
プラルエント (n=3340) |
対照 (n=1894) |
|
注射部位の反応* |
6.1% |
4.1% |
|
かゆみ |
1.0% |
0.4% |
|
上気道の兆候と症状** |
1.7% |
0.8% |
※紅斑・発赤、かゆみ、浮腫、痛み・圧痛を含みます。
**主に中咽頭の痛み、鼻水、くしゃみが含まれます。
選択された副作用の説明
注射部位の反応
紅斑/発赤、浮腫、痛み/圧痛などの注射部位の反応は、アリロクマブで治療された患者の6.1%で報告されたのに対し、対照群では4.1%でした。
注射部位のほとんどの反応は一時的で、程度は軽度でした。注射部位の反応による中止率は 2 つのグループ間で同等でした (アリロクマブ投与グループでは 0.2%、対照グループでは 0.3%)。
一般的なアレルギー反応
一般的なアレルギー反応は、主にそう痒症の発生率の違いにより、対照群よりもアリロクマブ群でより頻繁に報告されました。観察されたかゆみのケースは、通常、軽度で一過性のものでした。
さらに、過敏症、貨幣状湿疹、蕁麻疹、過敏性血管炎などの稀で時には重篤なアレルギー反応が対照臨床研究で報告されています。
肝酵素(肝臓)の異常
プラルエント治療を受けた患者の2.5%とプラセボ治療を受けた患者の1.8%で肝臓関連障害(主に肝酵素異常に関連する)が報告され、それぞれ患者の0.4%と0.2%で治療中止となった。
プラルエント治療を受けた患者の1.7%、プラセボ治療を受けた患者の1.4%で、正常値の上限の3倍を超える血清トランスアミナーゼ(肝損傷により血液中に増加する酵素)の増加が見られました。
免疫原性/抗薬物抗体 (ACAD)
すべてのタンパク質療法と同様に、免疫原性 (抗薬物抗体の形成) の可能性があります。第 3 相試験では、アリロクマブで治療された患者の 4.8% が治療中に出現した ACAD 反応を示したのに対し、対照群 (プラセボまたはエゼチミブ) では 0.6% でした。これらの患者の大部分は、中和活性を示さずに、一過性の低力価の ACAD 反応を示しました。
ACAD陰性の患者と比較して、ACAD陽性患者は、注射部位反応率が高かったこと(ACAD陽性患者では10.2%、ACAD陽性患者では5.9%)を除いて、アリロクマブへの曝露、有効性、安全性において何の違いも示さなかった。 ACAD陰性患者)。中和抗体(ACN)を持っていた患者はわずか1.2%で、全員がアリロクマブ投与群だった。
これらの患者の大部分は、陽性の中和サンプルを 1 つだけ持っていました。 2 つ以上の ACN サンプルが陽性だったのは 10 人の患者 (0.3%) のみでした。持続性ACNの存在下でプラルエント治療を継続した場合の長期的な影響は不明です。
注意: この製品は新薬であり、研究により許容できる有効性と安全性が示されていますが、たとえ正しく指示され使用されたとしても、予測できないまたは未知の有害事象が発生する可能性があります。この場合は医師または歯科医師に知らせてください。
プラルエント特別人口
妊娠と授乳
妊婦におけるプラルエントの使用に関する利用可能なデータはありません。他の IgG 抗体と同様に、アリロクマブは胎盤関門を通過すると予想されます。
スタチン併用療法での使用: スタチンは妊婦には禁忌です。それぞれの更新されたリーフレットを参照してください。
妊娠中のプラルエントの使用は推奨されません。
この薬は医師のアドバイスなしに妊婦が使用しないでください。妊娠が疑われる場合は、すぐに医師に知らせてください。
授乳期
アリロクマブが母乳中に排泄されるかどうかは不明です。
プラルエントは授乳中には推奨されません。プラルエントによる治療または授乳を中止する必要があるかどうかは医師が決定します。
スタチン併用療法での使用向け
スタチンは授乳中の女性には禁忌です。それぞれの更新されたリーフレットを参照してください。
車両の運転や機械の操作能力の変化
プラルエントは、機械の運転や使用能力にほとんど影響を与えないか、まったく影響しません。
プラルエントの成分
プレゼンテーション
使い捨てプレフィルドペン 75 mg/ml:
1個または2個のパック。
使い捨てプレフィルドペン 150 mg/ml:
1個入り。
皮下使用。
大人用。
構成
プラルエント 75mg/ml
皮下注射用のプラルエント溶液 1 ml には次のものが含まれます。
アリロクマブ 75 mg。
プラルエント 150mg/ml
皮下注射用のプラルエント溶液の各 mL には以下が含まれます。
アリロクマブ 150 mg。
賦形剤:
ヒスチジン、スクロース、ポリソルベート 20、注射用水。
プラルエントの過剰摂取
対照臨床研究では、推奨される 2 週間に 1 回の投与スケジュールよりも頻繁に投与しても、安全性の懸念は確認されていません。ただし、必要以上にプラルエントを使用した場合は、すぐに医師に知らせてください。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。
さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
プラルエント ストレージ ケア
プラルエントは冷蔵保存する必要があります (2°C ~ 8°C)。凍らせないでください。光から守ります。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。
投与前に、プラルエントを室温に戻してください。プラルエントは室温に達したらできるだけ早く使用してください。
プラルエントを冷蔵庫の外に放置して室温に戻す場合は、熱源の近くや直射日光の当たる場所に放置しないでください。冷蔵室外に置く時間は 30 °C で 24 時間を超えてはなりません。
身体的特徴
プラルエントは、無色から淡黄色の透明な溶液です。
すべての非経口薬は、投与前に粒子状物質の存在と変色について目視検査する必要があります。色の変化がある場合、または目に見える粒子状物質が含まれている場合は、その溶液を使用しないでください。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かない場所に保管する必要があります。
プラルエントの法律上の格言
登録 MS 1.1300.1160
農場。答え:
シルビア・レジーナ・ブロロ
CRF-SP No.9,815
登録者:
サノフィ・アベンティス・ファーマセウティカLTDA。
アヴ。シルビオ・デ・M・パディーリャ、5200
サンパウロ – SP
CNPJ 02.685.377/0001-57
製造元:
リジェネロン・ファーマシューティカルズ株式会社
81 コロンビア・ターンパイク・レンセラー
ニューヨーク 12144 – 米国
パッケージ化:
サノフィ ウィンスロップ インダストリー
ブールバード・インダストリアル
ゾーン インダストリエル 76580 ル
トレイト – フランス
梱包業者:
サノフィ・アベンティス・ドイツGmbH
Bruningstrasse 50、Industriepark Höchst、65926
フランクフルト・アム・マイン – ドイツ
輸入者:
サノフィ・アベンティス・ファーマセウティカLTDA。
Rua Conde Domingos Papaiz, 413
スザノ – SP
CNPJ 02.685.377/0008-23
ブラジルの産業
医師の処方箋に基づいて販売します。








-1024x576.jpg?resize=1024,576&ssl=1)


