また、ペニシリンまたはセファロスポリンにアレルギーのある患者の感染症の治療にも適応されます。

クロストリジウム・ディフィシルによって引き起こされる偽膜性大腸炎など、抗生物質の使用に伴う下痢の治療に経口的に使用できます。
グラム陽性微生物による感染が危険な患者(例えば、歯科または整形外科の手術が必要な患者)の予防に使用できます。
イミペネム + シラスタチンナトリウムの禁忌 – Nova Farma
この薬剤は、テイコプラニン(活性物質)に対する過敏症の病歴のある患者には禁忌です。
イミペネム + シラスタチンナトリウムの使い方 – Nova Farma
注射の準備手順:
アンプルからすべての希釈溶液をバイアルにゆっくりと加え、泡が発生しないように注意しながら、粉末が完全に溶解するまで手でゆっくりと転がします。
蓋近くの粉も含めて、すべての粉が確実に溶けていることを確認することが重要です。
溶液を撹拌すると泡が発生する可能性があり、必要な量を回復することが困難になります。ただし、すべての粉末が完全に溶解した場合、泡は溶液の濃度を変化させません。溶液が泡状になった場合は、ボトルを約 15 分間放置してください。ゴム栓の中央部分に針を置き、溶液の大部分を回収しようとして、バイアルから溶液をゆっくりと取り出します。
再構成された溶液には、3.0 mL 中に 200 mg のテイコプラニン (200 mg バイアルから)、および 3.0 mL 中に 400 mg (400 mg バイアルから) のテイコプラニンが含まれています。溶液を正しく調製し、シリンジに慎重に引き込むことが重要です。そうしないと、全用量が投与されなくなる可能性があります。
注射用希釈剤として水で戻した場合、溶液は室温で 48 時間、または冷蔵下 (温度 2 ~ 8°C) で 11 日間、効力を失うことなく安定です。ただし、医薬品の適正管理では、再構成した溶液を直ちに使用し、未使用部分は廃棄することが推奨されています。
再構成した溶液は直接注入することも、次のように希釈して注入することもできます。

医薬品の適正慣行として、溶液は調製後直ちに投与することが推奨されています。
非互換性
テイコプラニンとアミノグリコシドの溶液は直接混合すると混和しないため、注射前に混合しないでください。
管理モード:
テイコプラニンは、静脈内 (IV) または筋肉内 (IM) に投与できます。 IV 投与は、注射 (3 ~ 5 分) または点滴 (30 分) によって直接行うことができます。通常、1日の投与量は1回投与ですが、重篤な感染症の場合、最初の3回の投与は12時間間隔で初回投与量を投与することが推奨され、症状の重症度に応じて最大4日間持続する場合があります(初回投与は8回)。感染症。抗生物質感受性微生物による感染症の患者のほとんどは、最初の 48 ~ 72 時間以内に治療反応を示します。総治療期間は、感染症の種類と重症度、および患者の臨床反応によって決まります。心内膜炎や骨髄炎の場合は3週間以上の治療が推奨されます。
新生児には点滴投与のみが使用できます。テイコプラニンの用量を決定する際には、病気の重症度と感染部位を考慮する必要があります。
投与量
大人:
グラム陽性感染症全般の場合:
攻撃量:
12時間ごとに400 mg IVを3回投与。
維持量
:
1日1回400mgをIVまたはIMで投与します。
敗血症、骨関節感染症、心内膜炎、重度の肺炎、およびグラム陽性菌によって引き起こされるその他の重篤な感染症の場合、一般的に:
攻撃量:
最初の 3 回の投与では 400 mg を 12 時間ごとに IV で投与します。感染の重症度に応じて最大 4 日間持続します (初回投与は 8 回)。
維持量:
1日1回400mg IVまたはIM。
標準用量 400 mg は、約 6 mg/kg に相当します。
体重が 85 kg を超える患者には、6 mg/kg の用量を使用する必要があります。
臨床状況によっては、より高い用量が必要になる場合があります。
重度の感染熱傷や黄色ブドウ球菌による心内膜炎の患者など、状況によっては、最大 12 mg/kg の IV 維持量が必要となる場合があります。
黄色ブドウ球菌によって引き起こされる心内膜炎の場合、テイコプラニンを他の抗生物質と一緒に投与すると満足のいく結果が得られました。この適応症に対するテイコプラニン単独療法の有効性はまだ研究中です。
重篤な感染症で血清テイコプラニン濃度を監視する場合、そのレベル(次の投与の直前)はMIC(最小発育阻止濃度)の10倍、または少なくとも10 mg/Lに相当する必要があり、状況に応じて15~20 mg/Lになる場合があります。感染症の重症度。
併用療法:
感染症が最大限の殺菌活性を必要とする場合、適切な殺菌剤との併用が推奨されます(ブドウ球菌性心内膜炎など)、またはグラム陰性病原体との混合感染が排除できない場合(好中球減少症患者における発熱の経験的治療など)。
歯科外科および弁膜症患者におけるグラム陽性心内膜炎の予防:
麻酔導入時に 400 mg (6 mg/kg) を静脈内投与。
整形外科および血管外科におけるグラム陽性感染症の予防:
麻酔導入時に 400 mg (または 85 kg を超える場合は 6 mg/kg) の IV 用量。
抗生物質に関連したクロストリジウム・ディフィシルによって引き起こされる下痢:
バイアル内の粉末を希釈溶液で再構成した後、溶液は経口溶液として投与する必要があります(溶液には味がありません)。通常の用量は、200 mg を 1 日 2 回、7 ~ 14 日間経口投与します。
くも膜下腔内/腰腔内および脳室内経路を介したテイコプラニン投与の有効性と安全性は、対照臨床研究では研究されていません。しかし、テイコプラニンの脳室内使用による発作などの毒性例が報告されています。
特別な集団に対する投与量
お年寄り:
成人と同じ用量(腎機能が重度に低下している場合は、腎機能が低下している患者に対する指示に従う必要があります)。
生後2か月を超えて16歳までの子供:
一般的なグラム陽性感染症の場合: 推奨用量は、最初の 3 回の投与 (負荷用量) では 12 時間ごとに 10 mg/kg を静脈内投与します。その後の 1 日用量は、1 回の静脈内または筋肉内注射で 6 mg/kg とする必要があります (維持用量)。
グラム陽性微生物による重度の感染症または好中球減少症の小児の場合:
推奨される負荷用量は、最初の 3 回の投与では 12 時間ごとに 10 mg/kg を静脈内投与します。その後の毎日の維持用量は、1 回の静脈内または筋肉内注射で 10 mg/kg とする必要があります。
生後2か月未満の新生児:
初日には 16mg/kg の単回負荷用量を静脈内投与することが推奨されます。その後の毎日の維持用量は 8 mg/kg 静脈内投与する必要があります。 30 分間かけて静脈内点滴により投与することが推奨されます。
腎不全の患者:
腎不全患者の場合、治療4日目までは用量を減らす必要はありませんが、この期間以降は血清濃度が少なくとも10mg/Lを維持するように用量を調整する必要があります。 5 日目以降は、次の計画に従う必要があります。
- クレアチニンクリアランスが 40 ~ 60 mL/min である中等度の腎不全では、維持量を半分に減らす必要があります(通常の維持量を 2 日ごとに使用するか、この用量の半分を 1 日 1 回使用します)。
- クレアチニンクリアランスが40mL/分未満の重度の腎不全、および血液透析を受けている患者では、維持量を通常の用量の3分の1に減らす必要があります(この用量を3日ごとに使用するか、用量の3分の1を1日1回使用します)。 。テイコプラニンは透析可能ではありません。
腹膜炎に対する持続外来腹膜透析:
400 mg IV の単回負荷用量の後、1 週目にバッグあたり 20 mg/L、2 週目に交互のバッグで 20 mg/L、3週目にオーバーナイトバッグで 20 mg/L が投与されます。
したがって、安全性を確保し、この薬の有効性を保証するために、投与は静脈内または筋肉内にのみ行う必要があります。
イミペネム + シラスタチンナトリウムの注意事項 – Nova Farma
過敏反応
テイコプラニン(活性物質)では、重度で生命を脅かす、時には致死的な過敏反応(アナフィラキシーショックなど)が報告されています。テイコプラニン(活性物質)に対するアレルギー反応が発生した場合は、治療を直ちに中止し、適切な緊急措置を開始する必要があります。
致命的なアナフィラキシーショックを含む交差過敏症反応が起こる可能性があるため、バンコマイシンに対する過敏症の既往歴のある患者には本製品を慎重に投与する必要があります。しかし、バンコマイシンによる「レッドマン症候群」の病歴は、テイコプラニン(活性物質)の使用に対する禁忌にはなりません。
輸液関連の反応
「レッドマン症候群」(そう痒症、蕁麻疹、紅斑、血管神経性浮腫、頻脈、低血圧、呼吸困難などの症状の複合体)は、(初回投与時であっても)ほとんど観察されません。
注入を中止したり、注入を遅らせたりすると、これらの反応が中断される可能性があります。 1 日量をボーラスとして投与せず、30 分間かけて注入する場合、注入関連反応は限定される可能性があります。
重度の水疱性反応
テイコプラニン(活性物質)の使用により、生命を脅かす、あるいは致命的な皮膚反応、スティーブンス・ジョンソン症候群(SJS)および中毒性表皮壊死融解症(TEN)が報告されています。 SJS または TEN の症状または兆候 (例、水疱や粘膜病変を伴う進行性の皮膚発疹) が存在する場合は、テイコプラニン (活性物質) による治療を直ちに中止する必要があります。
監視
テイコプラニン(活性物質)による血液毒性、聴覚毒性、肝臓毒性、腎臓毒性の症例が報告されています。したがって、特に腎不全患者、長期治療を受けている患者、および聴器毒性および腎毒性効果を有する可能性のある薬剤の併用が必要な患者では、聴覚、血液、肝臓および腎臓の機能をモニタリングすることが推奨されます。
重複感染
他の抗生物質と同様、テイコプラニン (活性物質) の使用は、特に長期にわたる場合、耐性微生物の異常増殖を引き起こす可能性があります。患者の状態を繰り返し評価することが不可欠です。治療中に重複感染が発生した場合は、適切な措置を講じる必要があります。
血小板減少症
テイコプラニン(活性物質)の使用により血小板減少症が報告されています。治療中は全血球計算を含む定期的な血液検査が推奨されます。
非推奨ルートでの利用のリスク
くも膜下腔内/腰腔内および脳室内経路を介したテイコプラニン (活性物質) の投与の有効性と安全性は、対照臨床研究では研究されていません。しかし、テイコプラニン(活性物質)の脳室内使用による発作を含む毒性の症例が報告されています。
したがって、安全性を確保し、この薬の有効性を保証するために、投与は静脈内または筋肉内にのみ行う必要があります。
車両の運転や機械の操作能力の変化
テイコプラニン(活性物質)は、頭痛やめまいなどの副作用を引き起こす可能性があります。車両の運転や機械の操作能力に影響が出る可能性があります。これらの有害事象が発生した患者は、車両を運転したり機械を操作したりしてはなりません。
妊娠と授乳
動物生殖研究では生殖能力の変化や催奇形性の影響の証拠は明らかにされていませんが、医師の判断で潜在的な利点が潜在的なリスクを克服しない限り、テイコプラニン(活性物質)は妊娠が確認または推定されている間、または授乳中に使用すべきではありません。母乳中のテイコプラニン (活性物質) の排泄や、薬物の胎盤移行に関する情報はありません。
妊娠リスクカテゴリー:B.
この薬は、医師または歯科外科医のアドバイスなしに妊娠中の女性が使用すべきではありません。
イミペネム + シラスタチンナトリウムの副作用 – Nova Farma
- 非常に一般的な反応 (gt; 1/10)
- 一般的な反応 (gt; 1/100 および ?1/10)
- 異常な反応 (>1/1,000 および ~1/100)
- まれな反応 (gt; 1/10,000 および ~1/1,000)
- 非常にまれな反応(?1/10,000)
テイコプラニンは一般に忍容性が良好です。既知の副作用が治療の中断を必要とすることはほとんどなく、一般に穏やかで一時的な性質のものです。重篤な副作用はまれです。以下のような反応が報告されています。
一般的な障害および投与部位の変化:
筋肉内注射部位の紅斑、局所的な痛み、血栓性静脈炎および膿瘍。
免疫系の障害:
過敏症:発疹、そう痒症、発熱、硬直、気管支けいれん、アナフィラキシー反応、アナフィラキシーショック、蕁麻疹、血管浮腫、DRESS症候群(好酸球増加症および全身症状を伴う薬物反応)および稀な剥離性皮膚炎、中毒性表皮壊死融解症、多形紅斑、スティーブンス・ジョンソン。
さらに、輸液に関連した反応と呼ばれる、
「レッドマン症候群」
。
これらの事象は、過去にテイコプラニンへの曝露歴がなくても発生し、より遅い注入速度および/または濃度の低下による再曝露では再発しませんでした。これらの事象は、濃度や注入速度に特有のものではありませんでした。
胃腸障害:
吐き気、嘔吐、下痢。
血液およびリンパ系の障害:
好酸球増加症、白血球減少症、好中球減少症、血小板減少症、および可逆性無顆粒球症のまれなケース。
肝障害:
血清トランスアミナーゼおよび/または血清アルカリホスファターゼの増加。
腎臓および泌尿器疾患:
血清クレアチニンの上昇、腎不全。
神経系障害:
めまい、頭痛、けいれん。
耳迷路障害:
難聴/難聴、耳鳴り、前庭障害。
これらの場合、テイコプラニンの使用と難聴、耳鳴りおよび前庭障害との間の因果関係は確立されていません。テイコプラニンの聴器毒性はバンコマイシンよりも低いです。
感染症と蔓延:
重複感染(非感受性微生物の過剰増殖)。
有害事象が発生した場合は、健康監視通知システム – NOTIVISA (http://www.anvisa.gov.br/hotsite/notivisa/index.htm) または州または地方自治体の健康監視に通知してください。
イミペネム + シラスタチンナトリウムの薬物相互作用 – Nova Farma
動物実験では、ジアゼパム、チオペンタール、モルヒネ、神経筋遮断薬、またはハロタンとの相互作用は示されていません。
副作用が増加する可能性があるため、アミノグリコシド(抗生物質クラス)、アムホテリシンB(抗真菌薬)、シクロスポリン(免疫系抑制薬)、フロセミド(利尿薬)、エタクリン酸。
テイコプラニン(活性物質)とアミノグリコシド溶液は混合すると混和しないため、注射前に混合しないでください。
イミペネム + シラスタチンナトリウムという物質の作用 – Nova Farma
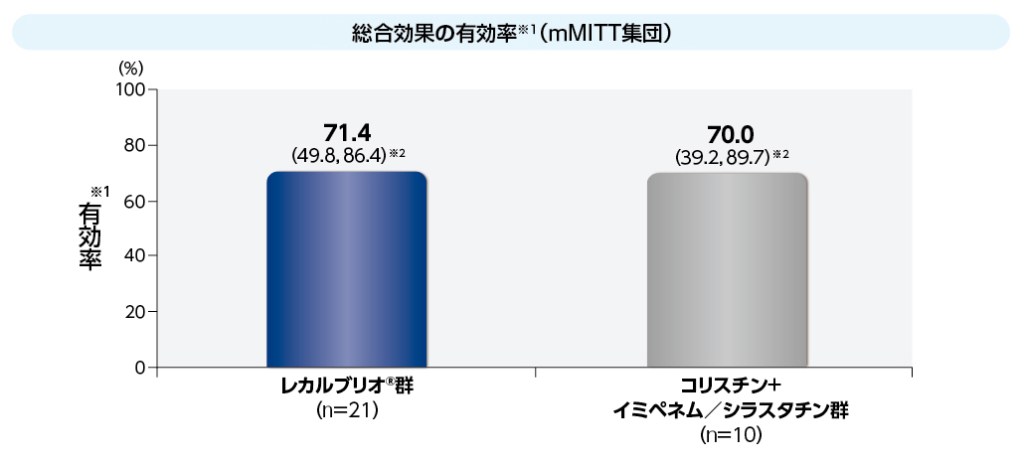
効果の結果
テイコプラニン (活性物質) は、グラム陽性菌によって引き起こされる心内膜炎の治療に効果があることが示されています。
テイコプラニン (活性物質) は、クロストリジウム ディフィシル関連下痢 (CDAD) の治療において他の薬剤と同様に有効でした。テイコプラニン(活性物質)を投与されたグループの再発率は低かった。 119人の患者が、CDADの治療のためにフシジン酸、メトロニダゾール、テイコプラニン(活性物質)またはバンコマイシンを受ける群に無作為に割り付けられた。テイコプラニン (活性物質) の用量は 400 mg、1 日 2 回、10 日間でした。治癒率はテイコプラニン(活性物質)で96%、フシジン酸で93%、メトロニダゾールで94%、バンコマイシンで94%でした。再発した患者の割合は、テイコプラニン (活性物質) で 7%、フシジン酸で 28%、メトロニダゾールで 16%、バンコマイシンで 16% でした。
ヒックマンカテーテルを使用した88人の患者を対象としたランダム化研究では、非テイコプラニン療法と比較して、テイコプラニン療法を行った場合、挿入部位の感染症とカテーテル関連のグラム陽性敗血症の数が減少しました。予防としてのテイコプラニン(活性物質)は、特に化学療法後の好中球減少症の期間中に、カテーテル関連敗血症の発生率を減らすためにヒックマンカテーテルの挿入を必要とする患者に日常的に使用できます。
テイコプラニン (活性物質) は、血液悪性腫瘍患者のカテーテル感染症におけるバンコマイシンの代替薬となります。バンコマイシンとテイコプラニン(活性物質)を比較したところ、奏効率はそれぞれ80%、69%でした。
公開臨床研究では、テイコプラニン(活性物質)はグラム陽性感染症患者 18 人の治療に有効でした(Walsh et al、1988)。患者は、維持療法として1日1回、400 mgの静脈内(IV)負荷用量、および200 mg(n = 13)および400 mg(n = 5)の筋肉内(IM)用量を受けました。平均17日。患者には次のような症状がありました:骨髄炎、プロテーゼ関連感染症、心内膜炎、皮膚および結合組織感染症、尿路感染症。 18 人中 11 人 (61%) の患者が臨床的に治癒しました。メチシリン耐性黄色ブドウ球菌に感染した患者の治癒率は 83% であると報告されています。骨と関節にプロテーゼ関連の感染症を患っていた 4 人の患者は、臨床的な改善が起こる前にプロテーゼの除去を必要としました。副作用は 2 人の患者に限定されており、肝機能検査の異常 (アスパラギン酸アミノトランスフェラーゼ、ビリルビン、尿素の上昇) が発生し、1 人の患者では黄疸を伴いました。テイコプラニン (活性物質) のトラフ血清濃度の範囲は 2.3 ~ 17.7 mcg/mL で、400 mg の用量で平均 2.9 mcg/mL 増加しました。テイコプラニン (活性物質) は、グラム陽性感染症の治療において安全で効果的であることが示されています。
テイコプラニン (活性物質) 400 mg の初回投与、その後 200 mg の IV を 1 日 1 回、5 ~ 7 日間続けると、重篤なグラム陽性感染症 (主に敗血症) の治療に効果的であることが報告されています。患者17人中15人で。最初に分離された微生物は表皮ブドウ球菌(患者 15 人)で、アミノグリコシド系抗生物質とベータラクタム系抗生物質の併用療法に耐性がありました。多施設共同研究では、テイコプラニン(活性物質)は、さまざまなグラム陽性細菌感染症の患者 29 人において安全で効果的でした。
テイコプラニン (活性物質) はバンコマイシンより安全であると考えられ、3 ~ 10 mg/kg の用量で投与しても用量関連の有害事象は示されません。
2 歳から 12 歳までの小児において、テイコプラニン (活性物質) は小児患者のグラム陽性感染症の治療に非常に効果的で忍容性が高いことが判明しています。用量は 3 ~ 6 mg/kg の間で変化しました。
新生児では、テイコプラニン(活性物質)による治療に関連した副作用の発生率が低いことが報告されています。この薬は急性腎不全の新生児では忍容性が良好です。新生児の推奨用量は、初日に 16 mg/kg (負荷用量)、その後 8 mg/kg を 1 日 1 回投与します。
発熱性好中球減少症患者におけるグラム陽性感染症の実証的治療として、セフタジジムにテイコプラニン(活性物質)を追加することは効果的でした。発熱性好中球減少症患者16人がテイコプラニン(活性物質)とセフタジジムで治療された。この非盲検臨床研究では、過去 48 時間または 72 時間以内にセフタジジム療法が失敗した患者が使用されました。テイコプラニン (活性物質) を 400 mg の負荷用量として静脈内投与し、その後 200 mg を 1 日 1 回投与しました。患者は、真菌の定着を防ぐために、セフタジジム 2 g を 8 時間ごとに静注し、ケトコナゾール 200 mg を 1 日 1 回経口投与するか、アムホテリシン 400 mg を 6 時間ごとに投与し続けました。併用療法による臨床治癒は患者の 69% (n = 11) で達成されました。感染症の91%(11人中10人)で細菌学的治癒が確認された。治療に成功した細菌の中には、黄色ブドウ球菌、表皮ブドウ球菌(メチシリン耐性の2株)、および大便連鎖球菌による感染症が含まれていました。 4人の患者は肝臓酵素の上昇を発症した。しかし、テイコプラニン (活性物質) が原因であると考えられたのは 1 件のみでした。
発熱性好中球減少症のがん患者に対する抗生物質レジメンの最初の経験的治療にテイコプラニン(活性物質)を含めることには利点がある可能性があります。テイコプラニン (活性物質) は、血液悪性腫瘍を伴う発熱性好中球減少症患者における経験的治療法として評価されました。アミノグリコシドおよびβ-ラクタム系抗生物質に対して高い耐性を持つ株によって引き起こされるグラム陽性感染症が蔓延している状況下で、88%の奏効率が得られました。
テイコプラニン(活性物質)は、骨髄移植を受ける患者の重篤な敗血症の治療において、アミノグリコシドおよびベータラクタムと組み合わせると効果的であることが示されています。テイコプラニン(活性物質)400mg、1日1回、ネチリマイシン400mg、1日1回、およびセフタジジム2g、1日3回、IVが11人の患者に投与された。 11人の患者全員が反応し、10人は臨床的に治癒した。テイコプラニン (活性物質) は、アミノグリコシドやベータラクタムに反応しない感染症を患う骨髄移植患者において、潜在的に効果的で忍容性の高い薬剤です。
テイコプラニン (活性物質) は、発熱性顆粒球減少症患者を対象とした 3 件の研究で効果があることが示されています。最初の研究では、経験的治療にテイコプラニン(活性物質)を追加した場合、発熱性顆粒球減少症の65エピソードのうち67%が反応を示しました。 120人の患者を対象とした2番目の研究では、63%がセフタジジムとテイコプラニン(活性物質)に反応したのに対し、セフタジジム単独では49%でした。 3番目の研究では、ヒックマンカテーテルを使用したグラム陽性菌血症の125例のうち、微生物に応じて72%から90%が反応した。
テイコプラニン(活性物質)とシプロフロキサシンは、発熱性好中球減少症の患者に有効でした。テイコプラニン (活性物質) とシプロフロキサシンをゲンタマイシンとピペラシリンを加えたものと比較しました。テイコプラニン(活性物質)とシプロフロキサシンを投与された患者のうち、78%が良好な反応を示したのに対し、ゲンタマイシンとピペラシリンを投与された患者では49%でした。シプロフロキサシンとテイコプラニン(活性物質)は、発熱性好中球減少症患者の経験的治療においてゲンタマイシンとピペラシリンの併用と少なくとも同等の効果があり、グラム陽性菌が蔓延している状況ではより効果的である可能性があります。
アミノグリコシドまたはキノロンと併用するテイコプラニン(活性物質)は、好中球減少熱の経験的治療における適切なアプローチであると考えられており、がん患者のカテーテル感染を防ぐことができます。
非対照研究では、テイコプラニン(活性物質)は、皮膚または骨髄炎を伴う MRSA 感染症の治療に有効でした。好中球減少症を患っている患者は除外された。 26人の患者は、200または400mgのテイコプラニン(活性物質)を24時間ごとに筋肉内または静脈内投与された。臨床治癒率は84.6%でした。患者の 73% で細菌学的治癒が達成されました。
公開研究では、テイコプラニン(活性物質)とリファンピンの組み合わせが、黄色ブドウ球菌によって引き起こされる重篤な感染症に対する効果的で忍容性の高い治療法であることが示されました。両方の抗生物質をIV投与し、テイコプラニン(活性物質)は最初の24時間に400 mgを2回ボーラス投与し、その後は1日1回400 mg、リファンピシンは1日1回600 mgを2回、投与期間に応じて投与した。感染症の重症度について。評価可能な患者15人のうち、13人(86.7%)は臨床的に治癒したが、2人(うち1人は治療とは無関係の自然原因で死亡、1人はリファンピシン耐性を発現)は改善しなかった。黄色ブドウ球菌は除去され、臨床的に治癒した患者では再発しませんでした。
ブドウ球菌および他のグラム陽性菌によって引き起こされる感染症をテイコプラニン(活性物質)で治療する研究結果が発表されました。患者の64人中39人(61%)が治癒し、64人中16人(25%)が改善し、64人中9人(14%)が治療に失敗した。テイコプラニン (活性物質) は、グラム陽性菌によって引き起こされる感染症に効果的で忍容性の高い抗生物質であり、メチシリン耐性ブドウ球菌に対して効果的です。
テイコプラニン (活性物質) は、骨および関節の感染症の治療におけるテイコプラニン (活性物質) について議論されている他の治療手段と組み合わせることで、感受性の病原体によって引き起こされる骨および関節の感染症の治療に安全かつ効果的です。全体的な臨床成功率は 60 人の患者で 88% でした。
骨または関節の感染症を患う 35 人の患者に対するテイコプラニン (活性物質) による治療により、患者の 78% が完全に解消されました。テイコプラニン (活性物質) 4 mg/kg/日で反応しなかった患者は、用量を 15 mg/kg/日以上に増量しました。患者は、テイコプラニン(活性物質)の高いトラフおよびピークレベルに耐えました。テイコプラニン (活性物質) 12 mg/kg/日以上を投与された患者 18 人中 5 人で、薬剤関連の発熱と皮膚発疹が発生しました。
テイコプラニン (活性物質) は、骨や関節のグラム陽性菌によって引き起こされる感染症の治療に効果があることがわかっています。テイコプラニン (活性物質) の有効性と安全性が、急性または慢性の骨髄炎および敗血症性関節炎の患者 66 人の治療において評価されました。患者は、12時間ごとに12 mg/kg/日の負荷用量を3回投与され、その後12 mg/kg/日が投与されました。 45 人中 39 人、つまり 87% では良好な臨床反応が得られましたが、45 人中 6 人、つまり 13% では失敗または再発が見られました。
テイコプラニン(活性物質)は、評価可能な皮膚および結合組織感染症患者 62 人の治療に効果がありました。テイコプラニン (活性物質) に使用される通常の初回用量は 400 または 800 mg、その後は毎日 200 ~ 400 mg を IV または IM で投与します。一部の患者は、その他の不特定の用量を受けた。研究前の30日間に、25人の患者が抗生物質、主にペニシリン系またはセファロスポリン系の抗生物質を投与され、続いてキノロン系抗生物質とマクロライド系抗生物質が投与された。治療中止の最も一般的な理由は治療の失敗であり、症例の 3 分の 2 で発生しました。テイコプラニン (活性物質) は、患者 64 人中 54 人から分離された唯一の治療薬でした。 5人の患者にはアミノグリコシドも投与され、3人と2人の患者にはそれぞれペニシリンとセファロスポリンも投与された。細菌感染の除去は、黄色ブドウ球菌感染症の35例中27例(77%)、コアグラーゼ陰性ブドウ球菌の5例中5例(100%)、および連鎖球菌の7例中5例(71%)で発生した(Lang etアル、1991)。
テイコプラニン(活性物質)による治療により、骨または結合組織の感染症患者の 93% が治癒または改善しました。有効性は30人の患者で評価されました。細菌学的治癒は 25 人の患者 (83.3%) で発生しました。
テイコプラニン (活性物質) は 1 日 1 回投与され、皮膚および結合組織の感染症に対して安全かつ便利であると考えられます。特に、テイコプラニン(活性物質)は外来非経口治療に適していると思われる。
テイコプラニン(活性物質)は 1 日 1 回投与され、グラム陽性菌によって引き起こされる皮膚および結合組織の感染症に対する安全かつ効果的な治療法であると考えられています。
予備的な臨床研究では、テイコプラニン(活性物質)を透析液に添加すると、グラム陽性腹膜炎の治療に効果がある可能性があることが示されました(Neville et al、1987)。持続的携帯型腹膜透析(CAPD)を受けた慢性腎不全患者11人がグラム陽性腹膜炎を呈した。
患者には、テイコプラニン (活性物質) 400 mg を非公開で単回投与し、続いて各透析処置中に 20 mg/L の透析液を投与しました。患者のうち 10 人 (91%) が臨床的治癒を達成しました。唯一の失敗は、再発性黄色ブドウ球菌腹膜炎の患者で発生しました。
患者はテイコプラニン療法(活性物質)による2回の治療を受けましたが、その後バンコマイシン療法は失敗しました。テイコプラニン (活性物質) は忍容性が高く、聴器毒性や残存腎機能の低下の証拠はありませんでした。臨床的に治癒を示した10人の患者は4週間から11か月間追跡調査され、良好な状態が続いた。テイコプラニン(活性物質)はグラム陽性菌の根絶に成功しました。
薬理的特性
薬力学的特性と抗菌スペクトル。
テイコプラニン (活性物質) は、好気性および嫌気性グラム陽性菌に対して in vitro で殺菌作用を示す糖ペプチドグループの抗生物質です。テイコプラニン (活性物質) は、ベータラクタムの影響を受ける場所とは異なる場所で細胞壁の生合成に作用し、感受性のある微生物の増殖を阻害します。
テイコプラニン(活性物質)は、ブドウ球菌(メチシリンおよび他のベータラクタム系抗生物質に耐性のあるものを含む)、連鎖球菌、腸球菌、リステリアモノサイトゲネス、小球菌、J/K グループコリネバクテリア、およびクロストリジウム・ディフィシルやペプト球菌を含むグラム陽性嫌気性菌に対して活性があります。
テイコプラニン(活性物質)をアミノグリコシドと組み合わせると、黄色ブドウ球菌に対して in vitro での殺菌相乗効果が実証されています。これらの微生物に対する相乗効果はイミペネムでも実証されています。テイコプラニン (活性物質) とリファンピシンの in vitro 組み合わせは、黄色ブドウ球菌に対する相加効果および相乗効果を実証しました。インビトロでの相乗効果は、表皮ブドウ球菌に対するシプロフロキサシンでも観察されました。
テイコプラニン (活性物質) に対する in vitro 耐性は 1 段階で獲得することはできず、複数継代後にのみ獲得されます。溶血性ブドウ球菌のいくつかの菌株におけるテイコプラニン (活性物質) の MIC (最小発育阻止濃度) が高いという報告があります。
テイコプラニン (活性物質) は、他のクラスの抗生物質と交差耐性を示しません。
腸球菌において、テイコプラニン(活性物質)と糖ペプチドバンコマイシンとの間に交差耐性が観察された。
テイコプラニン(活性物質)は白血球およびマクロファージに取り込まれ、これらの細胞内で抗ブドウ球菌活性を維持します。
薬物動態学的特性
吸収
3 ~ 6 mg/kg の 1 回の筋肉内注射のバイオアベイラビリティは 90% 以上です。テイコプラニン (活性物質) は、経口投与後、正常な胃腸管ではほとんど吸収されません。経口投与量の 40% が活性薬剤として糞便中に検出されます。
分布
テイコプラニン (活性物質) は皮膚、皮下組織、心筋、肺、胸水、骨、滑液、皮膚小胞液に急速に拡散し、脳脊髄液にはゆっくりと拡散します。テイコプラニン (活性物質) は 90 ~ 95% 血漿タンパク質に結合しています。 、弱い親和性結合を持ちます。
代謝
生体内変換は小さく (約 3%)、非経口投与した場合、投与された薬物の約 80% が尿中に除去されます。 3~6 mg/kg の IV 投与後の腎クリアランスは 10.4~12.1 mL/h/kg です。
排除
3 ~ 6 mg/kg の静脈内投与後、血漿中濃度は 150 時間の最終排泄半減期で低下し、血漿クリアランスは 11.9 ~ 14.7 mL/h/kg となり、1 日 1 回の投与が可能になります。
0、12、24時間目および24時間ごとに30分間の点滴として6mg/kgをIV投与した後、4日目までに最小血清濃度10mg/Lに達するであろう。定常状態における最大血清濃度は約 64mg/L、最小血清濃度は 28 日目までに約 19mg/L に達します。








-1024x576.jpg?resize=1024,576&ssl=1)


