デスロラタジン + 硫酸プソイドエフェドリンの禁忌 – Biosintética
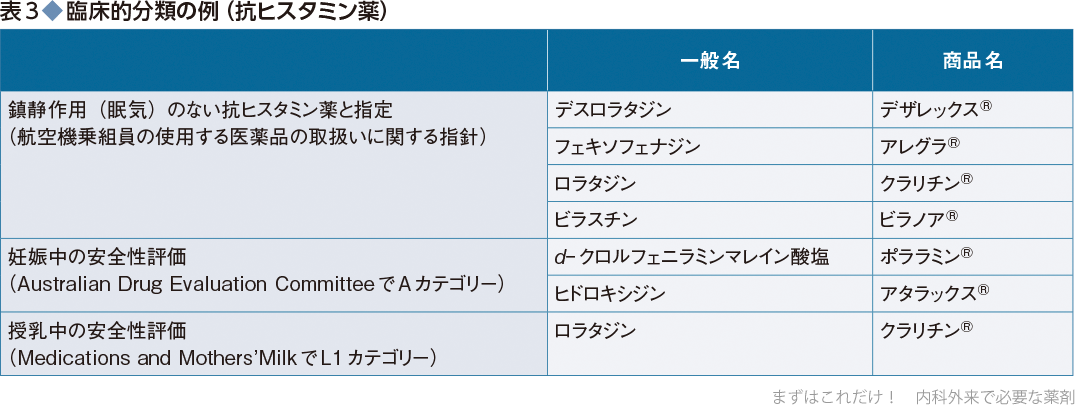
この薬は、その成分またはロラタジンに対して過敏症のある患者による使用は禁忌です。
プソイドエフェドリン成分のため、この薬剤は狭隅角緑内障または尿閉の患者、モノアミンオキシダーゼ (MAO) 阻害剤治療を受けている患者、またはそのような治療の中断から 14 日間の患者の使用は禁忌です。 。
この薬は、重度の高血圧症、重度の冠動脈疾患のある患者、およびアドレナリン作動薬または同様の化学構造を持つ他の薬剤に対して過敏症の患者の使用は禁忌です。
デスロラタジン + 硫酸プソイドエフェドリンの使用方法 – Biosintética
大人と12歳以上の子供:デスロラタジン+硫酸プソイドエフェドリン(活性物質)の推奨用量は1錠、1日2回です。
デスロラタジン + 硫酸プソイドエフェドリン (活性物質) は、食物の存在下または非存在下で投与できます。
デスロラタジン + 硫酸プソイドエフェドリン (活性物質) は、液体を使用して経口投与する必要があります。
この薬は割ったり、開けたり、噛んだりしないでください。
デスロラタジン + 硫酸プソイドエフェドリンの注意事項 – Biosintética
高齢者への使用
高齢の患者は、交感神経興奮性アミンに対して副作用を経験する可能性が高くなります。高齢者に対する用量は慎重に定義する必要があり、選択される用量は、この集団における肝臓、腎臓、または心臓の機能低下、および付随する疾患や他の薬物療法の頻度がより高いことを反映する必要があります。
小児患者への使用
デスロラタジン + 硫酸プソイドエフェドリン (活性物質) は小児患者には適しておらず、12 歳未満の患者には推奨されません。これは、この年齢層における安全性と有効性に関する利用可能なデータがないためです。
妊娠中の使用
カテゴリーC。
この薬は、医師または歯科外科医のアドバイスなしに妊婦が使用しないでください。デスロラタジンとプソイドエフェドリンの併用による生殖研究は行われていません。妊婦を対象とした適切な、または十分に管理された研究はありません。デスロラタジンは動物実験では催奇形性があることは示されていません。ただし、動物で行われた生殖研究は必ずしも人間の反応を示すとは限らないため、デスロラタジンは明らかに必要な場合にのみ妊娠中に使用する必要があります。
授乳中
デスロラタジンとプソイドエフェドリンは両方とも母乳中に排泄されます。したがって、母親にとっての薬物療法の重要性を考慮して、母乳育児を継続するか、デスロラタジン + 硫酸プソイドエフェドリン (有効成分) の使用を中止するかを選択する必要があります。授乳中の女性にデスロラタジン + 硫酸プソイドエフェドリン (有効成分) を投与する場合は注意が必要です。
肝不全での使用
デスロラタジン + 硫酸プソイドエフェドリン (有効成分) は、肝障害のある患者には注意して使用する必要があります。
腎不全での使用
デスロラタジン + 硫酸プソイドエフェドリン (有効成分) は、腎障害のある患者には注意して使用する必要があります。
その他
デスロラタジン + 硫酸プソイドエフェドリン (活性物質) は、高血圧、糖尿病、虚血性心疾患、眼圧上昇、甲状腺機能亢進症、腎障害、前立腺肥大、狭窄性消化性潰瘍、幽門ブロックまたは十二指腸ブロック、膀胱頸部および既往歴のある患者には注意して使用する必要があります。気管支けいれんの。交感神経興奮性アミンによって、けいれんや心血管虚脱を伴う中枢神経系の刺激とそれに伴う低血圧が引き起こされる可能性があります。
プソイドエフェドリンを含む製品では、急性汎発性発疹性膿疱症 (AGEP) などの重篤な皮膚反応が発生する可能性があります。患者は注意深く監視する必要があります。発熱、紅斑、小さな膿疱などの症状が現れた場合には、投与を中止し、必要に応じて適切な処置を行ってください。
高血圧、頻脈、動悸または不整脈、吐き気、またはその他の神経学的兆候(頭痛または頭痛の増加など)が発生した場合には、治療を中止する必要があることを患者に通知する必要があります。
手術の場合、患者は治療を中止しなければなりません(揮発性ハロゲン化麻酔薬を使用すると、急性高血圧発症のリスクがあります)。
デスロラタジンは、発作の病歴または家族歴のある患者には注意して投与する必要があります。特に、幼い子供は、デスロラタジンによる治療下で新たな発作を起こしやすい可能性があります。医療専門家は、治療中に発作を起こした患者に対してデスロラタジンの中止を検討する場合があります。
この薬はドーピングを引き起こす可能性があります。
デスロラタジン + 硫酸プソイドエフェドリンの副作用 – Biosintética
デスロラタジン + 硫酸プソイドエフェドリン (活性物質) の安全性は、デスロラタジン + 硫酸プソイドエフェドリン (活性物質) を 1 日 2 回、最長 2 週間投与された 414 人の患者を対象に研究されました。デスロラタジン + 硫酸プソイドエフェドリン (活性物質) による治療後に発生した有害事象の大部分は、プソイドエフェドリン単独で治療した患者で観察された有害事象と種類および頻度が同様でした。治療に関連した有害事象は?によって報告されました。患者の 2% が表 3 に記載されています。
表 3: によって報告された、治療に関連する有害事象の発生率。身体系/器官クラス別、任意の治療グループの患者の 2%: 研究 P00355/362 からの統合データ (全患者をランダム化)
デスロラタジン + 硫酸プソイドエフェドリン (活性物質) に関連する一般的な副作用 (患者 100 人に少なくとも 1 人に発生) には、頻脈、体の動きの増加に伴う落ち着きのなさ、口渇、めまい、喉の痛み、食欲不振、便秘、血糖、高血糖が含まれます。 、喉の渇き、疲労感、頭痛、睡眠障害、神経過敏、眠気。
珍しい:
腹痛、吐き気、消化不良
非常にまれです:

幻覚、筋肉痛、嘔吐。
不明な周波数:
行動、攻撃性、QT 延長の変化 有効成分としてデスロラタジンのみを含む製品の販売中に、非常にまれに次のような自発的有害事象が報告されています: 過敏反応 (アナフィラキシーや皮膚発疹を含む)、頻脈、動悸、精神運動亢進、けいれん、および肝臓酵素の上昇(ビリルビンおよび肝炎を含む)。
プソイドエフェドリンを含む製品により、急性汎発性発疹性膿疱症(AGEP)などの重篤な皮膚反応が発生した例が報告されています。
注意: この製品は新薬であり、研究により許容できる有効性と安全性が示されていますが、たとえ正しく指示され使用されたとしても、予測できないまたは未知の有害事象が発生する可能性があります。この場合、健康監視通知システム – NOTIVISA (www.anvisa.gov.br/hotsite/notivisa/index.htm) を通じて有害事象を報告するか、州または地方自治体の健康監視局に報告してください。
デスロラタジン + 硫酸プソイドエフェドリンの薬物相互作用 – Biosintética
デスロラタジン + 硫酸プソイドエフェドリン (活性物質) との特異的な相互作用研究は行われませんでした。しかし、健康なボランティアを対象とした薬理学的研究では、心電図パラメータ(補正されたQT間隔を含む)の評価によると、エリスロマイシン、ケトコナゾール、アジスロマイシン、フルオキセチンおよびシメチジンと同時投与した場合、デスロラタジンの安全性プロファイルに臨床的に関連する変化は見られませんでした。 、臨床検査、バイタルサインおよび有害事象(表 2 を参照)。
表 2: 健康な男性および女性ボランティアにおけるデスロラタジンおよび 3-ヒドロキシデスロラタジンの薬物動態の変化
β-アドレナリン遮断薬であるメチルドーパ、メカミルアミン、レセルピン、ベラトラムアルカロイド、およびグアネチジンの降圧効果は、交感神経興奮薬によって低下する可能性があります。
片頭痛に対するデスロラタジン + 硫酸プソイドエフェドリン(活性物質)と麦角アルカロイド(ジヒドロエルゴタミン、エルゴタミン、メチルエルゴメトリンなど)の併用、うっ血除去薬(経口または鼻)、食欲抑制薬またはアンフェタミン、ブロモクリプチン、カベルゴリン、リネゾリド、リスリドおよびペルゴリド。デスロラタジン + 硫酸プソイドエフェドリン (活性物質) をこれらの薬剤と併用すると、血圧が上昇する可能性があります。
プソイドエフェドリンをジギタリスと併用すると、異所性ペースメーカー活動が発生する可能性があります。制酸薬と併用すると、硫酸プソイドエフェドリンの吸収速度が増加する可能性があります。また、カオリンを使用すると、硫酸プソイドエフェドリンの吸収を低下させることができます。
臨床検査への干渉
皮膚テストを行う前に、少なくとも 48 時間はデスロラタジン + 硫酸プソイドエフェドリン (有効成分) を服用しないでください。プソイドエフェドリンを使用すると、メタンフェタミンの検査結果が偽陽性となる可能性があります。
物質デスロラタジン + 硫酸プソイドエフェドリンの作用 – Biosintética
有効性の結果
デスロラタジン + 硫酸プソイドエフェドリン (活性物質) の臨床有効性と安全性は、12 歳から 78 歳の季節性アレルギー性鼻炎患者 1,248 名を対象とした 2 つの 2 週間の多施設共同無作為化並行群間臨床研究で評価され、そのうち 414 名がデスロラタジンの投与を受けました。 + 硫酸プソイドエフェドリン (活性物質)。どちらの研究でも、対象者は、デスロラタジン + 硫酸プソイドエフェドリン (活性物質) (デスロラタジン + 硫酸プソイドエフェドリン) を 1 日 2 回、またはデスロラタジン + 硫酸プソイドエフェドリン (活性物質) を 5 mg の錠剤で 1 日 1 回、2 週間投与する群に無作為に割り付けられました。 120 mg の徐放性プソイドエフェドリン錠剤を 1 日 2 回投与します。患者の大多数は 18 歳から 18 歳まででした。年齢は65歳(平均35.8歳)、大部分が女性(64%)でした。民族に関しては、82%が白人、9%が黒人、6%がヒスパニック、3%がアジア人またはその他の民族でした。主な有効性変数は、4 つの鼻症状 (鼻漏、鼻閉塞/鼻詰まり、鼻のかゆみおよびくしゃみ)、および 4 つの非鼻症状 (目のかゆみ/灼熱感、目の充血、涙と鼻のかゆみ) の反射スコア (1 日 2 回) でした。口蓋と耳)を 4 段階スケール(0 = 症状なし、1 = 軽度、2 = 中等度、3 = 重度)で表します。両方の研究において、デスロラタジン + 硫酸プソイドエフェドリン (活性物質) の抗ヒスタミン作用は、2 週間の治療期間中、鼻づまりを除く総症状スコアで測定した場合、プソイドエフェドリン単独の場合よりも有意に高かった。デスロラタジン + 硫酸プソイドエフェドリン (活性物質) の鼻詰まり除去効果は、2 週間の治療期間中、鼻閉塞/鼻詰まりによって測定され、デスロラタジンの効果よりも有意に高かった。
2 つの研究のうち 1 つからの主要な有効性変数の結果を表 1 に示します。
表1:季節性アレルギー性鼻炎患者を対象とした2週間の臨床研究における症状の変化
デスロラタジン + 硫酸プソイドエフェドリン (活性物質) の有効性には、性別、年齢、人種によるサブグループ間に有意差はありませんでした。
薬理学的特徴
薬物療法グループ:
デスロラタジン + 硫酸プソイドエフェドリン (有効成分) には、抗ヒスタミン薬 (H1 アンタゴニスト) と交感神経興奮薬が含まれています。
作用機序
デスロラタジンは、ヒスタミン H1 受容体拮抗薬としての選択的活性を持つ、長時間作用型の三環系ヒスタミン拮抗薬です。受容体結合データは、2~3 ng/mL (7 nM) の濃度で、デスロラタジンがヒト ヒスタミン H1 受容体と顕著な相互作用を示すことを示しています。デスロラタジンの抗ヒスタミン作用は、in vitro ではロラタジンの約 3.5 ~ 20 倍、動物ではロラタジンの 2.5 ~ 4 倍です。デスロラタジンは、インビトロでヒト肥満細胞からのヒスタミン放出を阻害しました。ラットで行われた放射性標識された組織分布の研究、およびモルモットで行われた放射性リガンドへのH1受容体の結合の研究の結果は、デスロラタジンが血液脳関門を直ちに通過しないことを示した。丘疹と紅斑:ヒスタミン誘発性丘疹に関する研究では、デスロラタジン 5 mg を単回または反復投与した後、その薬剤が 1 時間以内に抗ヒスタミン効果を生み出すことが実証されました。このアクティビティは最大 24 時間持続することがあります。デスロラタジン 5 mg 群では、28 日間の治療を通じてヒスタミン誘発性膨疹タキフィラキシーの証拠はありませんでした。硫酸プソイドエフェドリンは、鼻粘膜の充血除去作用を発揮する経口活性交感神経刺激アミンです。硫酸プソイドエフェドリンは、アレルギー性鼻炎によって引き起こされる鼻づまりを軽減するのに有効な薬剤であると認識されています。プソイドエフェドリンは、エフェドリンで観察されるものと同様の末梢効果、およびアンフェタミンよりも弱いが同様の中枢効果をもたらします。プソイドエフェドリンには興奮性副作用の可能性がある
薬物動態
吸収とバイオアベイラビリティ
単回投与の薬物動態研究では、デスロラタジンがピーク血漿濃度 (Tmax) に達するまでの平均時間は投与後約 4 ~ 5 時間で発生し、平均ピーク血漿濃度 (Cmax) と投与量下の面積が観察されました。曲線(AUC)はそれぞれ約 1.09 ng/mL および 31.6 ng?h/mL でした。別の薬物動態研究では、食品とグレープフルーツ ジュースはデスロラタジンの生物学的利用能 (Cmax と AUC) に影響を与えませんでした。プソイドエフェドリンの場合、平均 Tmax は投与後 6 ~ 7 時間で発生し、平均ピーク血漿濃度 (Cmax) および濃度時間曲線下面積 (AUC) は約 263 ng/mL および 4588 ng?h/mL でした。それぞれ。食物は、デスロラタジンまたはプソイドエフェドリンの生物学的利用能 (Cmax および AUC) に影響を与えませんでした。
正常な健康なボランティアに、デスロラタジン + 硫酸プソイドエフェドリン (活性物質) を 1 日 2 回、14 日間経口投与した後、デスロラタジン、3-ヒドロキシデスロラタジンおよびプソイドエフェドリンは 10 日目に定常状態に達しました。デスロラタジンでは、定常状態での平均ピーク血漿濃度 (Cmax) と濃度時間曲線下面積 (AUC、0 ~ 12 時間) がそれぞれ約 1.7 ng/mL と 16 ng?h/mL でした。プソイドエフェドリンでは、定常状態における平均ピーク血漿濃度 (Cmax) および濃度時間曲線下面積 (AUC、0 ~ 12 時間) がそれぞれ 459 ng/mL および 4658 ng?h/mL であったことが観察されました。
分布
デスロラタジンおよび 3-ヒドロキシデスロラタジンは、それぞれ約 82% ~ 87% および 85% ~ 89% が血漿タンパク質に結合しています。デスロラタジンと 3-ヒドロキシデスロラタジンのタンパク質への結合は、腎機能障害のある患者では変化しませんでした。
生体内変換
すべての前臨床種において、デスロラタジンの主な代謝経路には 5 位と 6 位の水酸化 (37 ~ 57%) が含まれていましたが、ヒトでは gt;投与されたデスロラタジンの 50% は、3-ヒドロキシデスロラタジン (抱合グルクロニドとともに抱合されていない) として排泄されました。デスロラタジンから 3-ヒドロキシデスロラタジンへの代謝は、単一の肝細胞調製物でのみ観察されました。デスロラタジン代謝は、CYP2D6 阻害剤である 50 μM キニジンによって完全に阻害されました。
CYP2D6スーパーソームは、微量の 3-ヒドロキシデスロラタジン (全生成物の 1% 未満) およびデスロラタジンの他のヒドロキシル化生成物を生成しました。 CYP1A1 および CYP2D6 スーパーソームは、デスロラタジンから 5-ヒドロキシデスロラタジンおよび 6-ヒドロキシデスロラタジンを生成しました。インビトロ研究では、デスロラタジンから 3-ヒドロキシデスロラタジンへの代謝に関与するヒト酵素を決定的に特定することはできませんでした。
濃度 16.1 μM (試験最大値) のデスロラタジンは、CYP2C19 および CYP2D6 を阻害しました (gt; 25%)。デスロラタジンは、試験した濃度では CYP1A2、CYP2C9、または CYP3A4 を有意に阻害しませんでした。したがって、CYPを有意に阻害するために必要なデスロラタジンの濃度は、ヒトにおいて臨床用量の5 mgのデスロラタジンを投与した後に測定される血漿Cmax(3.98~4.98 ng/mL)よりも400倍以上高い。デスロラタジンは、Pgp 媒介輸送の既知の基質の流出を阻害する能力について試験されました。
デスロラタジンは、既知の Pgp 阻害剤で観察された最大阻害の約 17% という、試験した基質の流出をわずかに阻害しました。推定された IC50 は 111 μM で、これはヒトに 5 mg 用量のデスロラタジンを投与した後に観察されたデスロラタジンの血漿 Cmax よりも 9,000 倍以上大きくなっています。これらの研究の結果は、提案されているデスロラタジンの臨床用量が、Pgp を介した他の薬剤や生体異物の排出に影響を及ぼさないことを示唆しています。
代謝
デスロラタジン (ロラタジンの主な代謝産物) は広範囲に代謝されて、その後グルクロン酸抱合される活性代謝産物である 3-ヒドロキシデスロラタジンになります。デスロラタジンと 3-ヒドロキシデスロラタジンの血漿濃度の分析では、両方の化合物の Tmax と半減期の値が同様であることが示されました。
3-ヒドロキシデスロラタジンの生成に関与する酵素は特定されていません。デスロラタジンを用いて実施された臨床研究のデータは、一般集団の一部が 3-ヒドロキシデスロラタジンを形成する能力が低下しており、デスロラタジンの代謝が不十分であることを示しています。薬物動態研究 (n = 3,748) では、患者の約 6% がデスロラタジンの代謝不良者でした (3-ヒドロキシデスロラタジンとデスロラタジンの AUC 比が 0.1 未満の患者、またはデスロラタジンの半減期が 50 時間を超える患者として定義) )。これらの薬物動態研究には、2~5歳の患者977人、6~11歳の患者1,575人、12~70歳の患者1,196人を含む、2~70歳の患者が含まれていました。年齢グループ間で代謝不良者の優勢さに差はなかった。代謝不良の頻度は、白人 (2%、n = 1,462) やヒスパニック系 (2%、n = 1,063) と比較して、黒人 (17%、n = 988) で高かった。代謝不良患者のデスロラタジンへの曝露中央値(AUC)は、代謝不良でない患者の曝露中央値(AUC)より約6倍高かった。デスロラタジンの代謝が低い患者を前向きに特定することはできず、推奨用量のデスロラタジンよりも高用量のデスロラタジンに曝露されることになります。これらの研究では、代謝の悪い人と正常な代謝者の間で全体的な安全性の違いは観察されませんでした。
単独療法としてのプソイドエフェドリンは、N-脱メチル化により肝臓で不完全に代謝されて不活性代謝物になります。薬剤とその代謝物は尿中に排泄されます。塩酸プソイドエフェドリンの投与量の約 55 ~ 96% が変化せずに尿中に排泄されます。
排除
デスロラタジン + 硫酸プソイドエフェドリン (活性物質) を単回投与した後、デスロラタジンの平均血漿排出半減期は約 24 時間でした。単剤療法として投与した場合、プソイドエフェドリンの平均排出半減期は、尿の pH に応じて約 4 ~ 6 時間です。排泄半減期は、尿の pH が 6 未満の場合には減少し、尿の pH が 8 を超える場合には増加する可能性があります。
高齢者の患者
限られた患者数で?デスロラタジン + 硫酸プソイドエフェドリン (活性物質) で治療を受けた 65 歳のグループでは、若いグループと比較して有効性または安全性に関連する差異は観察されませんでした。
セックス
デスロラタジン + 硫酸プソイドエフェドリン (活性物質) の投与後、デスロラタジン、3-ヒドロキシデスロラタジン、またはプソイドエフェドリンの薬物動態パラメーターに臨床的に有意な性関連の差は観察されませんでした。
前臨床毒性学
デスロラタジンと硫酸プソイドエフェドリンを組み合わせた製品について、発がん性、突然変異誘発、生殖能力の障害を評価するための動物実験や実験室研究は行われていません。
発がん性と突然変異誘発

デスロラタジンの発がん性の可能性は、ラットにおけるロラタジンの研究とマウスにおけるデスロラタジンの研究を使用して評価されました。 2年間のラット研究では、ロラタジンが最大25 mg/kg/日の用量で食餌中に投与されました(デスロラタジンおよびデスロラタジン代謝物への推定曝露量は、推奨される1日の経口用量でヒトAUCの約30倍でした)。 10 mg/kg/日のロラタジンで治療した男性、および25 mg/kg/日のロラタジンで治療した男性と女性では、肝細胞腫瘍(腺腫と癌腫を合わせたもの)の有意に高い発生率が観察されました。 10 mg/kg ロラタジンで治療されたラットにおけるデスロラタジンおよびデスロラタジン代謝物の推定暴露量は、推奨される 1 日経口用量におけるヒトの AUC の約 7 倍でした。デスロラタジンの長期使用におけるこれらの所見の臨床的重要性は不明です。それぞれ最大 16 mg/kg/日および 32 mg/kg/日のデスロラタジンで治療された雄と雌のマウスの 2 年間の食餌研究では、腫瘍の発生率に有意な増加はありませんでした。これらの用量でのマウスにおけるデスロラタジンと代謝物の推定曝露量は、推奨される 1 日の経口用量におけるヒトの AUC のそれぞれ 12 倍と 27 倍でした。
デスロラタジンを用いて行われた遺伝毒性研究では、復帰突然変異アッセイ (サルモネラ菌/大腸菌による哺乳類ミクロソームにおける細菌変異原性アッセイ)または 2 つの染色体異常アッセイ (ヒト末梢血リンパ球の染色体異常誘発性) では遺伝毒性の可能性の証拠はありませんでした。およびマウス骨髄小核アッセイ)。プソイドエフェドリンには変異原性があるとは報告されていません。
生殖能力
最大 24 mg/kg/日の用量で治療した雌ラットの生殖能力には影響はありませんでした(デスロラタジンおよびデスロラタジン代謝物への推定曝露量は、推奨される 1 日経口用量におけるヒト AUC の約 130 倍でした)。男性の生殖能力の具体的な低下は、女性の受胎率の低下、精子の数と運動性の低下、および12 mg/kgの経口用量で発生した精巣の組織病理学的変化によって実証されました(推定デスロラタジン曝露量とデスロラタジン代謝物は約45でした)。推奨される1日の経口用量におけるヒトAUCの倍)。デスロラタジンは、3 mg/kg/日の経口用量ではラットの生殖能力に影響を与えませんでした(デスロラタジンおよびデスロラタジン代謝物の推定曝露量は、推奨される 1 日の経口用量におけるヒト AUC の約 8 倍でした)。








-1024x576.jpg?resize=1024,576&ssl=1)


