- 下気道感染症;
- 複雑な感染症を含む尿路感染症。
- 腹腔内感染症;
- 婦人科感染症(産後感染症を含む)
- 皮膚および付属器の感染症。
- 髄膜炎;
- 敗血症;
- 好中球減少症患者における推定細菌感染症に対する初期単独療法を含む経験的治療。
- メロペネムは、グラム陽性菌とグラム陰性菌、好気性細菌と嫌気性細菌に対する広範囲の殺菌活性により、多重微生物感染症の治療に効果的です。
- 嚢胞性線維症、メロペネムの静脈内投与は、単独療法としても他の抗菌薬と併用しても、嚢胞性線維症および慢性下気道感染症の患者に効果的に使用されています。これらの治療法では病原体が常に根絶されたわけではありません。
メロペネムの禁忌 – サンド
メロペネム(活性物質)または無水炭酸ナトリウムに対する過敏症。
カルバペネム系抗生物質、ペニシリン、またはその他のベータラクタム系抗生物質に対する過敏症の病歴のある患者は、メロペネム(活性物質)に対しても過敏症である可能性があります。
すべてのβ-ラクタム系抗生物質と同様に、まれに過敏反応(重度の、場合によっては致死的な反応)が報告されています。
メロペネムの使い方 – Sandoz
成人の投与量:
投与量の範囲は1日1.5g〜6.0gで、3回に分けて投与します。
通常の投与量:
感染症の種類と重症度、病原体の既知または予想される感受性、および患者の状態に応じて、500mg~1gを8時間ごとに静脈内投与します。
例外:
好中球減少症患者における発熱エピソード:
投与量は8時間ごとに1gです。
髄膜炎/嚢胞性線維症:
投与量は8時間ごとに2gです。
緑膿菌によって引き起こされることがわかっている、または疑われる感染症に対処する場合、成人には8時間ごとに少なくとも1gの用量(最大用量は1日あたり6gを超えてはならず、3回に分けて)、毛髪には少なくとも20mg/kgの用量が推奨されます。小児の場合は8時間ごと(最大用量は1日当たり120mg/kgを3回に分けて超えてはなりません)。
緑膿菌感染症の治療では、定期的な感受性検査が推奨されます。
メロペネム(活性物質)は、約 5 分間かけて静脈内ボーラス注射として、または約 15 ~ 30 分間かけて静脈内注入として投与する必要があります。
2g ボーラス投与を裏付けるために利用できる安全性データは限られています。
腎機能が変化した成人の場合の投与量:
以下に概説するように、クレアチニンクリアランスが51mL/min 未満の患者では用量を減らす必要があります。
|
クレアチニンクリアランス(mL/分) |
用量(8時間ごとの500mg~2.0gの用量単位範囲に基づく) |
頻度 |
| 26~50 | 1用量単位 |
12時間ごと |
| 10~25日 | 1/2 用量単位 | 12時間ごと |
| lt; 10 | 1/2 用量単位 | 24時間ごと |
メロペネム (活性物質) は血液透析および血液濾過によって除去されます。メロペネム (活性物質) による治療を継続する必要がある場合は、血液透析手順の終了時に、タイプに応じた適切な用量で効果的な治療を再開することが推奨されます。そして感染の重症度。
腹膜透析の経験はありません。
肝疾患のある成人の場合の投与量:
肝代謝機能障害のある患者には用量調整は必要ありません。

高齢者向けの投与量:
正常な腎機能またはクレアチニンクリアランス値が 50mL/分を超える高齢者には、用量調整は必要ありません。
小児の投与量:
生後3か月を超え、12歳までの小児の場合、静脈内投与量は、感染症の種類と重症度、病原体の既知または予想される感受性、および患者の症状に応じて、8時間ごとに10~40mg/kgです。状態。
体重が50kgを超える子供の場合は、成人用量を使用する必要があります。
例外:
好中球減少症患者における発熱エピソード:
用量は 8 時間ごとに 20mg/kg とする必要があります。
髄膜炎/嚢胞性線維症:
用量は 8 時間ごとに 40mg/kg とする必要があります。
メロペネム(活性物質)は、約 5 分間かけて静脈内ボーラス注射として、または約 15 ~ 30 分間かけて静脈内注入として投与する必要があります。
小児への 40 mg/kg のボーラス投与を裏付けるために利用できる安全性データは限られています。
腎機能が変化した小児の経験はありません。
メロペネム(有効成分)の注射を忘れた場合は、できるだけ早く注射する必要があります。通常、2 つの注射を同時に行うべきではありません。
再構成と互換性
メロペネム製剤(有効成分):
静脈内ボーラス注射の場合、メロペネム (活性物質) は、以下の表に従って注射用水 (500 mg あたり 10 mL) で戻さなければなりません。
この再構成により、最終濃度が約 50 mg/mL の溶液が得られます。
再構成された溶液は透明または淡黄色です。
|
ボトル |
添加する希釈剤の含有量 |
| 500mg | 10mL |
| 1g | 20mL |
静脈内注入の場合、メロペネム(活性物質)のバイアルを適合する輸液で直接再構成し、この溶液を必要に応じて同様に適合する別の輸液用溶液で希釈することができます。
できれば新しく調製したメロペネム溶液(活性物質)を使用してください。ただし、メロペネム(活性物質)の再構成溶液は、15 °C ~ 25 °C の温度または冷蔵下 (4 ° C) で十分な効力を維持します。
再構成した溶液は使用前に振盪する必要があります。
メロペネム (有効成分) は、他の薬物を含む溶液に混合したり添加したりしないでください。

メロペネム溶液(活性物質)は凍結させないでください。
医師の知識なしに治療を中止しないでください。
メロペネムの予防措置 – サンド
他の抗生物質と同様に、感受性のない微生物が異常増殖する可能性があるため、各患者に対して繰り返しの評価が必要になります。
ほとんどすべての抗生物質で発生するように、まれに偽膜性大腸炎 (腸の炎症) が報告されています。したがって、メロペネム(活性物質)の使用に関連して下痢を呈する患者では、偽膜性大腸炎の診断を考慮することが重要です。他の抗生物質の服用により重度の下痢を起こしたことがある場合は、医師に伝えてください。
したがって、メロペネム(活性物質)の使用に関連して下痢を呈する患者では、偽膜性大腸炎の診断を考慮することが重要です。
メロペネム (有効成分) とバルプロ酸/バルプロ酸ナトリウムの併用は推奨されません。
メロペネム(活性物質)は、血清バルプロ酸レベルを低下させることができます。一部の患者は治療量以下のレベルを示す可能性があります
小児への使用:
生後 3 か月未満の新生児に対する有効性と忍容性は確立されていません。したがって、メロペネム(有効成分)は、この年齢層未満での使用は推奨されません。
肝疾患患者への使用:
既存の肝障害のある患者は、メロペネム(活性物質)による治療中に肝機能を監視する必要があります。
直接的または間接的なクームズテストが陽性となる場合があります。
車両の運転や機械の操作能力への影響:
機械を運転および操作する能力に関する研究は行われていません。ただし、車を運転したり機械を操作したりする場合は、メロペネム(有効成分)の使用中に頭痛、知覚異常、けいれんの症例が報告されていることに留意する必要があります。
妊娠中および授乳中の使用:
人間の妊娠におけるメロペネム(活性物質)の安全性は確立されていませんが、動物実験では発育中の胎児に対する悪影響は実証されていません。
メロペネム(有効成分)は、医学的裁量により、母親への潜在的な利益が胎児への潜在的なリスクを正当化しない限り、妊娠中に使用すべきではありません。
妊娠中のリスクカテゴリー B。
この薬は、医師または歯科外科医のアドバイスなしに妊婦が使用しないでください。
母乳中にメロペネム (有効成分) が排泄された例が報告されています。メロペネム(有効成分)は、潜在的な利点が赤ちゃんへの潜在的なリスクを正当化しない限り、授乳中の女性に使用すべきではありません。
メロペネムの副作用 – サンド

メロペネム (有効成分) は一般に忍容性が良好です。重篤な有害事象はまれであり、治療の中断が必要になることはほとんどありません。
副作用は頻度に従って分類されます。
- 非常に一般的 (? 10%)。
- 一般的 (? 1% ~ 10%)。
- 珍しい (?0.1% および <1%)。
- まれ (?0.01% かつ <0.1%);
- 非常にまれです (lt; 0.01%)。
- 頻度は不明です (入手可能なデータから推定できません)。
メロペネム (活性物質) の臨床研究中に以下の副作用が確認されました。
|
頻度 |
システム、オルガン、クラス |
副作用 |
|
一般的 (?1% および lt; 10%) |
血液およびリンパ系の障害 | 血小板血症 |
| 神経系障害 | 頭痛 | |
| 胃腸障害 | 吐き気、嘔吐、下痢 | |
| 肝胆道疾患 | アラニンアミノトランスアミナーゼの増加、アスパラギン酸アミノトランスフェラーゼの増加、血中アルカリホスファターゼの増加、血中乳酸デヒドロゲナーゼの増加、およびガンマグルタミルトランスフェラーゼの増加 | |
| 皮膚および皮下組織の疾患 | 発疹やかゆみ | |
| 一般的および適用部位の障害 | 炎症と痛み | |
|
珍しい (?0.1% および <1%) |
感染症と蔓延 | 口腔および膣カンジダ症 |
| 血液およびリンパ系の障害 | 好酸球増加症、血小板減少症、白血球減少症、好中球減少症 | |
| 神経系障害 | 感覚異常 | |
| 肝胆道疾患 | 血中ビリルビンの増加 | |
| 皮膚および皮下組織の疾患 | 蕁麻疹 | |
| 一般的および適用部位の障害 | 血栓静脈炎 | |
|
まれ (?0.01% および <0.1%) |
神経系障害 | 発作 |
以下の副作用が市販後の臨床研究および自発的報告中に確認されています。
|
頻度 |
システム、オルガン、クラス |
副作用 |
|
まれ (?0.01% および <0.1%) |
血液およびリンパ系の障害 | 無顆粒球症 |
|
非常に珍しい (lt; 0.01%) |
血液およびリンパ系の障害 | 溶血性貧血 |
| 免疫系の障害 | 血管浮腫、アナフィラキシーの症状 | |
| 胃腸障害 | 偽膜性大腸炎 | |
| 皮膚および皮下組織の疾患 | 多形紅斑、スティーブンス・ジョンソン症候群、中毒性表皮壊死融解症 | |
|
未知 |
皮膚および皮下組織の疾患 | 好酸球増加症および全身症状(DRESS症候群)を伴う薬物反応 |
有害事象が発生した場合は、健康監視通知システム – NOTIVISA (www.anvisa.gov.br/hotsite/notivisa/index.htm)、または州または地方自治体の健康監視機関に通知してください。
メロペネムとサンドの薬物相互作用
プロベネシドは、活性尿細管分泌に関してメロペネム (活性物質) と競合し、メロペネム (活性物質) の腎排泄を阻害し、排泄半減期とその血漿濃度の増加を引き起こします。
プロベネシドなしで投与したメロペネム(活性物質)の効力と作用持続時間は十分であるため、メロペネム(活性物質)とプロベネシドの同時投与は推奨されません。
他の薬剤の血漿タンパク質への結合や代謝に対するメロペネム(活性物質)の潜在的な影響は研究されていません。ただし、タンパク質の結合は非常に低いため、このメカニズムを考慮すると、他の薬物との相互作用は期待できません。
カルバペネム剤と併用投与すると、バルプロ酸の血漿濃度が低下し、約 2 日でバルプロ酸レベルが 60 ~ 100% 減少することが報告されています。
濃度低下は急速に始まり、長引くため、バルプロ酸で安定化されている患者へのメロペネム(活性物質)の併用は管理可能とは考えられず、避けるべきです。
メロペネム(活性物質)は、他の多くの薬剤と同時に投与されていますが、明らかな有害相互作用はありません。しかし、プロベネシドを用いた研究以外に、特定の薬物との相互作用研究は行われていません。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
物質メロペネムの作用 – サンド
効果の結果
メロペネム(有効成分)は、通常のルーチンシステムを使用して実施できる感受性試験において安定しています。インビトロ試験では、メロペネム(活性物質)がいくつかの抗生物質と相乗的に作用することが示されています。
メロペネム(活性物質)は、インビトロおよびインビボの両方で、グラム陽性微生物およびグラム陰性微生物に対して抗生物質後の効果があることが示されています。
メロペネム (活性物質) は、他のβ-ラクタム系抗生物質に耐性のある多くの菌株に対してin vitro で活性を示します。これは、β-ラクタマーゼに対する安定性が高いことによって部分的に説明されます。
アミノグリコシドやキノロンなど、無関係なクラスの抗生物質に耐性のある株に対するin vitro活性は正常です。
獲得耐性の有病率は、選択された種では地理的および時間の経過とともに異なる可能性があり、耐性に関する地域情報は、特に重篤な感染症の治療に関連する場合に重要です。
局所的な耐性の蔓延により、少なくともいくつかの種類の感染症における薬剤の有用性が疑問視される場合には、必要に応じて専門家のアドバイスを求めるべきである。
薬理学的特徴
薬力学特性
メロペネム(活性物質)は、ヒトデヒドロペプチダーゼ-I(DHP-I)に対して安定な非経口使用用のカルバペネム系抗生物質です。メロペネム (有効成分) はイミペネムと構造的に似ています。
メロペネム (活性物質) は、細菌の細胞壁の合成を阻害することで殺菌作用を発揮します。細菌細胞への浸透の容易さ、ほとんどのセリン ベータ ラクタマーゼに対するその高レベルの安定性、および複数のペニシリン結合タンパク質 (PBP) に対する顕著な親和性により、メロペネム (活性物質) の広範囲の好気性細菌に対する強力な殺菌活性が説明されます。細菌性で嫌気性。

殺菌濃度は通常、最小発育阻止濃度 (MIC) の希釈の 2 倍以内です。
抵抗メカニズム
メロペネム (活性物質) に対する細菌耐性は、1 つまたは複数の要因の結果である可能性があります。
- グラム陰性菌の外膜の透過性の低下(ポリンの産生の低下による)。
- 標的 PBP の親和性の低下。
- 排出ポンプ成分の発現の増加。
- カルバペネムを加水分解できるベータラクタマーゼの生成。
一部の地域では、カルバペネムに対する細菌の耐性による局所的な感染クラスターが報告されています。
分離された臨床データのメロペネム (活性物質) に対する感受性は、標準化された方法によって決定する必要があります。
検査結果の解釈は、地域の感染症および臨床微生物学のガイドラインに従って実行できます。
臨床経験と治療ガイドラインに基づいて、メロペネム (有効成分) の抗菌スペクトルには以下の種が含まれます。
一般的に感受性の高い種:グラム陽性好気性菌
Enterococcus faecalis ( E. faecalis は自然に中程度の感受性を示す可能性があることに注意)、黄色ブドウ球菌(メチシリン感受性株のみ: MRSA [オキサシリン耐性黄色ブドウ球菌] を含むメチシリン耐性ブドウ球菌はメロペネム (活性物質) に耐性があります)、ブドウ球菌、表皮ブドウ球菌種を含む(メチシリン感受性株のみ:MRSE[メチシリン耐性表皮ブドウ球菌]を含むメチシリン耐性ブドウ球菌はメロペネム(活性物質)に耐性がある)、ストレプトコッカス・アガラクティエ(レンサ球菌グループB)、ストレプトコッカス・ミレリグループ( S anginosus、 S.constellatusおよびS.intermedius )、肺炎球菌、化膿性連鎖球菌(A群連鎖球菌)。
一般的に感受性の高い種:グラム陰性好気性菌
シトロバクター・フロインディ、シトロバクター・コセリ、エンテロバクター・エアロゲネス、エンテロバクター・クロアカエ、大腸菌、インフルエンザ菌、髄膜炎菌、肺炎桿菌、クレブシエラ・オキシトカ;モルガネラ・モルガニ、プロテウス・ミラビリス、プロテウス・ブルガリス、セラチア・マルセッセンス。
一般的に感受性の高い種: グラム陽性嫌気性菌
シトロバクター・フロインディ、シトロバクター・コセリ、エンテロバクター・エアロゲネス、エンテロバクター・クロアカエ、大腸菌、インフルエンザ菌、髄膜炎菌、肺炎桿菌、クレブシエラ・オキシトカ;モルガネラ・モルガニ、プロテウス・ミラビリス、プロテウス・ブルガリス、セラチア・マルセッセンス。
一般的に感受性の高い種: グラム陰性嫌気性菌
Clostridium perfringens、Peptoniphilus asaccharolyticus、Peptostreptococcus 種( P. micros、P. anaerobius、P. magnus を含む)。
獲得した耐性が問題となる可能性がある種: グラム陽性好気性菌
Enterococcus faecium ( E. faecium は、獲得した耐性機構がなくても、自然に中程度の感受性を示す可能性があります)。
獲得した耐性が問題となる可能性がある種: グラム陰性好気性菌
アシネトバセル種、バークホルデリア・セパシア、緑膿菌。
本質的に耐性のある微生物: グラム陰性好気性菌
レジオネラ属のStenotrophomonas maltophiliae種。
その他の本質的に耐性のある微生物
クラミドフィラ・ニューモニエ、クラミドフィラ・オウム病、コクシエラ・バーネティ、マイコプラズマ・ニューモニエ。
出版された医学文献には、他のいくつかの細菌種におけるin vitro でのメロペネム (活性物質) に対する感受性が記載されています。しかし、これらのin vitro所見の臨床的意義は不明です。
in vitro所見の臨床的重要性に関するアドバイスは、地域の感染症専門家、地域の臨床微生物学の専門家、および地域の専門ガイドラインから得るべきです。
薬物動態学的特性
健康な患者の場合、メロペネム (活性物質) の排出半減期は約 1 時間です。平均分配量は約 0.25L/kg、平均クリアランスは 239mL/min です。 500mg では 205mL/min に低下します。 2gで。
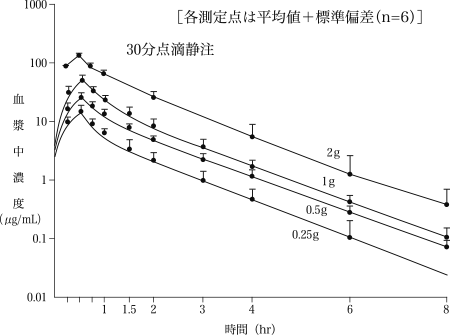
30 分間の点滴で 500、1,000、および 2,000 mg のメロペネム (活性物質) を投与すると、500 mg の用量でピーク血漿濃度は約 23μg/mL になります。 1g用量では49?g/mL、2g用量後は115?g/mLで、それぞれ39.3、62.3、153?gh/mLのAUC値に相当します。 5分間の注入後の最大濃度値(C max )は、500mg/mLおよび1,000mgの用量後のそれぞれ52μg/mLおよび112μg/mLである。
腎機能が正常な個体に 8 時間間隔で複数回投与しても、メロペネム (活性物質) の蓄積は起こりません。
手術後の腹部感染症に対してメロペネム(活性物質)1,000mgを8時間ごとに投与した12人の患者を対象とした研究では、C maxと半減期は正常患者と同等であることが示されましたが、分布量はより多かった(27L)。
分布
メロペネム (活性物質) の血漿タンパク質への結合は約 2% であり、濃度には依存しませんでした。メロペネム (活性物質) は、肺、気管支分泌物、胆汁、脳脊髄液、婦人科組織、皮膚、筋膜、筋肉、腹膜滲出液など、ほとんどの組織や体液によく浸透します。
代謝
メロペネム (活性物質) は、β-ラクタム環の加水分解によって代謝され、微生物学的に不活性な代謝産物が生成されます。インビトロでは、メロペネム(活性物質)はイミペネムと比較してヒトデヒドロペプチダーゼ-1(DHP-I)による加水分解に対する感受性が低下しており、DHP-I阻害剤の同時投与は必要ありません。
排除
メロペネム(活性物質)は主に腎臓から排泄されます。投与量の約 70% (50% – 70%) は 12 時間以内に変化せずに排泄されます。 28% 以上が微生物学的に不活性な代謝産物として回収されます。糞便の排泄は用量の 2% に相当します。測定された腎クリアランスとプロベネシドの効果は、メロペネム(活性物質)が濾過と尿細管分泌を受けることを示しています。
腎不全
腎障害により、血漿 AUC (曲線下面積) と半減期が増加します。中等度の腎障害のある患者(CrCL 33 ~ 74mL/分)では AUC が 2.4 倍、重度の腎障害のある患者(CrCL 4 ~ 23mL/分)では 5 倍、患者では 10 倍増加します。血液透析を受けている患者(CrCL lt; 2mL/分)を健康な患者(CrCL gt; 80mL/分)と比較した場合。
微生物学的に不活性な開環代謝産物の AUC も、腎障害のある患者ではかなり高かった。中等度または重度の腎機能障害のある人には用量の調整が必要です。
メロペネム (活性物質) は血液透析によって除去され、無尿患者の約 4 倍のクリアランスを示します。
肝不全
アルコール性肝硬変患者を対象とした研究では、メロペネム(活性物質)の反復投与後の肝臓に対する疾患関連の影響の薬物動態は実証されませんでした。
大人
患者を対象に実施された薬物動態研究では、同等の腎機能を持つ健常者との薬物動態における有意差は証明されていません。
腹腔内感染症または肺炎の患者 79 人のデータから作成されたモデル集団は、コア体積が体重、クレアチニン クリアランス、および年齢に依存することを示しました。
子供たち
感染症のある青年および小児における薬物動態は、10、20、および40 mg/kgの用量で、それぞれ500、1,000、および2,000 mgの用量での成人の薬物動態と同様のC max値を示しました。
この比較により、最年少患者(lt; 6ヶ月t 1?2 1.6時間)を除くすべての患者について、用量および半減期間の一貫した薬物動態が成人と同様であることが実証された。メロペネム(活性物質)の平均クリアランスは、5.8mL/分/kg(6~12歳)、6.2mL/分/kg(2~5歳)、5.3mL/分/kg(6~23ヵ月)、4.3でした。 mL/分/kg (2 ~ 5 か月)。
用量の約 60% がメロペネム (活性物質) として 12 時間以内に尿中に排泄され、12% 以上が代謝産物として排泄されます。髄膜炎の小児の脳脊髄液中のメロペネム(活性物質)濃度は、個人差が大きいものの、現在の血漿レベルの約 20% です。
抗感染症治療を必要とする新生児におけるメロペネム(活性物質)の薬物動態では、暦年または在胎期間が長い新生児でクリアランスの増加が示され、平均排泄時間は 2.9 時間でした。
PK 集団モデルに基づくモンテカルロ シミュレーションでは、8 時間ごとに 20mg/kg の用量レジメンが 60% の T gt を達成することが実証されました。未熟児の 95%、および非未熟児の 91% における緑膿菌の MIC。
お年寄り
健康な高齢者(65~80歳)を対象とした薬物動態研究では、年齢に伴うクレアチニンクリアランスの低下と相関する血漿クリアランスの低下と、非腎クリアランスのわずかな低下が実証されました。
中等度から重度の腎障害の場合を除き、高齢患者では用量調整は必要ありません。
前臨床安全性データ
動物実験では、メロペネム (活性物質) が腎臓によく耐えられることが示されています。
腎尿細管損傷の組織学的証拠は、マウスおよびイヌにおいて 2,000 mg/kg 以上の用量でのみ観察されました。
メロペネム (有効成分) は、一般に中枢神経系 (CNS) によく耐えられます。影響は 2,000mg/kg 以上の非常に高用量でのみ観察されました。
げっ歯類におけるメロペネム(活性物質)の LD 50 IV は 2,000mg/kg を超えています。最長 6 か月の反復投与試験では、500 mg/kg の用量で犬の赤血球パラメータのわずかな減少と肝臓重量の増加を含む副作用のみが観察されました。
実施された5つの試験では変異原性の可能性の証拠はなく、ラットとサルにおける可能な限り最高用量(F1体重のわずかな減少に影響を及ぼさない用量レベル)での研究では催奇形性の可能性を含む生殖毒性の証拠はなかった。ラットは120mg/kgでした)。
成体動物と比較して、若い動物ではメロペネム(活性物質)に対する感受性が増加するという証拠はありませんでした。
静脈内製剤は動物実験で良好な忍容性を示しました。筋肉内製剤は注射部位に可逆的な壊死を引き起こしました。
メロペネムの唯一の代謝物 (活性物質) は、動物実験でも同様の低毒性プロファイルを示しました。








-1024x576.jpg?resize=1024,576&ssl=1)


