リドジェットはどのように機能しますか?
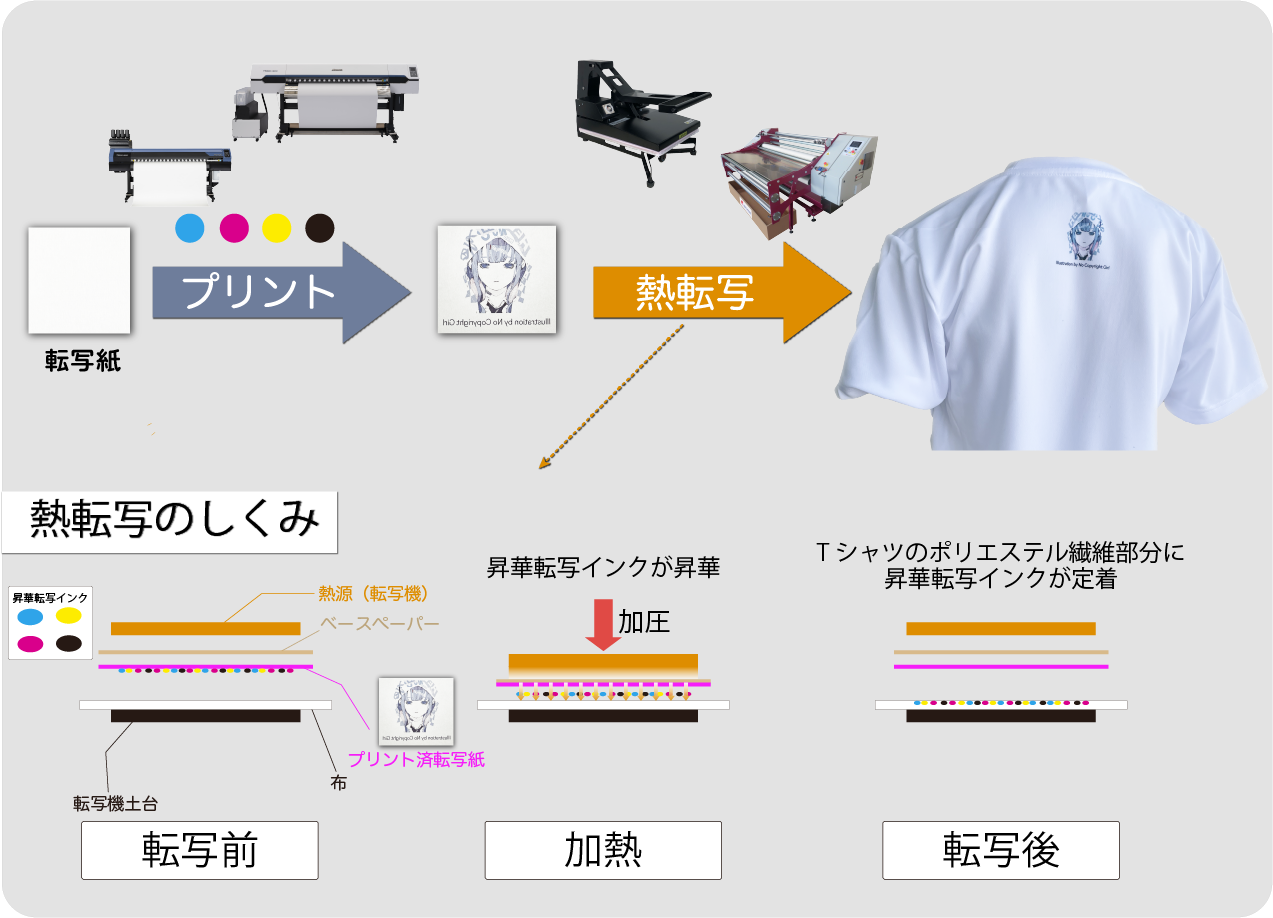
Lidojet 注射液には、浸潤および神経ブロックに適応される局所麻酔薬リドカイン塩酸塩が含まれています。リドカインは、インパルスの開始と伝達に必要なイオンの流れを阻害することで神経膜を安定化し、局所麻酔薬の作用に影響を与えます。
リドジェットの禁忌
リドカインは、アミド型局所麻酔薬またはその配合成分のいずれかに対して過敏症が知られている患者には禁忌です。
リドジェットの使い方
以下の推奨用量表は、さまざまなタイプの麻酔処置に対する塩酸リドカインの量と濃度をまとめたものです。この表で提案されている用量は、正常な健康な成人に対するものです。
大量の薬が必要な場合は、血管収縮薬が禁忌である場合を除き、血管収縮薬のみを使用する必要があります。
これらの推奨用量は、ほとんどの日常的な処置に必要な麻酔薬の量のガイドとしてのみ機能します。実際に使用する量と濃度は、外科手術の種類と範囲、必要な麻酔の強度と筋肉弛緩の程度、必要な麻酔時間、患者の身体状態などの要因によって異なります。いずれの場合も、望ましい結果が得られる最低濃度と最低用量を採用する必要があります。小児、高齢者、衰弱した患者、心臓疾患や肝臓疾患のある患者の場合は、投与量を減らす必要があります。
麻酔の開始、麻酔の持続時間、筋肉弛緩の程度は、使用する局所麻酔薬の量と濃度(総用量)に比例します。
したがって、塩酸リドカイン注射剤の濃度と量を増やすと、麻酔の開始時間が短縮され、麻酔時間が延長され、筋肉の弛緩が大幅に促進され、麻酔の部分的な拡張が増加します。
ただし、硬膜外麻酔に使用した場合、塩酸リドカインの量と濃度を増やすと、血圧が大幅に低下する可能性があります。
リドカインによる他の影響の発生率は非常に低いですが、他の影響の発生率は注入された局所麻酔薬の総用量に直接比例するため、大量および高濃度の使用には注意が必要です。
投与量
塩酸リドカイン注射液の推奨用量
浸潤
経皮浸潤
集中:
0.5 または 1.0%。
音量:
1~60mL。
総線量:
5~300mg。
静脈内局所浸潤
集中:
1.5%。
音量:
15~20mL。
総線量:
225から300まで。
上腕末梢神経ブロック
集中:
1.5%。
音量:
15~20mL。
総線量:
225~300mg。
歯科末梢神経ブロック
集中:
2.0%。
音量:
1~5mL。
総線量:

20~100mg。
肋間末梢神経ブロック
集中:
1.0%。
音量:
3mL。
総線量:
30mg。
脊椎傍末梢神経ブロック
集中:
1.0%。
音量:
3~5ml。
総線量:
30~50mg。
陰部末梢神経ブロック(両側)
集中:
1.0%。
音量:
10ml。
総線量:
100mg。
子宮頸管傍
産科鎮痛(両側)
集中:
1.0%。
音量:
10ml。
総線量:
100mg。
交感神経遮断
子宮頸部(星状神経節)
集中:
1.0%。
音量:
5ml。
総線量:
50mg。
腰部
集中:
1.0%。

音量:
5~10ml。
総線量:
50〜100mg。
中枢神経ブロック
硬膜外*胸部
集中:
1.0%。
音量:
20~30ml。
総線量:
200~300mg。
硬膜外・腰椎
集中:
1.0%。
音量:
25~30ml。
総線量:
250~300mg。
硬膜外麻酔・鎮痛
集中:
1.5%。
音量:
15~20ml。
総線量:
225~300mg。
硬膜外麻酔・麻酔
集中:
2.0%。
音量:
10~15ml。
総線量:
200~300mg。
尾部の産科鎮痛
集中:
1.0%。
音量:
20~30ml。
総線量:
200~300mg。
尾部の外科的鎮痛

集中:
1.5%。
音量:
15~20ml。
総線量:
225~300mg。
※投与量は麻酔するダーマトームの数によって決まります(2~3mL/ダーマトーム)。
注: 推奨される濃度と量は目安としてのみ使用してください。最大推奨用量を超えない限り、他の容量および濃度も使用できます。
尾部および腰部硬膜外ブロック
くも膜下腔に意図せず穿孔ができた場合に観察される副作用の可能性に対する予防措置として、腰部または尾部硬膜外ブロックに必要な全量を注射する前に、試験用量の 1.5% リドカイン塩酸塩 2 ~ 3 mL を少なくとも 5 分間投与する必要があります。 。カテーテルが外れてしまった患者には、試験用量を再度投与する必要があります。
鎮静された患者は、15 秒以上の間、1 分あたり 20 拍以上の脈拍数の増加のみを示す場合があります。
ベータ遮断薬を服用している患者は心拍数の変化を経験しない可能性がありますが、血圧を監視すると収縮期血圧のわずかな上昇が検出される場合があります。各試験用量の投与後、麻酔が始まるまでに十分な時間が必要です。
くも膜下腔に大量の局所麻酔液を注入したことが知られている場合、適切な蘇生の後、カテーテルが留置されている場合は、硬膜外から適量の脳脊髄液 (約 10 mL) を排出して薬剤を回収することを検討してください。カテーテル。 。
最大推奨投与量
大人
正常な健康な成人の場合、塩酸リドカインの最大個別投与量は体重 1 kg あたり 4.5 mg を超えてはならず、最大総投与量は 300 mg を超えないようにすることが一般に推奨されます。
継続的な尾部麻酔の場合、推奨最大用量を 90 分未満の間隔で投与しないでください。
産科以外の処置に継続的な尾部麻酔を使用する場合、適切な麻酔を実現するために大量の薬剤を投与することができます。
産科患者および非産科患者における子宮頸管傍ブロックに対する塩酸リドカインの 90 分あたりの最大推奨用量は 200 mg です。
通常、総線量の 50% が両側に適用されます。両側で 5 分間待って、ゆっくりと注入します。
子供たち
年齢や体重に応じて変動するため、小児に対して薬物の最大用量を推奨することは困難です。正常な除脂肪体重と正常な身体発育を有する 3 歳以上の小児の場合、最大推奨用量は小児の年齢と体重によって決まります。たとえば、体重約 25 kg の 5 歳児の場合、塩酸リドカインの用量は 75 ~ 100 mg (3.0 ~ 4.0 mg/kg) を超えてはなりません。
全身毒性を防ぐには、低濃度および有効量のみを使用する必要があります。場合によっては、必要な最終濃度を得るために、0.9% 注射用塩化ナトリウムで希釈した濃度を用意する必要があります。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。医師の知識なしに治療を中断しないでください。
リドジェットの使用を忘れた場合はどうすればよいですか?
この薬は病院内で医療従事者によって投与されるため、その使用を忘れてはいけません。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
リドジェットの予防措置
この製品は、使用される用量依存性の毒性の診断と制御、および使用されるブロックの種類によって生じる可能性のあるその他の急性緊急事態の診断と制御に経験のある専門家のみが、蘇生のための酸素およびその他の薬剤がすぐに利用できることを確認した後にのみ投与されるべきです。 、心肺蘇生装置、および中毒反応および関連する緊急事態の治療と制御に必要な訓練を受けた職員。
理由や感受性の変化が何であれ、薬物の用量関連毒性および低換気に対する応答の欠如または遅延は、アシドーシスの発症、心停止、および死亡の可能性を引き起こす可能性があります。
必要に応じて、硬膜外麻酔の投与後に下半身の感覚と運動活動が一時的に失われる可能性があることを患者に事前に通知する必要があります。
リドカインの安全性と有効性は、正しい用量、適切な技術、適切な予防策、緊急時のスピードに依存します。
蘇生装置、酸素、その他の蘇生薬はすぐに使用できるように用意しておく必要があります。
高い血漿レベルや重篤な副作用を避けるために、効果的な麻酔が得られる最低用量を使用する必要があります。カテーテル技術を使用する場合は、追加の各注射の前および最中にシリンジ吸引も実行する必要があります。硬膜外麻酔の投与中は、最初に試験用量を投与し、続行する前に中枢神経系毒性と心血管毒性、および意図しないくも膜下腔内投与の兆候について患者をモニタリングすることが推奨されます。臨床条件が許せば、エピネフリンを含む局所麻酔液の使用を試験用量として考慮する必要があります。エピネフリンと一致する循環変化は、意図しない血管内注射の警告サインとしても機能する可能性があるためです。
血液吸引が陰性の場合でも血管内注射も可能です。リドカインを繰り返し投与すると、薬物またはその代謝産物の蓄積が遅いため、繰り返し投与するたびに血漿レベルが大幅に増加する可能性があります。
高血中濃度に対する耐性は患者の状態によって異なります。高齢者や衰弱している患者、急性疾患の患者、小児は、年齢や体調に応じて投与量を減らしてください。
リドカインは、重度のショックや心臓ブロックのある患者にも注意して使用する必要があります。腰部または尾部の硬膜外麻酔は、神経疾患の存在、脊椎変形、敗血症、重度の高血圧などの症状のある人には細心の注意を払って使用する必要があります。
局所麻酔薬を注射するたびに、心臓血管および呼吸器の監視 (適切な換気)、バイタルサイン、および患者の意識状態を注意深く継続的に監視する必要があります。このようなときは、動揺、不安、耳鳴り、めまい、かすみ目、震え、憂鬱、眠気などが中枢神経系毒性の最初の兆候である可能性があることも覚えておく必要があります。アミド系局所麻酔薬は肝臓で代謝されるため、肝疾患のある患者さんへのリドカインの使用は注意が必要です。重度の肝疾患を患っている患者は、局所麻酔薬の代謝能力が低下しているため、有毒な血漿濃度が発生するリスクが高くなります。リドカインは、これらの薬剤によって引き起こされる房室伝導の延長に伴う機能変化を補う能力が低下するため、心血管機能に変化がある患者にも注意して使用する必要があります。
リドカインは、薬物過敏症があることがわかっている人には注意して使用する必要があります。
パラアミノ安息香酸誘導体(プロカイン、テトラカイン、ベンゾカインなど)にアレルギーのある患者は、リドカインに対して交差感受性を示していません。
血管内注射を避けるために、麻酔液を注入する前に吸引を実行する必要があります。

吸引中に血液が戻らなくなるまで、針の位置を変更する必要があります。
ただし、注射器内に血液が存在しないからといって、血管内注射が回避されたとは限りません。
抗菌防腐剤(メチルパラベンなど)を含む局所麻酔液は、意図的か偶発的かにかかわらず、くも膜下腔内注射に関して安全性が確立されていないため、硬膜外麻酔や脊椎麻酔には使用しないでください。
頭と首の領域に使用します
眼球後ブロック、歯科ブロック、星状神経節ブロックなど、頭頸部の領域に少量の局所麻酔薬を注射すると、意図しない大量の血管内注射で観察される全身毒性と同様の副作用が生じる可能性があります。
混乱、けいれん、一時的な失明、呼吸抑制および/または呼吸停止、心血管の刺激または抑制が報告されています。これらの反応は、脳循環への逆流を伴う局所麻酔薬の動脈内注射によるものである可能性があります。これらのブロックを受ける患者は、循環と呼吸を監視し、常に観察しなければなりません。蘇生装置と副作用に対処する訓練を受けた人員をすぐに利用できるようにする必要があります。推奨用量を超えないようにしてください。
発がん性、変異原性、生殖能力の低下
リドカインの発がん性や変異原性の可能性、生殖能力への影響を評価するための動物実験は行われていません。
妊娠
カテゴリーB。
催奇形性の影響
生殖研究は、ヒト用量の最大6.6倍の用量でラットで行われており、リドカインによって引き起こされる胎児への害の証拠は明らかにされていない。しかし、妊婦を対象とした適切でよく管理された研究はありません。
動物の生殖研究は、人間の反応を再現するのに必ずしも役立つとは限りません。
妊娠の可能性のある女性、特に器官形成が最大限に行われる妊娠初期の女性にリドカインを投与する前に、一般的な考慮事項を考慮する必要があります。
この薬は、医師または歯科外科医のアドバイスなしに妊婦が使用しないでください。
労働と出産
局所麻酔薬は胎盤を素早く通過し、硬膜外麻酔、子宮頚管傍麻酔、陰部ブロックまたは尾部ブロックに使用すると、母体、胎児、新生児にさまざまな強度の毒性を引き起こす可能性があります。潜在的な毒性は、実行される処置、使用される薬剤の種類と量、および薬剤投与技術によって異なります。妊婦、胎児、新生児における副作用には、中枢神経系の末梢血管の緊張や心臓機能の変化が含まれます。
母体の低血圧は局所麻酔の結果です。局所麻酔薬は交感神経を遮断することで血管拡張を引き起こします。
下肢を挙上し、患者を左側臥位にすると、血圧の低下を防ぐことができます。
胎児の心拍数も常に監視する必要があり、電子的な胎児モニタリングが非常に推奨されます。
硬膜外麻酔、脊椎麻酔、子宮頚管傍麻酔、または陰部ブロックは、子宮の収縮性や駆出力の変化により、分娩中の収縮を変化させる可能性があります。
子宮頚管傍麻酔ブロックの研究では、分娩第 1 期の平均期間の短縮と子宮頸部の拡張の容易さとが関連していることがわかりました。
しかし、脊椎麻酔および硬膜外麻酔は、駆出反射を除去したり、運動機能を妨げたりすることにより、分娩の第 2 段階を延長することが示されています。産科での麻酔薬の使用により、鉗子の必要性が増加する可能性があります。
分娩時に局所麻酔薬を使用した後、新生児の生後 1 日目または 2 日目に筋力や緊張が低下することがあります。
これらの影響が長期間持続することがどれほど重要であるかは不明です。胎児徐脈は、アミドタイプの局所麻酔薬による子宮頸傍神経を介したブロック麻酔を受けた患者の 20% ~ 30% で発生する可能性があり、胎児アシドーシスと関連している可能性があります。
子宮頸部傍麻酔中は胎児の心拍数を常に監視する必要があります。
医師は、早産における子宮頸管傍ブロックのリスクと利益の可能性、妊婦の中毒症、胎児の危険性を分析する必要があります。
産科子宮頸管傍ブロックでは、推奨用量を遵守することが最も重要です。
推奨用量で十分な鎮痛が得られない場合は、胎児の血管内または頭蓋内注射の疑いが生じます。
子宮頚管傍ブロックまたは陰部ブロック、またはその両方の後に、意図せずに胎児に局所麻酔液が頭蓋内に注入されたケースが報告されています。
このような影響を受けた赤ちゃんは、出生直後に原因不明の新生児鬱状態を示しますが、これは局所麻酔薬の血清レベルが高いことに関連している可能性があり、多くの場合 6 時間以内に脳卒中を発症します。
この合併症を制御するには、局所麻酔薬の強制尿排泄と組み合わせた支持療法の即時使用が成功しています。
早産妊娠における子宮頚管傍ブロック(選択的中絶のための麻酔)のための局所麻酔薬の使用後に母体のけいれんや心血管虚脱が報告されており、これらの状況では全身への吸収が急速である可能性があることを思い出してください。各薬剤の最大推奨用量を超えてはなりません。
注射はゆっくりと頻繁に吸引しながら行う必要があります。両サイドの間には 5 分間の休憩が必要です。
授乳
他の局所麻酔薬と同様に、リドカインは母乳を通じて排泄されますが、その量は少量であるため、治療用量で使用しても通常は子供に危険はありません。
小児用
小児の場合は、年齢、体重、体調に応じて投与量を減らす必要があります。
薬物相互作用
この製品との薬物相互作用の報告はありません。
臨床検査の変化

リドカインの筋肉内注射は、クレアチニンホスホキナーゼのレベルの上昇を引き起こす可能性があります。したがって、アイソザイム分離を行わずにこの酵素を測定することを、急性心筋梗塞の有無の診断検査として使用することは、リドカインの筋肉内注射によって損なわれる可能性があります。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
リドジェットの副作用
全身性
リドカイン投与後の副作用は、他のアミド系局所麻酔薬で観察される副作用と性質が似ています。これらの副作用は一般に用量に関連しており、過剰な用量、急速な吸収、または偶発的な血管内注射によって引き起こされる高血漿レベルによって生じる場合があり、また患者側の過敏症、特異性、または耐性の低下によって生じる場合もあります。重篤な副作用は一般に全身性の性質を持っています。
最も頻繁に報告されている副作用の種類は次のとおりです。
中枢神経系
CNS 症状は興奮性および/または抑制性であり、欠神発作、神経過敏、不安、多幸感、錯乱、めまい、眠気、耳鳴り、かすんだまたは複視、嘔吐、熱感、冷感またはしびれ、収縮、震え、けいれんを特徴とする場合があります。 、意識不明、うつ病、呼吸停止。興奮症状は非常に短期間である場合もあれば、まったく起こらない場合もあり、毒性の最初の症状は眠気であり、意識消失および呼吸停止に進行します。
リドカイン投与後の眠気は、通常、薬物の血中濃度が高いことの初期の兆候であり、薬物の急速な吸収の結果として発生する可能性があります。
心臓血管系
心血管症状は通常、徐脈、低血圧、心血管虚脱を特徴とする抑うつ状態であり、心停止を引き起こす可能性があります。
アレルギー
アレルギー反応は、皮膚病変、蕁麻疹、浮腫、またはアナフィラキシー様反応を特徴とします。アレルギー反応は、局所麻酔薬または複数回用量バイアルの防腐剤として使用されるメチルパラベンに対する過敏症によって引き起こされる可能性があります。リドカインに対する過敏症に起因するアレルギー反応は非常にまれであり、発生した場合には従来の手段で監視する必要があります。皮膚テストによる過敏症の検出には価値が疑われます。
神経系
局所麻酔薬の使用に伴う副作用の発生率は、投与される総用量に関連する可能性があり、使用される薬剤の特殊性、投与経路、患者の身体状態にも依存します。
脊椎麻酔のためにリドカインを投与された10,440人の患者を対象に実施された研究では、姿勢性頭痛、低血圧、腰痛について報告された副作用の発生率は約3%でした。震えの場合は2%、末梢神経症状、吐き気、不十分な呼吸、複視の場合は1%未満です。これらの観察の多くは、局所麻酔薬の影響の有無にかかわらず、使用された麻酔技術に関連している可能性があります。
尾部または腰部硬膜外ブロックを行う場合、意図せずにカテーテルがくも膜下腔に挿入されることがあります。その後の副作用は、特にくも膜下腔に投与された薬剤の量に依存する可能性があります。これには、さまざまな程度の脊椎ブロック(全脊椎ブロックを含む)、脊椎ブロックに続発する低血圧、膀胱と腸の制御の喪失、会陰感覚と性機能の喪失が含まれる場合があります。尾部または腰部硬膜外ブロックを行った場合、回復が遅い(数か月)または不完全な回復を伴う一部の脊椎下部セグメントの持続的な運動、感覚、および/または自律神経の欠陥(括約筋制御)が報告されることはほとんどありません。これらの麻酔処置を使用すると、腰痛や頭痛が観察されます。
眼球後投与により外眼筋に永久的な損傷が生じ、修復手術が必要になった例の報告があります。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。また、顧客サービスを通じて会社に通知してください。
リドジェットの構成
各 mL には次のものが含まれます。
塩酸リドカイン一水和物を21,330mg *配合。
※無水リドカイン塩酸塩20mgに相当します。
車両:
塩化ナトリウム、水酸化ナトリウム、メチルパラベン、注射用水。
リドジェットの過剰摂取
局所麻酔薬の投与によって生じる緊急事態は、一般に、局所麻酔薬の治療的使用中に見られる高い血漿レベル、または麻酔液の偶発的なくも膜下注射に関連しています。
局所麻酔薬による緊急事態の管理
最初に考慮すべきことは、局所麻酔薬を注射するたびに、呼吸器および心臓血管のバイタルサインと患者の意識状態を注意深く継続的にモニタリングすることによる予防です。変化の最初の兆候が現れたら、直ちに酸素を投与する必要があります。
けいれん、およびくも膜下腔への意図しない注射による低換気または無呼吸を制御するための最初のステップは、気道を維持するためのアクセスと酸素による補助的かつ効果的な換気を即座に確立することで構成され、即時かつ積極的な気道を確保できるリリースシステムを使用します。マスクによる圧迫。
これらの換気手段を導入した直後に、発作の治療に一般的に使用される薬剤を静脈内に注射すると循環が抑制される場合があることを常に念頭に置きながら、循環の適切性を評価する必要があります。
呼吸補助を行った後もけいれんが持続し、循環状態が許せば、少量の超短時間作用型バルビツレート系薬剤(チオペントン 1 ~ 3 mg/kg など)またはベンゾジアゼピン系ジアゼパム系薬剤(0.1 mg/kg)を静脈内投与することがあります。 kg)。医師は、局所麻酔薬を使用する前に、これらの薬剤と併用することについてよく知っておく必要があります。
心室細動または心停止が発生した場合は、心肺蘇生治療を開始する必要があります。
循環抑制の支持療法には、臨床状況のニーズに応じて輸液の静脈内投与、および必要に応じて昇圧剤の投与が必要な場合があります。
直ちに治療しなければ、発作と心血管抑制はいずれも低酸素症、アシドーシス、徐脈、不整脈、心停止を引き起こす可能性があります。
意図しないクモ膜下注射によって生じる低換気または無呼吸も同様の症状を引き起こす可能性があり、換気補助が行われていない場合は心停止につながる可能性もあります。
臨床医がよく知っている薬剤と技術を使用した気管内挿管は、マスクを介した最初の酸素投与後、また患者の気道の維持が困難な場合、または補助または制御による長期間の換気補助が必要な場合にも適応されることがあります。
リドカインの急性過剰摂取の治療において透析はほとんど価値がありません。
局所麻酔薬の投与によって生じる緊急事態は、一般に、局所麻酔薬の治療的使用中に見られる高い血漿レベル、または麻酔液の偶発的なくも膜下注射に関連しています。
この薬を大量に使用した場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
リドジェットの薬物相互作用
注射可能な溶液
産科遮断に関連する低血圧の治療のための昇圧薬とエルゴタイプのオキシトシス物質を同時に投与すると、重度の持続性高血圧や脳血管障害を引き起こす可能性があります。
臨床検査の変化
塩酸リドカイン (活性物質) を筋肉内注射すると、クレアチニン ホスホキナーゼのレベルが上昇する可能性があります。したがって、アイソザイム分離を行わずにこの酵素を測定する、急性心筋梗塞の有無の診断検査としての使用は、塩酸リドカイン (活性物質) の筋肉内注射によって損なわれる可能性があります。
ゼリー
塩酸リドカイン (活性物質) は、毒性効果が相加的なものであるため、構造的に局所麻酔薬に関連する薬剤を投与されている患者には注意して使用する必要があります。
塩酸リドカイン (活性物質) およびクラス III 抗不整脈薬 (アミオダロンなど) との特異的な相互作用研究は行われていませんが、注意が必要です。
塩酸リドカイン (活性物質) の血漿クリアランスを低下させる薬剤 (シメチジンやベータ遮断薬など) は、塩酸リドカイン (活性物質) が高用量で長期間繰り返し投与されると、潜在的に有毒な血漿濃度を引き起こす可能性があります。しかし、このような相互作用は、推奨用量の塩酸リドカイン (活性物質) による短期治療では臨床的に重要ではありません。
注射液 2.0%
塩酸リドカイン(活性物質)は、毒性効果が相加的なため、トカイニドなどの抗不整脈薬で治療されている患者や、ベータ遮断薬、シメチジン、ジギタリスを使用している患者には注意して使用する必要があります。塩酸リドカイン (活性物質) をフェニトインの静脈内投与すると、付加的な心臓への影響が発生する可能性があります。ただし、フェニトインやその他の酵素誘導剤を長期間使用すると、塩酸リドカインの必要用量(活性物質)が増加する可能性があります。アセタゾラミド、ループ利尿薬およびチアジドによって引き起こされる低カリウム血症は、塩酸リドカイン (活性物質) の効果に拮抗します。
出典: 医療キシレステシン®のプロフェッショナル インサート。
リドジェット物質の作用
有効性の結果
注射可能な溶液
心毒性を低くし、満足のいく運動遮断を目的として、異なる製剤のブピバカインエナンチオマーの混合物、S75-R25 または S90-R10 が提案されました。この研究の目的は、顔面神経において鏡像異性体過剰率 50% のブピバカイン (S75-R25) 0.5%、ラセミ体ブピバカイン 0.5%、および塩酸リドカイン (活性物質) 2% を使用して、運動遮断の発症時間と程度を比較することでした。オブライエンテクニックを使用してブロックします。この研究には、オブライエン無動症が先行して球後ブロックによる白内障の外科的治療が予定されている60歳以上の患者45人が含まれていた。 2% 塩酸リドカイン (活性物質) を使用すると、運動ブロックの開始と最大程度のブロックがより迅速に得られました。
参照:
カンジャーニ・ルイス・エンリケ、カンジャーニ・ルイス・マルシアーノ、ペレイラ・アントニオ・マルシオ・デ・サフィム・アランテス。オブライエン法を用いた顔面神経ブロックにおけるエナンチオマー過剰率 (S75-R25) 0.5% のブピバカイン、ラセミ体ブピバカイン 0.5%、およびリドカイン 2%: 比較研究。ブラス牧師。麻酔薬。 2007年; 57(2): 136-146。
ゼリー
Valkevic DSらは、尿道局所麻酔下で膀胱鏡検査を受ける18人の患者を対象に、処置の5分前に2%ゼリーの製剤形態の塩酸リドカイン(活性物質)10mLを使用した研究で、次の結果を得た。塩酸リドカイン(活性物質)をゼリー状の製剤で投与した患者と投与しなかった患者の疼痛の比較(それぞれ、視覚的アナログ疼痛スケール 1.6 および 4.87)。著者らは、2%ゼリーの医薬形態の塩酸リドカイン(活性物質)は有効であり、膀胱鏡検査の患者に許容されると結論付けた(Valkevic DS et al. Pharmacology amp; Toxicology 2001; 89(suppl 1): 135-6、abs) 546)。
注射液 2.0%
2009年、Nevesらは、塩酸リドカイン(活性物質)とエピネフリンを用いた歯科における局所麻酔が、心臓弁膜症の妊婦とその乳児の心血管パラメータに及ぼす影響を調査した。妊娠 28 週目から 37 週目までのリウマチ性弁膜症のある妊婦 31 名を対象に、心電図検査、血圧、心電図パラメータを評価しました。患者はランダムに 2 つのグループに分けられました。 LSA グループ – 14 名 (45.2%) の患者が、血管収縮剤を含まない塩酸リドカイン (活性物質) 2% の麻酔液を投与されました。 LCA グループ – 塩酸リドカイン (活性物質) 2%、アドレナリン 1:100,000 で 17 名 (54.8%)。両グループに臨床的合併症はありませんでした。収縮期血圧と拡張期血圧、胎児の心拍数、母体の子宮収縮には変化は観察されませんでした。処置中、両方のグループで母体の心拍数が減少しました。
Balakrishnanらは総説記事でこう述べている。歯科における局所麻酔薬に関連する血管収縮薬の使用の禁忌を評価します。心血管疾患(不安定狭心症、心室頻拍、重度の高血圧、最近の冠動脈手術)のある患者、または褐色細胞腫、制御不能な甲状腺機能亢進症の患者、三環系抗うつ薬、コカインを使用している患者は、血管収縮剤が不適切に使用されると生命を脅かす可能性があります。 101件の研究を対象に実施されたメタ分析では、局所麻酔薬を単独で使用した場合、昇圧薬と併用した場合よりも患者が副作用を発症するリスクが低いことが観察されました。したがって、心臓血管に問題がある患者では、アドレナリン作動性血管収縮薬の使用を避けることが推奨されます。
2010年の研究で、Ezmekらは、全身性動脈性高血圧症が成人の最も一般的な慢性疾患であり、年齢とともに発生率が増加していることを考慮して、高血圧患者の血行動態状態に関して歯科麻酔の診療で広く使用されている局所麻酔薬の安全性を比較しようと試みた。年齢が進む。 60人の高血圧患者(女性29人、男性31人、平均年齢:66.95±10.87歳、範囲:38~86歳)が抜歯(大臼歯57本、第二小臼歯8本)の研究に含まれた。下部肺胞および頬神経ブロックは、塩酸リドカイン (活性物質) 2%、メピバカイン 3%、プリロカイン 2% を使用して、すべて血管収縮剤を使用せずに実施されました。収縮期血圧 (SBP)、拡張期血圧 (DBP)、平均動脈圧 (MAP)、心拍数 (HR)、飽和速度 (TS)、圧力積率 (TPP)、および心拍数商圧力 (QTP) などの血行力学的パラメーター) は、麻酔投与前と麻酔投与後のさまざまな間隔で測定されました。実験中、血圧値は、麻酔薬グループ間でも、ベースラインの血行力学的パラメータとの関係でも、大きな変化が見られなかったことが観察されました。
参考文献:
ネベス ILI、アビラ WS、ネベス RS、ジョルジ DMA、サントス JFK、オリベイラ フィリョ RMO、他心臓弁膜症患者の歯科処置中の母体と胎児のモニタリング。 Arq Bras Cardiol 2009 Nov;93(5):463-72。
Balakrishnan R、Ebenezer V. 歯科における血管収縮薬の禁忌。バイオメディカルアンプ;薬理学ジャーナル。 2013年; 6(2): 409-414。
Ezmec B、Arslan A、Delilbasi、Semcift K. 高血圧患者における血管収縮剤を含まないリドカイン、プリロカインおよびメピバカイン溶液の血行動態効果の比較。 J Appl Oral Sci 2010 7-8 月;18(4):354-9。
出典: 医療キシレステシン®のプロフェッショナル インサート。
薬理学的特徴
注射可能な溶液
説明
塩酸リドカイン (活性物質) 1% および 2% の注射液には、浸潤および神経ブロックを適応とする、エピネフリンと関連するかまたは関与しない局所麻酔薬塩酸リドカイン (活性物質) が含まれています。
塩酸リドカイン(活性物質)はアミド型の局所麻酔薬で、化学的には2-(ジエチルアミノ)-N-(2,6-ジメチルフェニル)-アセトアミド一塩酸塩一水和物と呼ばれます。白い粉末で、水によく溶けます。
エピネフリンを含まない塩酸リドカイン (活性物質) 1% および 2% は、無菌の非発熱性溶液です。血管収縮剤を含まない溶液の pH は 5.0 ~ 7.0 です。
バイアルには防腐剤としてメチルパラベンが含まれています。
臨床薬理学
作用機序
塩酸リドカイン (活性物質) は、インパルスの開始と伝導に必要なイオン流を阻害することで神経膜を安定化し、局所麻酔薬の作用に影響を与えます。
血行動態
過剰な血中濃度は、心拍数、全末梢抵抗、平均動脈圧の変化を引き起こす可能性があります。中枢神経遮断の場合、これらの変化は自律神経線維の遮断、心血管系のさまざまな構成要素および/またはベータアドレナリン受容体に対する局所麻酔薬の直接的な抑制効果に起因する可能性があります。推奨用量を超えない場合、通常は中等度の低血圧が生じます。
薬物動態と代謝
さまざまな製剤からの情報







-1024x576.jpg?resize=1024,576&ssl=1)


