閉経後の女性に対して塩酸ラロキシフェン(活性物質)による治療か他の治療法を選択する場合は、閉経期の症状、乳房や子宮への影響、心臓血管へのリスクと利点を考慮する必要があります。
塩酸ラロキシフェンの禁忌 – Blanver
塩酸ラロキシフェン(活性物質)は、妊娠中または妊娠する可能性のある女性には禁忌です。妊娠中の塩酸ラロキシフェン(活性物質)による治療は、胎児の先天異常のリスク増加と関連している可能性があります。
妊娠
カテゴリX。
この薬は、妊娠している女性、または治療中に妊娠する可能性のある女性は使用しないでください。
塩酸ラロキシフェン(活性物質)は、深部静脈血栓症、肺塞栓症、網膜静脈血栓症などの静脈血栓塞栓症エピソードの現在または過去の病歴がある患者には禁忌です。
塩酸ラロキシフェン(活性物質)は、ラロキシフェンまたは錠剤中の賦形剤に対して過敏症のある患者には禁忌です。
ラロキシフェン塩酸塩の使用方法 – Blanver
推奨用量は、塩酸ラロキシフェン(活性物質)1 錠(塩酸ラロキシフェン 60 mg)を 1 日 1 回経口投与し、食事に関係なくいつでも服用できます。高齢患者の場合、用量調整は必要ありません。

カルシウムとビタミンDの少ない食事をしている女性には、これらの物質のサプリメントを投与することが推奨されます。
この薬は割ったり、開けたり、噛んだりしないでください。
ラロキシフェン塩酸塩の使用上の注意 – Blanver
脳血管障害(CVA)
脳血管障害(CVA)や、一過性脳虚血発作や心房細動などの脳卒中の他の重大な危険因子の病歴がある閉経後の女性に塩酸ラロキシフェン(活性物質)を使用する場合のリスクと利益のバランスを考慮する必要があります。物質)が処方されています。
冠状動脈性心疾患の病歴がある、または冠状動脈イベントのリスクが高い閉経後の女性を対象とした塩酸ラロキシフェン(活性物質)を使用した研究では、脳卒中、心筋梗塞、急性冠状動脈症候群(ACS)による入院、心血管死亡率または全死亡率の発生率が減少しました。プラセボと同等でした。しかし、脳卒中による死亡率は増加しています。脳卒中死亡率は、プラセボ投与群では年間女性1,000人中1.5人であったのに対し、塩酸ラロキシフェン(活性物質)投与群では女性1,000人中2.2人でした。
静脈血栓塞栓症イベント
塩酸ラロキシフェン(活性物質)は、静脈血栓塞栓性イベントを発症するリスクの増加と関連しており、これはホルモン補充療法に関連するリスクと同様です。あらゆる病因による静脈血栓塞栓性イベントのリスクがあるすべての患者において、リスク/ベネフィット比を考慮する必要があります。長期間の固定化につながる病気や症状の場合、塩酸ラロキシフェン(活性物質)による治療を中断する必要があります。
リスクの大きさは、ホルモン補充療法の使用に関連して報告されているリスクと同様であると考えられます。病気の場合、または固定化が起こる3日前に、治療をできるだけ早く中止する必要があります。初期状態が解消され、患者が完全に動けるようになるまで、治療を再開しないでください。

肝不全
ラロキシフェン塩酸塩 (活性物質) は主に肝臓で代謝されます。塩酸ラロキシフェン(活性物質)の有効性は、肝不全患者では研究されていません。塩酸ラロキシフェン (活性物質) は、血清ビリルビンが 0.6 ~ 2.0 mg/dL の範囲の肝硬変 (チャイルド ピュー クラス A) 患者を対象に単回投与で研究されました。ラロキシフェンの血漿濃度は対照群より約 2.5 倍高く、総ビリルビン濃度と関連していました。
この患者集団では、塩酸ラロキシフェン (活性物質) の使用は推奨されません。総血清ビリルビン、ガンマ-グルタミルトランスフェラーゼ、アルカリホスファターゼ、TGOおよびTGPの値の上昇が観察された場合は、治療中にモニタリングする必要があります。
腎不全
塩酸ラロキシフェン(活性物質)の使用は、重度の腎不全患者には推奨されません。中等度および軽度の腎不全の患者では、その使用には注意が必要です。
閉経前に使用する
閉経前における塩酸ラロキシフェン(活性物質)の使用に関する適応はありません。
全身ホルモン療法との併用
塩酸ラロキシフェン(活性物質)と全身ホルモン療法(プロゲスチンの有無にかかわらずエストロゲン)の併用に関する安全性情報は限られているため、塩酸ラロキシフェン(活性物質)と全身エストロゲンの併用は推奨されません。
子宮内膜
塩酸ラロキシフェン (活性物質) は子宮内膜の増殖とは関係ありません。ラロキシフェン塩酸塩(活性物質)による治療中に予期せぬ子宮/膣出血が発生した場合は、徹底的に調査する必要があります。
エストロゲン誘発性高トリグリセリド血症
経口エストロゲン誘発性高トリグリセリド血症(gt; 5.6 mmol/L)の病歴のある患者では、塩酸ラロキシフェン(活性物質)は血清トリグリセリドの増加に関連している可能性があります。このような病歴を持つ患者は、塩酸ラロキシフェン (活性物質) を使用する際、血清トリグリセリドを監視する必要があります。
乳がんリスク軽減の限界
遺伝性変異(BRCA1、BRCA2)を持つ女性における浸潤性乳がんの発生率に対する塩酸ラロキシフェン(活性物質)の影響について、これらの症例における適応と有効性を正当化するデータは存在しない。塩酸ラロキシフェン(活性物質)も、非浸潤性乳がんの軽減、浸潤性乳がんの治療、または再発リスクの軽減には適応されていません。
血管拡張
塩酸ラロキシフェン(活性物質)は、エストロゲン欠乏に関連する血管拡張(ほてり)やその他の更年期症状を軽減する効果はありません。
発がん、突然変異誘発、生殖能力へのダメージ
ラットでの 2 年間の発がん性研究では、279 mg/kg/日を投与された雌で顆粒膜細胞由来の卵巣腫瘍の発生率の増加が観察されました。このグループにおけるラロキシフェンの全身曝露(AUC)は、60 mg を投与された閉経後の女性よりも約 400 倍高かった。マウスを用いた 21 か月の発がん性研究では、41 または 210 mg/kg を投与された雄では精巣間質細胞腫瘍、腺腫、および前立腺腺癌の発生率が増加し、210 mg/kg を投与された雄では前立腺平滑筋芽腫の発生率が増加しました。
9~242 mg/kg (ヒトの AUC の 0.3~32 倍) を投与されたラットでは、顆粒膜細胞由来の良性および悪性卵巣腫瘍および上皮細胞由来の良性腫瘍の発生率が増加しました。これらの研究におけるメスのげっ歯類は、卵巣が活動的でホルモン刺激に非常に反応しやすい生殖周期中に治療されました。この齧歯動物モデルの非常に反応性の高い卵巣とは異なり、閉経後のヒト卵巣は生殖ホルモン刺激に対して比較的反応性が低い。
ラロキシフェンは、日常的な従来のin vivoまたはin vitro試験系のいずれにおいても遺伝毒性を示さなかった。
交尾前および交尾中にラロキシフェン(?5 mg/kg)を雄および雌のラットに投与した場合、妊娠は起こらなかった。雌ラットでは、ラロキシフェンを 0.1 ~ 10 mg/kg/日の用量で投与すると、治療中に発情周期が中断されましたが、治療終了後も、産子の数がわずかに減少したにもかかわらず、繁殖可能な交配は遅れませんでした。妊娠期間と新生児の発育時間の変化。
交配した雌ラットの着床前期間中の治療は、胚の着床を遅延および/または中断し、その結果、妊娠期間が延長し、産子数が減少しましたが、離乳までの産子発育には影響がありませんでした。これらの生殖効果は、塩酸ラロキシフェン (活性物質) の薬理学的プロファイルと一致しています。
催奇形性の研究はウサギとラットで行われました。ウサギでは、流産、低率の心室中隔欠損症 (? 0.1 mg/kg) および水頭症 (? 10 mg/kg) が観察されました。
ラットでは、胎児の発育に遅れがあり、腎臓の壁および空洞に変化が見られました (? 1 mg/Kg)。
塩酸ラロキシフェン (活性物質) は、ラットの子宮における強力な抗エストロゲン剤であり、雌のマウスおよびラットにおけるエストロゲン依存性の乳腫瘍の増殖を防止しました。
妊娠中および授乳中の使用
ラロキシフェン塩酸塩(活性物質)は、妊娠の可能性のある女性は服用しないでください。塩酸ラロキシフェン(活性物質)を妊婦に投与すると、胎児に害を及ぼす可能性があります。この薬を妊娠中に使用する場合、または患者がこの薬の服用中に妊娠した場合は、胎児に悪影響を与える可能性があることを患者に通知する必要があります。
塩酸ラロキシフェン (有効物質) は、授乳中の女性には使用されるべきではありません。ラロキシフェンが母乳中に排泄されるかどうかは不明です。塩酸ラロキシフェン(有効成分)は、赤ちゃんの発育に影響を与える可能性があります。
小児用
18歳未満の患者に対する有効性と安全性は確立されていません。
男性の使用は推奨されません。
機械を運転および操作する能力への影響
塩酸ラロキシフェン (活性物質) は、機械の運転および操作能力にほとんど、またはまったく影響を与えません。
この薬はドーピングを引き起こす可能性があります。
この薬には乳糖が含まれています。したがって、乳糖不耐症の患者は注意して使用する必要があります。
ラロキシフェン塩酸塩の副作用 – Blanver
臨床研究データ
血管拡張はプラセボで治療された患者で一般的に観察され、塩酸ラロキシフェン(活性物質)で治療された患者では中程度に増加しました。臨床研究中に発生した副作用の大部分は軽度であり、治療を中止する必要はありませんでした。ラロキシフェンの主な有害事象とその頻度を次の 2 つの表に示します。
表 1. 少なくとも 6 か月間継続したプラセボ対照試験による、塩酸ラロキシフェン (活性物質) (60 mg/日) で治療された患者における静脈血栓塞栓症の頻度
|
臨床研究 |
頻度: ラロキシフェン塩酸塩 (有効成分) |
頻度: プラセボ |
|
閉経後の女性: 骨粗鬆症の治療と予防に関する臨床研究 |
患者 1,000 人あたり 3.05 人 – 年 (累積発生率 0.9%) |
0.81/1,000 患者 – 年 (累積発生率 0.2%) a |
|
閉経後の女性: 冠状動脈性心疾患または冠状動脈性イベントのリスク増加が記録されている |
3.88/1,000 患者 – 年 (累積発生率 2.0%) b |
2.70/1,000 患者 – 年 (累積発生率 1.4%) b |
曝露期間の中央値は 42 か月でした。
b暴露期間の中央値は 61 か月でした。
異常な反応 (gt; 0.1% lt; 1%)
静脈血栓塞栓症(VTE)には、深部静脈血栓症、肺塞栓症、網膜静脈血栓症が含まれます。他の静脈血栓塞栓症イベントも発生する可能性があります。
発売後に報告されたイベント
リンパ系および血液系の障害
異常な反応 (>1/1,000 および ~1/100):
血小板減少症a .
神経系障害
一般的な反応 (gt;1/100 および ?1/10):
片頭痛を含む頭痛。
異常な反応 (>1/1,000 および ~1/100):
致命的な脳卒中。
血管障害
非常に一般的な反応 (gt;1/10):
血管拡張(ほてり)。
異常な反応 (>1/1,000 および ~1/100):
深部静脈血栓症、肺塞栓症、網膜静脈血栓症、表在静脈血栓静脈炎、動脈血栓塞栓反応などの静脈血栓塞栓イベント(VTE)。
胃腸障害
非常に一般的な反応 (>1/10):
吐き気、嘔吐、腹痛、消化不良などの消化器症状。
皮下組織および皮膚の疾患
一般的な反応 (gt;1/100 および ?1/10):
皮膚の発疹
結合組織および筋骨格系疾患
一般的な反応 (gt;1/100 および ?1/10):
足がけいれんする。
乳房および生殖器系の疾患
非常に一般的な反応 (>1/100 および ~1/10):
痛み、腫れ、圧痛などの軽度の乳房症状。
一般的な疾患と投与部位の状態
非常に一般的な反応 (>1/10):
インフルエンザ症候群。
一般的な反応 (gt;1/100 および ?1/10):
末梢浮腫。
調査
非常に一般的な反応 (>1/10):
血圧の上昇
a市販後の経験に基づいて含まれる用語。
ラロキシフェン塩酸塩の薬物相互作用 – Blanver
塩酸ラロキシフェン (活性物質) は、 in vitro でワルファリン、フェニトイン、タモキシフェンと相互作用しません。ラロキシフェン塩酸塩 (活性物質) とワルファリンを併用しても、どちらの薬剤の薬物動態も変化しません。ただし、プロトロンビン時間のわずかな減少が観察されました。したがって、塩酸ラロキシフェン(活性物質)をワルファリンまたは他のクマリン誘導体と一緒に投与する場合は、プロトロンビン時間を監視する必要があります。すでにクマリン系抗凝固薬による治療を受けている患者では、プロトロンビン時間に対する影響は、塩酸ラロキシフェン(活性物質)による治療開始から数週間後に現れることがあります。
塩酸ラロキシフェン (活性物質) は、塩酸ラロキシフェン (活性物質) の吸収と腸肝サイクルを大幅に低下させる陰イオン交換樹脂であるコレスチラミンと一緒に投与しないでください。具体的には研究されていませんが、他の陰イオン交換樹脂でも同様の効果があることが予想されます。
塩酸ラロキシフェン(活性物質)は、ジゴキシンの薬物動態に影響を与えません。塩酸ラロキシフェン(活性物質)の全身分布は、炭酸カルシウムと水酸化アルミニウムまたは水酸化マグネシウムを含む制酸薬の同時投与によって影響を受けません。アンピシリンを併用すると、塩酸ラロキシフェン(活性物質)の最大濃度が低下します。塩酸ラロキシフェン(活性物質)の全体的な吸収と排泄には影響がないため、塩酸ラロキシフェン(活性物質)はアンピシリンと併用して投与できます。
塩酸ラロキシフェン(活性物質)の慢性投与は、単回投与で与えられるメチルプレドニゾロンの薬物動態に影響を与えません。
他の薬剤の併用投与が塩酸ラロキシフェン(活性物質)の血漿濃度に及ぼす影響は、予防および治療の研究において評価されました。頻繁に併用投与される薬剤には、アセトアミノフェン、非ステロイド性抗炎症薬 (アスピリン、イブプロフェン、ナプロキセンなど)、経口抗生物質、H1 および H2 アンタゴニスト、ベンゾジアゼピンなどが含まれます。これらの薬剤の併用によるラロキシフェンの血漿濃度に対する臨床的に関連する影響は確認されませんでした。
臨床研究プログラムでは、エストロゲン様膣製剤の併用が一般的でした。相互作用は認められず、プラセボと比較して、塩酸ラロキシフェン(活性物質)で治療された患者における使用の増加はありませんでした。
塩酸ラロキシフェン(活性物質)による治療中に、一般に次の血清変化が観察されます:コレステロールの HDL-2 サブフラクションとアポリポタンパク質 A1 の増加、総コレステロール、LDL コレステロール、フィブリノーゲン、アポリポタンパク質 B、およびリポタンパク質の減少 (a)。塩酸ラロキシフェン(活性物質)は、性ステロイド結合グロブリン(SHBG)、チロキシン結合グロブリン、コルチコステロイド結合グロブリンなどのグロブリンに結合するホルモンの濃度をわずかに増加させ、それに対応して総ホルモン濃度も増加します。これらの変化は、対応する遊離ホルモンの濃度には影響しません。
塩酸ラロキシフェン(活性物質)と漢方薬、ニコチン、アルコール、臨床検査および非臨床検査の間の可能性のある相互作用を調査する目的で臨床研究は行われていません。
ラロキシフェン塩酸塩の食品との相互作用 – Blanver
ラロキシフェン塩酸塩 (活性物質) と食品の間には相互作用はありません。そのため、食事に関係なく投与することができます。
物質の作用 ラロキシフェン塩酸塩 – Blanver
有効性の結果
骨格への影響
閉経期に起こるエストロゲンの利用可能量の減少は、骨吸収の顕著な増加、骨量の減少、および骨折のリスクを引き起こします。骨量の減少は、閉経後の最初の 10 年間に特に急速に起こります。この時期には、骨形成の代償的な増加が吸収による損失を回復するのに十分ではありません。骨粗鬆症を引き起こす可能性のあるその他の危険因子には、早期閉経、骨減少症(ピーク骨量より少なくとも 1 標準偏差を下回る)、低体重、白人またはアジア人の民族的起源、骨粗鬆症の家族歴などがあります。通常、置換治療により過剰な骨吸収が解消されます。閉経後の女性において、塩酸ラロキシフェン(活性物質)は骨折の発生率を減らし、骨量を維持し、骨密度(BMD)を増加させます。
骨折の発生率
塩酸ラロキシフェン(活性物質)は、骨粗鬆症の閉経後女性(初期椎骨骨折の有無にかかわらず)における椎骨骨折の発生率を減少させました。平均年齢66歳で、骨粗鬆症または骨粗鬆症で既に椎骨骨折を患っている7,705人の閉経後女性を対象とした研究では、塩酸ラロキシフェン(活性物質)による3年間の治療により、椎骨骨折の発生率が47%減少しました[相対リスク] (RR) 0.53;信頼区間 (CI) 0.35-0.79; plt;0.001]および31% (RR 0.69; CI 0.56-0.86; plt;0.001)。
骨粗鬆症の女性 45 人、または骨折が存在する骨粗鬆症の女性 15 人は、1 つ以上の椎骨骨折を予防するために塩酸ラロキシフェン (活性物質) で 3 年間治療する必要があります。塩酸ラロキシフェン(活性物質)による4年間の治療により、骨粗鬆症患者または骨折患者の椎骨骨折の発生率がそれぞれ46%(RR 0.54; CI 0.38-0.75)および32%(RR 0.68; CI 0.56-0.83)減少しました。 4 年目だけで、塩酸ラロキシフェン (有効物質) は新たな椎骨骨折のリスクを 39% 減少させました (RR 0.61; CI 0.43-0.88)。 4 年目には、ビスホスホネート、カルシトニン、フッ化物の併用が患者に許可されました。非脊椎骨折に対する効果は実証されていません。この研究のすべての患者は、カルシウムとビタミンDのサプリメントを受けました。
統計的に有意ではありませんが、非脊椎骨折の発生率は、プラセボと比較して、塩酸ラロキシフェン(活性物質)への曝露期間が増加するにつれて減少しました。
骨塩密度 (BMD)
子宮の有無にかかわらず、60歳までの閉経後女性に毎日投与される塩酸ラロキシフェン(活性物質)の有効性は、予防研究では24か月、治療研究では36か月の治療期間にわたって確立されました。これらの女性は 2 ~ 8 年間閉経していました。塩酸ラロキシフェン (活性物質) またはプラセボを投与された 1,764 人の閉経後の女性を対象に、3 つの臨床研究が実施されました。研究の1つでは、女性は以前に子宮摘出術を受けていた。塩酸ラロキシフェン(活性物質)は、プラセボと比較して、股関節、脊椎および全身の骨密度を大幅に増加させました。
臨床研究では、すべての被験者にビタミン D の有無にかかわらずカルシウムの補給を受けました。この BMD の増加は、プラセボと比較して一般に 2% でした。同様の BMD の増加が治療集団でも観察されました。予防研究において、塩酸ラロキシフェン(活性物質)治療中に骨密度の増加または減少を経験した女性の割合は次のとおりでした。脊椎では37%の減少、63%の増加が見られました。股関節では 29% 減少し、71% 増加しました。
カルシウムの薬物動態
塩酸ラロキシフェン (活性物質) とエストロゲンは、同様に骨のリモデリングとカルシウム代謝に影響を与えます。塩酸ラロキシフェン(活性物質)は、主に尿中カルシウム損失の減少により、骨再吸収の減少と 60 mg/日のプラスのカルシウムバランスに関連しています。
骨リモデリングマーカー
塩酸ラロキシフェン(活性物質)は、骨の吸収と形成の生化学マーカーによって証明されるように、骨のリモデリング速度を減少させました。
組織形態計測 (骨の質)
塩酸ラロキシフェン(活性物質)で治療された患者の骨は組織学的に正常で、石灰化欠陥、組織化されていない骨、または髄線維症の証拠はありませんでした。これらの発見は、塩酸ラロキシフェン (活性物質) の骨に対する主な作用機序が骨吸収の阻害であることを一貫して示しています。
脂質代謝と心血管リスクへの影響
臨床研究では、塩酸ラロキシフェン (活性物質) を 1 日あたり 60 mg 摂取すると、総コレステロール (3 ~ 6%) と LDL コレステロール (4 ~ 10%) が大幅に減少することが示されています。ベースラインのコレステロール濃度が最も高い女性の減少が最も大きかった。 HDL コレステロールとトリグリセリドの濃度は大きく変化しませんでした。
塩酸ラロキシフェン (活性物質) は、血清 HDL-2 コレステロール サブフラクションを有意に増加させ、血清フィブリノーゲン (塩酸ラロキシフェン (活性物質) による 3 年間の治療後 6.71%) とリポタンパク質 (a) を有意に減少させました。骨粗鬆症治療研究では、塩酸ラロキシフェン(活性物質)による治療で、プラセボと比較して、脂質低下療法の開始を必要とする患者の数が大幅に減少しました。
塩酸ラロキシフェン(活性物質)による 8 年間の治療は、骨粗鬆症治療研究に参加した患者の心血管イベントのリスクに大きな影響を与えませんでした。
塩酸ラロキシフェン(活性物質)による治療中に観察された静脈血栓塞栓エピソードの相対リスクは、プラセボと比較して1.60(CI 0.95-2.71)、エストロゲンまたはホルモン補充療法と比較して1.0(CI 0.3-6.2)でした。血栓塞栓性イベントのリスクは、治療開始から最初の 4 か月間で最も高くなりました。
子宮内膜と骨盤底への影響
臨床研究では、塩酸ラロキシフェン(活性物質)は閉経後の女性の子宮内膜を刺激しませんでした。プラセボと比較して、塩酸ラロキシフェンは子宮/膣部の出血や出血、または子宮内膜がんのリスク増加との関連はありませんでした。 831人の女性に対して異なる用量で約3,000回の経膣超音波検査を実施し、評価したところ、塩酸ラロキシフェン(活性物質)で治療した女性とプラセボで治療した女性の子宮内膜の厚さには差がないことが観察されました。
3年間の治療後、60 mg/日の塩酸ラロキシフェン(活性物質)で治療を受けた211人の女性のうち1.9%で、経膣超音波を使用して5 mm以上の子宮内膜厚さの増加が観察されました。 219人の女性がプラセボを受けています。また、塩酸ラロキシフェン(活性物質)またはプラセボで治療したグループ間で子宮出血の発生率に差はありませんでした。
塩酸ラロキシフェン(活性物質)60mg/日による6ヶ月の治療後に子宮内膜生検を行ったところ、どの患者にも子宮内膜増殖が発生していないことが証明された。さらに、1日推奨用量の2.5倍の塩酸ラロキシフェン(活性物質)を投与した研究では、子宮内膜の増殖も子宮体積の増加も観察されませんでした。
骨粗鬆症治療研究では、研究対象集団の一部(患者 1,644 人)を対象に子宮内膜の厚さが 4 年間にわたって毎年評価されました。ラロキシフェン塩酸塩(活性物質)で治療を受けた女性の子宮内膜厚さの測定値は、4年間の治療後の最初の測定値と変わりませんでした。塩酸ラロキシフェン(活性物質)で治療された女性とプラセボで治療された女性の間には、出血や膣分泌物の発生率に差はありませんでした。
塩酸ラロキシフェン(活性物質)で治療を受けた女性の数は、子宮脱に外科的介入を必要としたプラセボで治療された女性よりも少なかった。塩酸ラロキシフェン(活性物質)による 3 年間の治療後の安全性情報は、塩酸ラロキシフェン(活性物質)による治療は骨盤底手術後の弛緩を増加させないことを示唆しています。
4 年後、塩酸ラロキシフェン (活性物質) は子宮内膜がんまたは卵巣がんのリスクを増加させませんでした。塩酸ラロキシフェン(活性物質)による治療を4年間受けた閉経後の女性では、良性の子宮内膜ポリープが0.9%で報告されたのに対し、プラセボを受けた女性では0.3%でした。
乳房組織への影響
塩酸ラロキシフェン (活性物質) は、乳房組織に対して増殖作用を持ちません。すべてのプラセボ対照研究の中で、塩酸ラロキシフェン(活性物質)は、乳房症状(乳房の腫れ、圧痛、痛みがない)の頻度と重症度に関してプラセボと区別がつきませんでした。臨床研究では、ラロキシフェン治療により浸潤性乳がんの発生率の減少が観察されました。
4年間の骨粗鬆症治療研究(7,705人の患者が参加)を通じて、塩酸ラロキシフェン(活性物質)による治療は、プラセボと比較して、乳がんの全体的なリスクを62%減少させました(RR 0.38; CI 0.21-0.69)。浸潤性乳がんのリスクが71%(RR 0.29; CI 0.13~0.58)、エストロゲン受容体(ER)陽性浸潤性乳がんのリスクが79%(RR 0.21; CI 0.07~0.50)低下しました。塩酸ラロキシフェン(活性物質)は、ER 陰性乳がんのリスクに影響を与えません。これらの観察は、塩酸ラロキシフェン (活性物質) が乳房組織において固有のエストロゲン アゴニスト活性を持たないという結論を裏付けています。
認知機能への影響
認知機能に対する有害事象は観察されませんでした。
薬理学的特性
説明
塩酸ラロキシフェン(活性物質)は、選択的エストロゲン受容体調節物質(SERM)として作用するベンゾチオフェン誘導体です。
薬力学特性
選択的エストロゲン受容体調節因子(SERM)として、ラロキシフェンは、エストロゲンに反応する組織に対して選択的なアゴニストまたはアンタゴニスト活性を持ちます。骨およびコレステロール代謝(総コレステロールおよびLDLコレステロールを低下させる)に対してアゴニストとして作用しますが、子宮および乳房組織に対してはアンタゴニストとして作用します。
エストロゲンと同様に、ラロキシフェンの生物学的効果は、エストロゲン受容体への高親和性結合と遺伝子発現の制御によって媒介されます。この結合により、異なる組織における複数のエストロゲン調節遺伝子の発現差が引き起こされます。データは、エストロゲン受容体が組織リガンドおよび/または遺伝子特異的な少なくとも 2 つの異なる経路を通じて遺伝子発現を調節できることを示唆しています。
薬物動態学的特性
吸収
ラロキシフェンは経口投与後、急速に吸収されます。経口投与量の約 60% が吸収されます。絶対的なバイオアベイラビリティは 2% です。全身性グルクロン酸抱合は広く普及しています。最大の血漿濃度と生物学的利用能に達するまでの時間は、ラロキシフェンとそのグルクロン酸代謝物の全身性相互変換と腸肝サイクルによって異なります。
分布
ラロキシフェンは体内に広く分布しています。分布量は用量に依存しません。ラロキシフェンとモノグルクロニドの複合体は、アルブミンとα-1 酸性糖タンパク質の両方を含む血漿タンパク質と高度に結合します (98 ~ 99%)。
代謝
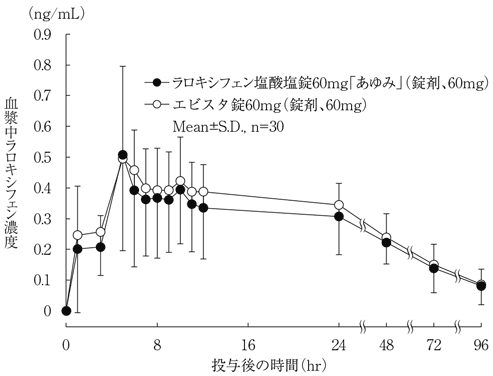
ラロキシフェンは、グルクロニド複合体(ラロキシフェン-4′-グルクロニド、ラロキシフェン-6-グルクロニド、およびラロキシフェン-6-4′-ジグルクロニド)の形成により広範な初回通過肝臓代謝を受けます。他の代謝物は検出されませんでした。ラロキシフェンとそのグルクロニド複合体は、可逆的な全身代謝と腸肝サイクルを通じて相互変換可能であり、経口投与後、半減期が 27.7 時間に延長されます。
ラロキシフェン塩酸塩 (活性物質) に含まれるラロキシフェンとそのグルクロン酸代謝物の濃度の合計は 1% 未満です。ラロキシフェン塩酸塩(活性物質)の単回経口投与の結果は、複数回投与の薬物動態を予測します。塩酸ラロキシフェン (活性物質) の用量が増加すると、血漿濃度 x 時間曲線 (AUC) の下の面積の比例増加がわずかに小さくなります。
排泄
ラロキシフェンとそのグルクロン酸代謝産物の投与量の大部分は、その後 5 日以内に主に糞便中に排泄されます。グルクロニド結合体として尿中に排泄されるのは用量の 6% 未満です。
特殊な状況
腎不全
総投与量の 6% 未満が尿中に排出されます。薬物動態研究では、除脂肪体重で調整したクレアチニンクリアランスの 47% 減少が観察され、その結果、ラロキシフェンクリアランスが 17% 減少し、ラロキシフェン複合体のクリアランスが 15% 減少しました。
肝不全
塩酸ラロキシフェン(活性物質)は、総血清ビリルビンが 0.6 ~ 2.0 mg/dL の肝硬変患者を対象に単回投与として研究されました。ラロキシフェンの血漿濃度は対照より約 2.5 倍高く、ビリルビン濃度と相関していました。肝障害患者における安全性と有効性は評価されていません。








-1024x576.jpg?resize=1024,576&ssl=1)


