具体的な適応症については、国の推奨事項をご確認ください。
FluQuadri はどのように機能しますか?
FluQuadri ® は免疫系を刺激して、インフルエンザからの防御に役立つ抗体を生成しますが、FluQuadri ®によるワクチン接種は、ワクチン接種を受けたすべての人を防御できるわけではありません。
ワクチン接種後1年間は免疫力が低下し、流行しているインフルエンザウイルスの株は年ごとに変化するため、最新のワクチンを毎年接種することが推奨されます。
FluQuadri の禁忌
以下の場合は、FluQuadri ® の投与を受けるべきではありません。
- ワクチンの成分(卵または卵を含む製品など)に対して重篤なアレルギー反応を起こしたことはありますか。
- インフルエンザワクチン接種後に重度のアレルギー反応を起こしたことがありますか。
- 彼は生後6か月未満です。
この薬は生後6か月未満の小児には禁忌です。
FluQuadri の使用方法
FluQuadri ® は、成人および生後 36 か月以上の小児に対して腕の筋肉に投与する必要があります。
生後12か月から35か月までのお子様向け
FluQuadri ® は、大腿筋 (筋肉量が十分であれば腕の筋肉) に投与する必要があります。
生後6ヶ月から11ヶ月のお子様向け
FluQuadri ® は大腿筋に投与する必要があります。
FluQuadri の投与量
インフルエンザウイルスの種類とワクチンによってもたらされる免疫の持続期間のため、熱帯諸国ではリスク期間の初めまたは前に、毎年インフルエンザワクチン接種を実施することが推奨されます。
生後6か月から35か月までのお子様(生後6か月を含む)
0.25 mL を少なくとも 4 週間の間隔で 2 回投与します。これらの小児が以前にワクチン接種を受けている場合は、0.25 mL の単回投与が推奨されます。
生後36か月から8歳までのお子様(含む)
0.5 mL を少なくとも 4 週間の間隔で 2 回投与します。これらの小児が以前にワクチン接種を受けている場合は、0.5 mL の単回投与が推奨されます。
大人と9歳以上の子供
1回量0.5mL。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中断しないでください。
FluQuadri の使用を忘れた場合はどうすればよいですか?
過去数年間にインフルエンザワクチン接種を受けていない生後6ヵ月から35ヵ月の間および生後36ヵ月から8歳の間の子供にFluQuadri ®を投与する特定のケースでは、0.25mLを2回投与するか、0.25mLを2回投与することが推奨されます。 .5mLを年齢層ごとに1か月間隔で投与します。
2回目のワクチン接種が行われない場合、反応が低下する可能性があります。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
FluQuadri の予防措置
あなたまたはあなたの子供が以下の症状に罹患しているか、または罹患している場合は、医療専門家に伝えてください。
- インフルエンザワクチン接種後のギラン・バレー症候群(重度の筋力低下)。
- 免疫反応が低下する可能性があるため、免疫系に問題が発生します。
- ホルムアルデヒドやオクチルフェノールエトキシレートなどのワクチン成分に対するアレルギー反応。
FluQuadri ® を免疫抑制療法を受けている人を含む免疫不全の人に投与した場合、期待される免疫反応が得られない可能性があります。
発熱の有無にかかわらず、中等度または重度の急性疾患の場合は、ワクチン接種を延期する必要があります。
針注射に対する反応として、ワクチン接種後またはワクチン接種前でも失神が起こることがあります。
専用バイアル
チメロサールは、いくつかの複数回投与ワクチンで防腐剤として使用されています。 FluQuadri ® multidose の組成にはこの防腐剤が含まれています。
FluQuadri の副作用
有害事象情報は、臨床研究および世界的な市販後の経験から得られます。
臨床研究の経験
臨床研究はさまざまな条件下で実施され、インフルエンザワクチンの組成は毎年変動するため、ワクチンの臨床研究で観察された副反応の発生率は、他のワクチンの臨床研究で観察された副作用の発生率と直接比較できず、反映されていない可能性があります。実際に観察された速度。 FluQuadri ®の安全性は、米国の 3 つの臨床試験の参加者 3,307 名(生後 6 ~ 35 か月の小児 1,223 名、3 ~ 8 歳の小児 1,669 名、18 歳以上の成人 190 名、65 歳以上の成人 225 名)を対象に評価されました。 2 回目の投与が必要な小児の場合、米国 ACIP ガイドラインに従って、約 4 週間の間隔をあけて投与されます。小児および成人におけるワクチン投与後の最も一般的な注射部位の反応は痛みでした。乳児および小児(生後6~35か月)で最も一般的な全身反応は過敏症で、小児(3~8歳)および成人で報告された最も一般的な全身反応は筋肉痛でした。
6か月から8歳までの参加者を対象とした研究では、FluQuadri ®グループでは16人(0.6%)の参加者が少なくとも1つの重篤な有害事象(SAE)を経験したが、ワクチン接種後28日間に死亡は発生せず、41人(1.4%)が死亡した。 ) 参加者は研究期間中に少なくとも 1 つの SAE を発症しました。
ワクチン接種後 6 か月以内に、FluQuadri ®ワクチン接種によって引き起こされたと考えられる重篤な有害事象が発生しました。生後 13 か月の乳児は、最初のワクチン接種から 3 日後に、主に吸気性の困難な呼吸器感染症であるクループを患いました。参加者は後遺症もなく18日以内に回復し、研究を続けた。
参加者の中にはワクチン接種に関連すると考えられる死亡者はいなかった。
18歳以上の成人参加者を対象とした研究の追跡期間中に、FluQuadri ®グループでSAEが1件発生しましたが、研究期間中に死亡は報告されませんでした。試験で報告された注射部位および全身反応の頻度を表 2 に示します。

表 2: FluQuadri ®ワクチン接種後の小児および成人における注射部位反応および全身性有害事象の割合
|
生後6か月から35か月までの赤ちゃんと子供 |
3歳から8歳までのお子様 |
大人 |
大人 |
|
|
注射部位の反応 |
||||
| 痛み |
57.0d |
66.6 | 47.4 | 32.6 |
| 感度 |
54.1 と |
– | – | – |
| 紅斑 | 37.3 | 34.1 | 1.1 | 2.7 |
| 腫れ | 21.6 | 24.8 | 0.5 | 1.8 |
| 硬化 | – | – | 0.5 | – |
|
紫色のスポットオン 注射部位 |
– | – | 0.5 | – |
|
全身反応 |
||||
| 筋肉痛 |
26.7日 |
38.6 | 23.7 | 18.3 |
| 頭痛 |
8.9d |
23.1 | 15.8 | 13.4 |
| 気質 |
38.1d |
31.9 | 10.5 | 10.7 |
| イライラ |
54.0 と |
– | – | – |
| 異常な泣き声 |
41.2 と |
– | – | – |
| めまい |
37.7 と |
– | – | – |
| 食欲不振 |
32.3 と |
– | – | – |
| 嘔吐 |
14.8 と |
– | – | – |
| 寒気 | – | – | 2.6 | – |
| 熱 | 14.3 | 7.0 | 0.0 | 1.3 |
aワクチン接種後 0 日目から 7 日目までに収集された注射部位と全身反応。
bワクチン接種後 0 日目から 3 日目までに収集された注射部位および全身反応。
cセキュリティレビューグループの参加者数。
d生後 24 ~ 35 か月の小児を対象に評価されます。
生後6か月から23か月の小児を対象に評価されます。
市販後の経験
現在、FluQuadri ®の市販後データは限られています。三価 (断片化および不活化) インフルエンザ ワクチンである Fluzone の承認後の使用中に、以下の追加の事象が自然発生的に報告されました。これらの事象は規模が未知の集団から自発的に報告されるため、頻度を推定したり、ワクチン曝露との因果関係を確立したりすることが常に可能であるとは限りません。
有害事象は、以下の要因の 1 つ以上に基づいて含まれています。
重症度、報告の頻度、または Fluzone との因果関係の証拠の程度。
血液およびリンパ系の障害
血小板減少症、リンパ節腫脹。
免疫系疾患
アナフィラキシー、その他のアレルギー反応または過敏症反応(蕁麻疹、血管浮腫を含む)。
目の病気
眼充血。
神経系疾患
ギラン・バレー症候群(GBS)、けいれん、熱性けいれん、脊髄炎(脳脊髄炎および横性脊髄炎を含む)、顔面麻痺(ベル麻痺)、視神経炎/神経障害、腕神経炎、失神(ワクチン接種直後)、めまい、感覚異常。
血管障害
血管炎、血管拡張/紅潮。
呼吸器、胸部、縦隔の疾患
呼吸困難、咽頭炎、鼻炎、咳、喘鳴(呼吸困難による喘鳴)、喉の圧迫感。
皮膚および皮下組織の疾患

スティーブンス・ジョンソン症候群。
一般的な病気と投与場所の状況
かゆみ、無力感・倦怠感、四肢の痛み、胸痛。
胃腸障害
嘔吐。
注意:
この製品は新薬であり、研究により許容できる有効性と安全性が示されていますが、たとえ正しく指示され使用されたとしても、予測できないまたは未知の有害事象が発生する可能性があります。この場合は医師または歯科医師に知らせてください。
また、適切なフォローアップのために、ワクチン接種情報サービス (SIV) に電話して会社に通知してください。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
FluQuadri 特別集団
妊娠と授乳
FluQuadri®を使用した動物の生殖研究は行われていません。 FluQuadri ® を妊婦に投与した場合に胎児に害を及ぼす可能性があるかどうか、あるいは生殖能力に影響を与える可能性があるかどうかも不明です。 FluQuadri ® は、明確な必要性があり、医療専門家によるリスクと利点の評価後にのみ妊婦に投与されるべきです。
このワクチンは医師のアドバイスなしに妊婦には使用しないでください。
FluQuadri ® が母乳中に排泄されるかどうかは不明です。いくつかの薬剤は母乳中に排泄されるため、授乳中の女性に FluQuadri ®を投与する決定は、潜在的なリスクと利点を慎重に考慮して決定する必要があります。
お年寄り
FluQuadri ®に対する抗体反応は、65 歳以上の人々では若い成人と比較して低くなります。
FluQuadri の構成
1回分の0.25mLには次のものが含まれます。
|
A/H1N1 |
7.5μgのHA |
|
A/H3N2 |
7.5μgのHA |
|
B/ |
7.5μgのHA |
|
B/ |
7.5μgのHA |
1回分の0.5mL中に次の成分が含まれています。
|
A/H1N1 |
15μgのHA |
|
A/H3N2 |
15μgのHA |
|
B/ |
15μgのHA |
|
B/ |
15μgのHA |
FluQuadri ® は、世界保健機関 (WHO) の要件および 2019 年南半球キャンペーンに関するブラジルの法律に従って標準化されており、0.5 mL の用量あたり 60 マイクログラム (mcg) の血球凝集素 (HA) を含むように配合されています。 2019 年のキャンペーンでは 4 つの株のそれぞれに 15 mcg の HA が含まれ、0.25 mL の用量あたり 30 mcg の HA が含まれ、2019 年のキャンペーンでは 4 つの株のそれぞれに平均 7.5 mcg の HA が含まれます。

FluQuadri ® は、発育鶏卵で増殖したインフルエンザ ウイルスから調製された、筋肉内注射用の不活化インフルエンザ ウイルスの水性懸濁液です。
FluQuadri ®の定性的および定量的な構成を以下に示します。
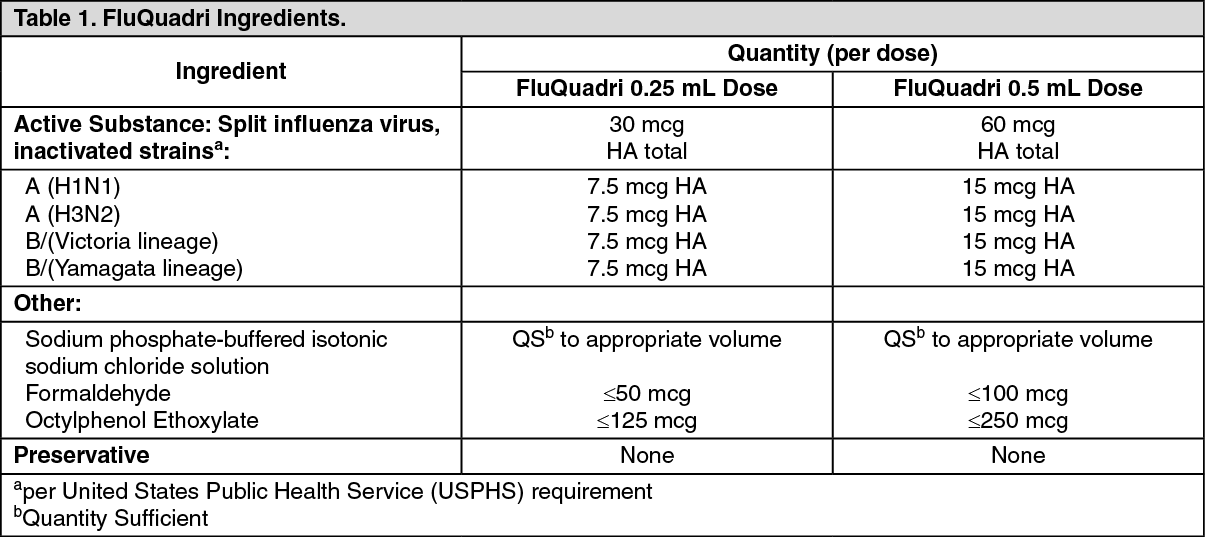
表 1: FluQuadri ®コンポーネント – 1 回分の 0.25 mL および 0.5 mL を含む 5 つのプレフィルドシリンジを備えたカートリッジ
|
成分 |
定量的(投与量あたり) |
定量的(投与量あたり) |
|
|
0.25mLの用量 |
0.5mLの用量 |
||
|
断片化され不活化されたインフルエンザウイルス株 |
合計 30 mcg の HA | 合計 60 mcg の HA |
活性物質 |
|
A/ミシガン/45/2015 (H1N1)pdm09 類似株 (A/ミシガン/45/2015 X-275 (H1N1)) |
7.5mcg HA | 15mcg HA |
活性物質 |
|
A/スイス/8060/2017 (H3N2) – 類似株 (A/ブリスベン/2018/1、NYMC X-311) |
7.5mcg HA | 15mcg HA |
活性物質 |
|
B/プーケット/3073/2013 (B/山形/16/88 系統) – 類似株 (B/プーケット/3073/2013 (B/山形系統) |
7.5mcg HA | 15mcg HA |
活性物質 |
|
B/コロラド/06/2017 (系統 B/ビクトリア/2/87) – 類似株 (B/メリーランド/15/2016 BX-69A) |
7.5mcg HA | 15mcg HA |
活性物質 |
|
その他 |
|||
|
塩化ナトリウム-リン酸ナトリウムの等張緩衝液 |
qsp b 適切な量 |
qsp b 適切な量 |
希釈剤 |
|
ホルムアルデヒド |
?50μg | ?100μg |
賦形剤 |
|
オクチルフェノールエトキシレート (Triton X ® -100) |
?125μg | ?250μg |
賦形剤 |
a世界保健機関 (WHO) の推奨による。
bに十分な量。
このワクチンにはアジュバントは使用されていません。
FluQuadri ®ワクチンの単回投与シリンジの製造プロセスでは、チオメルサールまたはゼラチンは使用されませんでした。
FluQuadri ®プレゼンテーションでは天然ゴムラテックスを使用しません。
表 2: FluQuadri ®コンポーネント – 5 mL バイアルを含むカートリッジ
|
成分 |
定量的(投与量あたり) |
定量的(投与量あたり) |
|
|
0.25mLの用量 |
0.5mLの用量 |
||
|
断片化され不活化されたインフルエンザウイルス株 |
合計 30 mcg の HA | 合計 60 mcg の HA |
活性物質 |
|
A/ミシガン/45/2015 (H1N1)pdm09 類似株 (A/ミシガン/45/2015 X-275 (H1N1)) |
7.5mcg HA | 15mcg HA |
活性物質 |
|
A/スイス/8060/2017 (H3N2) – 類似株 (A/ブリスベン/2018/1、NYMC X-311) |
7.5mcg HA | 15mcg HA |
活性物質 |
|
B/プーケット/3073/2013 (B/山形/16/88 系統) – 類似株 (B/プーケット/3073/2013 (B/山形系統) |
7.5mcg HA | 15mcg HA |
活性物質 |
|
B/コロラド/06/2017 (系統 B/ビクトリア/2/87) – 類似株 (B/メリーランド/15/2016 BX-69A) |
7.5mcg HA | 15mcg HA |
活性物質 |
|
その他 |
|||
|
塩化ナトリウム-リン酸ナトリウムの等張緩衝液 |
qsp b 適切な量 |
qsp b 適切な量 |
希釈剤 |
|
チメロサール |
0.01% w/v (12.5 水銀μg) |
0.01% w/v (水銀 25 mcg) |
防腐剤 |
|
ホルムアルデヒド |
?50μg | ?100μg |
賦形剤 |
|
オクチルフェノールエトキシレート (Triton X ® -100) |
?125μg | ?250μg |
賦形剤 |
a世界保健機関 (WHO) の推奨による。
bに十分な量。
このワクチンにはアジュバントは使用されていません。
FluQuadri ®にはゼラチンは含まれません。
FluQuadri ®プレゼンテーションでは天然ゴムラテックスを使用しません。
FluQuadri のプレゼンテーション
注射用懸濁液
それぞれ0.25mLの1回分を含む5つのプレフィルドシリンジを備えたカートリッジ;それぞれ0.5mLの1回分を含むプレフィルドシリンジ5本が入ったカートリッジ。
FluQuadri ® – 四価インフルエンザ ワクチン (断片化、不活化) は筋肉内に投与する必要があります。
成人および生後6か月以上の小児にご使用ください。
バイアル
5 mL バイアルが入ったカートリッジ。
FluQuadri ® – 四価インフルエンザ ワクチン (断片化、不活化) は筋肉内に投与する必要があります。
生後24か月以上の成人および小児が使用できます。
フルクアドリの過剰摂取
このテーマに関する具体的な研究は行われていません。ただし、過剰摂取の場合は、適切な監視のためにワクチン接種情報サービス (SIV) に連絡することをお勧めします。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
FluQuadri の薬物相互作用
FluQuadri ®と他のワクチンの併用を評価する利用可能なデータはありません。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
FluQuadri という物質の作用
有効性の結果
生後6~35か月の小児に対する有効性
四価インフルエンザワクチン(断片化、不活化)(活性物質)の有効性は、2011年からの季節期間中に実施された臨床研究D-QIV-004において、無作為化、盲検観察者、対照群に非インフルエンザワクチンを接種して評価されました。生後6ヵ月から35ヵ月までの健康な個人を、4価インフルエンザワクチン(断片化、不活化)(活性物質)(N = 6006)または非インフルエンザ対照ワクチン(N = 6012)を受ける群に無作為(1:1)に割り付けた。個人は、約 28 日の間隔で 1 回接種 (以前のインフルエンザワクチン接種の場合) または 2 回接種を受けました。
四価インフルエンザ ワクチン (断片化、不活化) (活性物質) の有効性は、次の原因によるインフルエンザ A および/または B (中等度から重度、およびあらゆる重症度) の予防について、逆転写ポリメラーゼ連鎖反応 (RT/PCR) を使用して評価されました。季節性インフルエンザのあらゆる株。この研究は、ワクチン接種後 2 週間からインフルエンザの季節の終わりまで (ワクチン接種後約 6 か月後) に開始され、インフルエンザ様事象の後に鼻腔スワブが採取され、RT によってインフルエンザ A および/または B について検査されました。 PCR。 RT-PCR 陽性のすべての検体は、細胞培養での生存率についてさらに検査され、ウイルス株がワクチン内のウイルス株と一致するかどうかが判定されました。
四価インフルエンザワクチン (断片化、不活化) (活性物質) は、表 1 に示す一次および二次有効性目標の事前に定義された基準を満たしました。
表 1: 四価インフルエンザ ワクチン (断片化、不活化) (活性物質): 生後 6 ~ 35 か月の小児における発病率とワクチンの有効性 (プロトコール (ATP) 有効性コホート – 発症時間による)
|
4価インフルエンザワクチン(断片化・不活化)(原体) |
アクティブコンパレータ1 |
ワクチンの有効性 |
||||||
|
N2 |
n3 |
攻撃率 (n/N) |
N2 |
n3 |
攻撃率 (n/N) (%) |
% |
IC |
|
|
重症度6のインフルエンザ |
||||||||
|
RT-PCR確認済み |
5707 | 344 | 6.03 | 5697 | 662 | 11.62 | 49.8 |
41.8; 56.8 4 |
|
文化が確認された |
5707 | 303 | 5.31 | 5697 | 602 | 10.57 | 51.2 |
44.1; 57.6 5 |
|
ワクチンに相当する菌株を培養で確認 |
5707 | 88 | 1.54 | 5697 |
216 |
3.79 | 60.1 |
49.1; 69.0 5 |
|
中等度から重度のインフルエンザ7 |
||||||||
|
RT-PCR確認済み |
5707 | 90 | 1.58 | 5697 | 242 | 4.25 | 63.2 |
51.8; 72.3 4 |
|
文化が確認された |
5707 | 79 | 1.38 | 5697 | 216 | 3.79 | 63.8 |
53.4; 72.2 5 |
|
ワクチンに相当する菌株を培養で確認 |
5707 | 20 | 0.35 | 5697 | 88 | 1.54 | 77.6 |
64.3; 86.6 5 |
|
RT-PCRで下気道疾患を確認 |
5707 | 28 | 0.49 | 5697 | 61 | 1.07 | 54.0 |
28.9; 71.0 5 |
|
RT-PCRで急性中耳炎を確認 |
5707 | 12 | 0.21 | 5697 | 28 | 0.49 | 56.6 |
16.7; 78.8 5 |
1小児は年齢に応じて非インフルエンザワクチン接種を受けました。
2 ATP(プロトコールコホートによる)有効性コホートに含まれる被験者の数 – 事象の発生時間。
このコホートには、適格基準を満たし、有効性を追跡調査し、エピソードが発生するまで研究プロトコールに従った個人が含まれていました。
3期間中に少なくとも 1 件の事象を報告した個人の数。
4両側 97.5% 信頼区間。
5両側 95% 信頼区間。
6重症度に関わらずインフルエンザ疾患は、インフルエンザ様疾患(インフルエンザ様疾患(ILI)、つまり咳、鼻水、鼻づまり、呼吸困難のいずれかの症状を伴う38℃以上の発熱)のエピソードとして定義されます。インフルエンザウイルス感染の結果[急性中耳炎(AOM)または下気道疾患(LRI)]。
7中等度から重度のインフルエンザは、以下のいずれかを伴うインフルエンザ疾患のサブセットであった: 39℃を超える発熱、医師の診断による急性中耳炎、医師の診断による下気道疾患、医師の診断による重篤な肺外合併症、集中治療室への入院、または8時間以上の酸素補給が必要です。
探索的分析は、12,018人を含むワクチン接種コホート全体に対して実施されました(四価インフルエンザワクチン(断片化、不活化)(活性物質)についてはN = 6006、対照についてはN = 6012)。
四価インフルエンザワクチン(断片化、不活化)(活性物質)は、ワクチン株のうちの 2 株(A/H3N2 および H3N2 および H3N2 とB/ビクトリア)。
表 2: 四価インフルエンザ ワクチン (断片化、不活化) (活性物質) – 6 ~ 35 か月の小児におけるインフルエンザ サブタイプ A およびインフルエンザ系統 B に対する RT-PCR によって確認された中等度から重度の疾患に対する攻撃率とワクチンの有効性 (ワクチン接種を受けたコホートの合計) )
|
4価インフルエンザワクチン(断片化・不活化)(原体) |
アクティブコンパレータ1 |
ワクチンの有効性 |
||||||
|
歪み |
N2 |
n3 |
攻撃率 (n/N) |
N2 |
n3 |
レート |
% |
IC |
|
ザ |
||||||||
|
H1N1 4 |
6006 | 13 | 0.22 | 6012 | 46 | 0.77 | 72.1 |
49.9; 85.5 |
|
H3N2 5 |
6006 | 53 | 0.22 | 6012 | 112 | 1.86 | 52.7 |
34.8; 66.1 |
|
B |
||||||||
|
ビクトリア6 |
6006 | 3 | 0.05 | 6012 | 15 | 0.25 | 80.1 |
39.7; 95.4 |
|
山形7 |
6006 | 22 | 0.05 | 6012 | 73 | 1.21 | 70.1 |
52.7; 81.9 |
1乳児は年齢に応じて非インフルエンザ対照ワクチンを受けました。
2ワクチン接種を受けたコホートの合計に含まれる個人の数。
3 4 から 7 の期間に少なくとも 1 件の事象を報告した人の数株と組み合わせた抗原比率は、A/H1N1、A/H3N2、B/ビクトリア、とB/山形。
さらに、RT-PCRによって確認された重症度の症例については、四価インフルエンザワクチン(断片化、不活化)(有効成分)により、医療機関受診のリスクが47%減少しました(相対リスク(RR):0.53 [95% CI: 0.46])。 %; 0.61]、つまり、来院数 310対583)、救急外来への受診率は 79%(RR: 0.21 [95% CI: 0.09; 0.47]、つまり、来院数 7対33)でした。抗生物質の使用は 50% 減少しました (RR: 0.50 [95% CI: 0.42; 0.60]、つまり処方された抗生物質の使用数 172対341)。
小児および成人における免疫原性

四価インフルエンザワクチン(断片化、不活化)(有効成分)の免疫原性を、最終投与後28日目(小児)と21日目のヘマグルチニン(HI)阻害抗体価(GMT)の幾何平均に基づいて評価しました。 (成人の場合)およびHI血清変換率(逆力価の4倍増加、または検出不能[lt;10]から逆力価≧40への変化)。研究 D-QIV-004(生後 6 ~ 35 か月の小児)では、評価は 1,332 人の小児のサブコホートで実施されました(四価インフルエンザワクチン(断片化、不活化)(活性物質)を投与されたグループは 753 人、ワクチン投与群は 579 人でした)。コントロールグループ)。結果を表 3 に示します。
研究 D-QIV-004 で実施された 2 回投与の初回レジメンの効果は、研究 D により、1 年後に 4 価インフルエンザワクチン (断片化、不活化) (活性物質) を 1 回投与した再ワクチン接種後の免疫応答を評価することによって分析されました。 -QIV-009。この研究は、ワクチン接種後 7 日で、生後 6 か月から 35 か月の小児の免疫記憶が 4 種類のワクチン株について誘発されたことを実証しました。
D-QIV-003 研究では、小児(3 歳から 18 歳までの約 900 人)を対象に、四価インフルエンザ ワクチン(断片化、不活化)(活性物質)の免疫原性の非劣性を三価インフルエンザ ワクチン(断片化、不活化)と比較して評価しました。 D-QIV-008試験の成人(いずれかのワクチンを1回または2回接種した治療群)および成人(4価インフルエンザワクチン(断片化、不活化)(活性物質)を1回接種した18歳以上の約1,800人の被験者)三価インフルエンザワクチン(断片化、不活化)の投与を受けた約600人)。
両方の研究において、四価インフルエンザワクチン(断片化、不活化)(活性物質)は、三価インフルエンザワクチン(断片化、不活化)と共通する3つの株に対して非劣性の免疫応答を引き起こし、追加のB株に対して優れた免疫応答を引き起こしました。ワクチン4価インフルエンザワクチン(断片化・不活化)(有効成分)に含まれます。結果を表 3 に示します。
表 3: 四価インフルエンザ ワクチン (断片化、不活化) (活性物質) – 小児 (6 ~ 35 か月、3 ~ 18 歳未満) および 18 歳以上の成人におけるワクチン接種後 (GMT) および血清変換率 (報告書による)コホートプロトコル)
|
生後6か月から35か月の子供 (D-QIV-004) |
||||
|
4価インフルエンザワクチン(断片化・不活化)(原体) |
コントロール1 |
|||
|
N=750-753 |
N’=742-746 |
N=578-579 |
N’=566-568 |
|
|
GMT 2 (95% CI) |
血清変換率2 (95% CI) |
GMT 2 (95% CI) |
血清変換率2 (95% CI) |
|
|
A/H1N1 |
165.3 (148.6;183.8) |
80.2% (77.2;83.0) |
12.6 (11.1;14.3) |
3.5% |
|
A/H3N2 |
132.1 (119.1;146.5) |
132.1 (119.1;146.5) |
14.7 (12.9;16 |
|








-1024x576.jpg?resize=1024,576&ssl=1)


