リュープリンはどのように作用しますか?
リュープロンという薬の活性物質である酢酸リュープロレリンは、毎日使用すると、体内の性腺刺激ホルモンの産生を減少させることによって作用する合成ホルモンです。この性腺刺激ホルモンの産生の減少により、卵巣と精巣の機能がブロックされます。薬の服用を中止すると、この遮断はなくなります。酢酸リュープロレリンの使用は、一部のホルモン依存性腫瘍 (たとえば、ある種の前立腺腫瘍など) の発生を予防します。
、子宮内膜症と子宮筋腫の復習.png)
薬は2~4週間で効果が出始めます。

リュープリンの禁忌

リュープロン注射剤は、酢酸リュープロレリン、または他の同様の薬、または薬の他の成分にアレルギーがある人は使用しないでください。毎月の酢酸リュープロレリン製剤によるアナフィラキシー (重度のアレルギー反応) の個別のケースが報告されています。

リュープリンは、妊娠している女性、または治療中に妊娠する可能性のある女性は使用しないでください。
リュープリンは、原因不明の性器出血のある女性には使用すべきではありません。
この薬は、妊娠している女性、または治療中に妊娠する可能性のある女性は使用しないでください。

リュープロンの使い方
リュープリンは経口摂取しても作用がありません。
リュープリンは医師の監督下で投与する必要があります。
Lupron の使用に関するガイダンス – 複数回用量バイアル
- 石鹸と水で手をよく洗ってください。
- 初めてバイアルを使用する場合は、ゴム製キャップが現れるまでバイアルから保護カバーを取り外します。製品を使用するたびに、金属リングとゴムキャップをアルコールに浸したコットンで拭いてください。ボトル内の液体を確認してください。粒子が入っていたり透明でない場合は使用しないでください。
- シリンジのプランジャーを 20 のマークまで引きます (このシリンジの 20 のマークは 0.2 mL に相当します)。
- 針カバーを取り外し、ゴムキャップの中央からバイアルに入れます。プランジャーを最後まで押して、シリンジからの空気がバイアルに入ります。バイアルとシリンジを逆さまにします。針の先端がバイアル内の液体に接触していることを確認してください。プランジャーをゆっくりと引いて、医師が処方した量のリュープリンを取り出します。数回塗布すると、バイアル内の液体の量が減少します。プランジャーを引く間、針の先端が常に液体中にあるように注意してください。シリンジ内に気泡がないか確認してください。空気がある場合は、プランジャーをゆっくりと押して、空気をボトルに戻します。必要に応じて、プランジャーを再度引いて、規定量に従ってシリンジ内の液体の量を増やします。
- 上記の手順を必要なだけ繰り返して気泡を取り除きます。バイアルから針を取り外します。針に触れたり、表面に触れさせたりしないでください。
- 申請サイトを選択します。注射部位の炎症を避けるために、体の部位を変えてください(注射部位は変える必要があります)。アルコールを含ませたコットンで皮膚を拭きます。
- 片手で注射器を持ちます。もう一方の場合は、皮膚をピンと張った状態に保つか、小さなひだを作ります。針を皮膚表面に対して垂直(90°)に押し込み、プランジャーを押して薬剤を注入します。
- アルコールで湿らせた綿パッドを針を挿入した場所に置き、挿入したときと同じ角度から取り外します。
- 各シリンジは 1 回のみ使用してください。廃棄する際はご注意ください。針を保護せずにゴミ箱に投げ込むと、誤って人を傷つける可能性があります。注射器、針、薬などを子供の手の届くところに絶対に置かないでください。
1日の最大投与限界は1mg、つまり注射用溶液の0.2mLです。
注: ボトルには、製品を取り出しやすくするために少し余分な部分が含まれています。したがって、2.8 mL バイアルは通常 14 回分の投与を目的としています。
付属のアルコール小袋は、リュープロンを使用する段階でアルコールを含ませたコットンの代わりとなります。
リュープリンの投与量
推奨用量は 1 mg (0.2 mL) を 1 日 1 回、単回皮下注射として投与します。長期皮下使用のための他の薬剤と同様に、注射部位は定期的に変更する必要があります。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。医師の知識なしに治療を中止しないでください。
ルポンを使い忘れた場合はどうすればよいですか?
服用量を忘れた場合は、医師に連絡して、服用量を忘れた場合の対処法についてアドバイスを受けてください。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
リュープリンの注意事項
人によっては、治療開始から最初の数週間で症状の悪化を経験する場合があります。症状の悪化は、致命的な合併症の有無にかかわらず、麻痺を引き起こす可能性があります。
ベンジルアルコール(薬の処方に含まれています)にアレルギーのある人は、注射部位にアレルギー反応が起こる可能性があります(その部位が赤くなって硬くなることがあります)。
骨密度
長期にわたる治療中の男性や低エストロゲン状態(エストロゲンホルモンの減少)にある女性では、骨密度の変化(骨量の減少)が発生する可能性があります。
酢酸リュープロレリン中止後の骨量減少の可逆性に関する男性を対象とした研究はありません。女性の場合、酢酸リュープロレリンの使用を中止すると骨量減少が回復する可能性があります。
発作
酢酸リュープロレリンによる治療中の患者で発作が観察されています。患者には、女性、小児集団、発作、てんかん、脳血管障害、中枢神経系の異常または腫瘍の病歴のある患者、およびブプロピオンやセロトニン再取り込み阻害剤などの発作に関連する併用薬を使用した患者が含まれます。上記の症状以外の患者でも発作が報告されています。
前立腺がん
最初に、酢酸リュープロレリンは、他の LH-RH アゴニストと同様に、治療の最初の 1 週間で血清テストステロン レベルを約 50% 増加させます。場合によっては、酢酸リュープロレリン デポー懸濁液 (Lupron Depot) による治療の最初の数週間に、症状の短期間の悪化、または前立腺がんの徴候や症状の発生の増加が発生することがあります。
少数の患者は骨の痛みが一時的に増加することがありますが、これは症状によって制御できます。腫瘍が脊椎の骨(椎骨)に広がっている人、および/または腫瘍による閉塞のために排尿できない人は、治療開始から最初の数週間はさらに注意を払い、悪化に気づいた場合はできるだけ早く医師に知らせる必要があります。またはその他の不快な反応の出現。
このリスクのある患者では、必要に応じて治療を中断しやすくするために、最初の 2 週間はリュープリンによる治療を毎日皮下投与で開始する必要があります。転移性脊椎病変および/または尿路閉塞のある患者は、治療開始から最初の数週間は注意深く観察する必要があります。
LH-RHアゴニストを投与されている男性では、高血糖(血糖濃度が高い)および糖尿病発症リスクの増加が報告されています。高血糖は、糖尿病の発症、または糖尿病患者の血糖(血糖)コントロールの悪化を表す可能性があります。医師は、LH-RH アゴニストを投与され、高血糖または糖尿病の現在の治療法に従って管理されている患者の血糖および/またはグリコシル化ヘモグロビン (HbA1c) の定期的なモニタリングを実施する必要があります。
LH-RH アゴニストの使用に関連して、心筋(心筋)梗塞、心臓突然死、脳卒中を発症するリスクの増加が男性で報告されています。報告されている確率と比率に基づくと、リスクは比較的低いため、前立腺がん患者の治療を決定する際には、心臓血管の危険因子とともに医師が慎重に評価する必要があります。 LH-RH アゴニストの投与を受けている患者は、心血管疾患の発症を示唆する兆候や症状がないか監視し、医師による管理を受ける必要があります。
心電図への影響
医師は、心電図の変化の既往歴または危険因子がある患者、および心電図の変化を引き起こす可能性のある薬剤を併用している患者に対して、酢酸リュープロレリンの投与を開始する前に、リスクと利益を評価しなければなりません。クラス IA (キニジン、ジソピラミド) またはクラス III (アミオダロン、ソタロール、ドフェチリド、イブチリド) の抗不整脈薬、メサドン、モキシロキサシン、抗精神病薬、または心電図の変化を引き起こす可能性のある薬剤の併用は、慎重に評価する必要があります。
臨床検査
酢酸リュープロレリンに対する反応は、血漿テストステロンレベルおよび前立腺特異抗原を評価することによって監視する必要があります。ほとんどの患者では、テストステロンレベルは治療の最初の週にベースライン値を超えて上昇し、2週目の終わりにはこれらの値以下に戻ります。去勢レベルは 2 ~ 4 週間以内に達成され、一度達成されると、患者が薬剤を使用している限り維持されます。
薬物相互作用
研究は行われなかった。ただし、他の薬剤との反応は予想されません。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
リュープリンの副作用
以下の副作用は一般に、ステロイド生成に対する酢酸リュープロレリンの薬理学的作用に関連していますが、これらの反応の頻度は不明です。
良性、悪性、または非特異的な新生物(嚢胞およびポリープを含む)
前立腺腫瘍の増加、前立腺がんの悪化。
代謝と栄養の変化
体重の増加と減少。
精神的な変化
リビドー(性欲)の減少または減少、リビドー(性的欲求)の増加。
神経系の変化
頭痛(頭痛)、筋力低下。
血管の変化
血管拡張(血管の拡張)、ほてり(ほてり)、低血圧(血圧低下)、起立性低血圧。
皮膚および皮下組織の変化
皮膚の乾燥、多汗症(過度の発汗)、発疹(皮膚の発赤・発疹)、蕁麻疹(皮膚アレルギー)、発毛異常、毛髪組織障害、寝汗、貧毛症(毛髪の減少)、皮膚色素沈着皮膚の変化、冷や汗、多毛症(過剰な毛の成長)。
生殖器系の変化
女性化乳房(男性の乳房の成長)、乳房痛(乳房の痛み)、勃起不全(勃起の維持または維持の困難)、精巣の痛み、乳房の増大、乳房の痛み、前立腺の痛み、陰茎の腫れ、陰茎の変化、精巣の萎縮(睾丸のサイズが小さくなる)。
一般的なおよびアプリケーションの場所の変更
粘膜の乾燥。
治験の変更
前立腺特異抗原(PSA)の増加、骨密度の減少。
長時間露光 (6 ~ 12 か月)
糖尿病、耐糖能障害、総コレステロールの増加、LDLの増加、中性脂肪の増加、骨粗鬆症。
以下の副作用が臨床研究および市販後の経験で報告されています。
前立腺がん
ほとんどの患者では、テストステロンレベルは治療の最初の週にベースラインを超えて増加しましたが、その後、治療の2週目の終わりまでに正常またはより低いレベルに減少しました。
脊椎転移や尿路閉塞、血尿のある患者では、治療開始から最初の数週間で兆候や症状が悪化する可能性が懸念されており、悪化すると一時的な衰弱や下肢の感覚異常などの神経学的問題を引き起こす可能性があります。または排尿症状の悪化。
副作用はシステムと頻度によって分布します。
- 非常に一般的です(この薬を使用している患者の 10% 以上で発生します)。
- 一般的(この薬を使用する患者の 1% ~ 10% の間で発生します)。
- まれです (この薬を使用している患者の 0.1% ~ 1% の間で発生します)。
ほとんどの副作用については、因果関係が確立されていません。
非常に一般的な反応 (この薬を使用している患者の 10% 以上で発生します)
血管の変化:
ホットフラッシュ(ほてり)。
一般的な反応 (この薬を使用している患者の 1% ~ 10% で発生します)
代謝と栄養の変化:
食欲不振(食欲不振)。
精神的な変化:
リビドー(性欲)の低下、不眠症(睡眠困難)。
神経系の変化:
めまい、頭痛、感覚異常(主観的な皮膚感覚)、嗜眠(一時的および完全な感受性の喪失)、眠気、記憶障害、味覚障害(味覚の歪みまたは低下)、無力症(脱力感)。
視覚的な変更:
視界がぼやける。
心血管の変化:
うっ血性心不全(血液を効率的に送り出す心臓の能力の喪失)、不整脈(心拍リズムの変化)、心筋梗塞。
呼吸器、胸部、縦隔の変化:
胸膜摩擦、肺線維症(正常な肺組織が瘢痕組織に置き換わる)。
胃腸の変化:
便秘(便秘)、吐き気、嘔吐、消化管出血(嘔吐物や便による出血)、腹部膨満(お腹が大きくなる)、下痢。
皮膚と皮下組織の変化:
紅斑(発赤)、脱毛症(脱毛)、斑状出血(あざ)。
筋骨格および結合組織の変化:
骨痛、筋肉痛(筋肉痛)、骨浮腫。
腎臓と尿路の変化:
血尿(尿中の血液)。
生殖器系の変化:
女性化乳房(男性の乳房の成長)、乳房痛(乳房の痛み)、勃起不全(勃起の維持または勃起の困難)、精巣萎縮(睾丸が小さい)、陰茎の水疱。
一般的なおよびアプリケーションの場所の変更:
痛み、浮腫(腫れ)、無力症(脱力感)、倦怠感、発熱(発熱)。
調査:
ヘマトクリットとヘモグロビンの減少(貧血)、血中尿素の増加、血中クレアチニンの増加。
市販後の医薬品安全性監視
この製品または他の酢酸リュープロレリン注射剤製剤では、製品の販売期間中に以下の副作用が観察されています。
ほとんどの場合、因果関係は確立されていません。これらの副作用の中には、すべての患者に当てはまるわけではないものもあります。
反応は、曝露率が不明の男性集団から自発的に報告されました。したがって、副作用の実際の発生率を推定することは不可能であり、その頻度は不明です。
感染症と蔓延
感染症、尿路感染症、咽頭炎(咽頭の炎症)、肺炎。
良性、悪性、または非特異的な新生物
皮膚がん(皮膚がん)。
血リンパの変化
貧血。
免疫システムの変化
アナフィラキシー反応(重度のアレルギー反応)。
内分泌の変化
甲状腺腫および下垂体脳卒中(下垂体における突然の重度の出血により、その機能が永久に損なわれる)。
代謝と栄養の変化
糖尿病、食欲亢進、低血糖(血糖濃度の低下)、低タンパク血症(血液中のタンパク質濃度の低下)、脱水症、高脂血症(血液中の脂肪濃度の増加)、高リン酸血症(血液中のリン酸濃度の増加) )。
精神的な変化
気分の変化、神経質、性欲の増加、不眠症、睡眠の変化、うつ病、不安、幻覚、自殺念慮、自殺未遂。
神経学的変化
めまい、頭痛、感覚異常(主観的な皮膚感覚)、嗜眠(一時的および完全な感覚の喪失)、記憶障害、味覚障害(味覚の歪みまたは低下)、感覚鈍麻(特定の領域の感覚の喪失または低下)。 )、失神(失神)、末梢神経障害(手や足の感度の変化)、脳卒中(脳卒中)、意識喪失、一過性虚血性クリーゼ、麻痺、神経筋症、発作。
視覚的な変化
かすみ目、視覚障害、視覚異常、弱視(かすみ目)、ドライアイ。
耳と迷路の変化
耳鳴り、聴覚障害。
心の変化
うっ血性心不全(血液を効率的に送り出す心臓の能力の喪失)、不整脈(心拍リズムの変化)、心筋梗塞(心筋)、狭心症(胸の痛み)、頻脈(心拍数の増加)、徐脈(心拍数の低下) 、心雑音(心臓の鼓動中の雑音)、心臓突然死。
血管の変化
リンパ浮腫(腫れ)、高血圧(高血圧)、静脈炎(静脈の炎症)、血栓症(静脈の詰まり)、低血圧(低血圧)、静脈瘤(静脈瘤)。
呼吸器、胸部、縦隔の変化
胸膜摩擦、肺線維症(正常な肺組織が瘢痕組織に置き換わる)、鼻出血(鼻血)、呼吸困難(息切れ)、咳、胸水(胸膜内の液体)、肺浸潤(検査用X線写真での特徴的な肺の変化) )、呼吸器疾患、副鼻腔閉塞(鼻および副鼻腔の詰まり)、肺塞栓症(肺血管の閉塞)、喀血(喀血)、間質性肺疾患(肺の深部組織の炎症)。
胃腸の変化
便秘(便秘)、吐き気、嘔吐、消化管出血、腹部膨満、下痢、嚥下障害(飲み込み困難)、口渇、十二指腸潰瘍、胃腸障害、消化性潰瘍、直腸ポリープ。
肝胆道の変化
肝機能の異常、重度の肝障害、黄疸(皮膚や粘膜が黄色くなる)。
皮膚および皮下組織の変化
脱毛症(脱毛)、斑状出血(紫色の斑点)、発疹(発赤)、皮膚の乾燥、光線過敏症(日光に対する過敏症)、蕁麻疹(赤く腫れたかゆみ)、皮膚炎(皮膚の炎症)、皮膚発毛異常、そう痒症(かゆみ)、色素沈着障害、皮膚損傷。
筋骨格および結合組織の変化
筋肉痛(筋肉痛)、骨浮腫(骨の腫れ)、関節症(関節障害)、関節痛(関節痛)、強直性脊椎炎、腱鞘炎(腱の炎症)の症状。
腎臓と尿路の変化
尿失禁(尿のコントロールの喪失)、頻尿(排尿回数の増加)、尿意切迫感、血尿(尿中の血液)、膀胱けいれん、尿路障害、尿路閉塞。
生殖器系の変化
女性化乳房(男性の乳房の成長)、乳房痛(乳房の痛み)、精巣萎縮(精巣サイズの減少)、精巣痛、乳房痛、精巣変化、陰茎浮腫(腫れ)、陰茎疾患、前立腺痛。
一般的な変更と管理場所
痛み、浮腫(腫れ)、無力症(筋力低下)、発熱(発熱)、反応、炎症、注射部位の痛みと硬結、無菌膿瘍、血腫(血液の蓄積)、悪寒、しこり、口渇、炎症、骨盤線維症。
調査
血液中の尿素、尿酸、クレアチニンまたはカルシウムの増加、心電図の異常、心電図(ECG)/虚血の変化、肝機能検査の異常、血小板数の減少、低カリウム血症(血中カリウム濃度の低下)、白血球減少症(白血球の減少)白血球増加症(血液中の白血球の増加)、プロトロンビン時間(PT)の増加、部分トロンボプラスチン時間(TTP)の増加、高脂血症(血液中の脂肪の増加)(LDLコレステロールおよびトリグリセリド) 、ビリルビンが増加しました。
怪我、中毒、処置上の合併症
脊椎骨折。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。また、顧客サービスを通じて会社に通知してください。
リュープロン特別集団
高齢者への使用
この年齢層に対する特別な推奨事項はありません。
小児や乳児への使用
現在の知識と製品の表示に基づいて、このプレゼンテーションを子供や乳児に使用することを正当化する根拠はありません。
妊娠中の使用
妊娠中のリュープリンの安全な使用は臨床的に確立されていません。治療を開始する前に、患者が妊娠していないことを確認することをお勧めします。リュープリンは避妊薬ではありません。避妊が必要な場合は、ホルモンを使用しない避妊方法を使用する必要があります。
この薬は妊娠中または治療中に妊娠する可能性のある女性には禁忌です。
妊娠中に薬を投与すると流産の可能性があります。治療中に患者が妊娠した場合は、薬の投与を中止する必要があります。
この薬は妊娠中に先天異常を引き起こします。
授乳中の使用:
酢酸リュープロレリンが母乳に移行するかどうかは不明です。したがって、授乳中の女性はリュープリンを使用すべきではありません。
リュープリンの構成
プレゼンテーション
5 mg/mL 注射可能溶液:
2.8 mL バイアル 1 本 (複数回の注射用)、使い捨て注射器 14 個、アルコール入り小袋 15 個が入ったパッケージ。
皮下ルート。
大人用。
構成
リュープリン 0.2 mL には次のものが含まれます。
1 mg *酢酸リュープロレリン。
※酢酸リュープロレリン 1 mg は、リュープロレリン 0.952 mg に相当します。したがって、5 mg の酢酸リュープロレリンは 4.76 mg のリュープロレリンに相当します。
賦形剤:
塩化ナトリウム、ベンジルアルコール、水酸化ナトリウムおよび/または氷酢酸および注射用水。
ユニットあたりの正味量:
2.8mL。
リュープリンの過剰摂取
過剰摂取の場合、つまりこの薬を大量に使用した場合は、できるだけ早く医師の診察を受ける必要があります。患者を注意深く監視し、支持策と対症療法を採用する必要があります。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
リュープリンの薬物相互作用
酢酸リュープロレリンと他の物質との相互作用に関する特別な研究は行われていません。しかし、特定の研究で観察されたように、リュープロレリンはチトクロム P450 酵素ではなく主にペプチダーゼによって代謝されるペプチドであること、およびこの物質が血漿タンパク質に約 46% しか結合していないことを考慮すると、薬物相互作用は予想されません。
治療中の臨床検査の変化
酢酸リュープロレリン デポー懸濁液を女性に投与すると、下垂体-生殖腺系が抑制されます。通常、治療中止後 3 か月以内に正常な機能が回復します。
したがって、製品の中止後 3 か月以内の治療中に行われる下垂体の性腺刺激ホルモンおよび性腺機能の診断検査は決定的なものではない可能性があります。
リュープリンの食品との相互作用
研究は行われていませんが、食品との反応は予想されません。
リュープリンという物質の作用
効果の結果
前立腺がん
酢酸リュープロレリンの有効性は、進行前立腺がん患者 205 人を対象に酢酸リュープロレリンを毎月 3.75 mg 投与し、その安全性と有効性を評価する前向き公開研究で証明されました。
この研究の主な目的は、45 か月の観察期間にわたって去勢レベル (? 50 ng/dL) に維持されるべきテストステロン レベルの観察を通じて有効性を評価することでした。治療前の平均テストステロンレベルは、4 週間後には 350 ng/dL から 21 ng/dL に減少し、45 か月の治療後には 20 ng/dL に減少しました。
長期的な臨床効果は、その期間における治療に対する最良の反応によって表すことができます: 完全反応 – 10.7%。部分奏効 – 49.8%;変化なし – 34.1%、進行 – 1.5%、データなし – 3.9%。進行までの期間の中央値は 12 (15 ± 11) か月でした。
研究 I1 では、進行性または転移性前立腺がん患者 237 人が無作為に割り付けられ、期間中、酢酸リュープロレリン 3.75 mg の月次投与(グループ 1)または酢酸リュープロレリン 11.25 mg の四半期ごとの投与(グループ 2)で治療されました。治療期間9ヶ月。
どちらのプレゼンテーションも同じ効果をもたらし、テストステロンとゴナドトロピンの血清レベルが顕著に低下し、「PSA」(前立腺特異抗原)レベルが低下しました。 9ヶ月の治療後、グループ1とグループ2の患者のそれぞれ65.2%と66.1%で「PSA」レベルが正常化した(≦4ng/ml)。
「EORTC」(欧州がん研究治療機構)の寛解基準によって評価された臨床反応は、両方の症状で同等でした。
|
グループ 1 (毎月 3.75 mg) |
グループ 2 (毎月 11.25 mg) |
|
|
N (%) |
N (%) |
|
|
完全寛解 (CR) |
4 (5.0) | 9 (5.7) |
|
部分寛解 (PR) |
29(36.3) | 53(33.8) |
|
安定化(E) |
32(40.0) | 64(40.8) |
|
進行状況 |
5 (6.3) | 8 (5.1) |
|
データの紛失 |
10(12.5) | 23(14.6) |
|
グローバルレスポンス「EORTC」(RC+RP+E) |
65(81.3) | 126(80.3) |
研究 II2 では、以前の研究の一部の患者を追跡調査することにより、長期反応 (43 か月) が評価されました。ドイツでは、62人の患者が四半期ごとに発表される酢酸リュープロレリン11.25mgを使用した。このグループの患者37人については、研究期間中に25人の患者が死亡したため、長期追跡研究は終了した。
血清テストステロンレベルの適切な抑制が達成され、治療期間中に患者 62 人全員に対して実施された 444 回の測定における抑制の合計パーセンテージは 98% でした。
婦人科
健康な女性 (N=20) を対象とした薬物動態学/薬力学研究では、エストラジオール抑制の発現が投与後 04 日から 04 週目までの患者で観察されました。
注射後 3 週間目までに、平均エストラジオール濃度 (8 pg/mL) は閉経期の範囲になりました。残りの投与期間にわたって、平均血清エストラジオールレベルは閉経期から初期卵胞期まで変化した。
血清エストラジオールは、治療後 4 週間以内にすべての患者で約 20 pg/mL に抑制され、2 人の患者が値を経験した 12 週間の投与間隔の終わりまで、患者の 80% で抑制されたまま (約 40 pg/mL) でした。 40~50 pg/mLの間。
他の 4 人の患者は、12 週間の投与間隔中に少なくとも 2 回連続してエストラジオール レベルの上昇 (範囲 43 ~ 240 pg/mL) を経験しましたが、この期間中にどの患者にも黄体機能の兆候はありませんでした。
酢酸リュープロレリン 11.25 mg を 3 か月ごとに投与すると、注射後の最初の 1 か月間に患者の 85% (N=17) に無月経が誘発され、2 か月目には患者の 100% に無月経が誘発されました。
すべての患者は、残りの 12 週間の投与間隔を通じて無月経のままでした。軽い出血と斑点のエピソードは、注射後最初の 1 か月間ほとんどの患者によって報告され、その後に他の患者からも報告されました。月経は、12 週間の投与間隔の終了後、平均して 12 週間 (2.9 ~ 20.4 週間の範囲) で再開しました。
酢酸リュープロレリン 11.25 mg を 3 か月ごとに投与すると、子宮内膜症および子宮筋腫による貧血の管理を目的とした対照臨床研究中に酢酸リュープロレリン 3.75 mg を投与された患者に対して、ホルモン抑制および月経抑制という点で同様の薬力学的効果が生じました。
子宮内膜症
対照臨床研究では、酢酸リュープロレリン 3.75 mg を月に 1 回、6 か月間投与すると、子宮内膜症の臨床徴候/症状 (骨盤痛、月経困難症、性交痛、骨盤の圧痛および硬直) の緩和においてダナゾール 800 mg/日と同等であることが実証されました。腹腔鏡検査の証拠によると、子宮内膜インプラントの減少。
子宮内膜病変の縮小の臨床的意義は現時点では不明であり、さらに、腹腔鏡による病期分類は症状の重症度と必ずしも相関するわけではありません。
酢酸リュープロレリン 3.75 mg を毎月投与すると、治療開始 1 か月目と 2 か月目にそれぞれ患者の 74% と 98% で無月経が誘発されました。ほとんどの患者は、軽い出血や斑点の症状を報告しました。治療後 1 か月目、2 か月目、3 か月目に、妊娠した患者を除き、患者のそれぞれ 7%、71%、95% で正常な月経周期が戻りました。
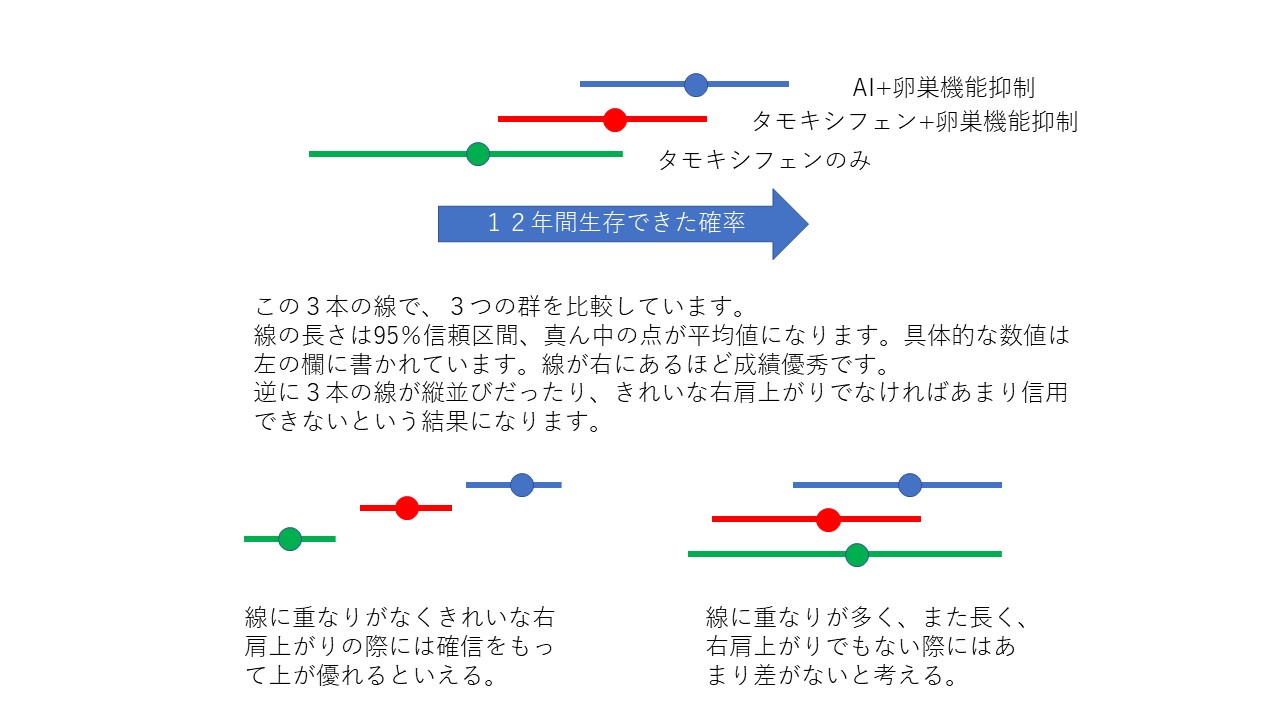
次の図は、2 つの対照臨床試験中に評価されたさまざまな症状について、ベースライン時、最終治療来院時、および治療中止後 6 か月および 12 か月後に症状が持続した症状を示した患者の割合(治療終了時点のすべての患者を含む)を示しています。治療および追跡期間への参加を選択した人。
元の患者の 75% が追跡調査を開始し、36% が 6 か月で評価され、26% が 12 か月で評価されたため、これは追跡期間の結果にわずかな偏りをもたらす可能性があります。
子宮平滑筋腫(子宮線維腫)
対照臨床研究では、酢酸リュープロレリン 3.75 mg を 3 ~ 6 か月間投与すると、子宮と筋腫の体積が減少し、臨床症状 (腹部の腫れ、骨盤の痛み、圧迫感) が軽減されることが示されています。
過剰な性器出血(月経過多および月経出血)が減少し、血液学的パラメータが改善されました。 3 件の臨床研究では、患者登録は血液学的状態に基づいていませんでした。超音波または磁気共鳴画像法 (MRI) の証拠によると、最終来院時には子宮体積が 41%、筋腫体積が 37% 減少しました。
さらに、これらの患者は、過剰な性器出血や骨盤の不快感などの症状の軽減を経験しました。この効果は治療開始から約 3 か月後に現れましたが、酢酸リュープロレリン 3.75 mg による治療をさらに 3 か月続けるとさらに効果が観察されました。
これらの患者の95%(95%)が無月経となり、それぞれ61%、25%、4%が治療開始1カ月目、2カ月目、3カ月目に無月経を経験した。治療後の追跡調査は、酢酸リュープロレリン 3.75 mg を投与された患者 77% のうち、? の増加を示した少数の患者 (N = 46) を対象に実施されました。治療中の子宮の容積の25%。
通常、月経は抑制療法後 2 週間以内に戻りました。治療前の子宮サイズに戻るまでの平均時間は 8.3 か月でした。新たな成長は、治療前の子宮の体積とは関連していないようでした。
別の対照臨床研究では、患者登録はヘマトクリットに基づいていましたか? 30% および/またはヘモグロビン? 10.2g/dL。鉄と併用した酢酸リュープロレリン 3.75 mg の投与により、β の増加が生じました。ヘマトクリット値は6%、? 3ヶ月の治療後、患者の77%でヘモグロビン値が2g/dL。ヘマトクリットの平均変化は 10.1%、ヘモグロビンの平均変化は 4.2 g/dL でした。
ヘマトクリット値が?の場合に臨床反応が起こると判断された。 36%と?のヘモグロビン12g/dLなので手術前の自己血献血が可能です。 3 か月時点で、患者の 75% がこの基準を満たしました。
3 か月後には、患者の 80% が月経過多または月経出血のいずれかの軽減を経験しました。以前の研究と同様に、一部の患者では斑点状出血と月経型出血のエピソードが認められました。
同じ研究では、?の減少が見られました。患者の60%と54%の子宮と筋腫の体積がそれぞれ25%である。酢酸リュープロレリン 3.75 mg は、腫れ、骨盤痛、圧迫感の症状を軽減することが観察されました。
酢酸リュープロレリン 3.75 mg の使用により妊娠率が増加したり悪影響を受けたという証拠はありません。
乳癌
進行乳がんの治療における酢酸リュープロレリンの有効性は、76人の閉経周辺期患者を対象とした前向き研究で証明されました。病気の進行が観察されるまで、毎月用量の酢酸リュープロレリン 3.75 mg を投与しました。
反応分析は、治療の 3 か月目と 6 か月目に実施されました。 3ヵ月後には患者の39人(51.3%)、6ヵ月後には患者の23人(30.3%)で客観的な奏効が得られ、
当時使用されていたWHOの基準(WHO 1979)に従って、疾患の完全または部分寛解または安定化として定義されました。
進行乳がんの治療における酢酸リュープロレリン 11.25 mg の有効性は、シクロホスファミド、メトトレキサート、フルオロウラシル (CMF) による標準化学療法を受けている患者を比較対象とした前向き第 III 相無作為化公開多施設共同研究で証明されました。
TABLE3研究では、エストロゲン受容体陽性と診断され、組織学的にII期またはIIIA期乳がんと診断された閉経前患者599名が研究の対象となり、外科的治療後6週間以内に2つの治療群に無作為に割り付けられた。
グループ 1 では、299 人の患者が酢酸リュープロレリン 11.25 mg で治療され、グループ 2 では、300 人の患者が標準的な CMF 化学療法レジメンで治療されました。平均追跡調査は5.8年で、無再発生存期間は両治療群で同様でした(P = 0.15)。全生存期間の探索的分析では、11.25 mg 酢酸リュープロレリン治療群が良好で、5 年生存率はグループ 1 で 81%、グループ 2 で 71.9% でした (P = 0.005)。
また、グループ 2 では乳がん関連死亡率がより高い傾向がありました。
この研究の結果は、乳がんと診断されたこの患者集団において、酢酸リュープロレリン 11.25 mg を四半期ごとに使用する治療は、CMF による標準的な化学療法と同等の効果があり、劣らないことを示しました。
その有効性データは、毎月 3.75 mg の製剤を裏付けるデータとも解釈できます。
思春期早発症
中枢性思春期早発症(CPP)の小児では、基礎性腺刺激ホルモンと刺激性性腺刺激ホルモンが思春期前のレベルまで低下します。テストステロンとエストラジオールは、それぞれ男子と女子では思春期前のレベルまで減少します。
ゴナドトロピンを減らすと、身体的および心理的な成長と発達が正常に行われるようになります。
酢酸リュープロレリンの中止後に性腺刺激ホルモンが思春期前のレベルに戻ると、自然な成熟が起こります。
研究は、中枢性思春期早発症の55人(女性49人、男性6人、これまでにGnRHアゴニストによる治療を受けたことがない)からなるグループを対象に実施され、思春期に適した年齢に達するまで酢酸リュープロレリンによる治療が毎月行われた。治療を中止した後、このグループの 40 人がモニタリングされました。
この患者集団における酢酸リュープロレリンの慢性投与により、次の生理学的効果が認められました。
骨格の成長:
骨端板が早期に閉じないことを考慮すると、体長の測定可能な増加に注目することができます。
臓器の成長:
生殖器官は思春期前の状態に戻ります。
月経:
月経が存在する場合、月経は停止します。
この研究では、中枢性思春期早発症の小児55人中22人に、デポー懸濁液中の酢酸リュープロレリンを4週間ごとに投与し、血漿中レベルを以下の表に示す体重カテゴリーに従って測定しました。
群の平均体重は、酢酸ロイプロライン注射剤の投与直前の第04週に測定される。 12 週目と 24 週目の薬物レベルは 4 週目のレベルと同様でした。
治療期間データ
治療期間中、酢酸リュープロレリンを毎月投与すると、ゴナドトロピンと性ステロイドのレベルが思春期前のレベルに抑制されました。 LH刺激によるピーク濃度のlt値への抑制。 1か月目で被験者の96%が1.75 mIU/mLを達成しました。
LH刺激によるスパイク抑制効果のある人の数と割合。 1.75 mIU/mL および経時的な LH 刺激ピークの平均ピーク + 標準偏差を表 1 に示します。
治療開始時の平均+SD年齢は7+2歳、治療期間は4+2年でした。治療期間終了から 6 か月後、LH 刺激ピークの平均は 20.6 + SD 13.7 mIU/mL (n=30) でした。
表 1: LH 刺激性サージ lt を患う患者の数と割合。各クリニック訪問時の 1.75 mIU/mL および平均 (SD) LH ピーク
思春期の臨床的/身体的兆候の抑制(退行または変化なしと定義される)は、大多数の患者で達成されました。女性では、治療開始から最初の5年間に乳房の発育が66.7~90.6%の範囲で抑制されました。
平均刺激エストラジオールはベースライン条件下で 15.1 pg/mL で、4 週目に最低検出レベル (5.0 pg/mL) まで減少し、治療の最初の 5 年間維持されました。男性の場合、治療開始から最初の5年間に生殖器の発達が60%から100%の範囲で抑制されました。
平均刺激テストステロンは、ベースライン条件下で 347.7 ng/dL であり、治療の最初の 5 年間は 25.3 ng/dL 以下のレベルに維持されました。
治療開始から最初の 4 週間における一過性の出血または性器出血の「リバウンド効果」が、ベースラインで初潮を迎えなかった女児 19.4% (36 人中 7 人) に観察されました。最初の 4 週間後および残りの治療期間中、月経様出血を報告した被験者はなく、まれな性器出血のみが観察されました。
多くの人では、治療中に成長率が低下し、骨年齢と暦年齢の比率も低下しました。 5 年後の平均成長率は 3.4 ~ 5.6 cm/年の間で変化しました。実年齢に対する骨年齢の平均比は、ベースラインの 1.5 から治療終了時には 1.1 に減少しました。
平均身長標準偏差スコアは、ベースライン状態の 1.6 から、治療段階の終了時には 0.7 に変化しました。
追跡調査期間のデータ
生殖機能(女性)と最終身長を評価するために、35 人の女性と 5 人の男性が治療後の追跡期間に参加しました。治療後 6 か月の時点で、被験者の大部分 (87.9%) が思春期の LH レベルの逆転を示し、思春期の進行再開の臨床兆候が明らかであり、女児では乳房の発育が増加し (66.7%)、男児では生殖器の発育が増加しました。 80%)。
追跡調査中に評価された40人の患者のうち、33人は決定的な、またはほぼ決定的な成人身長に達するまで観察された。これらの患者は、ベースライン条件で予測された成人身長と比較して、最終的な成人身長の平均増加を示しました。
平均の最終的な成人身長標準偏差スコアは -0.2 でした。治療中止後、追跡調査中に12歳に達したすべての女性被験者で定期的な月経が報告されました。月経までの平均期間は約1.5年でした。月経開始時の平均年齢は12.9歳でした。
生殖機能を評価するデータは、成人(18~26歳)に達した20人の少女を対象とした研究後の検査で得られた。正常な月経周期は女性の 80% で報告されました。被験者 20 名中 7 名で 12 件の妊娠が報告され、そのうち 4 名では複数の妊娠が報告されました。
酢酸リュープロレリン 11.25 mg を四半期ごとに使用する製剤で実施されたランダム化公開臨床研究では、1 歳から 11 歳までの 42 人の患者がこの薬の投与を受けました。研究グループには、思春期のLHレベルを有する未治療の患者と、研究開始時に思春期前のLHレベルを有し、毎月GnRHaアゴニストによる治療を受けた患者の同数が含まれていた。
刺激されたLHピークレベルがltまで抑制された患者の割合。 2、3、6 か月目の評価で決定された 4 mIU/mL は 78.6% でした。
表 2: 2 か月目から 6 か月目までの刺激による LH サージ レベルの抑制
すべての来院の平均刺激性LHサージを、用量およびサブグループ(未治療および治療歴あり)別に以下のグラフに示します。
患者の93%(42人中39人)は、すべての来院時において性ステロイドレベル(エストラジオールとテストステロン)が思春期前のレベルに抑制されていた。
女性患者の思春期の臨床的抑制は、生後 6 か月の時点で 32 人中 29 人 (90.6%) に観察されました。
男性患者における思春期の臨床的抑制は、6ヵ月目の患者2人中1人(50.0%)で観察された。骨年齢関連情報が完全に得られた患者では、被験者33人中29人(87.9%)で骨年齢と実年齢との比が減少していた。スクリーニング時と比較した場合の生後6か月。
薬理学的特徴
説明
この薬の有効成分である酢酸リュープロレリン(酢酸リュープロレリン)は、天然の性腺刺激ホルモン放出ホルモン(GnRH または LH-RH)の合成ノナペプチド類似体です。天然ホルモンよりも強力な効力を持ち、ゴナドトロピン生成の阻害剤として作用し、ステロイドとは化学的に異なります。化学名は5-オキソ-L-プロリル-L-ヒスチジル-L-トリプトファニル-L-seアセテートです。








-1024x576.jpg?resize=1024,576&ssl=1)


