ベタヒスチン二塩酸塩の禁忌 – Geolab

ベタヒスチン二塩酸塩は、活性物質または賦形剤のいずれかに対する過敏症が既知である患者、および褐色細胞腫のある患者による使用は禁忌です。
ベタヒスチン二塩酸塩の使用方法 – Geolab
成人のベタヒスチン二塩酸塩の推奨用量は、1日あたり24~48mgの範囲で、2~3錠に分けて経口摂取します。
ベタヒスチン二塩酸塩 16mg
半錠または1錠を1日3回服用してください。
ベタヒスチン二塩酸塩 24mg
1錠を1日2回。
投与量は治療反応に応じて個別に調整する必要があります。数週間の治療後にのみ改善が見られる場合もあります。場合によっては、数か月後に最良の結果が得られることもあります。
病気の初期から治療を行うことで、病気の進行や病気が進行した段階での難聴を防ぐことができるという証拠があります。
特別な集団に対する投与量
お年寄り
この患者グループにおける臨床研究からのデータは限られていますが、広範な市販後の経験は、高齢者では用量調整が必要ないことを示唆しています。
子供たち
ベタヒスチン二塩酸塩は、安全性と有効性に関する情報が不十分であるため、18 歳未満の子供には推奨されません。
腎不全と肝不全

このグループの患者を対象とした具体的な臨床研究はありませんが、市販後の経験によれば、用量調整は必要ないようです。
飲み忘れた場合の実施
患者が決められた時間に薬を飲むのを忘れた場合は、忘れた用量を無視し、指示された時間に次の用量を服用し、通常どおり推奨される用量スケジュールを継続するように指示します。
患者は、忘れた用量を補うために 2 回用量を服用すべきではありません。
ベタヒスチン二塩酸塩の予防措置 – Geolab
気管支喘息および消化性潰瘍疾患の病歴がある患者は、治療中に注意深く監視する必要があります。
妊娠
妊婦におけるベタヒスチンの使用に関する適切なデータはありません。
妊娠、胚・胎児の発育、分娩、出生後の発育への影響に関しては、動物実験は不十分です。人間に対する潜在的なリスクは不明です。ベタヒスチンは、明らかに必要な場合を除き、妊娠中に使用すべきではありません。
ベタヒスチン二塩酸塩はリスクカテゴリー B に分類されます。
授乳期
ベタヒスチンが母乳中に排泄されるかどうかは確立されていません。牛乳中のベタヒスチンの排泄に関する動物研究はありません。ベタヒスチンによる治療を開始する前に、授乳中の女性に対するベタヒスチンによる治療の考えられる利点と、子供に対する考えられるリスクを評価することが推奨されます。
妊娠中の女性は医師のアドバイスなしにこの薬を使用しないでください。
機械を運転または操作する能力への影響
ベタヒスチンはメニエール病とめまいに適応されます。どちらの病気も、機械の運転や操作に悪影響を与える可能性があります。機械を運転して操作する能力を調査するために特別に設計された臨床研究では、ベタヒスチンがこの能力にまったく影響を与えないか、無視できることが示されました。
ベタヒスチン二塩酸塩の副作用 – Geolab
ベタヒスチンで治療された患者を対象としたプラセボ対照臨床研究では、以下の副作用が以下に示す頻度で観察されました。
- 非常に一般的 (?1/10)。
- 一般的 (?1/100 ~ lt; 1/10)。
- 珍しい (?1/1,000 ~ <1/100)。
- 希少 (? 1/10,000 ~ lt; 1/1,000)。
- 非常にまれです (lt; 1/10,000)。
一般的な反応 (?1/100 ~ <1/10)
胃腸障害:
吐き気と消化不良。
神経系疾患:
頭痛。
臨床研究中に報告されたこれらの副作用に加えて、以下の副作用が市販後の使用中に自然発生的に報告され、科学文献でも報告されています。
周波数は入手可能なデータから推定できないため、「不明」として分類されます。
免疫系疾患:
過敏反応(アナフィラキシーなど)。
胃腸障害:
軽度の胃の症状(嘔吐、胃腸痛、腹部膨満、膨満感など)。これらの影響は通常、食事中に投与するか、投与量を減らすことで克服できます。
皮膚または皮下組織の疾患:
皮膚および皮下の過敏反応、特に血管神経性浮腫、蕁麻疹、発疹およびそう痒症。
有害事象が発生した場合は、健康監視通知システム (NOTIVISA) または州または地方自治体の健康監視機関に通知してください。

ベタヒスチン二塩酸塩の薬物相互作用 – Geolab
「生体内」研究における薬物相互作用に関するデータはありません。 「インビトロ」研究のデータに基づくと、「インビボ」でのシトクロム P450 酵素の阻害は予想されません。
「インビトロ」データは、モノアミンオキシダーゼ (MAO) サブタイプ B (セレギリンなど) を含むモノアミンオキシダーゼ (MAO) を阻害する薬剤によるベタヒスチン代謝の阻害を示しています。ベタヒスチンと MAO 阻害剤 (選択的 MAO-B を含む) を併用する場合は注意が推奨されます。
ベタヒスチンはヒスタミン類似体であるため、理論的には、ベタヒスチンと抗ヒスタミン薬の相互作用は、これらの薬剤の有効性に影響を与える可能性があります。
ベタヒスチン二塩酸塩の食品との相互作用 – Geolab
これまでのところ報告はありません。
物質ベタヒスチン二塩酸塩の作用 – Geolab
効果の結果
「クロスオーバー」モデルにおける二重盲検プラセボ対照研究が、18 の耳鼻咽喉科診療所で、さまざまな原因のめまいを患う 82 人の患者を対象に実施されました。
最初の治療期間では、患者はベタヒスチン (48 mg/日) またはプラセボを 5 週間投与されました。 2 回目の治療期間では、各グループが次の 5 週間に受ける薬剤投与量が逆転されました。
最初の治療期間中に、ベタヒスチン群はプラセボ群と比較して発作頻度の統計的に有意な改善を示しました。
このグループの患者がプラセボグループと投薬を中止した場合、発作頻度がわずかに増加しました。
しかし、プラセボ群から始めた患者がベタヒスチンの投与を開始すると、さらに良好な改善が見られました。ベタヒスチン二塩酸塩は、発作の重症度を軽減する点でプラセボよりも有意に優れた結果を示しました。
多施設共同プラセボ対照研究では、11の施設に集められたメニエール病または発作性頭位めまい症によりめまいを繰り返す患者144人にベタヒスチン二塩酸塩16mgを1日3回またはプラセボを3か月間投与した。
メニエール病患者における毎月のめまい発作の回数は、最初の 1 か月間および研究全体を通して、プラセボと比較した場合、ベタヒスチン二塩酸塩によって大幅に減少しました (3 か月後には 6.70 回の発作から 2.06 回の発作に) (plt; 0.05)。
発作の強さ、持続時間、めまいに伴う症状(耳鳴り、耳閉感、吐き気、嘔吐)を測定するための自己申告スケールでは、プラセボで治療したグループと比較した場合、ベタヒスチン二塩酸塩で治療したグループで有意に大きな改善が見られました。 0.001 – plt;
イヌとラットにそれぞれベタヒスチン二塩酸塩を 250 mg/kg 以上の経口量で 3 か月間投与した後でも、副作用は観察されませんでした。
神経系に対する副作用は、120 mg/kg 以上の用量を静脈内投与した後にイヌとヒヒで観察されました。
嘔吐は、イヌではそれぞれ 300 mg/kg と 120 mg/kg の経口投与と静脈内投与後に観察され、ヒヒでは散発的に観察されました。
ベタヒスチンには変異誘発作用がないことが示されています。
薬理学的特徴
薬力学
ベタヒスチンの正確な作用機序は部分的に解明されています。動物と人間の研究から得られたデータによって裏付けられた、もっともらしい仮説がいくつかあります。
ベタヒスチンはヒスタミン作動系に影響を与えます
ベタヒスチンは、神経組織内のヒスタミン H 1受容体に対して部分的なアゴニスト作用と H 3受容体に対してアンタゴニスト作用を持ち、H 2受容体に対しては無視できるほどの活性を持っています。ベタヒスチンは、シナプス前 H 3受容体をブロックし、H 3受容体の制御を誘導することにより、ヒスタミンの代謝回転と放出を増加させます。
ベタヒスチンは蝸牛領域と脳全体の両方への血流を増加させることができます
動物に対して行われた薬理学的試験では、ベタヒスチン二塩酸塩が、おそらく内耳微小循環の前毛細血管括約筋に対する弛緩作用を通じて、内耳の血液循環を改善することが実証されています。ベタヒスチンは人間の脳血流を増加させることも示されています。
ベタヒスチンは前庭代償を促進します
ベタヒスチンは、前庭代償を促進および促進することにより、動物の神経切除後の前庭の回復を促進します。この効果はヒスタミンの代謝回転と放出の調節を特徴とし、H 3受容体拮抗作用によって媒介されます。ヒトでは、ベタヒスチンで治療すると、前庭神経切除術後の回復時間が短縮されました。
ベタヒスチンは前庭核のニューロンの活性化を変化させる
また、ベタヒスチンには、側方前庭核および中前庭核における神経スパイクの生成に対して用量依存的な阻害効果があることが判明しました。
動物で実証された薬力学的特性は、前庭系に対するベタヒスチンの治療効果に寄与する可能性があります。
ベタヒスチンの有効性は、前庭性めまいとメニエール症候群の患者を対象とした研究で、めまいの発作の重症度と頻度を改善することによって証明されています。
薬物動態
吸収
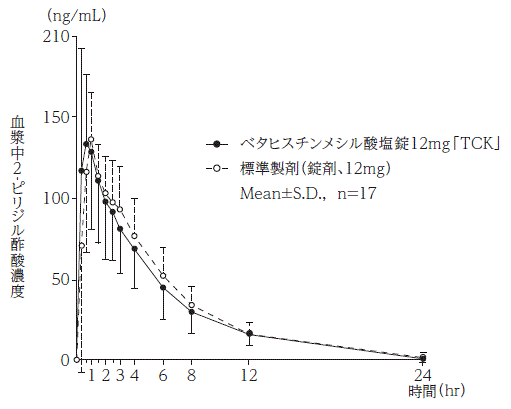
経口投与されたベタヒスチンは、胃腸管のあらゆる部分から容易かつほぼ完全に吸収されます。吸収後、ベタヒスチンは急速かつほぼ完全に 2-ピリジル酢酸 (2-PAA) に代謝されます。
ベタヒスチンの血漿レベルは非常に低いです。したがって、すべての薬物動態分析は血漿および尿中の 2-PAA の測定に基づいています。
食物摂取後のベタヒスチンの最大濃度(C max )は、絶食時に観察される濃度よりも低くなります。しかし、ベタヒスチンの総吸収量はどちらの条件でも同様であり、食物摂取はベタヒスチンの吸収を遅らせるだけであることを示しています。
分布
血漿タンパク質に結合するベタヒスチンの割合は 5% 未満です。
生体内変換
ベタヒスチンは吸収されると、急速かつほぼ完全に 2-PAA (薬理活性を持たない) に代謝されます。ベタヒスチンの経口投与後、2-PAA の最大血漿 (および尿中) 濃度は投与 1 時間後に観察され、約 3.5 時間の排出半減期で低下します。
排泄
2-PAA は尿中に急速に除去されます。ベタヒスチンの用量は 8 mg から 48 mg まで変化し、元の用量の約 85% が尿中に検出されます。ベタヒスチンの腎臓または糞便への排泄は最小限です。
直線性
回復率は 8 ~ 48 mg の経口投与期間を通じて一定であり、ベタヒスチンの薬物動態が直線的であることを示し、関与する代謝経路が飽和していないことを示唆しています。
前臨床安全性データ
慢性毒性
イヌとヒヒでは、約 120 mg/kg の静脈内投与後に神経系の副作用が観察されました。
ベタヒスチン二塩酸塩の慢性経口毒性に関する研究は、ラットで 18 か月間、イヌで 6 か月間実施されました。
ラットでは 500 mg/kg、イヌでは 25 mg/kg の用量が、臨床的な血液学的パラメータおよび化学的パラメータに変化を引き起こすことなく耐容されました。
これらの用量での治療に関する組織学的所見は報告されていません。用量を 300 mg/kg に増やした後、イヌは嘔吐しました。
ベタヒスチンとラットを 6 か月間 39 mg/kg 投与した研究では、一部の組織に充血が生じたことが文献に報告されています。出版物に掲載されているデータは限られています。したがって、この研究におけるこれらの発見の影響は不明です。
変異原性および発がん性の可能性
ベタヒスチンには変異原性の可能性はありません。
ベタヒスチン二塩酸塩については、特別な発がん性研究は行われていません。しかし、ラットでの 18 か月の慢性毒性研究では、組織病理学的検査で腫瘍、新生物、または過形成の兆候はありませんでした。
したがって、ベタヒスチン二塩酸塩は 500 mg/kg の用量まで、この限られた 18 か月の研究では発がん性の可能性を示す証拠は示されませんでした。
生殖毒性
生殖におけるベタヒスチンについて入手できるデータは限られています。ラットを用いた一世代研究では、経口投与量 250 mg/kg/日のベタヒスチンは、雄と雌の生殖能力、胎児の着床、分娩、および授乳中の子の生存率に悪影響を及ぼしませんでした。
離乳期のラットでは異常は観察されなかった。 10 または 100 mg/kg のベタヒスチンを経口投与した妊娠ウサギでは、着床、胎児の活力または体重に対する悪影響はなく、胎児の骨格または軟組織の異常は観察されませんでした。
これらの研究から、記載された研究では、関連する生殖パラメータに対する影響はラットとウサギでは検出されなかったと結論付けることができます。
ベタヒスチンには催奇形性はありません。ただし、研究の性質上、リスクを完全に排除することはできません。








-1024x576.jpg?resize=1024,576&ssl=1)


