フランカルボン酸モメタゾンの禁忌 – ルグラン

フラン酸モメタゾン (活性物質) は、フラン酸モメタゾン (活性物質) または乳糖に対する過敏症が知られている患者には禁忌です。
フランカルボン酸モメタゾン(活性物質)による治療は、喘息重積症または集中的な対策が必要な喘息のその他の急性症状の一次治療には禁忌です。
各症例の臨床的特徴に応じて、この製品は活動性または潜在性肺結核、未治療の真菌、細菌、ウイルスまたは寄生虫感染症の場合、および眼ヘルペスを含む単純ヘルペスの場合には禁忌です。

この薬は12歳未満の子供には禁忌です。

フランカルボン酸モメタゾンの使用方法 – ルグラン
カプセルは使用直前にブリスターから取り出す必要があります。穿刺中にゼラチンカプセルが砕け、吸入時にゼラチンの小片が口や喉に入る可能性があることを患者が理解することが重要です。

吸入器を使用するには、次の手順を実行します。
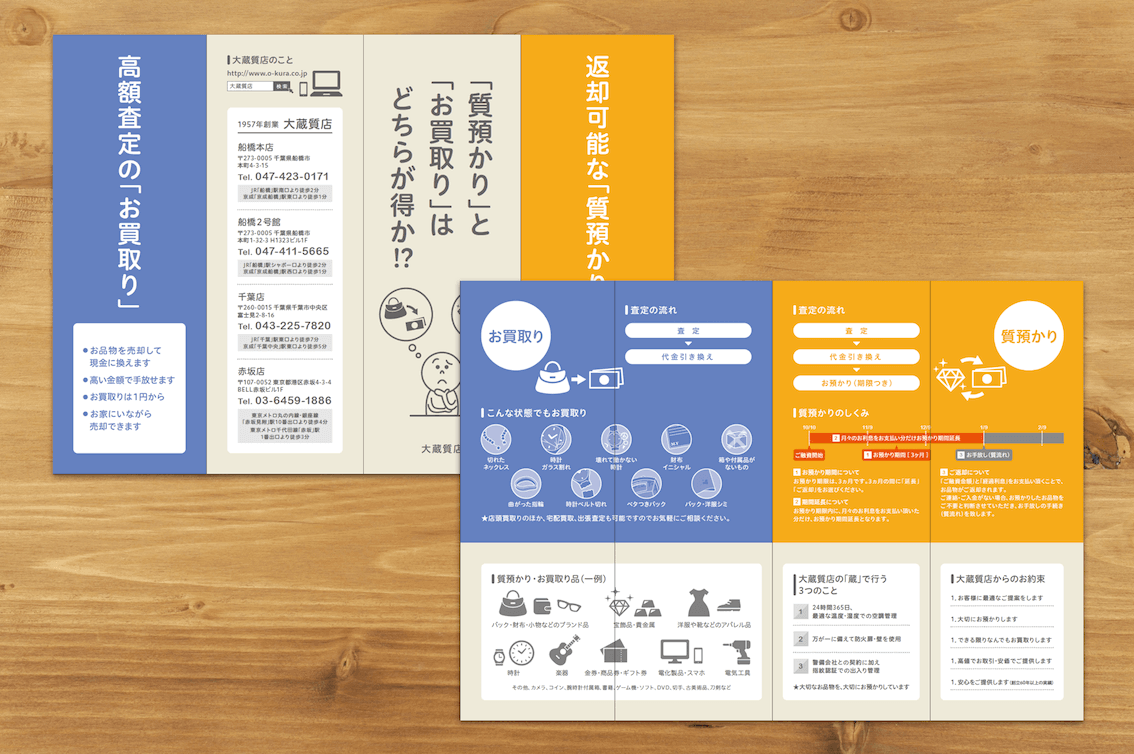
- カバーを取り外します (図 1)。
- 吸入器の根元をしっかりと持ち、マウスピースを矢印の方向に回して開けます(図2)。
- アルミニウムのタブを持ち上げて引っ張って、ブリスターからカプセルを取り外します。カプセルは使用直前にのみブリスターから取り出すことが重要です (図 3)。
- カプセルを吸入器の底部にある適切なコンパートメントに置きます (図 4)。
- 吸入器を垂直位置に保ち、カプセルの両端の穴に沿ってサイドボタンを 1 回完全に押します (図 5)。
- ボタンを放し、いずれかのボタンを軽く押して、カプセルの片側を押して、コンパートメントの底で緩んでいることを確認します。ドリル中にカプセルがコンパートメントの底に詰まる可能性があるため、カプセルの解放は吸引の有効性を保証する操作です (図 6)。
- ノズルを回転させて閉じた位置に戻します (図 7)。
- 肺からできるだけ多くの空気を放出します (図 8)。
- 吸入マウスピースの約 2/3 を口の中に入れ、その周りで唇を閉じます。できるだけ早く、できるだけ深く吸い込みます。製品が分散するにつれて、吸入チャンバー内でカプセルが回転したかのような振動音が聞こえるはずです (図 9)。
- 振動音が聞こえたら、無理のない範囲で息を止めてください (約 10 秒)。その間に、吸入器を口から外します。その後、普通に呼吸してください。吸入器を開け、カプセル内に粉末がまだ残っているかどうかを確認します。カプセル内に粉末が残っている場合は、手順5~9を繰り返してください。
- 使用後は吸入器を開け、空のカプセルを取り出してください。カプセルが小さな破片に砕け、ゼラチンの破片が口や喉に入った可能性があります。ゼラチンは食用であるため、有害ではありません。同様に、ゼラチンの破片がコンパートメントの底に残る場合があるため、これらの残留物は柔らかいブラシまたはブラシを使用して取り除く必要があります。ノズルを閉じてキャップを取り付けます。
- 口腔病変の出現を防ぐために、吸入後は口をすすぐことが推奨されます。この手順は、カンジダ症のリスクを軽減するのに役立ちます。
吸入器の掃除
吸入器をより良く保存するには、使用後に毎回柔らかいブラシまたはブラシを使用して残留物を取り除きます。その日の最後の使用後は、マウスピースとカプセルコンパートメントを柔軟な綿棒で掃除し、時々消毒液 (10 倍量の過酸化水素など) で湿らせます。プラスチックの表面を損傷する可能性があるため、アルコールは使用しないでください。これらの保存上の注意事項に従うことで、吸入器の推定耐用年数は 3 か月になります。治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
フランカルボン酸モメタゾンの投与量
ほとんどの患者にとって、これまで気管支拡張薬のみで治療されていたか、吸入コルチコステロイドのみで治療されていたかに関係なく、フロ酸モメタゾン(活性物質)による治療で推奨される初回用量は、デバイスを使用して 1 日 1 回 400 mcg です。患者によっては、400mcgを1日2回(200mcgを1日2回)に分けて投与すると、より適切にコントロールできる場合があります。一部の患者では、効率的な維持のために用量を 1 日 1 回 200mcg に減らすことが代替手段になる可能性があります。
経口コルチコステロイドを必要とする可能性のある重度の喘息患者の場合、フロ酸モメタゾン(活性物質)の推奨開始用量は 1 日 2 回 400mcg であり、これが推奨最大用量です。経口コルチコステロイドの減量が完了したら(以下を参照)、フロ酸モメタゾン(活性物質)の用量を最低有効用量まで漸増します。個々の患者は、症状の軽減が始まるまでの時間や改善の度合いが異なることに気づくでしょう。治療開始後1~2週間以上は最大の効果が得られない可能性があります。
最初は、重度の喘息患者全員に、フラン酸モメタゾン (活性物質) を患者の通常の維持用量の全身性コルチコステロイドと同時に使用することができます。約 1 週間後、1 日の用量を減らすか、一日おきに投与することで、全身性コルチコステロイドの段階的な中止が始まります。
患者の反応に応じて、1 ~ 2 週間の間隔を置いて新たな減量を行う必要があります。一般に、これらの用量の減量は、1 日あたりプレドニゾロン 2.5 mg またはその同等物を超えてはなりません。撤退計画は段階的に実行することをお勧めします。
経口コルチコステロイドの中止中は、肺機能や副腎不全の可能性の客観的測定など、不安定な喘息の兆候がないか患者を注意深く監視する必要があります。減量中に、一部の患者は全身性コルチコステロイド離脱症候群を経験する可能性があります。たとえば、肺機能が維持されている、あるいは改善されているにもかかわらず、関節痛や筋肉痛、衰弱や憂鬱などです。このような患者にはフランカルボン酸モメタゾン(活性物質)による治療を継続することが奨励されるべきですが、副腎不全の客観的な兆候がないか監視する必要があります。
副腎機能不全の証拠が現れた場合は、全身性コルチコステロイドの用量を一時的に増加し、その後はよりゆっくりと徐々に用量を中止する必要があります。
ストレスや重度の喘息発作の期間中、患者は全身性コルチコステロイドによる補足治療が必要になる場合があります。
喘息が安定したら、有害事象の可能性を減らすために最小有効量に徐々に調整することが望ましい。
初回用量で適切に反応しない 12 歳以上の患者の場合、2 週間の治療後、より用量を増やすことで喘息をより良くコントロールできる可能性があります。
この薬は割ったり、開けたり、噛んだりしないでください。
フランカルボン酸モメタゾンの使用上の注意 – ルグラン
乳タンパク質アレルギーを持つ人々におけるアレルギー反応、局所的な顔の浮腫や蕁麻疹、過敏症、喉の圧迫感が報告されています。
他の吸入コルチコステロイド製剤と同様に、母親、胎児、または乳児に対する潜在的なリスクが正当化される場合を除き、フランカルボン酸モメタゾン(活性物質)は妊娠中や授乳中の母親によって使用されるべきではありません。妊娠中にコルチコステロイドを投与された母親から生まれた子供は、薬剤性副腎皮質機能不全について注意深く観察する必要があります。妊娠中はコルチコステロイドの産生が自然に増加します。したがって、ほとんどの女性は、より少ない用量の外因性コルチコステロイドを必要とし、妊娠中はコルチコステロイド治療が必要ないか、用量が減らされる可能性があります。
妊娠 – リスクカテゴリー C
動物実験ではリスクが明らかになりましたが、妊婦を対象とした研究はありません。
妊娠中および授乳中に使用してください。妊婦におけるフランカルボン酸モメタゾン(活性物質)の使用について、適切かつ十分に管理された研究はありません。マウス、ラット、ウサギを用いた動物生殖研究により、催奇形性の証拠が明らかになりました。喘息は重篤で、生命を脅かす可能性のある病気です。妊娠中の喘息がうまくコントロールできていないと、母体と胎児にとって悪影響となります。
この薬は、医師または歯科外科医のアドバイスなしに妊婦が使用しないでください。
この薬剤が母乳中に排泄されるかどうかは確立されていません。この可能性があるため、母乳育児や投薬の中止を決定する必要があります。
授乳中の使用
フランカルボン酸モメタゾン (活性物質) 400 mcg の単回吸入量の全身再吸収は 1% 未満でした。フランカルボン酸モメタゾン (有効成分) が母乳中に排泄されるかどうかは不明です。他のコルチコステロイドは母乳中に排泄されるため、授乳中の女性にフロ酸モメタゾン(有効成分)を投与する場合は、その使用に注意が必要です。
他の人と共有したり、他の病気に使用したりしないでください。
推奨用量を超えて投与した場合のフランカルボン酸モメタゾン(活性物質)の安全性と有効性は確立されていません。コルチコステロイドを中止すると、安定した喘息が数日間続くことがあります。
局所的な影響
臨床研究中に、カンジダ・アルビカンスによる口と咽頭の局所感染症が発生しました。中咽頭カンジダ症が発症した場合は、フラン酸モメタゾン(活性物質)による治療を継続しながら、適切な局所または全身の抗真菌療法で治療する必要がありますが、フラン酸モメタゾン(活性物質)による治療を中断する必要がある場合もあります。この影響は、フロ酸モメタゾン (有効成分) を吸入した後、飲み込まずに水で口をすすぐことで部分的に回避できます。したがって、フランカルボン酸モメタゾン (有効成分) を吸入した後は、口をすすぐように患者に推奨する必要があります。
気管支けいれん
他の吸入喘息薬と同様に、投与後にすぐに喘鳴が増加する気管支けいれんが起こることがあります。フランカルボン酸モメタゾン(活性物質)の投与後に気管支けいれんが発生した場合は、即効性の吸入気管支拡張薬による即時治療が推奨されます。フランカルボン酸モメタゾン(活性物質)による治療を中断し、代替療法を開始する必要があります。
全身コルチコステロイド療法からの患者の転院
全身活性コルチコステロイドからモメタゾンフロ酸塩(活性物質)に移行する患者には特別な注意が必要である。これは、全身コルチコステロイドから全身バイオアベイラビリティの低い吸入コルチコステロイドへの変更中および変更後に喘息患者の副腎不全による死亡が発生しているためである。全身性コルチコステロイドの中止後、視床下部-下垂体-副腎(HPA)軸の機能が回復するまでに数か月かかる場合があります。
以前に 1 日あたり 20 mg 以上のプレドニゾロン (またはその同等物) を投与されていた患者は、特に全身性コルチコステロイドがほぼ完全に中止された場合、より感受性が高くなる可能性があります。
HPA 機能が抑制されているこの期間中、患者は外傷、手術、感染症 (特に胃腸炎)、または重度の電解質喪失に関連するその他の状態にさらされた場合、副腎皮質機能不全 (アジソン病危機) の兆候や症状を示すことがあります。フロ酸モメタゾン(活性物質)は、これらの症状の発症時の喘息症状のコントロールを改善する可能性がありますが、推奨用量では、通常の生理学的量よりも少ない量のコルチコステロイドを全身に投与し、これらの緊急事態に対処するために必要なミネラルコルチコイド活性を提供しません。
ストレスまたは重度の喘息発作の期間中、吸入コルチコステロイドに移行した患者には、直ちに経口コルチコステロイドを(大量に)再開し、追加の指示について医師に連絡するよう指示されるべきです。
このような患者には、ストレスまたは重篤な急性喘息発作の期間中の全身コルチコステロイドの必要性と推奨用量を示すリマインダーカードを保管することが推奨されます。
経口コルチコステロイドを必要とする患者は、フロ酸モメタゾンに移行した後、全身性コルチコステロイドを徐々に中止する必要があります。プレドニゾロン(または同等物)の減少は、フロ酸モメタゾン(活性物質)による治療中に、プレドニゾロンの 1 日用量を毎週 2.5 mg 減らすことによって達成できます。
肺機能 (FEV1 または PEF)
経口コルチコステロイドの中止中は、β-アゴニストの使用と喘息の症状を注意深く監視する必要があります。喘息の兆候や症状を監視することに加えて、疲労、脱力感、脱力感、吐き気や嘔吐、動脈性低血圧などの副腎機能不全の兆候や症状がないか患者を観察する必要があります。
経口コルチコステロイドの中止中、一部の患者は、呼吸機能が維持または改善しているにもかかわらず、関節痛や筋肉痛、脱力感、抑うつなどの全身性コルチコステロイド離脱症状を経験することがあります。
全身性コルチコステロイドで治療されている患者では、フランカルボン酸モメタゾン(活性物質)に移行すると、全身性コルチコステロイド療法によって以前は抑制されていた既存のアレルギー症状、たとえば鼻炎、結膜炎、湿疹、関節炎、好酸球増加症を引き起こす症状が悪化する可能性があります。
急性喘息のエピソード
フラン酸モメタゾン (活性物質) は気管支拡張薬ではなく、気管支けいれんやその他の喘息の急性エピソードの迅速な軽減には適応されていません。フロ酸モメタゾン(活性物質)による治療中に喘息症状が気管支拡張薬に反応しない場合、患者は直ちに医師に連絡するように指示されるべきです。これらのエピソードの間、患者は経口コルチコステロイド療法を必要とする場合があります。
皮質過剰症と副腎抑制
フランカルボン酸モメタゾン(活性物質)は、多くの場合、治療上同等の経口用量のプレドニゾロンよりも HPA 軸機能の抑制が少なく、喘息の症状をコントロールするのに役立ちます。コルチゾール産生に対する影響には個人差があるため、医師はフロ酸モメタゾン (活性物質) を処方する際にこの情報を考慮する必要があります。
不適切な副腎反応の証拠を検出するために、術後またはストレス期間中の患者を観察する際には特別な注意を払う必要があります。特にフランカルボン酸モメタゾン(有効成分)が推奨用量を超える用量で長期間投与された場合、皮質過剰症や副腎抑制などの全身性コルチコステロイドの影響が少数の患者に現れる可能性があります。このような影響が生じた場合は、全身性コルチコステロイドの減量および喘息の制御に関する一般的な手順に従って、フロ酸モメタゾン (活性物質) の用量をゆっくりと減らす必要があります。
免疫抑制
免疫システムを抑制する薬を使用している人は、健康な人よりも感染症にかかりやすくなります。たとえば、水痘や麻疹は、コルチコステロイドで治療を受けている感受性の高い子供や成人にとって、より重篤な、あるいは致命的な結果を引き起こす可能性があります。これらの病気にかかったことがない、または正しく予防接種を受けていない子供や成人では、曝露を避けるために特別な注意が必要です。コルチコステロイドの投与量、投与経路、投与期間が播種性感染症の発症リスクにどのように影響するかは不明です。
また、基礎疾患や以前のコルチコステロイド治療がリスクにどのような影響を与えているかも不明です。水痘にさらされた場合は、水痘・帯状疱疹免疫グロブリン(VZIG)による予防が必要となる場合があります。麻疹にさらされた場合は、筋肉内免疫グロブリン (IG)プールによる予防が必要となる場合があります。 (VZIG および IG の詳しい処方情報については、それぞれのリーフレットを参照してください。) 水痘が発症した場合は、抗ウイルス剤による治療が考慮される場合があります。
注意:
吸入コルチコステロイドは注意して使用する必要があり、気道の活動性または潜在性結核患者、未治療の真菌、細菌、ウイルスまたは寄生虫感染症、または目を含む単純ヘルペス患者では、場合によっては使用を避けるべきです。
骨ミネラル密度の減少
フランカルボン酸モメタゾン(活性物質)などの吸入コルチコステロイドを含む製品の長期投与により、骨密度(BMD)の減少が観察されています。 BMD の小さな変化が長期的な転帰に及ぼす臨床的重要性は不明です。長期間の固定、骨粗鬆症の家族歴、または骨量を減少させる可能性のある薬剤(抗けいれん薬やコルチコステロイドなど)の慢性使用など、骨ミネラル含有量の減少に関する重要な危険因子を持つ患者は、監視され、確立された標準治療に従って治療される必要があります。
緑内障と白内障
臨床研究では、フロ酸モメタゾン(有効成分)の投与後に緑内障、眼圧上昇、白内障が報告されています。視力に変化がある患者や、眼圧上昇、緑内障、白内障の既往歴がある患者では、綿密なモニタリングが必要です。
肝障害
フランカルボン酸モメタゾンの濃度(活性物質)は、肝障害の重症度に応じて増加するようです。
患者はフランカルボン酸モメタゾン(活性物質)による治療を突然中止することについて警告されるべきです。
高齢者向けの使用
高齢患者と若年患者の間で安全性や有効性における全体的な差異は観察されなかったが、一部の高齢者の感受性がより高いことは除外できない。
この薬はドーピングを引き起こす可能性があります。
フランカルボン酸モメタゾンの副作用 – ルグラン
以下に記載する安全性データは、12 歳以上の患者におけるフランカルボン酸モメタゾン(活性物質)への曝露を反映しており、合計 1,750 人の患者を対象とした 8 ~ 12 週間続く 10 件のプラセボ対照臨床研究と、 1年間フラン酸モメタゾン(活性物質)を投与された475人の患者が含まれていた。
フランカルボン酸モメタゾンの副作用を発生率の降順に示します。
非常に一般的な反応 (gt; 1/10)
- 頭痛;
- 喘息を伴うアレルギー性鼻炎。
- 急性咽頭炎;
- 急性上気道感染症;
- 関節痛;
- うつ。
一般的な反応 (gt; 1/100 および lt; 1/10)
- 副鼻腔炎;
- 口腔カンジダ症;
- 月経困難症;
- 筋骨格系の痛み。
- 腰痛;
- 消化不良;
- 筋肉痛;
- 腹部および骨盤の痛み;
- 吐き気と嘔吐。
- 倦怠感;
- インフルエンザ様症候群(発熱を伴う悪寒、筋肉痛)。
- 胃腸炎(非感染性胃腸炎および大腸炎)。
- 拒食症;
- オタルジア;
- 感染;
- 発声障害。
- 鼻出血。
異常な反応 (>1/1,000 および <1/100)
白内障。
まれな反応 (gt; 1/10,000 および lt; 1,000)
緑内障、眼圧上昇。
重大な副作用には次のようなものがあります。
- 口と喉の真菌感染症。喘息のために吸入ステロイドを使用している患者は、口の真菌感染症を発症する可能性があります。
- ステロイドの使用による免疫力の低下により、感染症のリスクが増加する可能性があります。
- 副腎不全。死亡が起こる可能性があります。手術中、手術後、外傷などで患者がストレスにさらされている場合、再び経口ステロイドが必要になる可能性があります。
- 骨量(骨密度)の減少。吸入ステロイドを長期間使用する患者は、骨量が減少するリスクが高く、骨の強度に影響を与える可能性があります。
吸入コルチコステロイドの使用により、特に高用量で長期間処方された場合、全身影響が発生する可能性があります。
他の糖質コルチコイドで観察されたように、次のような過敏反応が発生する可能性を考慮する必要があります。
- 皮膚の発疹;
- 蕁麻疹;
- そう痒症と紅斑。
- 目、顔、唇、喉の浮腫。
フロ酸モメタゾン – ルグランの薬物相互作用
主にコルチコステロイドのクラスに関連して、いくつかの相互作用が文書化されており、リスクカテゴリに従って分類されています。
アルデスロイキン
コルチコステロイドは、アルデスロイキンの抗腫瘍効果を低下させる可能性があります。
リスク X: 組み合わせを避けます。
アムホテリシンB
コルチコステロイド(経口吸入)は、アムホテリシン B の低カリウム血症効果を高める可能性があります。
リスク C: 治療を監視する。
抗糖尿病薬
コルチコステロイド(経口吸入)は、抗糖尿病薬の血糖降下作用を軽減する可能性があります。場合によっては、コルチコステロイド媒介の HPA 軸抑制により、特にインスリンのプロフィールや別の抗糖尿病薬の使用において、重度の低血糖として現れる急性副腎危機が引き起こされることがあります。
リスク C: 治療を監視する。
コルチコレリン
コルチコステロイドは、コルチコレリンの治療効果を低下させる可能性があります。具体的には、コルチコレリンに対する血清 ACTH 応答は、最近または現在のコルチコステロイドの使用によって鈍化している可能性があります。
リスク C: 治療を監視する。
CYP3A4 (強力) 阻害剤
血清コルチコステロイドが増加する可能性があります。吸入コルチコステロイドと CYP3A4 阻害剤の併用は推奨されません。
リスク C: 治療を監視する。
デフェラシロクス
コルチコステロイドは、デフェラシロクスの副作用/毒性作用を増大させる可能性があります。具体的には、消化管潰瘍/炎症または出血のリスクの増加です。
リスク C: 治療を監視する。
ヒアルロニダーゼ
コルチコステロイドはヒアルロニダーゼの治療効果を低下させる可能性があります。コルチコステロイド(特に高用量)を受けている患者は、標準用量のヒアルロニダーゼに対して望ましい臨床反応を達成できない可能性があります。より高用量のヒアルロニダーゼが必要になる場合があります。
リスク D: 治療法の変更を検討してください。
ループ利尿薬
コルチコステロイド(経口吸入)は、ループ利尿薬の低カリウム血症効果を増強する可能性があります。
リスク C: 治療を監視する。
テラプレビル
コルチコステロイドはテラプレビルの血清濃度を低下させる可能性があり、またコルチコステロイドの血清濃度を上昇させる可能性があります。テラプレビルと全身性コルチコステロイドの併用は推奨されません。可能な場合は代替案を検討してください。併用する場合は特に注意し、過剰なコルチコステロイド効果やテラプレビル効果の低下を監視してください。
リスク D: 治療法の変更を検討してください。
サイアザイド系利尿薬
コルチコステロイド(経口吸入)は、サイアザイド系利尿薬の低カリウム血症効果を増強する可能性があります。
リスク C: 治療を監視する。
フラン酸モメタゾン (活性物質) と CYP3A4 酵素の強力な阻害剤であるケトコナゾールを同時投与すると、フラン酸モメタゾン (活性物質) の血漿レベルが増加する可能性があります。
物質モメタゾンフロエートの作用 – ルグラン
有効性の結果
成人向け
フロ酸モメタゾン(活性物質)は 3 件の二重盲検臨床研究で評価され、737 人の患者がプラセボと比較して肺機能の良好な回復と喘息増悪の発生率の低下を示しました。 2件の臨床研究では、440mcgのフロ酸モメタゾン(活性物質)を1日1回投与し、220mcgのフロ酸モメタゾン(活性物質)を1日2回投与すると、プラセボと比較してFEV1の改善が見られました。さらに、努力呼気流量 (PEFR) は、プラセボと比較して大幅に改善されました。また、プラセボと比較した場合、喘息の悪化が減少し(毎日440μgの摂取で)、β2作動薬による救急薬の使用が減少しました。 3番目の臨床研究では、200μgのフランカルボン酸モメタゾン(活性物質)を1日1回夜間投与した患者は、プラセボを摂取した患者と比較して、FEV1の有意に大きな改善を達成した。夜間に測定したピーク呼気流量(PEF)は、フランカルボン酸モメタゾン(活性物質)投与群ではベースラインから7%改善したが、プラセボ投与群ではベースラインから4%改善した。 1
軽度から中程度の重症度までの喘息患者を対象とした多施設二重盲検無作為化研究において、フロ酸モメタゾン(有効成分)を吸入粉末(MF-DPI)により投与しました。吸入コルチコステロイドを使用していない喘息患者(12 歳以上)は、朝に 200 mcg の MF-DPI (n=72)、400 mcg の MF-DPI (n=77)、またはプラセボを投与された場合に気道疾患の改善を示しました。 n =87) を 12 週間継続します。 MF-DPIを受けた患者は、FEVおよびFVC(FEV、努力呼気量、FVC、努力肺活量)によって検証されるように、治療中に優れた反応を示しました。 400mcgのMF-DPIを投与された患者は、プラセボと比較してPEFRの改善を示しました。 MF-DPIを受けた患者は、プラセボを受けた患者と比較して、β2アゴニストのレスキュー用量が少なくて済みました。 MF-DPI はどちらの用量でも忍容性が良好でした。有害事象は軽度から中等度でした。 PFER に対して 200 mcg の MF-DPI を投与したグループと比較して、PFER に対して 400 mcg の MF-DPI を投与したグループの反応が優れていたため、著者らは毎日の治療計画における理想的な用量として MF-DPI の初回用量 400 mcg を推奨しています。 2
12週間続く二重盲検多施設プラセボ対照研究では、フランカルボン酸モメタゾン粉末(活性物質)(MF-DPI)400μgを1日1回吸入し、夜間に同じ薬剤200μgを1日2回吸入することを比較した。肺機能と喘息の症状を改善します。喘息の症状、アルブテロール(レスキュー)の使用は、プラセボグループと比較した場合、MF-DPIで治療されたグループで有意に減少し、睡眠の質も改善されました。喘息の症状間の唯一の違いは、MFDPI の 400mcg 投与中に咳が少なくなったことでした。どちらの用量でも有害事象は主に気道感染症と頭痛で、範囲は軽度から中等度でした。 3
小児用
12週間続く二重盲検、用量設定、ランダム化研究。 12 歳以上の患者は、有効性を検証するために、吸入粉末 (MD-DPI) によって投与されるフランカルボン酸モメタゾン (活性物質) の吸入を受けました。フラン酸モメタゾン(活性物質)は、HPA 軸機能の抑制を引き起こすことなく、持続性喘息の症状を軽減するのに効果的でした。患者は、プラセボ、ジプロピオン酸ベクロメタゾン 168 mcg、またはフランカルボン酸モメタゾン (有効成分) 100 mcg、200 mcg、または 400 mcg による吸入治療を受けるために 12 時間ごとに無作為に割り付けられました。 200 mcg のフランカルボン酸モメタゾン (活性物質) による治療は、100 mcg のモメタゾンよりも一貫して効果的でした。有害事象はすべての研究グループで同様でした:頭痛、口および咽頭のカンジダ症。 4
12週間の多施設共同二重盲検プラセボ対照並行群間研究では、4~11歳の小児296人を対象に、フランカルボン酸モメタゾン(活性物質)吸入粉末の2つのレジメン(夜間100μg vs 1日2回100μg)を評価した。喘息持ちの歳。両方のレジメンで、FEV1、努力呼気流量、努力肺活量、朝夕の最大呼気流量、喘息症状スコア、アルブテロールの使用(レスキュー)、夜間覚醒、治療への反応、および生活の質に関して、プラセボと比較して有意な改善が観察されました。フランカルボン酸モメタゾン(活性物質)の両方の DPI レジメンは忍容性が良好で、肺機能が大幅に改善され、効果的な喘息コントロールが維持され、小児の生活の質が向上しました。 5
吸入粉末(MF-DPI)によって投与されるフラン酸モメタゾン(活性物質)が、肺活動の改善、喘息症状の軽減、および必要性の軽減または排除を伴う、持続性喘息の重症度の治療に効果的であることが示された研究経口コルチコステロイドの場合。 1日1回の用量の治療計画は、以前に吸入コルチコステロイド(ICS)計画を受けた軽度から中等度の持続性喘息の患者、および症状を軽減するためにβ2作動薬のみを投与された患者に有効であった。 200μgの1日1回の夕方用量のレジメンは、200μgの1日1回の朝の用量のレジメンよりも多くの利点を明らかにしました。経口コルチコステロイド (OCS) と高用量の ICS に依存していた重度の喘息患者は、薬剤を MF-DPI に切り替えると喘息をより良くコントロールできるようになりました。 1 年間の研究では、MF-DPI の忍容性は良好で、ほとんどの副作用は軽度から中等度であると考えられました。軽度から中等度の喘息症状を持つ患者に 200 ~ 400 mcg の MF-DPI を投与すると、肺機能の改善と喘息の制御に効果がありました。 400mcgのMF-DPIによる治療により、経口コルチコステロイドの使用を大幅に減らすことができました。 6
現在、喘息治療ガイドラインでは、幼児を含むあらゆる年齢層の患者において、軽度から中等度の喘息を制御するための治療の選択肢として、吸入コルチコステロイド(ICS)の投与が推奨されています。広範な文献レビュー研究では、有効性、長期安全性、全身影響の欠如、FDA(アメリカの医薬品規制庁)が小児に対して承認した用量などの臨床データが分析されました。分析の結果、4~11歳の小児の毎日の投与により、肺機能と生活の質が大幅に改善され、救急薬の使用や他のICSとの併用による悪化が減少したことが示されました。視床下部-下垂体-副腎軸に対する全身的な影響、または成長の低下がないことが確認されました。小児研究の結果は一貫しており、1 回の投与計画で安全性が示されています。 MF-DPI の使いやすさは、治療を適切に遵守することで喘息のコントロールを維持するのに役立ちます。 7
参考文献:
1. 製品情報: アズマネックス ツイスターラー(R) 経口吸入粉末、フランカルボン酸モメタゾン経口吸入粉末。シェリング コーポレーション、ニュージャージー州ケニルワース、2008 年。
2. Nayak AS、Banov C、Corren J、他。持続性喘息患者の治療における 1 日 1 回モメタゾンフランカルボン酸塩乾燥粉末吸入器。アンアレルギー喘息免疫。 2000年; 84:417-24。
3. Karpel JP、Busse WW、Noonan MJ、他。持続性喘息における肺機能および症状制御に対する、1日1回夕方に投与されるフランカルボン酸モメタゾンの効果。アン薬剤師。 2005;39(12):1977-83。
4. バーンスタイン DI、バーコウィッツ RB、チャービンスキー P、他。喘息用の新しいステロイド、モメタゾンフランカルボン酸乾燥粉末吸入器の用量範囲研究。レスピア医学、1999年。 93:602-12。
5. Berger WE、Milgrom H、Chervinsky P、他。持続性喘息の小児におけるフランカルボン酸モメタゾン乾燥粉末吸入器による治療の効果。アンアレルギー喘息免疫。 2006;97:672–80。
6. Karpel JP、Nelson H. モメタゾンフランカルボン酸塩ドライパワー吸入器:持続性喘息の治療のための 1 日 1 回吸入コルチコステロイド。現在の医学研究所の見解。 2007 11 月;23(11):2897-911。
7. 軽度から中等度の持続性喘息の小児に対するミルグロム H. フランカルボン酸モメタゾン、証拠のレビュー。小児科の薬。 2010年。 12(4):213-21。
薬理学的特徴
これは、炎症の内因性化学メディエーター (キニン、ヒスタミン、リポソーム酵素、プロタグランジン) の形成、放出、および活性を低下させることによって作用します。上記の物質によって媒介される反応を開始するには、白血球とマクロファージが存在する必要があります。それは、損傷領域への辺縁化とその後の細胞遊走を阻害し、また拡張と血管透過性の増加を逆転させ、これらの損傷部位への細胞のアクセスを減少させます。
フランカルボン酸モメタゾン (有効成分) は、強力な抗炎症作用を示すコルチコステロイドです。喘息におけるコルチコステロイドの作用機序はまだ完全には理解されていません。炎症は喘息の発症における重要な要素です。コルチコステロイドは、炎症や喘息反応に関与するさまざまな細胞型(マスト細胞、好酸球、好中球、マクロファージ、リンパ球など)やメディエーター(ヒスタミン、エイコサノイド、ロイコトリエン、サイトカインなど)に対して多くの阻害効果をもたらします。コルチコステロイドのこれらの抗炎症作用は、喘息におけるコルチコステロイドの有効性に寄与している可能性があります。フランカルボン酸モメタゾンの機能は、コルチコステロイド受容体への結合に基づいています。これらの受容体はほとんどの細胞型の細胞質に存在し、肺上皮および気管支上皮で高度に発現しています。受容体に結合すると、抗炎症タンパク質を生成する遺伝子が活性化されます。また、気管支の過敏性にも効果があり、1秒間に努力呼気量(PC20)を20%減少させることができます。
フロ酸モメタゾン (活性物質) は、主に CYP3A4 酵素系によって肝臓によって広範囲に代謝されます。 in vitro研究では、フロ酸モメタゾン (活性物質) がヒト糖質コルチコイド受容体との親和性が高く、デキサメタゾン、フルチカゾン、ブデソニド、またはトリアムシノロンよりもはるかに高いことが実証されています。コルチコステロイドには、視床下部下垂体-副腎 (HPA) 軸の活性を抑制する能力があり、負のフィードバックを通じて阻害を引き起こします。フロ酸モメタゾン (活性物質) は、軽度から中等度の喘息患者の HPA 軸機能に最小限の影響を与えます。この薬剤は吸入後の全身への吸収が非常に低く、その影響は主に肺に起こります。フランカルボン酸モメタゾン (活性物質) の半減期は約 5 時間、平均流通量は 152 L です。インビトロでのタンパク質結合率は 98 ~ 99% です。








-1024x576.jpg?resize=1024,576&ssl=1)


