- ピオグリタゾン単独では不十分にコントロールされており、禁忌または不耐症のためにメトホルミンが不適切な患者の血糖コントロール(血糖値)を改善するための食事と運動の補助として。
- メトホルミンとピオグリタゾンの最大耐用量では疾患をコントロールできない、管理が不十分な成人患者の血糖コントロールを改善するための、食事と運動の補助としてのメトホルミンとの併用(すなわち、三剤併用療法)。
この薬は、1 型糖尿病患者や糖尿病性ケトアシドーシス (血液および尿中のケトン体の増加) の治療には推奨されません。

ネシーナ ピオはどのように機能しますか?
Nesina Pio には、2 型糖尿病患者の血糖コントロールを改善するために作用する、相補的で異なる作用機序を持つ 2 つの有効成分が含まれています。 DPP-4 酵素の高度に選択的な阻害剤であるアログリプチンと、チアゾリジンジオン クラスのメンバーであるピオグリタゾン。
ネシナピオの禁忌
次の場合はネシーナ ピオを服用しないでください。
- アログリプチン、ピオグリタゾン、またはこの薬の他の成分に対してアレルギーがある場合。
- 血糖値を制御するために服用している他の同様の薬に対して重篤なアレルギー反応を起こしたことはありますか。重篤なアレルギー反応の症状には、発疹、皮膚の盛り上がった赤い斑点 (蕁麻疹)、顔、唇、舌、喉の腫れが含まれ、呼吸困難や嚥下困難を引き起こす可能性があります。
- 心不全を患っている、または過去に心不全を患ったことがある。
- あなたは肝臓病を患っています。
- あなたは糖尿病性ケトアシドーシス(コントロールが難しい糖尿病の重篤な合併症)を患っています。症状には、過度の喉の渇き、排尿回数の増加、食欲不振、吐き気または嘔吐、および急激な体重減少が含まれます。
- 膀胱がんに罹患している、または罹患したことがある。
- 尿に血が混じっていますが、医師の検査がまだ受けられていない場合は、ネシーナ ピオを服用せず、できるだけ早く医師に尿検査を依頼してください。
ネシナピオの使い方
Nesina Pio の用量は、現在の治療に基づいて医師が決定し、有効成分の推奨最大用量 (アログリプチン 25 mg、ピオグリタゾン 45 mg) を超えない範囲で、薬に対する反応と耐性に応じて調整されます。 )。
ネシーナ ピオは、食事の有無にかかわらず、1 日 1 回服用する必要があります。
治療中に、血糖値をコントロールするために医師がネシーナ ピオの用量を変更する場合があります。医師の指示がない限り、投与量を変更しないでください。
医師の指示に従って、食事と運動のプログラムを維持し、血糖値をチェックしてください。
発熱や感染症などのストレスの多い状況下、事故に遭った場合、または手術を受けた場合には、糖尿病をコントロールするために服用する薬の用量を調整する必要がある場合があります。これらの症状のいずれかに該当する場合は、すぐに医師に相談してください。
腎機能障害のある患者さん
Nesina Pio は、中等度または重度の腎不全、または末期腎疾患の患者には推奨されません。腎機能に応じて投与量を調整する必要があるため、ネシーナ ピオの治療開始前および治療中は定期的に腎機能を評価することが推奨されます。
肝臓病変のある患者
Nesina Pio は肝障害のある患者には投与しないでください。
この薬は割ったり噛んだりしないでください。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
ネシーナピオを使い忘れた場合はどうすればよいですか?
飲み忘れた分は、気づいたらすぐに服用してください。ただし、次の服用時間を覚えている場合は、忘れた分は服用せず、通常の服用時間に戻ってください。ネシーナ ピオを同時に 2 回分服用しないでください。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
ネシナピオの予防措置
次の場合は、ネシーナ ピオを服用する前に医師に相談してください。
- あなたは 1 型糖尿病を患っています (あなたの体はインスリンを生成しません)。
- スルホニル尿素(グリピジド、トルブタミド、グリベンクラミドなど)またはインスリンとして知られる抗糖尿病薬をすでに服用している。ネシーナ ピオと併用した場合、低血糖(血糖値の低下)のリスクを最小限に抑えるために、これらの薬剤の用量を減らす必要がある場合があります。
- 心臓病または体液貯留がある。抗炎症薬を服用している場合は、医師に相談してください。抗炎症薬も体液貯留や腫れを引き起こす可能性があります。体重増加やむくみが生じた場合は医師に相談してください。糖尿病の治療には食事管理も含まれるため、治療ではカロリーを管理した食事に従うことが重要です。
- あなたは高齢で、心臓疾患のリスクが高い可能性があるためインスリンを服用しています。
- 肝臓または腎臓に問題がある。この薬の服用を開始する前に、肝臓と腎臓の機能をチェックするために血液検査を受ける必要があります。この制御は定期的に繰り返す必要があります。原因不明の吐き気、嘔吐、腹痛、倦怠感、食欲不振、尿の色が濃いなど、肝障害を示唆する症状が現れた場合は、肝酵素をチェックする必要があります。 Nesina Pio による治療を継続するかどうかの決定は、検査結果に基づく臨床評価に基づいて行う必要があります。黄疸(皮膚が黄色くなる)が観察された場合は、薬の投与を中止する必要があります。腎臓病の場合、医師はネシーナ ピオの投与量を減らすことがあります。この薬は、透析を必要とする重度の機能障害または末期腎臓病の患者には推奨されません。
- あなたは、黄斑浮腫(目の奥の腫れ)と呼ばれる、糖尿病によって引き起こされる特殊な種類の眼疾患を患っています。
- 卵巣に嚢胞がある(多嚢胞性卵巣症候群)。ネシーナ ピオの治療中に再び排卵する可能性があるため、妊娠の可能性が高くなる可能性があります。これに該当する場合は、予期せぬ妊娠を避けるために適切な避妊を行ってください。
- 血中の糖分の量を制御するために服用している他の薬に対してアレルギー反応を起こしたことがある。症状には、全身のかゆみや熱感が含まれる場合があり、特に頭、口、喉、手のひら、足の裏に影響を及ぼします (スティーブンス・ジョンソン症候群)。アレルギー反応が疑われる場合は、ネシナ ピオの服用を中止する必要があります。
- 膵臓疾患に罹患している、または罹患したことがある。膵炎が疑われる場合は、ネシーナ ピオの投与を中止する必要があります。急性膵炎が確認された場合は、ネシーナ ピオによる治療を再開すべきではありません。膵炎の既往歴のある患者には注意が必要です。
血液検査の細胞数にわずかな変化が現れる場合があります。結果について医師が説明します。
ピオグリタゾンで治療された患者、特に女性では、より多くの骨折が観察されました。医師は糖尿病を治療する際にこの要素を考慮に入れます。
2つの大規模な長期研究では、ピオグリタゾンを使用した糖尿病患者における膀胱がんのリスクに有意な増加は見られなかった。しかし、他の短期研究データは、膀胱がんのリスクがわずかに増加する可能性を示唆しています。小さなリスクを完全に排除することはできないため、活動性膀胱がん患者では治療を開始すべきではなく、膀胱がんの既往歴のある患者では慎重に治療を行う必要があります。治療中に血尿や尿意切迫感などの症状が現れた場合は、直ちに医師の診察を受けるよう患者にアドバイスしてください。
米国で実施された10年間にわたる広範な研究では、ピオグリタゾンに曝露された糖尿病患者では、ピオグリタゾンに曝露されなかった患者と比較して、膀胱がんのリスクが有意に増加することは見出されなかった。さらに、ピオグリタゾン曝露の開始またはその期間以来、累積用量または時間の増加に伴う膀胱がんのリスクの増加はありませんでした。
ヨーロッパ4か国で実施された別の大規模な10年間の研究では、ピオグリタゾンに曝露された糖尿病患者では、ピオグリタゾンに曝露されなかった患者と比較した場合、膀胱がんのリスクに有意な増加は見られなかった。さらに、ピオグリタゾンへの曝露量または曝露期間の累積増加によるリスクの増加は観察されませんでした。ネシーナ ピオによる治療を開始する前に、膀胱がんの危険因子を評価する必要があります(リスクには、年齢、喫煙、一部の作業療法薬や化学療法(シクロホスファミドなど)への曝露、または骨盤領域への以前の放射線療法が含まれます)。治療を開始する前に、尿中の血の発生を調査する必要があります。
治療中に血尿、または排尿困難や尿意切迫感などの症状が現れた場合は、すぐに医師に相談してください。
ネシナ ピオには乳糖が含まれています
医師から特定の糖類に対する不耐症があると言われた場合は、ネシーナ ピオを服用する前に医師に相談してください。
妊娠中および授乳中の使用
ネシーナ ピオが胎児に害を及ぼす可能性があるか、あるいは母乳に移行する可能性があるかどうかは不明です。したがって、妊娠中、妊娠を計画している、または授乳中の場合は、このような状況で血糖値をコントロールする最善の方法について医師に相談してください。授乳中の場合は Nesina Pio を投与しないでください。Nesina Pio の投与が必須であると考えられる場合は、授乳を中止する必要があります。
妊娠リスクカテゴリー C – この薬は医師または歯科外科医のアドバイスなしに妊娠中の女性が使用すべきではありません。
他の薬と併用する
処方薬、市販薬、ビタミン、漢方薬など、服用しているすべての薬について医師に伝えてください。ネシーナ ピオまたは他のいくつかの薬を一緒に使用すると作用に影響を与える可能性があり、その場合はネシーナ ピオの用量または他の薬の用量を変更する必要がある場合があります。
特に、以下の薬を服用している場合は、医師または薬剤師に伝えてください。
- ゲムフィブロジル(コレステロールを下げるために使用);
- リファンピシン(結核およびその他の感染症の治療に使用されます)。
血糖値をチェックし、ネシーナ ピオの投与量を変更する必要がある場合があります。
心臓血管の安全性
アログリプチン
13件の研究データを組み合わせた解析では、心血管死、非致死性心筋梗塞、非致死性脳卒中の全体的な発生率は、アログリプチン25mgを投与された患者と投与されなかった患者(プラセボ投与)で同等であった。
さらに、心血管疾患のリスクが高い患者5,380人を対象に心血管安全性アウトカム研究が実施され、心血管疾患以外の死亡複合イベントの最初の発生までの時間を含む、主要な心血管イベント(MACE)に対するアログリプチンの影響が調べられた。最近(15~90日前)に急性冠動脈イベントを起こした患者における致死性心筋梗塞および非致死性脳卒中。研究開始時の患者の平均年齢は61歳、糖尿病の平均罹患期間は9.2年、平均HbA1c(グリコシル化ヘモグロビン)は8.0%でした。
この研究では、アログリプチンを投与されなかった患者と比較して、アログリプチンはMACE発症のリスクを増加させないことが実証されました。アログリプチン群では患者の 11.3% が MACE を経験し、非アログリプチン群では患者の 11.8% が MACE を経験しました。
ピオグリタゾン
対照臨床研究では、ピオグリタゾン治療による心不全報告の発生率は、プラセボ、メトホルミン、スルホニル尿素(グリピジド、トルブタミド、グリベンクラミドなど)治療群と同等でしたが、心不全治療に関連して使用された場合には増加しました。インスリン。ピオグリタゾンの販売時に心不全が報告されることはほとんどありませんが、ピオグリタゾンをインスリンと併用した場合、または心不全の病歴のある患者に使用した場合に報告されることが多くなりました。
PROactive 心血管アウトカム臨床研究では、2 型糖尿病および既存の重度大血管疾患を有する 5,238 人の患者が、既存の抗糖尿病薬および心血管療法に加えてピオグリタゾンまたはプラセボを最長 3.5 年間投与する群に無作為に割り当てられました。
この結果は、ピオグリタゾンの使用に関して長期的な心血管疾患の懸念がないことを示唆しています。しかし、浮腫(腫れ)、体重増加、心不全の発生率は増加しています。心不全による死亡率の増加は観察されませんでした。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
ネシナ・ピオの副作用
すべての薬と同様に、この薬も副作用を引き起こす可能性がありますが、すべての人が副作用を経験するわけではありません。
以下の重篤な副作用が発生した場合は、Nesina Pio の使用を中止し、直ちに医師に相談してください。
一般的(最大 10 人に 1 人が影響を受ける可能性があります)
突然の重度の骨の痛みまたは動けなくなる(特に女性)。
珍しい(最大 100 人に 1 人が影響を受ける可能性があります)
- 血尿などの膀胱がんの症状。
- 排尿時の痛み。
- 突然の尿意。
不明(入手可能なデータから推定できない)
アレルギー反応の症状には次のようなものがあります。
- 発疹;
- 蕁麻疹;
- 嚥下または呼吸困難。
- 唇、顔、喉、舌の腫れ。
- 失神するような感覚。
重篤なアレルギー反応の症状には次のようなものがあります。
- 全身的なかゆみ(そう痒症)および熱感、特に頭(頭皮)、口、喉、手のひらまたは足の裏に影響を与える(スティーブンス・ジョンソン症候群)。
- 腹部(胃部)の激しく持続的な痛みは背中まで広がる場合があり、膵臓の炎症(膵炎)の兆候である可能性があるため、吐き気や嘔吐を引き起こします。
次の副作用が発生した場合も、医師に相談してください。
一般
ネシーナ ピオをインスリンまたはスルホニル尿素(グリピジド、トルブタミド、グリベンクラミドなど)と組み合わせて摂取すると、低血糖(低血糖)の症状が発生することがあります。
症状には次のようなものがあります。
- 震え、発汗、不安、かすみ目、唇のチクチク感、顔面蒼白、気分の変化、混乱感。血糖値は正常レベルより下がることがありますが、砂糖を摂取すると再び血糖値が上昇することがあります。砂糖、お菓子、ビスケット、または加糖フルーツジュースのパックを常に持ち歩くことをお勧めします。
- 喉の痛み、鼻詰まり、鼻水など、風邪やインフルエンザに似た症状。
- 皮膚のかゆみ;
- 頭痛;
- 胃の痛み;
- 下痢;
- 消化不良、胸やけ;
- 倦怠感;
- 筋肉痛;
- 睡眠困難。
- 体のどの部分のしびれ;
- 視界がぼやけたり歪んだりする。
- 体重増加。
- 手と足の腫れ。
珍しい
- 皮膚の発疹。
未知
- 視力障害(黄斑浮腫と呼ばれる問題によって引き起こされる)。
- 吐き気や嘔吐、腹痛、異常または原因不明の倦怠感、食欲不振、尿の色が濃くなる、皮膚や白目が黄色くなるなどの肝臓の問題。
注意:
この製品は国内で新たに承認された医薬品であり、研究により許容できる有効性と安全性が示されていますが、たとえ正しく適応され使用されたとしても、予測できないまたは未知の副作用が発生する可能性があります。この場合は医師に知らせてください。
ネシナ ピオの特別人口
小児および青少年への使用
ネシーナ ピオは、18 歳未満の小児および青少年には、これらの患者に関するデータが不足しているため推奨されません。
車両の運転と機械の使用
この薬による治療中に視覚障害が発生する場合があります。このような場合は、運転したり、機械や工具を使用したりしないでください。ネシーナ ピオを他の抗糖尿病薬と組み合わせて服用すると、血糖値の低下(低血糖)を引き起こす可能性があり、運転や機械の使用能力に影響を与える可能性があります。
ネシナ・ピオの組成
プレゼンテーション
コーティング錠 25 mg + 15 mg – 30 錠が入ったパック。
コーティング錠 25 mg + 30 mg – 10 錠または 30 錠が入ったパック。
経口使用。
大人用。
構成
各コーティング錠剤には次のものが含まれます。
ネシーナ ピオ 25 mg + 15 mg:
| アログリプチン安息香酸塩 |
34mg* |
| 塩酸ピオグリタゾン |
16.53mg** |
※アログリプチン25mgに相当します。
**ピオグリタゾン 15 mg に相当します。
賦形剤:
マンニトール、微結晶セルロース、ヒドロキシプロピルセルロース、クロスカルメロースナトリウム、ステアリン酸マグネシウム、乳糖一水和物、ヒプロメロース、ポリエチレングリコール、二酸化チタン、タルク、黄酸化鉄。
ネシーナ ピオ 25 mg + 30 mg:
| アログリプチン安息香酸塩 |
34mg* |
| 塩酸ピオグリタゾン |
33.06mg** |
※アログリプチン25mgに相当します。
**ピオグリタゾン 30 mg に相当します。
賦形剤:
マンニトール、微結晶セルロース、ヒドロキシプロピルセルロース、クロスカルメロースナトリウム、ステアリン酸マグネシウム、乳糖一水和物、ヒプロメロース、ポリエチレングリコール、二酸化チタン、タルク、黄色酸化鉄および赤色酸化鉄。
ネシナ・ピオの過剰摂取
ネシーナ ピオを過剰に投与した場合は医師に相談してください。治療は、その人が示す症状と臨床徴候に応じて決定されます。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。
さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
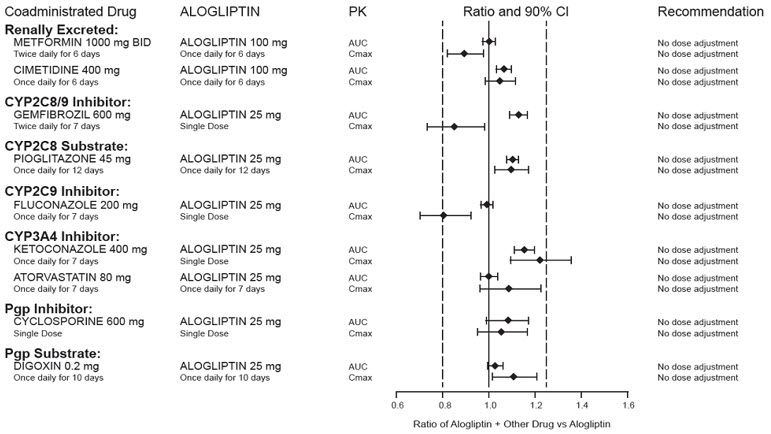
ネシナ・ピオの薬物相互作用
アログリプチン
アログリプチンは主に腎臓を介して排泄され、シトクロム (CYP) 関連の代謝は重要ではありません。試験したCYP基質や阻害剤、あるいは腎臓から排泄される医薬品との薬物相互作用は観察されなかった。
強力なCYP2C8阻害剤
ピオグリタゾン
CYP2C8 阻害剤(ゲムフィブロジルなど)は、ピオグリタゾンの曝露量(濃度時間曲線下面積または AUC)と半減期を大幅に増加させます。したがって、ゲムフィブロジルまたは他の強力な CYP2C8 阻害剤と組み合わせて使用する場合、ピオグリタゾンの推奨最大用量は 1 日あたり 15 mg です。
CYP2C8誘導剤
ピオグリタゾン
CYP2C8 誘導剤 (リファンピシンなど) は、ピオグリタゾンの曝露 (AUC) を大幅に減少させる可能性があります。したがって、Nesina Pio による治療中に CYP2C8 誘導剤の投与を開始または中止した場合、ピオグリタゾンの 1 日最大推奨用量 45 mg を超えない範囲で、臨床反応に基づいて糖尿病治療を変更する必要がある可能性があります。
ピオグリタゾンをスルホニル尿素またはインスリンと一緒に投与すると、低血糖が発生することがあります。
インスリンまたは他の抗糖尿病薬(特にスルホニルウレアなどのインスリン分泌促進薬)と組み合わせてピオグリタゾンを投与されている患者は、低血糖症のリスクがある可能性があります。低血糖のリスクを軽減するには、併用投与される抗糖尿病薬の用量を減らすことが必要な場合があります。
アログリプチン
アログリプチンは主に腎臓を介して排泄され、シトクロム (CYP) 関連の代謝は重要ではありません。試験したCYP基質や阻害剤、あるいは腎臓から排泄される医薬品との薬物相互作用は観察されなかった。
強力なCYP2C8阻害剤
ピオグリタゾン
CYP2C8 阻害剤(ゲムフィブロジルなど)は、ピオグリタゾンの曝露量(濃度時間曲線下面積または AUC)と半減期を大幅に増加させます。したがって、ゲムフィブロジルまたは他の強力な CYP2C8 阻害剤と組み合わせて使用する場合、ピオグリタゾンの推奨最大用量は 1 日あたり 15 mg です。
CYP2C8誘導剤
ピオグリタゾン
CYP2C8 誘導剤 (リファンピシンなど) は、ピオグリタゾンの曝露 (AUC) を大幅に減少させる可能性があります。したがって、Nesina Pio による治療中に CYP2C8 誘導剤の投与を開始または中止した場合、ピオグリタゾンの 1 日最大推奨用量 45 mg を超えない範囲で、臨床反応に基づいて糖尿病治療を変更する必要がある可能性があります。
ピオグリタゾンをスルホニル尿素またはインスリンと一緒に投与すると、低血糖が発生することがあります。
インスリンまたは他の抗糖尿病薬(特にスルホニルウレアなどのインスリン分泌促進薬)と組み合わせてピオグリタゾンを投与されている患者は、低血糖症のリスクがある可能性があります。低血糖のリスクを軽減するには、併用投与される抗糖尿病薬の用量を減らすことが必要な場合があります。
物質ネシナ・ピオの作用
有効性の結果
アログリプチンとピオグリタゾンの併用投与は、食事と運動だけでは、またはメトホルミンだけでは適切にコントロールできない2型糖尿病患者を対象に研究されています。
この薬の有効性と安全性を裏付けるために行われた臨床研究では、アログリプチンとピオグリタゾンを別々の錠剤として同時投与することが含まれていました。生物学的同等性研究の結果、この医薬品は、対応する用量のアログリプチンとピオグリタゾンを別々の錠剤として同時投与した場合と生物学的に同等であることが実証され、アログリプチンとピオグリタゾンの併用の有効性は、4件の第III相有効性研究で実証されました。
2 型糖尿病患者において、この薬による治療は、アログリプチンまたはピオグリタゾン単独と比較して、臨床的および統計的に HbA1C の有意な改善をもたらしました。 2 型糖尿病の治療薬の研究では典型的なことですが、この薬による HbA1C の平均低下は、ベースライン HbA1C の上昇の程度に関連しているようです。
食事と運動で適切にコントロールできない2型糖尿病患者におけるアログリプチンとピオグリタゾンの併用投与
二重盲検、実薬対照、26週間の研究では、食事と運動だけでは適切にコントロールされていない655人の患者(平均ベースラインHbA1C = 8.8%)が、アログリプチン25 mg単独、ピオグリタゾン単独30 mg、アログリプチン12.5 mgの投与を受ける群に無作為に割り付けられた。 1日1回、30 mgのピオグリタゾンと30 mgのピオグリタゾン、または25 mgのアログリプチンと30 mgのピオグリタゾンを併用します。 25 mgのアログリプチンと30 mgのピオグリタゾンの同時投与による治療では、25 mgのアログリプチン単独または30 mgのピオグリタゾン単独と比較して、ベースライン値と比較して糖化ヘモグロビン(Hb A1C)および空腹時血糖値が統計的に有意に減少しました(表1) )。アログリプチン 25 mg とピオグリタゾン 30 mg を 1 日 1 回同時投与すると、薬物単独の投与と比較して、第 2 週から第 26 週まで空腹時血糖値が統計的に有意に減少しました。 25 mgのアログリプチンと30 mgのピオグリタゾンを併用した患者の合計3%、25 mgのアログリプチンを単独で投与された患者の11%、および30 mgのピオグリタゾンを単独で投与された患者の6%が高血糖救済を必要とした。
HbA1C の減少は、性別、年齢、ベースライン BMI の影響を受けませんでした。
体重の平均増加は、ピオグリタゾン単独とアログリプチンをピオグリタゾンと同時投与した場合との間で同様であった。
表1:食事と運動のコントロールが不十分な患者におけるアログリプチンとピオグリタゾンの同時投与の研究における26週目の血糖パラメータ
a 研究の最後の観察を使用した治療意図のある集団。
b最小二乗とは、治療、地理的地域、およびベースライン値に対して調整されたことを意味します。
c plt;25 mg アログリプチンまたは 30 mg ピオグリタゾンと比較して 0.01。
メトホルミン単独では適切にコントロールできない2型糖尿病患者におけるアログリプチンとピオグリタゾンの併用投与

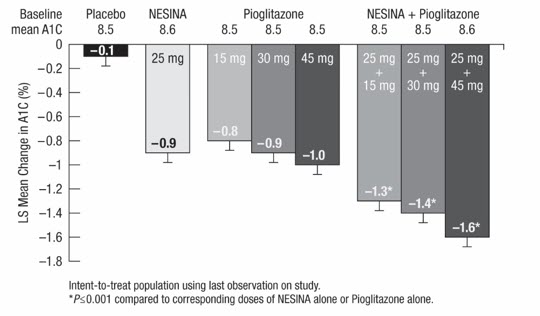
2 番目の 26 週間の二重盲検プラセボ対照研究では、メトホルミンを投与されている 1,554 人の患者 (ベースライン平均 HbA1C = 8.5%) が、12 の二重盲検治療群の 1 つに無作為に割り付けられました。アログリプチン単独 12.5 mg または 25 mg。 15 mg、30 mg、または45 mgのピオグリタゾン単独、または12.5 mg、または25 mgのアログリプチンと15 mg、30 mg、または45 mgのピオグリタゾンの併用。患者は、治療期間を通じて安定した用量の塩酸メトホルミン(用量中央値 = 1700 mg)を維持されました。アログリプチンとピオグリタゾンの同時投与は、メトホルミンによる基本治療に加えた場合、アログリプチン単独またはピオグリタゾン単独の場合、プラセボと比較して、HbA1Cおよび空腹時血糖値の統計的に有意な改善をもたらしました(表2、図1)。 25 mgのアログリプチンと15 mg、30 mg、または45 mgのピオグリタゾンを投与された患者は、プラセボ(33%)、25 mgのアログリプチンを単独で投与された患者(13%)と比較して、高血糖救済の必要性が低かった(4%、5%、2%)。またはピオグリタゾン単独 15 mg、30 mg、または 45 mg (10%、15%、9%)。
HbA1C レベルの改善は、性別、年齢、ベースライン BMI の影響を受けませんでした。
体重の平均増加は、ピオグリタゾン単独とアログリプチンをピオグリタゾンと同時投与した場合との間で同様であった。
表 2: 2 型糖尿病患者におけるアログリプチンとピオグリタゾンの単独および併用の 26 週目の血糖パラメーター
ALO = アログリプチン; IOP = ピオグリタゾン。
a 研究中の最後の観察を使用した、治療意図のある集団。
b最小二乗は、治療、地理的地域、メトホルミン用量、およびベースライン値について調整されたことを意味します。ピオグリタゾンおよびアログリプチン単独と比較した場合、cp -0.01。
図 1: アログリプチンとピオグリタゾン単独、およびメトホルミンにアログリプチンとピオグリタゾンを組み合わせた場合の 26 週目でのベースライン HbA1C の変化
ベースライン平均 A1C = ベースライン平均 HbA1C。
アログリプチン=アログリプチン。
ピオグリタゾン = ピオグリタゾン。
アログリプチン + ピオグリタゾン = アログリプチン + ピオグリタゾン。
A1C の LS 平均変化 (%) = HbA1C の最小二乗平均変化 (%)。
研究の最後の観察を使用した治療意図のある集団。
*対応する用量のアログリプチンまたはピオグリタゾン単独と比較した場合の plt;0.001。
メトホルミンとピオグリタゾンの併用で適切にコントロールされていない2型糖尿病患者における補助療法としてのアログリプチン
52週間の積極的な比較研究では、803人の患者が、ピオグリタゾン30 mgと1日あたり少なくとも1500 mgのメトホルミン、または最大耐用量までの現在のレジメンでは適切にコントロールされなかった(平均ベースラインHbA1C = 8.2%)。 25 mgのアログリプチンを追加するか、4週間の単盲検プラセボ登録期間後にピオグリタゾンを30 mgから45 mgに用量漸増するかのいずれかです。患者は安定した用量の塩酸メトホルミン(用量中央値 = 1700 mg)を維持しました。
52週間の治療期間中に事前に指定された血糖値を達成できなかった患者は血糖レスキュー療法を受けた。
ピオグリタゾンおよびメトホルミンと併用した場合、25 mg 用量のアログリプチンは、ピオグリタゾンを 30 mg から 45 mg に漸増した場合と比較して、26 週目から 52 週目までの HbA1C および空腹時血糖値の低下において統計的に優れていました (表 3、結果は 52 週目のみを示しています)。 。アログリプチン 25 mg とピオグリタゾン 30 mg およびメトホルミンの併用投与を受けた患者(11%)は、ピオグリタゾン 30 mg から 45 mg に用量漸増でメトホルミンと併用投与された患者(22%)と比較して、高血糖救済を必要とする患者が有意に少なかった。
HbA1C レベルの改善は、性別、年齢、人種、ベースライン BMI の影響を受けませんでした。体重の平均増加量は両治療群で同様でした。一般に、脂質の影響は中立でした。
表 3: メトホルミンとピオグリタゾンの補助併用療法としてのアログリプチンの実薬対照研究における 52 週目の血糖パラメーター
|
アログリプチン 25 mg + ピオグリタゾン 30 mg + メトホルミン |
ピオグリタゾン 45 mg + メトホルミン |
|
|
HbA1C (%) |
N = 397 |
N = 394 |
|
基礎値(平均) |
8.2 |
8.1 |
|
ベースラインからの変動 (調整平均b ) |
-0.7 |
-0.3 |
|
45 mg ピオグリタゾン + メトホルミンと比較した差 (95% 信頼区間による調整平均b ) |
-0.4c (-0.5; -0.3) |
— |
|
HbA1c を達成した患者の割合 (n/N) 7% c,d |
33% (134/404) d |
21% (85/399) |
|
空腹時血糖値 (mg/dL) c |
N=399 |
N=396 |
|
基礎値(平均) |
162 |
162 |
|
ベースラインからの変動 (調整平均b ) |
-15 |
-4 |
|
45 mg ピオグリタゾン + メトホルミンと比較した差 (95% 信頼区間による調整平均b ) |
-11日(-16; -6) |
— |
|
a 研究中の最後の観察を使用した、治療意図のある 集団 。 b 最小二乗は、治療、ベースライン、地理的地域、およびベースラインのメトホルミン用量について調整されたことを意味します。 c 片側有意水準 0.025 では、メトホルミンとピオグリタゾンより非劣性であり、統計的に優れています。 メトホルミン + ピオグリタゾン 45 mg と比較した d plt;0.001。 |
||
チアゾリジンジオンによるアログリプチンの補助療法
チアゾリジンジオン単独またはメトホルミンとの併用でコントロールが不十分な2型糖尿病患者計493人を対象に、ピオグリタゾンへの追加療法としてのアログリプチンの有効性と安全性を評価するために、26週間のプラセボ対照試験が実施された。またはスルホニル尿素(平均ベースライン HbA1C = 8%)を、アログリプチン 12.5 mg、アログリプチン 25 mg、またはプラセボのいずれかに無作為に割り付けました。患者は治療期間中、安定した用量のピオグリタゾン(用量中央値 = 30 mg)で維持され、ランダム化前に以前にメトホルミン(用量中央値 = 2000 mg)またはスルホニル尿素(用量中央値 = 10 mg)でも治療されていた患者も維持された。治療期間中に併用治療を受けている。すべての患者は、無作為化の前に 4 週間の単盲検プラセボ登録期間に入りました。無作為化後、すべての患者は引き続き食事と運動についての指導を受けました。 26週間の治療期間中に事前に指定された高血糖レベルを達成できなかった患者は、血糖レスキューを受けました。
ピオグリタゾン治療に 1 日 1 回 25 mg のアログリプチンを追加すると、プラセボの追加と比較して、26 週目にベースライン HbA1C および空腹時血糖が大幅に改善されました (表 4)。研究期間中、25 mgのアログリプチンを投与された患者の9%が高血糖救済を必要としたのに対し、プラセボを投与された患者では12%でした。
HbA1C の改善は、性別、年齢、ベースライン BMI、またはピオグリタゾンのベースライン用量の影響を受けませんでした。ピオグリタゾンと組み合わせて投与した場合、体重の平均増加量はアログリプチンとプラセボの間で同様でした。脂質の影響は中立でした。
表4:ピオグリタゾンの追加療法としてのアログリプチンのプラセボ対照研究における26週目の血糖パラメータ
|
アログリプチン 25 mg + ピオグリタゾン |
プラセボ + ピオグリタゾン |
|
|
HbA1C (%) |
N = 195 |
N = 95 |
|
基礎値(平均) |
8 |
8 |
|
ベースラインからの変化 (調整平均b ) |
-0.8 |
-0.2 |
|
プラセボとの違い (95% 信頼区間による調整平均b ) |
-0.6 ℃ (-0.8; -0.4) |
— |
|
HBA1C に達した患者の割合 (n/n)? |
49% (98/199) C |
34 % (33/97) |
|
空腹時血糖値 (mg/dL) |
N = 197 |
N = 97 |
|
基礎値(平均) |
170 |
172 |
|
基礎値に対する変化(調整平均値b ) |
-20 |
-6 |
|
プラセボとの差(95%の信頼区間による調整平均B) |
-14 ℃ (-23; -5) |
— |
|
研究中の最後の観察を使用した 治療 集団。 B 治療、基礎値、地理的地域、基礎治療スキーム (ピオグリタゾン、メトホルミン ピオナグリタゾン、またはスルホニルウレア ピオグリタゾン) およびピオグリタゾンの基礎用量について調整された最小二乗の平均。 CPLT ;プラセボと比較して 0.01 |
||
薬理学的死骸
作用機序
この薬は、2 型糖尿病患者の血糖コントロールを改善するための相補的かつ異なる作用機序を持つ 2 つの抗血糖薬の組み合わせです。アログリプチンはジペプチジル ペプチダーゼ 4(DPP-4)の選択的阻害剤であり、ピオノグリタゾンはチアゾリジンジオンのクラスのメンバー。
アログリプチン
グルカゴン様ペプチド 1 (GLP-1) やインスリン分泌性グルコース (GIP) ポリペプチドを含むインクレデチン ホルモンの濃度が増加し、食事の摂取に反応して小腸から血流中に放出されます。これらのホルモンは、グルコースに依存して膵臓ベータ細胞からのインスリン放出を引き起こしますが、DPP-4 酵素によって数分以内に不活化されます。 GLP-1 はまた、α膵臓細胞からのグルカゴン分泌を減少させ、肝グルコースの生成を減少させます。 2 型糖尿病患者では、LPG-1 濃度は低下しますが、LPG-1 に対するインスリンの応答は維持されます。アログリプチンは、インクレデチン ホルモンの不活性化を遅らせる DPP-4 阻害剤で、インクレデチン ホルモンの血流中濃度を高め、2 型糖尿病患者の食後血糖値と空腹時血糖値を低下させます。
ピオグリタゾン

薬理学的研究は、ピオグリタゾンが肝臓の糖新生を阻害しながら、筋肉および脂肪組織のインスリン感受性を改善することを示しています。スルホニル尿素とは異なり、ピオネゾンはインスリンを分泌しません。ピオグリタゾンは、ペルオキシソーム (PPAR?) 増殖因子によって活性化されるガンマ受容体のアゴニストです。 PPAR受容体は、脂肪組織、骨格筋、肝筋などのインスリン作用にとって重要な組織に存在します。核内受容体PPARの活性化?それは、グルコースおよび脂質代謝の制御に関与する多くのインスリン応答性遺伝子の転写を調節します。
糖尿病の動物モデルでは、ピオグリタゾンは、2 型糖尿病などのインスリン抵抗性状態の高血糖、高インスリン血症、および高トリグリセリド血症の特徴を軽減します。ピオグリタゾンによって引き起こされる代謝変化は、インスリン依存性組織からの反応の増加をもたらし、多くのインスリン抵抗性動物モデルで観察されます。
ピオナグリタゾンは(インスリン抵抗性を低下させることにより)循環インスリンの効果を高めるため、内因性インスリンを持たない動物モデルでは血糖値を低下させません。
薬力学特性
アログリプチン / ピオノグリタゾン
2型糖尿病の患者が30 mgピオグリタゾン、12.5 mgのピオグリプチンピオグリプチン30 mgのアログリプチン、25 mgのアログリプチン分離または30 mgの分離または30 mgの分離または30 mgの分離または30 mgの分離または30 mgの分離または30 mgの分離または30 mgの分離アログリプチンを含む25 mgの同時アログリプチンを投与された26週間の資産制御研究では、無作為化された26週間の資産制御研究で、30 mgピオグリタゾンを含む25 mgのアログリプチンに無作為化された患者は、1つの平均基底値と比較して、トリグリセリドレベルで26.2%の減少であり、1つの平均基底値と比較して、分離アログリプチンで11.5%減少し、21.8%の減少とともに11.5%減少しました。パイオノゾーン。さらに、コレステロールHDLレベルの14.4%の増加も観察されました。平均基底値は、30 mgのピオナグリタゾンを使用した平均基底値43.2 mg/dLから25 mgのアログリプチンで、分離アログリプチンの1.9%の増加と増加と比較して、孤立したパイオゾンの13.2%。 LDLコレステロールと総コレステロール測定の変化は、アログリタゾン30 mgとアログリプチン分離および単離されたピオグリタゾンとのアログリプチン25 mgの間で類似していた。同様のパターンの脂質効果が、26週間のプラセボ制御要因検査で観察されました。
アログリプチン
アログリプチンから健康な個人への単回投与の投与は、投与後2〜3時間以内にDPP-4阻害のピークをもたらしました。 DPP-4阻害ピークは1の用量で93%を超えました








-1024x576.jpg?resize=1024,576&ssl=1)


