ロタウイルスによる下痢を患う小児のほとんどは、大きな問題なく治癒する病気です。重度の嘔吐や下痢、体液の喪失などの重篤な症状に陥る人もおり、脱水症状による死亡の危険があり、入院が必要になります。ロタウイルス感染は、世界中で、特に栄養と医療が依然として最適とは言えない発展途上国で、毎年数十万人の死者を出しています。
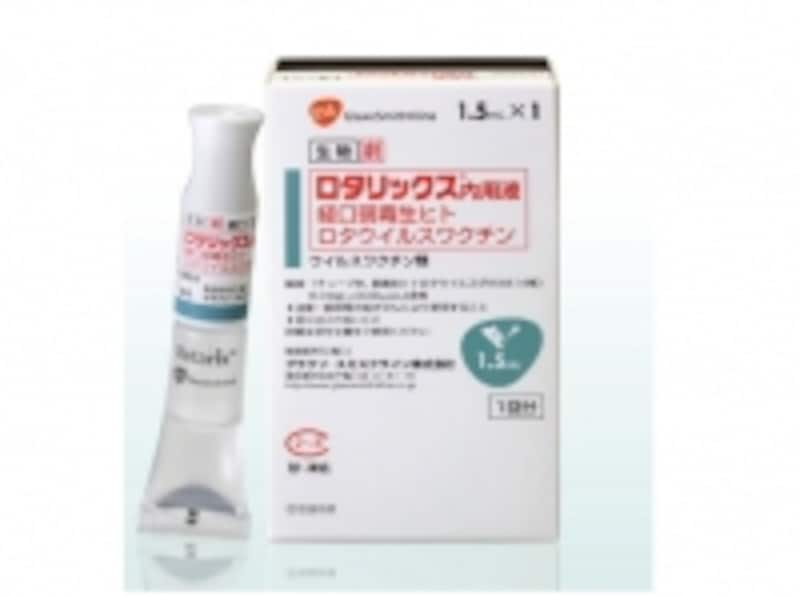
ロータリックスはどのように機能しますか?
個人がワクチンを受けると、その免疫系(体の自然防御システム)は、最も頻繁に発生するタイプのロタウイルスに対する抗体を生成します。このような抗体は、ロタウイルスによって引き起こされる将来の感染を防ぎます。
ロタリックス® は、ロタウイルスによる胃腸炎からお子様のみを保護します。ワクチンは、胃腸炎を引き起こす他の感染症からお子様を守ることはできません。

すべてのワクチンと同様、ロタリックス® はワクチン接種を受けたすべての子供を完全に保護できるわけではありません。
ロタリックスの禁忌

Rotarix ® は、このワクチンまたはその配合成分に対して過敏症 (アレルギー) があることがわかっている小児には投与しないでください。アレルギー反応の兆候には、かゆみのある発疹、息切れ、顔や舌の腫れなどがあります。
ロタリックス® は、腸重積症(腸の一部分が別の部分の中に折り畳まれてしまう腸閉塞)の病歴のある小児には投与しないでください。

ロタリックス® は、腸重積を起こしやすい消化管の未矯正の先天奇形(メッケル憩室など)を持つ小児には投与すべきではありません。
ロタリックス® は、HIV 陽性患者や、重症複合免疫不全症 (SCID) と呼ばれる、免疫系に影響を与える稀な遺伝性疾患を患っている患者など、既知の一次免疫不全症または続発性免疫不全症のある小児には投与しないでください。
ロタリックスの使い方
経口使用。
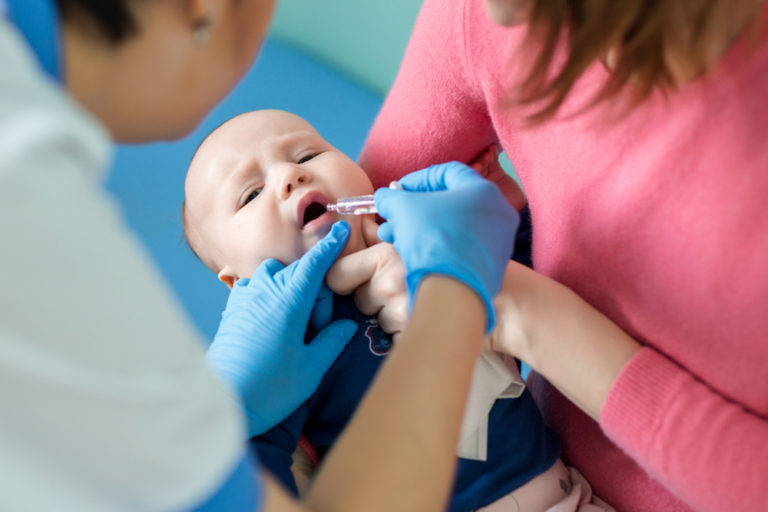
使用および取り扱い上の注意事項
ワクチンは、経口投与用に、目に見える粒子を含まない透明な無色液体として提供されます。
ワクチンはすぐに使用できます (再構成または希釈する必要はありません)。
ワクチンは、他のワクチンや溶液と混合せずに経口投与する必要があります。

投与前に、ワクチンに異物や異常な外観がないか目視検査する必要があります。観察された場合は、ワクチンを廃棄してください。
ワクチンは経口投与のみです。ワクチンを受けるときは、お子様は横たわった姿勢で座らなければなりません。シリンジの内容物をすべて頬の内側に経口投与します。未使用のワクチンや廃棄物は注射しないでください。地域の要件に従って処分する必要があります。
経口アプリケーターを使用してワクチンを投与するための説明書
- 口腔アプリケーターから保護キャップを取り外します。
- このワクチンは経口投与のみです。お子様はリクライニングした姿勢で座らなければなりません。経口アプリケーターの内容物全体を経口(つまり、子供の口の中、頬の内側)に投与します。
注射しないでください。
非互換性
この製品は他の医薬品と混合しないでください。
ロタリックスの投与量
ワクチン接種は2回の接種で構成されます。初回の投与は生後6週間以降に行う必要があります。投与間隔は少なくとも 4 週間空ける必要があります。ワクチン接種スケジュールは、できれば生後 16 週までに接種する必要がありますが、生後 24 週まで完了することができます。
ロタリックス® は、少なくとも妊娠 27 週以降に生まれた未熟児に投与できます。
臨床研究では、乳児がワクチンを吐き出したり吐き戻したりすることはほとんど観察されず、そのような状況が発生した場合、補充用量は投与されませんでした。ただし、万が一、乳児がワクチン投与量の大部分を吐き出したり吐き戻したりした場合には、同じワクチン接種予約時に代替用量を 1 回投与することがあります。 Rotarix ®を 1 回接種した乳児は、同じワクチンの 2 回目の接種でスケジュールを完了することが強く推奨されます。
Rotarix® は経口使用のみを目的としています。
Rotarix ® は、いかなる状況においても注射してはなりません。
ワクチン接種の前後において、乳児が母乳を含む食べ物や飲み物を摂取することに制限はありません。
入手可能な臨床研究で得られた証拠に基づいて、Rotarix ®が提供するロタウイルスによって引き起こされる胃腸炎に対する母乳育児の防御力は低下しないことが判明しました。したがって、ワクチン接種スケジュール中は母乳育児を維持できます。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。医師の知識なしに治療を中止しないでください。
ロタリックスの使用を忘れた場合はどうすればよいですか?
再診に関しては医師または看護師の指示に従うことが重要です。予防接種を予約日に忘れた場合は、医師に相談してください。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
ロタリックスの予防措置
Rotarix ® は経口のみで投与する必要があります。
Rotarix ® は、いかなる状況においても注射してはなりません。
ワクチン接種の前に、病歴(主に以前のワクチン接種と望ましくない事象の発生の可能性に関する)の評価と臨床検査が行われることが優良臨床実践の原則です。
他のワクチンと同様、急性の重度の発熱性疾患を患っている小児へのロタリックス®の投与は延期する必要があります。ただし、風邪などの軽度の感染症の場合はワクチン接種を延期せず、まず医師に相談してください。
下痢または嘔吐のある乳児へのロタリックス®の投与は延期する必要があります。
胃腸疾患のある乳児におけるロタリックス®の安全性と有効性に関するデータはありません。医師の意見において、投与しない方がリスクが大きくなる場合には、これらの乳児へのロタリックス®の投与は慎重に検討する必要があります。
腸重積症のリスクは、ラテンアメリカとフィンランドで実施された大規模な安全性研究(63,225人の子供を対象)で評価されました。この臨床研究では、ロタリックス®の投与後にプラセボと比較して腸重積症のリスクの増加は観察されませんでした。
しかし、市販後の安全性研究では、ワクチン接種後の腸重積の発生率が一時的に高く、主に初回接種後 7 日以内、程度は低いが 2 回目の接種後であることが示されています。腸重積症の全体的な発生率は依然としてまれです。ロタリックス® が腸重積症の全体的なリスクに影響を与えるかどうかは確立されていません。
したがって、予防措置として、医療専門家は腸重積を示す症状(重度の腹痛、持続的な嘔吐、血便、腹部の腫れ、および/または高熱)を監視する必要があります。保護者には、これらの症状を直ちに報告するようアドバイスしてください。
研究で観察された G2P[4] および G3P[8] 血清型の症例数が限られていたため、信頼区間が広く、統計的有意性を証明することはできませんでした。
免疫抑制療法を受けている小児を含め、免疫不全状態の小児へのロタリックス®の投与は、潜在的な利益とリスクを慎重に考慮して行う必要があります。
糞便中のワクチンウイルスの除去はワクチン接種後起こり、平均して10日間続き、7日目あたりに排泄のピークとなることが知られています。臨床研究では、臨床症状を引き起こすことなく、排泄されたワクチンウイルスがワクチン接種者の血清反応陰性接触者に伝播するケースが観察された。ロタリックス®は、悪性腫瘍などによる免疫不全状態、またはその他の免疫不全状態にある患者、または免疫抑制療法を受けている患者の濃厚接触者がいる場合には、慎重に投与する必要があります。
最近ワクチン接種を受けた子供たちと接触した人は、子供たちのおむつを交換する際に(手洗いを含む)衛生状態を注意深く観察するようアドバイスする必要があります。
他のワクチンと同様に、すべてのワクチン接種者に防御免疫反応が誘導されるわけではありません。
臨床研究では流行していないロタウイルス株に対して Rotarix ® がどの程度の防御を提供できるかは不明です。
ロタリックス® は、ロタウイルス以外の病原体によって引き起こされる胃腸炎を予防するものではありません。
妊娠中または授乳中の使用に関するヒトのデータは入手できず、動物の生殖に関する研究も行われていません。
糖尿病の方は注意:砂糖が含まれています。
ロタリックスの副作用
すべての子供が経験するわけではありませんが、他の医薬品と同様に、ロタリックス® も望ましくない反応を引き起こす可能性があります。ロタリックス®を単独で投与した(定期的なワクチン投与を時間差で投与した)3件のプラセボ対照臨床研究では、要求された症状、下痢、嘔吐、食欲不振、発熱、イライラ、咳/鼻水の発生率と重症度は評価されませんでした。ロタリックス®を投与されたグループでは、プラセボを投与されたグループと比較して、有意な差がありました。ロタリックス®を定期小児ワクチンと併用投与した研究(「薬物相互作用」の項目を参照)を含む、17件のプラセボ対照臨床研究の統合解析では、以下に挙げる副作用(ワクチン接種後31日後に収集)が発生する可能性があると考えられました。ワクチン接種に関連して。
一般的な反応 (>1/100 および <1/10)
下痢、イライラ。
まれな反応 (>1/1,000 および <1/100)
腹痛(以下の非常にまれな腸重積反応の兆候も参照)、鼓腸、皮膚炎。
腸重積症のリスクは、ラテンアメリカとフィンランドで63,225人を対象に実施された大規模な臨床研究で評価された。この研究では、次の表に示すように、ロタリックス®を投与されたグループではプラセボと比較して腸重積症のリスクが増加していないという証拠が得られました。
|
– |
ロタリックス® |
プラセボ |
相対リスク (95% CI) |
|
投与後31日以内に腸重積を起こした場合 |
n=31,673 |
n=31,552 |
– |
|
初回投与量 |
1 | 2 |
0.50 (0.07; 3.80) |
|
2回目の投与 |
5 | 5 |
0.99 (0.31; 3.21) |
|
1歳までの腸重積 |
n=10,159 |
n=10,010 |
– |
|
初回接種は1歳まで |
4 | 14 |
0.28 (0.10; 0.81) |
CI:
信頼区間。
未熟児に対する安全性
臨床研究では、1,009 人の未熟児に Rotarix ®凍結乾燥粉末またはプラセボが投与されました (198 人は在胎週数 27 ~ 30 週、801 人は在胎週数 31 ~ 36 週)。初回投与は生後6週間から行いました。重篤な有害事象は、ロタリックス®を服用した患者の 5.1% で観察されたのに対し、プラセボを服用した患者では 6.8% でした。 2つのグループは、研究で観察された要請症状と非要請症状の割合が同様でした。腸重積症の症例は報告されていません。
超未熟児(妊娠 28 週で生まれた)、特に呼吸器未熟の既往歴のある乳児に初回投与を行う場合は、無呼吸の潜在的なリスクと 48 ~ 72 時間の呼吸モニタリングの必要性を考慮する必要があります。
市販後データ
まれな反応 (>1/10,000 および <1/1,000)
血便(血便)、重度複合免疫不全症と呼ばれる稀な遺伝性疾患を患っている子供は、便中のワクチンウイルスの除去に伴って胃や腸に炎症(胃腸炎)を起こすことがあります。胃腸炎の兆候には、倦怠感、吐き気、胃けいれん、下痢などがあります。
非常にまれな反応 (lt; 1/10,000)
腸重積症(腸の一部が詰まっているか、ねじれている状態)。兆候には、重度の腹痛、持続的な嘔吐、血便、腹部の腫れ、および/または高熱が含まれる場合があります。お子様にこれらの症状がある場合は、直ちに医師/医療提供者に連絡してください。
注意:本製品は国内で新たな治療適応を有する医薬品であり、研究により許容できる有効性と安全性が示されていますが、たとえ正しく適応・使用されたとしても、予測できない、または未知の有害事象が発生する可能性があります。この場合は医師に知らせてください。
ロータリックス特別集団
大人や高齢者の使用
Rotarix ® は成人または高齢者への使用を目的としていません。
ロタリックスの構成
ワクチンの各 1.5 mL 用量には次のものが含まれます。
生弱毒化ヒトロタウイルス RIX4414 株、最小濃度 106.0 CCID50。
賦形剤:
スクロース、アジピン酸二ナトリウム、ダルベッコ変法イーグル培地、滅菌水。
無駄:
ブタサーコウイルス 1 型 (PCV-1) 物質が Rotarix ®で検出されました。 PCV-1 が動物に病気を引き起こすことは知られておらず、また人間に感染したり病気を引き起こしたりすることも知られていません。 PCV-1 の存在が安全上のリスクを引き起こすという証拠はありません。
ロタリックスのプレゼンテーション
経口懸濁液。 Rotarix ® は、1 回分 (1.5 mL) を含む経口投与用のプレフィルドシリンジ 1 本が入ったパッケージで提供されます。
経口使用。
小児には6週目から使用可能。
ロタリックスの過剰摂取
過剰摂取の事例も報告されています。一般に、これらの場合の副作用のプロファイルは、推奨用量の Rotarix ®の投与後に観察されたものと同様でした。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
ロタリックスの薬物相互作用
ロタリックス® は、以下の一価ワクチンまたは混合ワクチン [六価ワクチン (DTPa-HBV-IPV/Hib) を含む] と同時に投与できます。
ジフテリア・破傷風・百日咳全細胞ワクチン(DTPw)、ジフテリア・破傷風・無細胞百日咳ワクチン(DTPa)、インフルエンザ菌b型(Hib)ワクチン、不活化ポリオワクチン(IPV)、B型肝炎ワクチン(HBV)、肺炎球菌結合型ワクチン、および血清型 C 髄膜炎菌結合型ワクチン。
ロタリックス®と経口ポリオワクチン(OPV)の同時投与は、ポリオ抗原に対する免疫反応に影響を与えません。 OPV の併用投与はロタウイルス ワクチンに対する免疫反応をわずかに低下させる可能性がありますが、重度のロタウイルス胃腸炎に対する臨床的防御は維持されます。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
物質の作用 Rotarix
有効性の結果
凍結乾燥ヒトロタウイルスワクチン G1 P1 [8] (弱毒化) 製剤の防御効果
ロタウイルスによる胃腸炎に対するヒトロタウイルスワクチン G1 P1 [8] (弱毒化) (有効成分) の保護効果を評価するために、プラセボ対照臨床研究がヨーロッパ、ラテンアメリカ、アフリカ、アジアで実施されました。
胃腸炎の重症度は、次の 2 つの異なる基準に従って定義されました。
- 20 段階のベシカリ スケール。下痢と嘔吐の重症度と期間、発熱と脱水症状の重症度、および治療の必要性を考慮して、ロタウイルス胃腸炎の臨床像全体を評価します。または
- 世界保健機関 (WHO) の基準に基づく臨床症例の定義。
ヨーロッパでの予防効果
欧州で4,000人を対象に実施された臨床研究では、ヒトロタウイルスワクチンG1 P1 [8] (弱毒化) (活性物質) の欧州の異なるスケジュール(2~3ヶ月、2~4ヶ月、3~4ヶ月、および3〜5か月)。
ヒトロタウイルスワクチン G1 P1 [8] (弱毒化) (活性物質) を 2 回投与した後、生後 1 年目と 2 年目、および 2 年間を合わせた場合に観察されたワクチンの予防効果を表 1 に示します。
表 1. ヨーロッパで実施された研究
|
生後1年目 |
人生2年目 |
生後1年目と2年目を合わせたもの |
||||
|
ヒトロタウイルスワクチン G1 P1 [8] (弱毒化) (N=2,572) § |
ヒトロタウイルスワクチン G1 P1 [8] (弱毒化) (N=2,554) § |
ヒトロタウイルスワクチン G1 P1 [8] (弱毒化) (N=2,572) § |
||||
|
プラセボ (N=1,302) § |
プラセボ (N=1,294) § |
プラセボ (N=1,302) § |
||||
|
あらゆる重症度および重度のロタウイルス胃腸炎に対するワクチンの有効性 (%) |
||||||
|
歪み |
任意の重大度 |
記録† |
任意の重大度 |
記録† |
任意の重大度 |
記録† |
|
G1P[8] |
95.6 [87.9; 98.8] |
96.4 [85.7; 99.6] |
82.7 [67.8; 91.3] |
96.5 [86.2; 99.6] |
89.5 [82.5; 94.1] |
96.4 [90.4; 99.1] |
|
G2P[4] |
62.0* [lt;0,0; 94.4] |
74.7* [lt;0,0; 99.6] |
57.1 [lt;0,0; 82.6] |
89.9 [9.4; 99.8] |
58.3 [10.1; 81.0】 |
85.5 [24.0; 98.5] |
|
G3P[8] |
89.9 [9.5; 99.8] |
100 [44.8; 100] |
79.7 [lt;0,0; 98.1] |
83.1* [lt;0,0; 99.7] |
84.8 [41.0; 97.3] |
93.7 [52.8; 99.9] |
|
G4P[8] |
88.3 [57.5; 97.9] |
100 [64.9; 100] |
69.6* [lt;0,0; 95.3] |
87.3 [lt;0,0; 99.7] |
83.1 [55.6; 94.5] |
95.4 [68.3; 99.9] |
|
G9P[8] |
75.6 [51.1; 88.5】 |
94.7 [77.9; 99.4] |
70.5 [50.7; 82.8] |
76.8 [50.8; 89.7] |
72.5 [58.6; 82.0】 |
84.7 [71.0; 92.4] |
|
遺伝子型 P を持つ株[8] |
88.2 [80.8; 93.0] |
96.5 [90.6; 99.1] |
75.7 [65.0; 83.4] |
87.5 [77.8; 93.4] |
81.8 [75.8; 86.5] |
91.9 [86.8; 95.3] |
|
循環しているロタウイルス株 |
87.1 [79.6; 92.1] |
95.8 [89.6; 98.7] |
71.9 [61.2; 79.8] |
85.6 [75.8; 91.9] |
78.9 [72.7; 83.8] |
90.4 [85.1; 94.1] |
|
医師の診察を必要とするロタウイルス胃腸炎に対するワクチンの有効性 (%) [95% CI] |
||||||
|
循環しているロタウイルス株 |
91.8 [84; 96.3] |
76.2 [63.0; 85.0】 |
83.8 [76.8; 88.9] |
|||
|
ロタウイルス胃腸炎による入院に対するワクチンの有効性 (%) [95% CI] |
||||||
|
循環しているロタウイルス株 |
100 [81.8; 100] |
92.2 [65.6; 99.1] |
96.0 [83.8; 99.5] |
|||
†重度の胃腸炎は、Vesikari スケールでスコア 11 未満として定義されました。
§ ATP 有効性コホート。このコホートには、有効性追跡期間に入った ATP 安全性コホートのすべての被験者が含まれます。
* 統計的に有意ではありません (p?0.05)。これらのデータは注意して解釈する必要があります。
ロタウイルス胃腸炎の重症度を20点のベシカリスケールを使用して計算したところ、生後1年間のワクチンの有効性は疾患の重症度が増すにつれて徐々に上昇し、このスケールのスコアが以下の場合に100%(95%CI:84.7-100)に達しました。 ?17.
ラテンアメリカにおける予防効果
ラテンアメリカで20,000人以上を対象に実施された臨床研究では、生後約2か月と4か月でのヒトロタウイルスG1 P1ワクチン[8](弱毒化)(活性物質)の投与が評価されました。胃腸炎の重症度は、WHOの基準に従って定義されました。
ヒトロタウイルスワクチン G1 P1 [8] (弱毒化) (活性物質) を 2 回投与した後、臨床現場での入院および/または水分補給療法を必要とする重篤なロタウイルス胃腸炎に対するワクチンの予防効果は 84.7% (95% CI: 71.7; 95% CI: 71.7; 92.4) 生後 1 年間。重篤な胃腸炎に対するヒトロタウイルスワクチン G1 P1 [8] (弱毒化) (活性物質) の防御効果は、生後 2 年目まで 79.0% (95% CI: 66.4; 87.4) の割合で維持されました。
ロタウイルス胃腸炎の重症度を計算するために 20 点のベシカリ スケールを使用した場合、生後 1 年間のワクチンの有効性は疾患の重症度が増加するにつれて徐々に上昇し、このスケールは?19でした。
G1P[8] および G9P[8] 株によって引き起こされる胃腸炎の十分な症例が観察され、Vesikari スケールスコアが 18 以上の場合、ワクチンが 100% の有効性 (95% CI: gt;72.2; 100) を達成したことが実証されました。
重篤なロタウイルス胃腸炎に対して観察されたワクチンの予防効果を表 2 に示します。
表 2. ラテンアメリカで実施された研究
|
株 |
重症ロタウイルス胃腸炎(生後1年目) † |
重度のロタウイルス胃腸炎(生後2年目) |
|
ヒトロタウイルスワクチン G1P[8] (N=7,175) § |
||
|
ヒトロタウイルスワクチン G1P[8] (N=9,009) § |
プラセボ (N=7,062) § |
|
|
プラセボ (N=8,858) § |
||
|
有効性 (%) |
有効性 (%) |
|
|
G1P[8] |
91.8 |
72.4 |
|
G3P[8] |
87.7 [8.3; 99.7] |
71.9* |
|
G9P[8] |
90.6 [61.7; 98.9] |
87.7 |
|
遺伝子型 P を持つ株[8] |
90.9 [79.2; 96.8] |
79.5 |
†重度のロタウイルス胃腸炎は、臨床現場で入院および/または水分補給療法を必要とする、嘔吐の有無にかかわらず下痢のエピソードとして定義されました (WHO 基準)。
§ ATP 有効性コホート。このコホートには、有効性追跡期間に入った ATP 安全性コホートのすべての被験者が含まれます。
* 統計的に有意ではありません (p?0.05)。これらのデータは注意して解釈する必要があります。
4 つの有効性研究* を統合した解析により、ロタウイルスの G2P[4] 株によって引き起こされる重篤な胃腸炎 (ベシカリ スケール スコア 11) に対して 71.4% (95% CI: 20.1、91.1) の有効性が示されました。
* これらの研究における点推定値と信頼区間はそれぞれ: 100% (95% CI: -1,858.0; 100)、100% (95% CI: 21.1; 100)、45.4 % (95% CI: -81.5; 86.6)および74.7% (95% CI: -386.2; 99.6)。
ヒトロタウイルス G1 P1 ワクチン [8] (弱毒化) (有効成分) は 2 回接種のワクチンですが、初回接種から効果が認められています。ヨーロッパでは、あらゆる重症度のロタウイルス胃腸炎に対するワクチンの有効性は、1回目から2回目までで89.8%(95% CI: 8.9; 99.8)でした。
ラテンアメリカで実施された2件の研究を組み合わせた解析では、1回目から2回目までの重症ロタウイルス胃腸炎に対する有効性が64.4%(95%CI:11.9-86.9)であることが示された。
アフリカにおける予防効果
アフリカで4,900人以上を対象に実施された臨床研究では、生後10週目と14週目(2回接種)または生後6週目、10週目、生後6週目、14週目に投与されたヒトロタウイルスG1 P1ワクチン[8](弱毒化)(活性物質)を評価した。 14週齢(3回接種)。生後1年間の重症ロタウイルス胃腸炎に対するワクチンの有効性は61.2%(95% CI: 44.0; 73.2)でした。この研究には、ワクチンの有効性の観点から、2回投与と3回投与の違いを評価する能力はありませんでした。
あらゆる種類の胃腸炎または重篤なロタウイルス疾患で観察されたワクチンの予防効果を表 3 に示します。
表 3. アフリカで実施された研究
|
株 |
ロタウイルス胃腸炎(生後1年目、複合結果) |
重度のロタウイルス胃腸炎(生後1年目、複合結果) † |
|
ヒトロタウイルスワクチン G1 P1 [8] (弱毒化) (N=2,974) § |
ヒトロタウイルスワクチン G1 P1 [8] (弱毒化) (N=2,974) § |
|
|
プラセボ (n=1,443) § |
プラセボ (n=1,443) § |
|
|
有効性 (%) |
有効性 (%) |
|
|
G1P[8] |
68.3 [53.6; 78.5] |
56.6 |
|
G2P[4] |
49.3 [4.6; 73.0] |
83.8 |
|
G3P[8] |
43.4* [lt;0; 83.7] |
51.5* |
|
G8P[4] |
38.7* [lt;0; 67.8] |
63.6 |
|
G9P[8] |
41.8* [lt;0; 72.3] |
56.9* |
|
G12P[6] |
48.0 [9.7; 70.0】 |
55.5* |
|
遺伝子型 P を持つ株[4] |
39.3 [7.7; 59.9] |
70.9 |
|
遺伝子型 P を持つ株[6] |
46.6 [9.4-68.4] |
55.2* |
|
遺伝子型 P を持つ株[8] |
61.0 [47.3; 71.2] |
59.1 |
†重度の胃腸炎は、Vesikari スケールでスコア 11 未満として定義されました。
§ ATP 有効性コホート。これには、有効性追跡期間に入ったATP安全性コホートのすべての被験者が含まれます。
* 統計的に有意ではありません (p?0.05)。これらのデータは注意して解釈する必要があります。
アジアでは3歳まで効果が持続
アジア(香港、シンガポール、台湾)で10,000人以上を対象に実施された臨床研究では、ヒトロタウイルスG1 P1ワクチン[8](弱毒化)(有効成分)の投与を異なるスケジュール(生後2か月と4か月)で評価しました。 ; 生後3か月と4か月)。
ヒトロタウイルス G1 P1 ワクチン [8] (弱毒化) (活性物質) を 2 回投与した後、3 歳までに観察されたワクチンの予防効果を表 4 に示します。
表 4. アジアで実施された研究
|
有効期限は2歳まで |
有効期限は3歳まで |
|
|
ヒトロタウイルスワクチン G1 P1 [8] (弱毒化) (N=5,263) § |
ヒトロタウイルスワクチン G1 P1 [8] (弱毒化) (N=5,263) § |
|
|
プラセボ (N=5,256) § |
プラセボ (N=5,256) § |
|
|
ロタウイルス胃腸炎に対するワクチンの有効性 (%) [95% CI] |
||
|
歪み |
記録† |
記録† |
|
G1P[8] |
100.0 (80.8;100.0) |
100.0 |
|
G2P[4] |
100.0 (lt;0;100.0) |
100.0 |
|
G3P[8] |
94.5 (64.9;99.9) |
95.2 |
|
G9P[8] |
91.7 (43.8;99.8) |
91.7 |
|
遺伝子型 P を持つ株[8] |
95.8 (83.8;99.5) |
96.6 |
|
循環しているロタウイルス株 |
96.1 (85.1;99.5) |
96.9 |
|
臨床現場で入院および/または水分補給療法を必要とするロタウイルス胃腸炎に対するワクチンの有効性 (%) [95% CI] |
||
|
循環しているロタウイルス株 |
94.2 (82.2;98.8) |
95.5 |
†重度の胃腸炎は、Vesikari スケールのスコア gt;11 として定義されました。
§ ATP 有効性コホート。このコホートには、有効性追跡期間に入った ATP 安全性コホートのすべての被験者が含まれます。
* 統計的に有意ではありません (p?0.05)。これらのデータは注意して解釈する必要があります。
ヒトロタウイルスワクチン G1 P1 液体製剤の防御効果 [8] (弱毒化)
ただし、ヒトロタウイルスワクチン G1 P1 [8] (弱毒化) (活性物質) の液体製剤の 2 回投与後に観察された免疫学的応答は、ヒトロタウイルスワクチン G1 P1 [8] の凍結乾燥製剤の 2 回投与後に観察された免疫学的応答と同等であったと仮定します。 (弱毒化)(活性物質)、凍結乾燥製剤で記録されたワクチンの有効性レベルを液体製剤に外挿することができます。
出典:Rotarix Medication Professional の添付文書。
薬理学的特徴
薬力学特性
免疫反応
ヒトロタウイルスワクチン G1 P1 [8] (弱毒化) (活性物質) がロタウイルスによって引き起こされる胃腸炎を防御する免疫学的メカニズムは完全には理解されていません。ロタウイルスワクチン接種に対する抗体反応とロタウイルス胃腸炎に対する防御との間に関連性は確立されていません。
以下の表 5 は、ワクチンまたはプラセボの 2 回目の投与後 1 ~ 2 か月後に血清抗ロタウイルス IgA 抗体力価が 20 IU/mL 以上で、当初ロタウイルス血清陰性 (抗体力価 IgAlt;20IU/mL (ELISA による)) であった個体の割合を示しています。 、凍結乾燥ワクチンを用いて実施されたいくつかの研究で観察されたように。
表 5. ヒトロタウイルス G1 P1 ワクチン接種後の抗ロタウイルス IgA 抗体の血清変換 [8] (弱毒化) (活性物質)
|
スキーム |
ヨーロッパで行われた研究 |
ワクチン (n=794) |
プラセボ (n=422) |
| 2、3ヶ月 | フランス | 84.3% | 14.0% |
| ドイツ | 82.1% |
6.0% |
|
| 2、4ヶ月 | スペイン | 85.5% | 12.4% |
| 3、5ヶ月 | フィンランド | 94.6% | 2.9% |
| イタリア | 92.3% |
11.1% |
|
| 3、4ヶ月 | チェコ共和国 | 84.6% | 2.2% |
|
スキーム |
ラテンアメリカで行われた研究 |
ワクチン (n=1,023) |
プラセボ (n=448) |
| 2、3~4ヶ月 | 11か国 | 77.9% | 15.1% |
| 2、4ヶ月 | 3か国 | 85.5% | 17.1% |
|
スキーム |
アジアで行われた研究 |
ワクチン (n=140) |
プラセボ (n=136) |
| 2、4ヶ月 | 台湾 | 100% | 4.5% |
|
3、4ヶ月 |
香港 | 95.2% |
0.0% |
| シンガポール | 97.8% |
2.1% |
|
|
スキーム |
アフリカで行われた研究 |
ワクチン (n=221) |
プラセボ (n=111) |
| 10、14 週間と 6、10、14 週間 (グループ化) | 南アフリカ、マレーシア | 58.4% | 22.5% |
3 件の対照比較研究において、経口懸濁液中のヒトロタウイルスワクチン G1 P1 [8] (弱毒化) (活性物質) によって誘発される免疫応答は、経口懸濁液中のヒトロタウイルスワクチン G1 P1 [8] (弱毒化) (活性物質) の免疫応答と同様でした。凍結乾燥粉末医薬品の形態。
未熟児の免疫反応:
凍結乾燥粉末の製剤形態を用いて未熟児を対象に実施された臨床研究では、ヒトロタウイルスワクチン G1 P1 [8] (弱毒化) (活性物質) に免疫原性がありました。小児の85.7%は、2回目の投与から1か月後に血清抗ロタウイルスIgA抗体力価が約20 IU/ml(ELISAによる)に達しました。
HIV 感染者の子供の安全性
臨床研究では、HIV に感染した 100 人の子供に凍結乾燥ヒトロタウイルス G1 P1 ワクチン [8] (弱毒化) (活性物質) またはプラセボが投与されました。安全性プロフィールはこれら 2 つのグループ間で同様でした。
ワクチンの排泄
中空便中のワクチンウイルスの排泄








-1024x576.jpg?resize=1024,576&ssl=1)


