クエン酸タモキシフェンの禁忌 – Nova Química
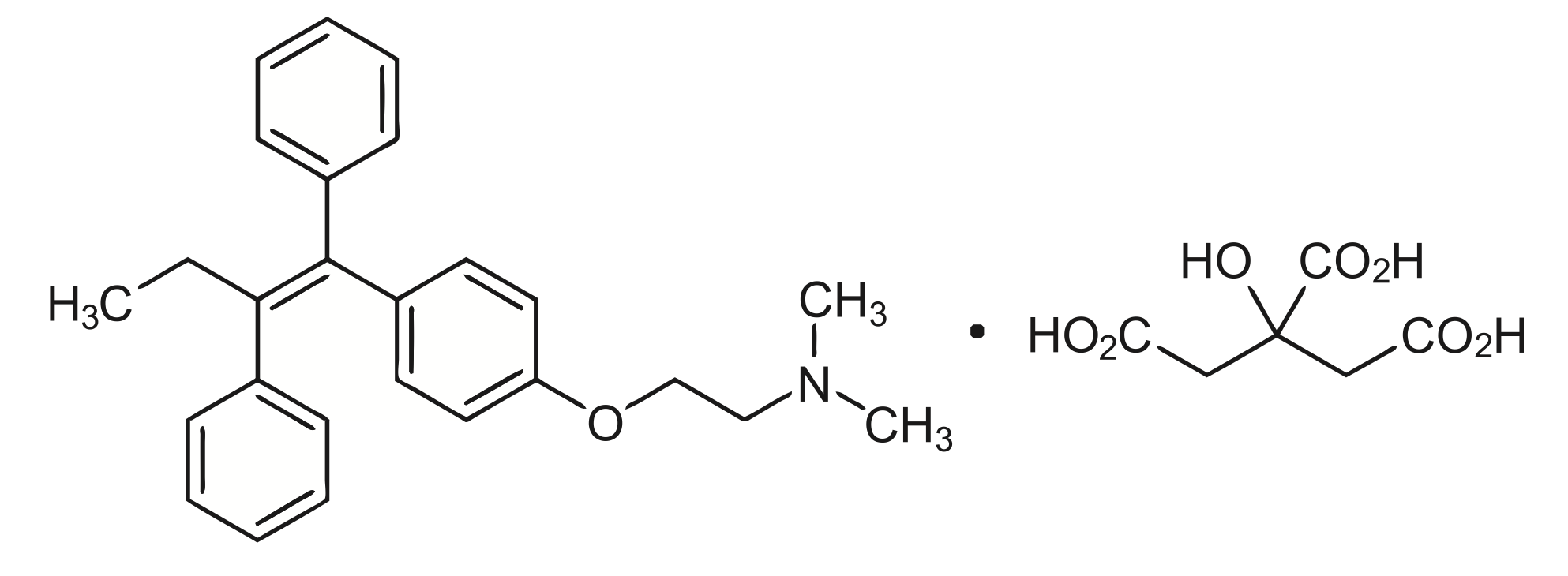
クエン酸タモキシフェンは妊娠中に投与すべきではありません。妊婦におけるクエン酸タモキシフェンの使用後に少数の自然流産、先天異常、胎児死亡が報告されていますが、因果関係は確立されていません。
クエン酸タモキシフェンは、製品またはその成分に対して過去に過敏症を患った患者には投与しないでください。
クエン酸タモキシフェンの使用方法 – Nova Química
クエン酸タモキシフェンは、できれば毎日同じ時間に水とともに経口投与する必要があります。
この薬は割ったり噛んだりしないでください。
大人(高齢者含む)
病気の初期には、クエン酸タモキシフェンによる治療を少なくとも5年間続けることが推奨されます。クエン酸タモキシフェンによる最適な治療期間はまだ確立されていません。
クエン酸タモキシフェンの推奨 1 日用量は 20 mg で、1 日 1 回投与または 2 回に分けて (10 mg の錠剤を 2 錠) 投与します。 1 か月または 2 か月後に満足のいく反応が得られない場合は、用量を 1 日 2 回 20 mg に増量する必要があります。
子供たち
安全性と有効性が確立されていないため、小児におけるクエン酸タモキシフェンの使用は推奨されません。

治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
クエン酸タモキシフェンの予防措置 – Nova Química
クエン酸タモキシフェンを服用している閉経前の女性の一部で月経が抑制されます。
クエン酸タモキシフェンによる治療に関連して、子宮内膜がんおよび子宮肉腫(最も悪性で、ミュラー管腫瘍に関連する)の発生率が増加することが報告されています。そのメカニズムは不明ですが、クエン酸タモキシフェンのエストロゲン様特性に関連している可能性があります。
クエン酸タモキシフェンを服用している、または以前に服用していた女性で、異常な婦人科症状、特に性器出血を報告した女性は、直ちに検査を受ける必要があります。
子宮内膜および対側乳房以外の部位での二次原発腫瘍の発生が、乳がんの治療としてタモキシフェンを受けた患者の臨床研究で報告されています。関連性は確立されておらず、これらの観察の臨床的重要性は不明です。
クエン酸タモキシフェンは、乳房再建手術が遅れた場合に微小血管移植合併症のリスクを高める可能性があります。
マッキューン・オルブライト症候群(SMA)の2歳から10歳の女児28名を対象とした非対照臨床研究では、タモキシフェン20mgを1日1回、最長12ヶ月間投与したところ、6ヶ月の治療後に平均子宮体積が増加し、治療終了時には2倍になった。 -年間の勉強。この所見はタモキシフェンの薬力学特性と一致していますが、因果関係は確立されていません。
妊娠リスクカテゴリー:D.
この薬は医師のアドバイスなしに妊婦が使用しないでください。妊娠が疑われる場合は、すぐに医師に知らせてください。
クエン酸タモキシフェンは妊娠中に投与すべきではありません。妊婦におけるクエン酸タモキシフェンの使用後に少数の自然流産、先天異常、胎児死亡が報告されていますが、因果関係は確立されていません。
患者には、クエン酸タモキシフェンによる治療中に妊娠しないよう警告する必要があり、性的に活動的な場合はバリアまたは他の非ホルモン避妊法を使用する必要があります。
閉経前の女性は、妊娠を避けるために治療前に注意深く検査する必要があります。クエン酸タモキシフェンによる治療中、または治療中止後 2 か月以内に妊娠した場合、女性は胎児に対する潜在的なリスクについて知らされる必要があります。
授乳中
クエン酸タモキシフェンが母乳中に排泄されるかどうかは不明であり、このため授乳中には推奨されません。母乳育児を中止するか、クエン酸タモキシフェンの使用を中止するかを決定するには、母親にとっての薬物療法の重要性を考慮する必要があります。
発がん性と催奇形性
ラット、ウサギ、サルにおける生殖毒性研究では催奇形性の可能性は示されませんでした。
胎児生殖管発達のげっ歯類モデルでは、タモキシフェンは、エストラジオール、エチニルエストラジオール、クロミフェン、およびジエチルスチルベストロール (DES) によって引き起こされる変化と同様の変化と関連していました。
これらの変化の臨床的関連性は不明ですが、その一部、特に膣腺症は、子宮内で DES に曝露され、膣の明細胞癌または膣の明細胞癌を発症するリスクが 1,000 人に 1 人の若い女性に見られる症状と類似しています。頸部。 。
タモキシフェンに曝露された妊婦は少数です。子宮内でタモキシフェンに暴露された若い女性において、そのような暴露がその後の膣腺症や膣または子宮頸部の明細胞癌の原因として報告されていない。
車両の運転や機械の操作能力への影響
クエン酸タモキシフェンは、機械の運転や操作の能力を損なう可能性は低いです。しかし、クエン酸タモキシフェンの使用により疲労が報告されています。
この症状が続く間、患者は車の運転や機械の操作に注意する必要があります。
この薬には乳糖一水和物(クエン酸タモキシフェン10mgは1錠あたり102.30mg、クエン酸タモキシフェン20mgは1錠あたり204.60mg)が含まれています。
この薬はドーピングを引き起こす可能性があります。
クエン酸タモキシフェンの副作用 – Nova Química
明記されていない限り、頻度カテゴリーは、5年間治療を受けた手術可能な乳がんを患う9,366人の閉経後女性を対象に実施された第III相試験で報告された有害事象の数から計算されており、明記されていない限り、比較治療群内の頻度や研究者がそれを考慮したかどうかではありません。研究薬に関連するものがカウントされました。
以下の表は、クエン酸タモキシフェンの使用によって生じる副作用を示しています。
|
頻度 |
システム |
副作用 |
| 非常に一般的 (? 10%) | 胃腸の変化。 | 吐き気。 |
| 代謝と栄養の変化。 | 液体の滞留。 | |
| 生殖器系と乳房の変化。 | 膣出血と膣分泌物。 | |
| 皮膚および皮下組織の変化。 | 発疹。 | |
| 血管の変化。 | ホットフラッシュ。 | |
| 管理サイトの全体的な変更とステータス。 | 倦怠感。 | |
| 一般的 (? 1 – lt; 10%) | 血液およびリンパ系の変化。 | 貧血。 |
| ビジョンが変わります。 | 白内障と網膜症。 | |
| 免疫系の変化。 | 過敏反応。 | |
| 調査。 | 中性脂肪レベルの上昇。 | |
| 筋骨格および結合組織の変化。 | けいれんと筋肉痛。 | |
| 良性、悪性および不特定の新生物。 | 子宮筋腫。 | |
| 神経系が変化します。 | 虚血性脳血管イベント、頭痛、せん妄および感覚障害(感覚異常および味覚障害を含む)。 | |
| 生殖器系と乳房の変化。 | 外陰部のかゆみ、子宮内膜の変化(過形成やポリープを含む)。 | |
| 皮膚および皮下組織の変化。 | 脱毛症。 | |
| 胃腸の変化。 | 嘔吐、下痢、便秘。 | |
| 肝胆道の変化。 | 肝酵素と脂肪症の変化。 | |
| 複数の COS 用語 (器官およびシステムのクラス)。 | 血栓塞栓症(深部静脈血栓症、微小血管血栓症、肺塞栓症など)。 | |
| アンコモン (? 0.1 – lt; 1%) | 血液およびリンパ系の変化。 | 血小板減少症と白血球減少症。 |
| ビジョンが変わります。 | 視覚的な変化。 | |
| 胃腸の変化。 | 膵炎。 | |
| 代謝と栄養の変化。 |
高カリウム血症(以下の患者において) 骨転移)。 |
|
| 良性、悪性および不特定の新生物。 | 子宮内膜がん。 | |
| 呼吸器、胸部、縦隔の変化。 | 間質性肺炎。 | |
| 肝胆道の変化 | 肝硬変 | |
| レア (? 0.01 – lt; 0.1%) | 血液およびリンパ系の変化。 |
好中球減少症 a および無顆粒球症 a。 |
| ビジョンが変わります。 |
角膜の変化と神経障害 光学 系 |
|
| 良性、悪性および不特定の新生物(嚢胞およびポリープを含む)。 |
子宮肉腫(主に悪性混合ミュラー腫瘍) a. |
|
| 生殖器系と乳房の変化。 |
子宮内膜症、嚢胞性卵巣浮腫、膣ポリープ 、 フレア腫瘍 。 |
|
| 神経系が変化します。 | 視神経炎。 | |
| 肝胆道の変化。 |
肝炎、 胆汁うっ滞 、 肝不全 、 肝細胞 傷害、肝壊死 。 |
|
| 皮膚および皮下組織の変化。 |
血管浮腫、スティーブン・ジョンソン症候群 a 、皮膚血管炎 a 、水疱性天疱瘡 a および多形紅斑 a 。 |
|
| 非常にまれです (lt; 0.01%) | 皮膚および皮下組織の変化。 |
皮膚エリテマトーデス b. |
| 先天的、家族的、遺伝的変化。 |
遅発性皮膚ポルフィリン症 b. |
|
| 処置上の合併症、怪我、中毒。 |
放射線毒性に起因する皮膚疾患の再悪化 b. |
aこの副作用は、上記の研究のタモキシフェン群(n = 3094)では報告されていません。ただし、他の研究や他の情報源でも報告されています。頻度は、点推定値の 95% 信頼区間の上限を使用して計算されました (3/X に基づき、X は合計サンプル サイズ (例: 3094) を表します)。これは 3/3094 として計算され、「まれな」周波数カテゴリに相当します。
bこの事象は他の重要な臨床研究では観察されなかった。頻度は、点推定値の 95% 信頼区間の上限を使用して計算されました (3/X に基づき、X は重要な臨床研究における 13,357 人の患者の総サンプル サイズを表します)。これは 3/13357 として計算され、「非常にまれな」周波数カテゴリに相当します。
有害事象が発生した場合は、健康監視通知システム (NOTIVISA) または州または地方自治体の健康監視機関に通知してください。

クエン酸タモキシフェンの薬物相互作用 – Nova Química
クエン酸タモキシフェンをクマリン型抗凝固剤と組み合わせて使用すると、抗凝固効果が大幅に増加する可能性があります。併用投与を開始する場合には、患者の注意深くモニタリングを行うことが推奨される。
クエン酸タモキシフェンを細胞傷害性薬剤と組み合わせて使用すると、血栓塞栓性イベントのリスクが増加します。
補助療法としてタモキシフェンをアロマターゼ阻害剤と組み合わせて使用しても、タモキシフェンを単独で投与した場合と比較して有効性の改善は示されていません。
ヒトにおけるタモキシフェンの既知の主な代謝経路は、酵素 CYP3A4 によって触媒される脱メチル化です。リファンピシンによって誘導される CYP3A4 との薬物動態学的相互作用は、タモキシフェン血漿レベルの低下を示すことが文献で報告されています。この事実と臨床実践との関連性は不明です。
CYP2D6 阻害剤との薬物動態学的相互作用が文献で報告されており、タモキシフェンの活性代謝物である 4-ヒドロキシ-N-デスメチルタモキシフェン (エンドキシフェン) の血漿レベルの低下が示されています。この事実と臨床実践との関連性は不明です。一部の SSRI 抗うつ薬 (パロキセチンなど) と併用すると、タモキシフェンの有効性が低下することが報告されています。
クエン酸タモキシフェンの食品との相互作用 – 新しい化学
これまでのところ報告はありません。
クエン酸タモキシフェンという物質の作用 – 新しい化学
効果の結果
エストロゲン受容体陽性または未知の早期乳がん患者30,000人以上の女性において、アジュバントタモキシフェンは無治療(対照)と比較して乳がん再発を有意に減少させ(plt;0.00001)、10年生存期間を延長させました(plt;0.0003)。この治療は、1 年または 2 年よりも 5 年間投与した方が大幅に効果があることが示されています。
これらの利点は、年齢、閉経状態、タモキシフェンの用量 (通常 20 mg)、および投与された化学療法レジメンに関係なく発生すると思われます。
エストロゲン受容体陰性腫瘍を患う女性では、疾患の再発と生存に対するタモキシフェンの影響は小さいようです。しかし、ホルモン受容体の状態に関係なく、タモキシフェンは5年間投与すると、対側乳がんの発生率を有意に減少させ(plt; 0.00001)、より効果的になりました。
進行乳がんにおけるタモキシフェンによる治療の利点は、36 件の出版物からのデータを分析した研究によって実証され、エストロゲン受容体陽性疾患の患者の 47%、エストロゲン受容体陰性疾患の患者の 10% に客観的な奏効率があったことが示されました (完全な回答 + 部分的な回答)。
安定した疾患の基準を含めると、結果はそれぞれ62%と27%に増加した(Patterson Jら、Breast Cancer Res Treat 1982; 2: 363-374)。
薬理的特性
薬力学特性
クエン酸タモキシフェンは非ステロイド性トリフェニルエチレンであり、さまざまな組織においてエストロゲンアンタゴニストとアゴニストの両方の複雑な薬理学的効果を示します。乳がん患者において、タモキシフェンは主に腫瘍レベルで抗エストロゲン薬として作用し、エストロゲンがその受容体に結合するのを防ぎます。
エストロゲン受容体陽性/未知の乳房腫瘍では、アジュバントとしてタモキシフェンを使用すると疾患の再発が大幅に減少し、生存期間が10年延長され、1年または2年の治療と比較して5年の治療で有意に大きな効果が得られました。
これらの利点は、年齢、閉経期、タモキシフェンの用量、および追加の化学療法とは無関係であると考えられます。
臨床的には、タモキシフェンが閉経後の女性の血中総コレステロールおよび低密度リポタンパク質のレベルを 10 ~ 20% 程度低下させることが知られています。さらに、タモキシフェンは閉経後の患者の骨密度を維持できることが報告されています。
非対照臨床研究は、マッキューン・オルブライト症候群(SMA)の2歳から10歳の少女28人からなる異種混合グループを対象に実施され、彼女らにはタモキシフェン20mgが1日1回、最長12か月間投与された。研究前の期間中に性器出血を報告した患者のうち、62% (患者 21 人中 13 人) が 6 か月間出血がないと報告し、33% (患者 21 人中 7 人) が研究全体を通じて性器出血を報告しなかった。
平均子宮体積は 6 か月の治療後に増加し、1 年間の研究終了時には 2 倍になりました。この所見はタモキシフェンの薬力学特性と一致していますが、因果関係は確立されていません。
小児への長期使用に関する安全性データはありません。
特に、タモキシフェンの成長、思春期、一般的な発達に対する長期的な影響は研究されていません。
薬物動態学的特性
経口投与後、タモキシフェンは急速に吸収され、4 ~ 7 時間以内に最大血清濃度に達します。
動的定常状態濃度 (約 300 ng/mL) は、1 日あたり 40 mg での 4 週間の治療後に達成されます。タモキシフェンは、血清アルブミンに対するタンパク質結合性が高い (>99%)。
代謝はヒドロキシル化、脱メチル化、結合によって起こり、未変化の薬物と同様の薬理学的プロファイルを有するいくつかの代謝産物が生成され、治療効果に寄与します。
排泄は主に糞便を介して行われ、排泄半減期は薬剤自体で計算すると約 7 日ですが、主な循環代謝物である N-デスメチルタモキシフェンの場合は 14 日です。
マッキューン・オルブライト症候群(SMA)の2~10歳の女児にタモキシフェン20mgを1日1回、最長12か月間投与した臨床研究では、年齢に応じてクリアランスの減少と曝露量の増加(AUC値)が観察された。成人と比較して、若い患者では最大 50% 高い)。
前臨床安全性データ
タモキシフェンは、in vitroおよびin vivo試験において変異原性があることは示されていません。タモキシフェンは、げっ歯類を対象とした一部のin vitro試験およびin vivo試験において遺伝毒性がありました。タモキシフェンを投与されたラットの生殖腺腫瘍および肝臓腫瘍が長期研究で報告されています。これらの所見の臨床的関連性は確立されていません。タモキシフェンの使用に関しては豊富な臨床経験があります。








-1024x576.jpg?resize=1024,576&ssl=1)


