- 過去に治療を受けておらず、新たにフィラデルフィア染色体陽性(Ph + )慢性骨髄性白血病(CML)と診断された小児患者。
- 新たに診断されたフィラデルフィア染色体陽性慢性骨髄性白血病(CML)の成人患者、およびインターフェロンアルファ療法の失敗または不耐症後の急性転化期、加速期、または慢性期のフィラデルフィア染色体陽性CML患者の治療。
- 最近診断されたフィラデルフィア染色体陽性急性リンパ芽球性白血病(Ph + ALL)の成人患者の化学療法と統合された治療。
- 切除不能および/または転移性の消化管間質腫瘍(GIST)を有する成人患者の治療。
- 原発GIST切除後の成人患者の補助治療。
メシル酸イマチニブの禁忌
有効成分または賦形剤に対して過敏症のある患者への使用は禁忌です。
妊娠中のリスクカテゴリー D。
この薬は医師のアドバイスなしに妊婦が使用しないでください。妊娠が疑われる場合は、すぐに医師に知らせてください。
メシル酸イマチニブの使用方法
この薬は割ったり、開けたり、噛んだりしないでください。
治療は、必要に応じて、血液悪性腫瘍および肉腫患者の治療に経験のある医師によって開始される必要があります。
胃腸障害のリスクを最小限に抑えるために、処方された用量を食事中および大量の水と一緒に経口投与する必要があります。 400 mg または 600 mg を 1 日 1 回投与する必要がありますが、1 日用量 800 mg を 400 mg として 1 日 2 回、朝と夕方に投与する必要があります。薬物の一日の投与上限は、特定の適応症に従って推奨される一日用量を超えてはなりません。たとえば、CYP3A4 酵素を誘導する薬剤の併用投与がある場合、メシル酸イマチニブ (活性物質) の用量の少なくとも 50% の増加が許可されます。
コーティングされた錠剤を飲み込むことができない患者の場合は、コップ一杯の水またはリンゴジュースに溶かしてください。必要な錠剤数を適量の飲み物(100mg錠剤の場合は約50mL、400mg錠剤の場合は200mL)に入れ、スプーンで混ぜてください。懸濁液は、錠剤が完全に溶解した直後に投与する必要があります。治療は患者に利益が続く限り継続する必要があります。
Ph + CML患者におけるメシル酸イマチニブ(活性物質)による治療に対する反応のモニタリングは定期的に実施し、治療が変更された場合には、最適以下の反応、治療に対する反応の喪失、患者のアドヒアランスの低下、または薬物相互作用の可能性を特定する必要があります。モニタリング結果は、CML患者の適切な管理に役立つはずです。
CMLの投与量
メシル酸イマチニブ(活性物質)の推奨用量は、慢性期の CML 成人患者では 400 mg/日、加速期または急性転化の患者では 600 mg/日です(一次治療か二次治療かに関係なく)。処理)。
重篤な副作用がなければ、慢性期疾患の患者では1日あたり400 mgから600 mgまたは800 mg、加速期または急性転化の患者では1日あたり600 mgから最大800 mgへの用量の増加が考慮される場合があります。以下の状況における薬物反応および白血病とは無関係の重度の血小板減少症または好中球減少症: 疾患の進行(随時)。少なくとも3か月の治療後に満足のいく血液学的反応が得られない。 12か月の治療後に細胞遺伝学的反応が得られない。または、以前に達成された血液学的および/または細胞遺伝学的反応の喪失。
Ph + ALLの投与量
Ph + ALL の成人患者のメシル酸イマチニブ (活性物質) の推奨用量は 600 mg/日です。
GISTの投与量
切除不能および/または転移性 GIST の成人患者に対するメシル酸イマチニブ (活性物質) の推奨用量は 400 mg/日です。
評価により治療に対する反応が不十分であることが示された場合、副作用がない場合には、患者に投与する用量を 400 mg から 600 mg または 800 mg に増量することが考慮される場合があります。
GIST 切除後の成人患者の補助治療におけるメシル酸イマチニブ (活性物質) の推奨用量は 400 mg/日です。推奨される最低治療期間は36か月です。メシル酸イマチニブ(活性物質)による補助療法における最適な治療期間は不明です。
副作用による用量調整
非血液学的副作用
メシル酸イマチニブ (活性物質) の使用により重篤な非血液学的有害反応が発生した場合、その事象が解消されるまで治療を中断する必要があります。その後、反応の初期重症度に応じて、必要に応じて治療を再開することができます。
ビリルビン gt レベルの増加がある場合。 3 x 正常性上限 (ULN) または肝トランスアミナーゼレベル gt; 5×ULN、ビリルビンレベルがlt値に戻るまでメシル酸イマチニブ(活性物質)による治療を中止する必要があります。 lt 値で 1.5 x ULN およびトランスアミナーゼ レベル。 2.5×LSN。その後、メシル酸イマチニブ (活性物質) による治療を、より低い 1 日用量で継続できます。成人では、用量を1日あたり400 mgから300 mg、または600 mgから400 mg、または800 mgから600 mgに、小児では1日あたり340 mg/m 2 から260 mg/m 2に減量する必要があります。
血液学的副作用
重度の好中球減少症および血小板減少症の場合は、以下の表に示すように用量の減量または治療の中止が推奨されます。
好中球減少症および血小板減少症による用量調整:
| 慢性期のCMLとGIST(初回投与量400mg) |
できません。 1.0倍 10 9 /L および/または lt 血小板; 50倍 109 /L |
1. CAN?までメシル酸イマチニブ(有効成分)を一時停止します。 1.5 x 10 9 /L と血小板は? 75×10 9 /L。 2. メシル酸イマチニブ(活性物質)による治療を前回の用量(薬物に対する重篤な副作用の前から)で再開します。 3. CAN lt が再発した場合。 1.0 x 10 9 /L および/または lt 血小板; 50 x 10 9 /L、ステップ 1 を繰り返して再起動します。 |
|
慢性期の小児CML(投与量) 340mg/ m2 ) |
できません。 1.0倍 10 9 /L および/または血小板 |
1. CAN?までメシル酸イマチニブ(有効成分)を一時停止します。 1.5 x 10 9 /L と血小板は? 75×10 9 /L。 2. メシル酸イマチニブ(活性物質)による治療を前回の用量(薬物に対する重篤な副作用の前から)で再開します。 3. CAN lt が再発した場合。 1.0 x 10 9 /L および/または lt 血小板; 50×10 9 /L、繰り返し |
|
CMLは加速段階にあり、急性転化危機にある (初回投与量 600mgc) |
CAN lt; 0.5倍 10 9 /L および/または lt 血小板; 10倍 109 /L |
1. 血球減少症が白血病に関連しているかどうかを確認します (吸引または骨髄生検によって)。 2. 血球減少症が白血病に関連していない場合は、メシル酸イマチニブ (活性物質) の用量を 400 mg に減らします 。 3. 血球減少症が 2 週間続く場合は、300 mg d に減量します。 4. 血球減少症が 4 週間持続し、それでも白血病に関連していない場合は、CAN? までメシル酸イマチニブ (活性物質) の投与を中止します。 1 x 10 9 /L と血小板? 20倍 |
ANC = 絶対好中球数。
a少なくとも1か月の治療後に発生。
b小児では 260 mg/m 2 。
c小児では 340 mg/m 2 。
小児ではdまたは 200 mg/m 2 。
特別な集団
小児用
CMLの2歳未満の小児に対するメシル酸イマチニブ(有効成分)の使用経験はありません。他の適応症における小児におけるメシル酸イマチニブ(活性物質)の使用経験はほとんど、あるいはまったくありません。
小児における用量は体表面積(mg/m 2 )に基づいて決定する必要があります。慢性および進行性CMLの小児には、1日当たり340mg/m 2の用量が推奨されます(1日当たりの総用量が600mgを超えないようにしてください)。治療は1日1回の投与で行うことも、1日の投与量を朝と夕方の2回に分けて投与することもできます。
肝不全
イマチニブは主に肝臓を介して代謝されます。軽度、中等度、または重度の肝機能障害のある患者は、1 日あたり 400 mg の最小推奨用量を摂取する必要があります。不耐性がある場合は、用量を減らすことができます。
腎不全
イマチニブとその代謝物は腎臓からあまり排泄されません。腎機能障害のある患者または透析を受けている患者の場合、初回用量として 1 日あたり 400 mg の最小推奨用量を投与できます。ただし、これらの患者には注意が必要です。不耐性がある場合は、用量を減らすことができます。忍容性があれば、効果が不十分な場合には用量を増やすことができます。
高齢の患者さん
65歳以上の患者の20%以上を対象とした臨床研究では、成人患者において年齢に関連した薬物動態の有意な差は観察されなかった。高齢患者には用量の推奨は必要ありません。
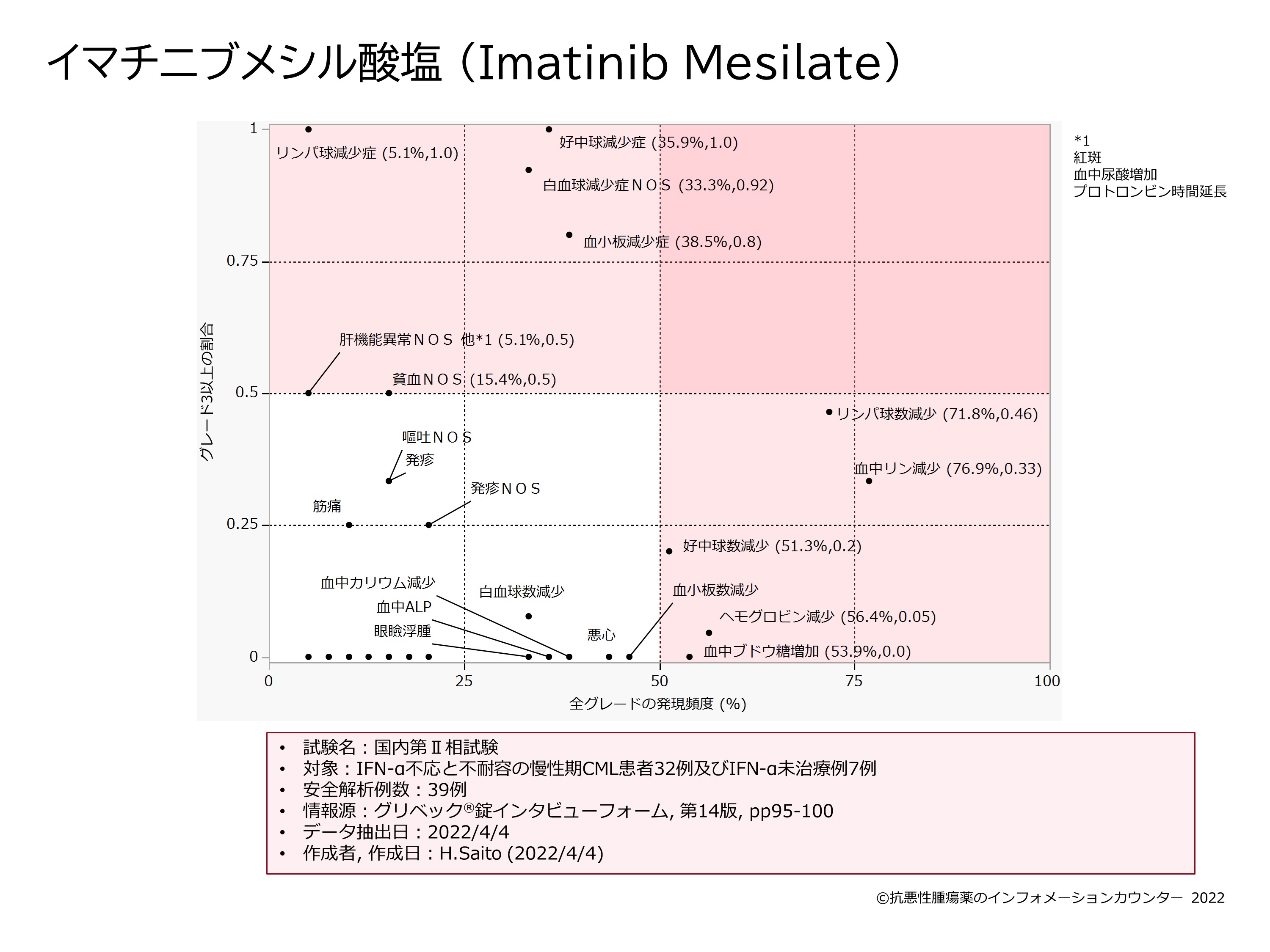
メシル酸イマチニブの副作用

セキュリティプロファイルの概要
ヒトの臨床使用におけるメシル酸イマチニブ (活性物質) の一般的な安全性プロファイルは、メシル酸イマチニブ (活性物質) の 12 年以上の経験により十分に特徴付けられています。臨床開発中、ほとんどの患者はある時点で有害事象を経験しました。最も頻繁に報告されたADR(副作用)(gt; 10%)は、好中球減少症、血小板減少症、貧血、頭痛、消化不良、浮腫、体重増加、吐き気、嘔吐、筋肉けいれん、筋骨格痛、下痢、発疹、疲労、腹痛でした。 。事象は軽度から中等度であり、薬物関連事象により治療を永久に中止した患者はわずか 2 ~ 5% でした。
Ph +白血病の成人患者と小児におけるメシル酸イマチニブ (活性物質) の安全性プロファイルは類似しています。
Ph +白血病と固形腫瘍の安全性プロファイルの違いは、Ph +白血病、GIST [消化管間質腫瘍] 患者の消化管および腫瘍内出血における骨髄抑制の発生率と強度が高いことであり、これはおそらく病気に関連する要因によるものです。
骨髄抑制、消化管の有害事象、浮腫、発疹は、これら 2 つの患者集団の間で共通しています。胃腸閉塞、穿孔、潰瘍形成などの他の消化器疾患は、明らかに適応症がより特異的です。メシル酸イマチニブ(活性物質)への曝露後に観察され、因果関係がある可能性のあるその他の注目すべき有害事象には、肝毒性、急性腎不全、低リン血症、重度の呼吸器有害反応、腫瘍溶解症候群、小児の成長遅延などがあります。
イベントの重症度に応じて、用量の調整が必要になる場合があります。非常にまれなケースでは、ADR に基づいて投薬を中止する必要があります。
副作用 (表 10 および 11) は、次の規則を使用して、頻度の高い順にランク付けされています。
- 非常に一般的 (? 1/10)。
- 一般的 (? 1/100、lt; 1/10);
- 珍しい (? 1/1000、lt; 1/100);
- 珍しい (? 1/10000、lt; 1/1000);
- 単独の報告を含め、非常にまれです (lt; 1/10000)。
表 10 に報告されている副作用とその頻度は、CML および GIST に関する登録済みの研究に基づいています。
表 10 – CML および GIST の臨床研究での副作用:
|
感染症と蔓延 |
|
|
普通でない |
帯状疱疹、単純ヘルペス、鼻咽頭炎、肺炎1、副鼻腔炎、蜂窩織炎、上気道感染症、インフルエンザ、尿路感染症、胃腸炎、敗血症。 |
|
レア |
真菌感染症。 |
|
リンパ系および血液系の障害 |
|
|
非常に一般的な |
好中球減少症、血小板減少症、貧血。 |
|
一般 |
汎血球減少症、発熱性好中球減少症。 |
|
普通でない |
血小板血症、リンパ球減少症、骨髄抑制、好酸球増加症、リンパ節腫脹。 |
|
レア |
溶血性貧血。 |
|
代謝と栄養障害 |
|
|
一般 |
拒食症。 |
|
普通でない |
低カリウム血症、食欲増加、低リン酸血症、食欲減退、脱水症、痛風、高尿酸血症、高カルシウム血症、高血糖、低ナトリウム血症。 |
|
レア |
高カリウム血症、低マグネシウム血症。 |
|
精神障害 |
|
|
一般 |
不眠症。 |
|
普通でない |
うつ病、性欲減退、不安。 |
|
レア |
精神的混乱。 |
|
神経系障害 |
|
|
非常に一般的な |
頭痛2. |
|
一般 |
めまい、感覚異常、味覚の変化、感覚鈍麻。 |
|
普通でない |
片頭痛、眠気、失神、末梢神経障害、記憶障害、坐骨神経痛、むずむず脚症候群、振戦、脳出血。 |
|
レア |
頭蓋内圧の上昇、けいれん、視神経炎。 |
|
目の病気 |
|
|
一般 |
まぶたの浮腫、涙液分泌過多、結膜出血、結膜炎、目の乾燥、かすみ目。 |
|
普通でない |
目の炎症、目の痛み、眼窩浮腫、強膜出血、網膜出血、眼瞼炎、黄斑浮腫。 |
|
レア |
白内障、緑内障、乳頭浮腫。 |
|
聴覚障害および迷路障害 |
|
|
普通でない |
めまい、耳鳴り、難聴。 |
|
心臓障害 |
|
|
普通でない |
動悸、頻脈、うっ血性心不全3 、肺水腫。 |
|
レア |
不整脈、心房細動、心停止、心筋梗塞、狭心症、心嚢液貯留。 |
|
血管障害 |
|
|
一般 |
紅潮、出血。 |
|
普通でない |
高血圧、血腫、硬膜下血腫、四肢の冷え、低血圧、レイノー現象。 |
|
呼吸器、胸部、縦隔の疾患 |
|
|
一般 |
呼吸困難、鼻出血、咳。 |
|
普通でない |
胸水5 、咽喉頭痛、咽頭炎。 |
|
レア |
胸膜炎性疼痛、肺線維症、肺高血圧症、肺出血。 |
|
胃腸障害 |
|
|
非常に一般的な |
吐き気、下痢、嘔吐、消化不良、腹痛。 6 |
|
一般 |
鼓腸、腹部膨満、胃食道逆流、便秘、口渇、胃炎。 |
|
普通でない |
口内炎、口内の潰瘍、胃腸出血7 、おくび、下血、食道炎、腹水、胃潰瘍、吐血、口唇炎、嚥下障害、膵炎。 |
|
レア |
大腸炎、腸閉塞、炎症性腸疾患。 |
|
肝胆道障害 |
|
|
一般 |
肝臓酵素の増加。 |
|
普通でない |
高ビリルビン血症、肝炎、黄疸。 |
|
レア |
肝不全9 、肝壊死。 9 |
|
皮膚および皮下組織の疾患 |
|
|
非常に一般的な |
眼窩周囲浮腫、皮膚炎/湿疹/発疹。 |
|
一般 |
そう痒症、顔面浮腫、皮膚乾燥、紅斑、脱毛症、寝汗、光線過敏症。 |
|
普通でない |
膿疱性発疹、挫傷、発汗の増加、蕁麻疹、斑状発疹、打撲傾向の増加、貧毛症、皮膚の色素沈着低下、剥離性皮膚炎、爪甲潰瘍、毛嚢炎、点状出血、乾癬、紫斑、皮膚の色素沈着過剰、水疱性発疹。 |
|
レア |
急性発熱性好中球性皮膚病(スウィート症候群)、爪の変色、血管神経性浮腫、水疱性発疹、多形紅斑、白血球破砕性血管炎、スティーブンス・ジョンソン症候群、急性汎発性発疹性膿疱症(SAEP)。 |
|
筋骨格疾患および結合組織疾患 |
|
|
非常に一般的な |
筋肉のけいれんやこむら返り、筋肉痛、関節痛、骨痛などの筋骨格系の痛み。 8 |
|
一般 |
関節浮腫。 |
|
普通でない |
関節と筋肉の硬直。 |
|
レア |
筋力低下、関節炎。 |
|
腎臓および泌尿器系の障害 |
|
|
普通でない |
腎臓の痛み、血尿、急性腎不全、頻尿。 |
|
生殖器系と乳房の疾患 |
|
|
普通でない |
女性化乳房、勃起不全、月経過多、月経不順、性機能不全、乳首の痛み、乳房の肥大、陰嚢浮腫。 |
|
全身状態の障害と治療に対する局所反応 |
|
|
非常に一般的な |
水分貯留と浮腫、疲労。 |
|
一般 |
脱力感、発熱、吐き気、悪寒、硬直。 |
|
普通でない |
胸の痛み、倦怠感。 |
|
調査 |
|
|
非常に一般的な |
体重増加。 |
|
一般 |
体重減少。 |
|
普通でない |
血中クレアチニンの増加、血中クレアチンホスホキナーゼの増加、血中乳酸デヒドロゲナーゼの増加、血中アルカリホスファターゼの増加。 |
|
レア |
血中アミラーゼの増加。 |
1肺炎は、形質転換型CML患者およびGIST患者でより一般的に報告されています。
2 GIST 患者で最も一般的な副作用は頭痛でした。
3患者年ベースで見ると、うっ血性心不全を含む心臓イベントは、慢性CML患者よりも形質転換型CML患者でより一般的に観察されました。
4紅潮は GIST 患者でより一般的に見られ、出血 (血腫、出血) は GIST および形質転換 CML (CML-FA および CML-CB) 患者でより一般的に見られました。
5胸水は、慢性 CML 患者よりも GIST 患者および形質転換 CML (CML-FA および CML-CB) 患者でより一般的に報告されています。
6/7腹痛と胃腸出血は、GIST 患者でより一般的に観察されました。
筋骨格系の痛みおよび関連事象は、GIST 患者よりも CML 患者でより一般的に観察されました。
9肝不全や壊死による死亡例も報告されています。
メシル酸イマチニブ(有効成分)の市販後および追加の臨床研究から、以下の副作用が報告されています。自発的な症例報告のほか、小規模または進行中の臨床研究やアクセス拡大プログラムからの重篤な副作用も含まれます。これらの副作用は規模が未知の集団から報告されているため、その頻度を確実に推定したり、メシル酸イマチニブ(活性物質)への曝露との因果関係を確立したりすることが常に可能であるとは限りません。
表 11 – 市販後報告による副作用:
|
神経系障害 |
|
| 普通でない | 脳浮腫。 |
|
目の病気 |
|
| レア | 硝子体出血。 |
|
心臓障害 |
|
| レア | 心膜炎、心タンポナーデ。 |
|
血管障害 |
|
| 普通でない | 血栓症/塞栓症。 |
| 非常に珍しい | アナフィラキシーショック。 |
|
呼吸器、胸部、縦隔の疾患 |
|
| 普通でない |
急性呼吸不全 1 、間質性肺疾患。 |
|
胃腸障害 |
|
| 普通でない |
腸閉塞/イレウス、出血/腫瘍壊死、消化管穿孔。 2 |
| レア | 憩室炎 |
|
皮膚および皮下組織の疾患 |
|
| 普通でない | 手掌足底赤血球感覚異常症候群。 |
| レア | 苔状角化症、扁平苔癬。 |
| 非常に珍しい | 中毒性表皮壊死。 |
| 未知 |
好酸球増加症および全身症状を伴う薬剤による 発疹 。 |
|
筋骨格疾患および結合組織疾患 |
|
|
非常に一般的な |
治療中止後の筋骨格系の痛み(筋肉痛、四肢の痛み、関節痛、骨の痛み、背中の痛みを含む)。 |
| レア | 無血管壊死/股関節骨壊死、横紋筋融解症/ミオパチー。 |
| 未知 | 子供の成長遅延。 |
|
生殖障害 |
|
| 非常に珍しい | 出血性黄体/出血性卵巣嚢腫。 |
|
良性、悪性、または非特異的な新生物(嚢胞およびポリープを含む) |
|
| レア | 腫瘍溶解症候群。 |
1進行した疾患、重度の感染症、重度の好中球減少症、およびその他の重篤な付随症状を有する患者での致死例が報告されています。
2 GIST における消化管穿孔による死亡例がいくつか報告されています。
選択された薬物副作用の説明
骨髄抑制
骨髄抑制は、メシル酸イマチニブ (活性物質) で治療されたがん患者に非常によく見られます。骨髄抑制、血小板減少症、好中球減少症、および貧血が、最も頻繁に報告されたグレード 3 および 4 の臨床検査異常でした。一般に、メシル酸イマチニブ(活性物質)で治療されたCML[慢性骨髄性白血病]患者にみられる骨髄抑制は、一般に可逆的であり、大多数の患者では中断や用量の減量をもたらさなかった。投薬を中止する必要がある患者はほとんどいませんでした。汎血球減少症、リンパ球減少症、骨髄抑制などの他の事象も報告されています。
血液学的抑制は、ほとんどの場合、最高用量で出現し、明らかにCML疾患の段階にも依存しており、グレード3または4の好中球減少症および血小板減少症は、芽球期および加速期では4〜6倍高かった(44%および63%)。 %)、新たに診断されたCF CML [慢性期]患者(それぞれ16.7%および8.9%)と比較した。これらの事象は通常、用量を減らすことで制御できますが、メシル酸イマチニブ(活性物質)による治療の中止や中断が必要になることはほとんどありません。血液毒性の発生率は、固形腫瘍(GIST)患者の方が Ph +白血病患者よりも低く、グレード 3/4 の好中球減少症と血小板減少症がそれぞれ約 10% と 1% で発生します。
出血
CNS 出血および GI 出血は、基底脊髄機能が損なわれた CML 患者では珍しいことではありません。出血は、急性白血病患者における合併症の一部としてよく知られており、血小板減少症、またはそれほど一般的ではありませんが血小板機能不全の結果である可能性があります。ただし、治療中にCNS出血またはGI出血を経験したすべての患者が血小板減少症を経験するわけではありません。
臨床的に重大な出血の最も一般的な症状は消化管出血で、これは進行性CML患者および転移性GIST患者で最も多く発生し、腫瘍からの出血(腫瘍出血/壊死)による基礎疾患の一部として出血が起こる可能性があります。 )。第一選択の CML およびアジュバント GIST の状況では、観察された消化管出血の頻度は一般に最も低かった。胃前庭部血管拡張症(GAVE)も、メシル酸イマンチニブの市販後使用でほとんど報告されていません。
浮腫と体液貯留
浮腫はイマチニブの一般的な毒性であり、すべての適応症にわたってすべての患者の 50% 以上に現れます。浮腫は用量に関連しており、明らかに、浮腫の発生と血漿レベルの間に相関関係があります。最も一般的な症状は眼窩周囲浮腫であり、わずかに一般的ではない症状は下肢浮腫です。一般に、特別な治療は必要ありません。他の体液貯留現象はあまり一般的ではありませんが、解剖学的部位の位置により、潜在的に重篤になる可能性があります。最も頻繁に起こる体液貯留事象は胸水であり、進行性CML患者および転移性GIST患者に最も多く見られました。
浮腫や体液貯留のある患者では、心不全の頻度は一般に低かった。進行性CMLでは他のグループよりもその頻度が高かった。これは、進行性CML患者の病状が悪化していることで説明できる可能性があります。浮腫や体液貯留のある患者の腎不全でも同じ傾向が観察されました。ある臨床研究では、うっ血性心不全を示唆する事象の頻度はイマチニブ群とイマチニブ群で 1.5% でした。新たにCMLと診断された患者におけるIFN-αの割合は1.1%。この頻度は、形質転換したCML(加速期または急性転化)を患う患者、高齢の患者、またはベースラインのヘモグロビンが8 g/dL未満の患者で有意に高かった。すべての適応症にわたって、GIST 患者よりも CML 患者で観察される CHF イベントの頻度が高いことは、これらの疾患関連危険因子の一部に違いがあることを示している可能性があります。さらに、最近発表された、切除不能または転移性GIST患者942人を対象としたEORTC研究における心臓イベントに関する特別な安全性分析では、イマチニブはGIST患者において左心不全を誘発しないと結論づけており、観察された割合は約0.2%であったが、既存の心臓病を患っている人口では、この割合は 2% に達する可能性があります。
皮膚の発疹と重篤な皮膚の副作用
全身性紅斑性斑状丘疹性そう痒性発疹が報告されており、治療を継続しても消失する可能性があります。
患者によっては発疹がなくてもかゆみを感じる場合があり、場合によっては剥離成分が存在することもあります。一部の患者では再曝露により新たに発疹が出現しましたが、すべての患者ではありませんでした。これらの発疹は通常、抗ヒスタミン薬や局所ステロイドに反応します。場合によっては、ステロイドの全身投与が必要になることがあります。
皮膚発疹は、すべての適応症にわたってイマチニブによる治療を受けた患者の最大 3 分の 1 で観察されています。これらの発疹は掻痒性であることが多く、最も一般的には前腕、体幹、顔面に紅斑性、斑状丘疹性、または剥離性病変として現れるか、または全身性発現を伴って全身に現れます。皮膚生検により、混合細胞浸潤物による薬物に対する毒性反応が明らかになった。ほとんどの発疹は軽度で自然に治りますが、まれにスティーブンス・ジョンソン中毒性表皮壊死融解症、多形紅斑、好酸球増加症や全身症状を伴う薬疹などのより重篤なケースでは、治療の中断または中止が必要となる場合があります。驚くことではないが、アジュバント GIST 研究では、プラセボよりも皮膚反応の発生率が高かった。
肝毒性
時には重度の肝毒性が発生する可能性があり、前臨床期および臨床期に観察されています。 TFH (肝機能検査) 異常は一般にトランスアミナーゼの軽度の上昇で構成されていましたが、少数の患者ではビリルビンレベルが上昇していました。発症は通常、治療開始から最初の 2 か月以内に起こりますが、治療開始後 6 ~ 12 か月以内に発症することもあります。通常、1~4週間治療を中止するとレベルは正常化します。
低リン血症
血清リン酸塩の低下および低リン酸血症(グレード 3/4 まで)は、すべての適応症にわたって比較的一般的に観察されました。しかし、この所見の起源と臨床的重要性はまだ確立されていません。
イマチニブは、ヒト単球の破骨細胞への分化を阻害することが示されています。この減少には、これらの細胞の再吸収能力の減少が伴いました。イマチニブの存在下では、破骨細胞において用量依存的な RANK-L の減少が観察されました。破骨細胞の活動が持続的に阻害されると、逆調節反応が起こり、PTH レベルが上昇することがあります。前臨床所見の臨床的関連性はまだ不確実であり、骨折などの骨格 AE との関連性はまだ証明されていません。
臨床開発プログラムでは、すべての研究において血清リン酸塩の定期的な測定は行われませんでした。当初の仮説は、低リン血症は用量依存性である可能性があるというものでしたが、新たにCMLと診断された患者における安全性転帰の用量依存性を調査することを目的とした第III相TOPS試験の解釈可能な24か月の結果は、19.1% vs. 1%であることを実証しました。 15.5% と 5.1%対それぞれ 400 mg と 800 mg を投与された患者の 0.9% では、血清リン酸塩または血清カルシウムがグレード 3/4 減少しました。
胃腸閉塞、穿孔、または潰瘍
極端な場合にはイマチニブによる局所的刺激を表す可能性がある消化管潰瘍形成が、すべての適応症にわたって少数の患者に観察されています。腫瘍出血/腫瘍壊死、消化管閉塞および穿孔は明らかにこの疾患に関連しており、GIST患者の間で独占的またはより頻繁に発生しています。
転移性 GIST の場合、腫瘍反応に伴って腫瘍壊死が発生する可能性があり、まれに穿孔に至ることがあります。消化管閉塞/イレウスは GIST 集団でより一般的に発生し、転移性 GIST による腫瘍閉塞が原因である可能性があり、アジュバント設定では以前の消化管手術による癒着が原因である可能性があります。
腫瘍溶解症候群
腫瘍崩壊症候群とメシル酸イマチニブ(活性物質)による治療との間に因果関係がある可能性があると考えられていますが、一部の症例では併用薬や他の独立したリスクによって混乱が生じています。
子供の成長遅延

どうやら、メシル酸イマチニブ(有効成分)は、子供、特に思春期前の子供の身長に影響を与えるようです。小児の成長遅延とメシル酸イマチニブ (活性物質) による治療との因果関係を排除することはできませんでしたが、一部の成長遅延のケースについては情報が限られています。
重度の呼吸器副作用
メシル酸イマチニブ(活性物質)による治療では、急性呼吸不全、肺高血圧、間質性肺疾患、肺線維症などの重篤な呼吸器事象(場合によっては致死的)が観察されています。これらの症例の多くでは、重篤な呼吸器事象に関連する可能性のある既存の心臓または肺の状態が報告されています。
臨床検査の変更
血液学的
CML患者では、血球減少症、特に好中球減少症と血小板減少症が研究全体で一貫した所見であり、高用量では頻度が高くなることが示唆されている。 750 mg (第 I 相試験)。しかし、血球減少症の発生は病気の段階にも明らかに依存していました。新たにCMLと診断された患者では、他のCML患者よりも血球減少症の頻度が低かった。グレード 3 または 4 の好中球減少症 (CAN lt; 1.0 x 10 9 /L) および血小板減少症 (血小板数 lt; 50 x 10 9 /L) の頻度は、急性転化期および加速期では 4 ~ 6 倍高くなります (59 –最近慢性期CMLと診断された患者(好中球減少症16.7%、血小板減少症8.9%)と比較した場合、好中球減少症と血小板減少症はそれぞれ64%、44~63%)。最近慢性期のCMLと診断された患者では、グレード4の好中球減少症(CAN lt; 0.5 x 10 9 /L)および血小板減少症(血小板数lt; 10 x 10 9 /L)が3.6%で観察され、3.6%ではグレード4の好中球減少症(CAN lt; 0.5 x 10 9 /L)が観察されました。それぞれ患者の1%。好中球減少症および血小板減少症のエピソードの平均持続期間は、通常、それぞれ 2 ~ 3 週間および 3 ~ 4 週間に限定されていました。これらの影響は通常、メシル酸イマチニブ(活性物質)の用量を減らすか治療を中断することで治療できますが、まれに治療が永久に中断される場合があります。 CMLの小児患者で最も頻繁に観察された毒性は、好中球減少症、血小板減少症、貧血を伴うグレード3または4の血球減少症でした。これらは通常、治療開始から最初の数か月以内に発生しました。
転移性または手術不能な GIST 患者(研究 B2222)では、グレード 3 および 4 の貧血がそれぞれ患者の 5.4% と 0.7% で報告されており、これらの患者の少なくとも一部では胃腸出血または腫瘍内出血に関連している可能性があります。グレード3および4の好中球減少症はそれぞれ患者の7.5%と2.7%で観察され、グレード3の血小板減少症は患者の0.7%で観察された。グレード 4 の血小板減少症を発症した患者はいませんでした。白血球数と好中球数の減少は主に治療開始から 6 週間の間に起こり、その後は値は安定しました。
生化学パラメータ
CML患者ではトランスアミナーゼ(lt; 5%)またはビリルビン(lt; 1%)の重度の上昇が見られ、一般にイマンチニブのメシル酸塩の用量を減らすか中断することで制御されました(これらのエピソードの平均期間は約1週間でした)。 。 CML患者の1%未満で肝臓検査異常があったため、治療が永久に中止されました。 GIST患者(研究B2222)では、TGPS(グルタミン酸転移酵素)の6.8%上昇が観察されました。








-1024x576.jpg?resize=1024,576&ssl=1)


