ミコフェノール酸ナトリウムの禁忌

ミコフェノール酸ナトリウム (活性物質) は、ミコフェノール酸ナトリウム (活性物質)、ミコフェノール酸、ミコフェノール酸モフェチル、または賦形剤のいずれかに対して過敏症のある患者には禁忌です。
ミコフェノール酸ナトリウムの使用方法
投与方法
胃耐性コーティングの完全性を維持するには、ミコフェノール酸ナトリウム (活性物質) が壊れてはなりません。
投与量
推奨用量は、720 mg(180 mg 4 錠または 360 mg 2 錠)を 1 日 2 回(1 日量 1,440 mg)、空腹時、食事摂取の 1 時間前または 2 時間後に投与します。ミコフェノール酸モフェチル (MMF) 2 g を投与されている患者では、ミコフェノール酸ナトリウム (活性物質) 720 mg を 1 日 2 回投与することで治療を置き換えることができます (1 日量 1,440 mg)。
一般対象者
ミコフェノール酸ナトリウム(活性物質)による治療は、適切な資格を持つ移植専門家によって開始および監視されなければなりません。ミコフェノール酸ナトリウム(活性物質)は、移植後 48 時間以内に新規患者に投与を開始する必要があります。
ミコフェノール酸ナトリウム(活性物質)は、食物なしで投与する必要があります。
特別な集団に対する投与量
腎不全
術後の腎機能が遅れている患者には用量調整は必要ありません。重度の慢性腎不全(糸球体濾過量 lt; 25 mL.min -1 .1.73 m -2 )の患者は、注意深く監視する必要があります。
肝不全
重度の肝実質疾患を有する腎移植患者には用量調整は必要ありません。
小児患者
小児患者における安全性と有効性は確立されていません。腎移植を受ける小児患者について利用できる薬物動態データは限られています。
高齢者の患者
この患者集団では用量調整は必要ありません。
拒絶反応時の治療
腎移植拒絶反応はミコフェノール酸の薬物動態の変化を引き起こしません。ミコフェノール酸ナトリウム(活性物質)の用量を減らしたり中断したりする必要はありません。
この薬は割ったり、開けたり、噛んだりしないでください。
ミコフェノール酸ナトリウムの副作用

セキュリティプロファイルの概要
以下の副作用には、2 件の対照臨床研究からの副作用が含まれます。研究では、新規腎移植を受ける 423 人の患者と維持期の腎移植を受ける 322 人の患者(ランダム化 1:1)を対象に、ミコフェノール酸ナトリウム(活性物質)とミコフェノール酸モフェチルの安全性が評価されました。副作用の発生率は各集団の治療間で同様でした。
マイクロエマルジョンおよびコルチコステロイド用のシクロスポリンと組み合わせたミコフェノール酸ナトリウム(活性物質)の投与に関連する最も一般的な副作用(約 10%)には、白血球減少症および下痢が含まれます。
悪性腫瘍
MPA を含む複数の薬剤を組み合わせた免疫抑制療法を受けている患者は、リンパ腫やその他の悪性腫瘍、特に皮膚の悪性腫瘍を発症するリスクが高くなります。ミコフェノール酸ナトリウム(活性物質)を用いた臨床研究で観察された悪性腫瘍の合計率は次のとおりです:ミコフェノール酸ナトリウム(活性物質)を最長で投与された新規患者2名(0.9%)および維持患者2名(1.3%)で発症したリンパ増殖性疾患またはリンパ腫1年。非黒色腫皮膚癌は新規症例の0.9%で発生し、最長1年間ミコフェノール酸ナトリウム(活性物質)を投与された維持患者では1.8%で発生した。他の種類の悪性腫瘍は新規患者で0.5%、維持患者で0.6%で発生しました。
日和見感染症
すべての移植レシピエントは日和見感染症のリスクが高くなります。リスクは総免疫抑制負荷とともに増加しました。腎移植を受けた患者を対象とした対照臨床研究で、別の免疫抑制剤とともにミコフェノール酸ナトリウム(活性物質)を投与され、1年間追跡された新規腎移植を受けた患者で最も一般的な日和見感染症は、CMV、カンジダ症、単純ヘルペスでした。ミコフェノール酸ナトリウム(活性物質)を用いた臨床研究で観察されたCMV感染症(血清学的検査、ウイルス血症または疾患)の合計率は、新規腎移植を受けた患者の21.6%、維持期に腎移植を受けた患者の1.9%で報告されました。
臨床研究の副作用をまとめた表
副作用 (表 6) は、次のカテゴリを使用して、頻度に応じて最も頻度の高いものから順にリストされています。
- 非常に一般的: (? 1/10);
- 一般: (? 1/100 および lt; 1/10);
- 珍しい: (? 1/1,000 および lt; 1/100);
- レア: (? 1/10,000 および lt; 1/1,000) 非常にレア: (lt; 1/10,000)。
各頻度グループ内で、副作用は重症度の降順に分類されます。
以下の表 6 には、2 件の多施設共同第 III 相無作為化二重盲検対照臨床試験で報告されたミコフェノール酸ナトリウム (活性物質) に関連する可能性のある、または予想される副作用が含まれています。1 件は新規腎移植レシピエントにおけるもので、もう 1 件は腎移植患者における腎移植患者におけるものです。メンテナンス段階。これらの研究におけるミコフェノール酸ナトリウム (活性物質) の投与量は、シクロスポリン マイクロエマルションおよびコルチコステロイドと合わせて、12 か月間 1,440 mg/日でした。結果は、MedDRA 臓器システムに従ってまとめられました。
表 6: 2 つの主要な第 III 相試験で報告されたミコフェノール酸ナトリウム (活性物質) に関連する可能性がある、またはおそらく関連する副作用
|
身体システム |
入射 |
副作用 |
|
感染症と蔓延 |
非常に一般的な | 真菌、細菌、ウイルスによって引き起こされる感染症 |
| 一般 | 上気道感染症、肺炎 | |
| 普通でない | 感染した傷、敗血症*、骨髄炎* | |
| 悪性および良性新生物 | 普通でない | 皮膚乳頭腫*、基底細胞癌*、カポジ肉腫*、リンパ増殖性疾患、扁平上皮癌* |
|
血液およびリンパ系の障害 |
非常に一般的な | 白血球減少症 |
| 一般 | 貧血、血小板減少症 | |
| 普通でない | リンパ節*、リンパ減少症*、好中球減少症*、リンパ節腫脹* | |
|
代謝と栄養障害 |
非常に一般的な | 低カルシウム血症、低カリウム血症、高尿酸血症 |
| 一般 | 高カリウム血症、低マグネシウム血症 | |
| 普通でない |
食欲不振、高脂血症、糖尿 病 *、高コレステロール血症*、高リン血症 |
|
|
精神障害 |
一般 | 不安 |
| 普通でない | 妄想的な認識* | |
|
神経系障害 |
一般 | めまい、頭痛 |
| 普通でない | 震え、不眠症* | |
| 目の病気 | 普通でない | 結膜炎*、かすみ目* |
| 心臓障害 | 普通でない | 頻脈、肺水腫* |
|
血管障害 |
非常に一般的 一般的 | 高血圧、低血圧 |
| 一般 | 高血圧の悪化 | |
|
呼吸器、胸部、縦隔の疾患 |
一般 | 咳、呼吸困難、労作時呼吸困難 |
| 普通でない | 致死性肺線維症、肺うっ血*、喘鳴*などの間質性肺疾患 | |
|
胃腸障害 |
非常に一般的な | 下痢 |
| 一般 | 腹部膨満、腹痛、便秘、消化不良、鼓腸、胃炎、排便、吐き気、嘔吐 | |
| 普通でない | 腹部の圧痛、膵炎、凜発、口臭*、イレウス*、食道炎*、消化性潰瘍*、亜腸レウス*、胃腸出血、口渇*、口内炎*、耳下腺管閉塞*、胃食道逆流症*、歯肉過形成*、腹膜炎* | |
| 肝胆道疾患 | 一般 | 肝機能検査の異常 |
| 皮膚および皮下組織の疾患 | 普通でない | 脱毛症、打撲傷*、ニキビ |
|
結合組織および筋骨格系疾患 |
一般 | 関節痛、無力症、筋肉痛 |
| 普通でない | 腰痛、筋肉疲労* | |
|
腎臓および泌尿器疾患 |
一般 | 血中クレアチニンの増加 |
| 普通でない | 血尿*、腎尿細管壊死*、尿道狭窄 | |
| 管理現場における一般的な混乱と状況 | 一般 | 疲労、末梢浮腫、発熱、インフルエンザ様疾患、下肢浮腫*、痛み、悪寒*、衰弱* |
* 事象は 1 人の患者 (372 人中) でのみ報告されました。
知らせ:
腎移植レシピエントは、最長 1 年間、毎日 1,440 mg のミコフェノール酸ナトリウム (活性物質) で治療されました。新たな移植を受ける集団と維持期でも同様のプロファイルが観察されましたが、維持期の患者では発生率が低い傾向があります。
市販後の副作用のリスト
以下の副作用は、自発的な症例報告および文献症例によるミコフェノール酸ナトリウム (活性物質) の市販後の経験に基づいています。これらの反応は規模が不確実な集団によって自発的に報告されたものであるため、その頻度を確実に推定することは不可能であり、したがって不明として分類されます。副作用は、MedDRA 臓器分類システムに従ってリストされています。各臓器のクラス内で、薬物有害反応が重症度の順に表示されます。
皮膚および皮膚組織の障害:
発疹は、承認後の臨床試験、市販後の調査、および自発的な報告により副作用として特定されています。
以下の追加の副作用は、クラス効果として MPA 誘導体に起因すると考えられます。
感染症と蔓延:
髄膜炎、感染性心内膜炎、結核、非定型抗酸菌感染症などの重篤な、時には生命を脅かす感染症。ポリオーマウイルス関連腎症 (NAP)、特に BK ウイルス感染によるもの。進行性多巣性白質脳症(PML)の症例が報告されており、一部は致死的です。
血液およびリンパ疾患:
無顆粒球症、好中球減少症、汎血球減少症。他の免疫抑制剤と組み合わせて MPA 誘導体で治療された患者における純粋赤血球形成不全 (PRCA) の症例が報告されています。

胃腸障害:
大腸炎、食道炎(CMV大腸炎および食道炎を含む)、CMV胃炎、膵炎、腸穿孔、胃腸出血、胃潰瘍、十二指腸潰瘍、イレウス。
高齢の患者さん
高齢の患者は、免疫抑制による副作用のリスクがより高いことがよくあります。ミコフェノール酸ナトリウム(活性物質)の臨床研究において、併用免疫抑制療法の一環としてミコフェノール酸ナトリウム(活性物質)を投与されている高齢患者は、若年者と比較して副作用のリスクが増加していることは示されていません。
有害事象が発生した場合は、健康監視通知システム – NOTIVISA (www.anvisa.gov.br/hotsite/notivisa/index.htm)、または州または地方自治体の健康監視機関に通知してください。
ミコフェノール酸ナトリウムの薬物相互作用
相互作用が観察されたため、併用は推奨されません
アザチオプリン:
ミコフェノール酸ナトリウム(活性物質)とアザチオプリンとの投与はまだ研究されていないため、これらの薬剤を一緒に投与すべきではありません。
微生物の生ワクチン:
免疫反応が低下している患者には投与すべきではありません。他のワクチンに対する抗体反応が低下する可能性があります。
観察された考慮すべき相互作用
アシクロビル:
腎機能障害がある場合、MPAG (ミコフェノール酸グルクロニド) およびアシクロビルの血漿濃度が高くなることがあります。したがって、これら 2 つの薬剤が尿細管分泌を巡って競合する可能性があり、その結果、MPAG とアシクロビルの両方の濃度が増加する可能性があります。この状況では、患者を注意深く監視する必要があります。
胃保護剤
水酸化アルミニウムおよび水酸化マグネシウムを含む制酸剤:
ミコフェノール酸ナトリウム(活性物質)の吸収は、制酸薬と併用すると減少しました。ミコフェノール酸ナトリウム(活性物質)と、水酸化マグネシウムおよび水酸化アルミニウムを含む制酸剤の同時投与により、MPA の全身曝露が 37% 減少し、MPA の最大濃度が 25% 減少します。制酸薬(水酸化アルミニウムおよび水酸化マグネシウムを含む)とミコフェノール酸ナトリウム(活性物質)を併用投与する場合は注意が必要です。
プロトンポンプ阻害剤:
健康なボランティアにおいて、1,000mgのMMFと40mgのパントプラゾールを1日2回同時投与すると、MPA AUCが27%減少し、MPA Cmaxが57%減少した。しかし、同じ研究では、ミコフェノール酸ナトリウム(活性物質)とパントプラゾールの併用投与によるMPAの薬物動態の変化は観察されませんでした。
ガンシクロビル:
MPA および MPAG の薬物動態は、ガンシクロビルの添加によって影響を受けません。ガンシクロビルのクリアランスは、MPA への治療的曝露の条件下では影響を受けません。ただし、ミコフェノール酸ナトリウム (活性物質) とガンシクロビルを同時投与する腎機能障害のある患者では、ガンシクロビルの推奨用量を遵守し、患者を注意深く監視する必要があります。
タクロリムス:
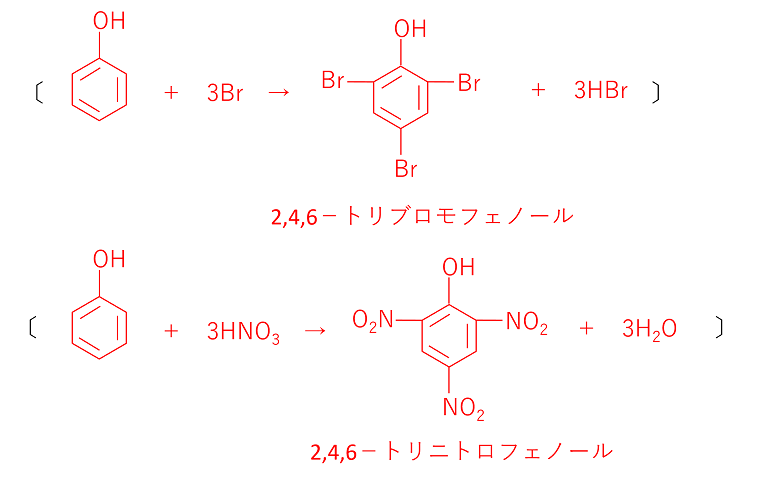
安定した腎移植患者におけるカルシニューリン阻害剤を用いたクロスオーバー研究では、Neoral® とタクロリムスによる治療中に定常状態でのミコフェノール酸ナトリウム (活性物質) の薬物動態が測定されました。 MPA の平均 AUC は 19% 高く、 Cmax は約 20% 低かった。逆に、MPAG の平均 AUC およびCmax は、Neoral® と比較してタクロリムスの方が約 30% 低かった。
シクロスポリンA:
シクロスポリン A の薬物動態は、定常状態に達する用量でミコフェノール酸ナトリウム (活性物質) を服用している腎移植を受ける安定した患者では影響を受けませんでした。
考慮すべき予想される相互作用
コレスチラミンと腸肝循環を妨げる薬剤:
コレスチラミンは薬剤の腸内循環を遮断する能力があるため、MPA への曝露を減らす可能性があります。コレスチラミンや腸肝循環を妨げる薬剤を併用する場合は、ミコフェノール酸ナトリウム(活性物質)の有効性を低下させる可能性があるため、注意が必要です。
経口避妊薬:
経口避妊薬は酸化代謝を受けますが、ミコフェノール酸ナトリウム (活性物質) はグルクロン酸抱合によって代謝されます。ミコフェノール酸ナトリウム(活性物質)の薬物動態に対する経口避妊薬の重大な臨床効果は期待されません。しかし、ミコフェノール酸ナトリウム投与(活性物質)が経口避妊薬の薬物動態に及ぼす長期的な影響は不明であるため、経口避妊薬の有効性が悪影響を受ける可能性があります。
ミコフェノール酸ナトリウムの予防措置
まれな遺伝性ヒポキサンチン-グアニンホスホリボシルトランスフェラーゼ(HGFRT)欠損症の患者
ミコフェノール酸ナトリウム(活性物質)は、IMPDH(イノシン一リン酸デヒドロゲナーゼ)の阻害剤です。したがって、理論的には、レッシュ・ナイハン症候群やケリー・シーグミラー症候群など、まれな遺伝性ヒポキサンチン・グアニン・ホスホリボシル・トランスフェラーゼ(HGFRT)欠損症の患者では、この治療法は避けるべきです。
出産適齢期、妊娠中および授乳中の女性
妊娠中のミコフェノール酸ナトリウム(活性物質)の使用は、流産や先天奇形などの妊娠喪失のリスクの増加と関連しています。ミコフェノール酸ナトリウム(活性物質)による治療は、妊娠検査結果が陰性になるまで開始しないでください。妊娠中の使用および避妊要件に関する情報。
ミコフェノール酸ナトリウム(活性物質)は授乳中に使用しないでください。
悪性腫瘍
ミコフェノール酸ナトリウム(活性物質)を含む複数の薬剤を組み合わせた免疫抑制療法を受けている患者は、リンパ腫やその他の悪性腫瘍、特に皮膚の悪性腫瘍を発症するリスクが高くなります。このリスクは、特定の薬剤の使用よりも、免疫抑制の程度の強さと持続に関連しているようです。皮膚がんのリスクを最小限に抑えるための一般的な推奨事項として、防護服を着用し、保護係数の高い日焼け止めを使用することにより、日光と紫外線への曝露を制限する必要があります。
感染症
ミコフェノール酸ナトリウムを投与されている患者には、感染、予期せぬ打撲、出血、またはその他の骨髄抑制の兆候があれば直ちに報告するよう指導されるべきである。
免疫系が過剰に抑制されると、日和見感染、致死的感染、敗血症などの感染症に対する感受性が高まります。
ミコフェノール酸(MPA)誘導体、ミコフェノール酸ナトリウム(活性物質)、MMFなどの免疫抑制剤で治療されている患者において、B型肝炎(HBV)およびC型肝炎(HCV)の再発が報告されています。感染患者の活動性 HBV または HCV 感染の臨床および検査室の兆候を監視することが推奨されます。
ミコフェノール酸モフェチルおよびミコフェノール酸ナトリウム(活性物質)を含むMPA誘導体で治療された患者において、進行性多巣性白質脳症(PML)の症例が報告されており、一部は致死的である。一般に、報告された症例は、免疫抑制療法や免疫機能障害などの PML の危険因子を示していました。免疫抑制患者の場合、臨床医は神経症状を報告する患者の鑑別診断においてPMLを考慮する必要があり、神経内科医との相談が臨床的に必要であると考慮される必要があります。特にBKウイルス感染によるポリオーマウイルス関連腎症(PAN)は、腎機能が悪化した免疫抑制患者の鑑別診断に含めるべきである。 PML または NAP を発症した患者の総免疫抑制を軽減することを考慮する必要があります。しかし、移植を受けた患者では、免疫抑制の低下により移植片が危険にさらされる可能性があります。
血液疾患

ミコフェノール酸ナトリウム(活性物質)を投与されている患者は、血液障害(MPA単独、併用薬、ウイルス感染、またはこれらの原因のいくつかの組み合わせに関連する可能性がある好中球減少症や貧血など)がないかモニタリングする必要があります。ミコフェノール酸ナトリウム(活性物質)を投与されている患者活性物質)は、治療の最初の 1 か月間は毎週、治療の 2 か月目と 3 か月間は月に 2 回、その後、患者に血液異常(例、絶対数による好中球減少症)がある場合は毎月血球数を測定する必要があります。 1.5 x 103/?L または貧血)、ミコフェノール酸ナトリウム(活性物質)を中断または中止することが適切です。
他の免疫抑制剤と組み合わせて MPA 誘導体で治療された患者における純粋赤血球形成不全 (PRCA) の症例が報告されています。 APCV によって誘導される MPA 誘導体のメカニズムは不明です。免疫抑制療法における他の免疫抑制剤およびそれらの組み合わせの相対的な寄与も不明です。ただし、MPA 誘導体は血液障害を引き起こす可能性があります。 APCV の一部の症例は、MPA 誘導体による治療の用量を減らすか中止することで回復することが示されています。ただし、移植患者の場合、免疫抑制の低下により移植片が危険にさらされる可能性があります。移植レシピエント患者におけるミコフェノール酸ナトリウム療法(活性物質)の変更は、移植片拒絶反応のリスクを最小限に抑えるために、適切な監督下でのみ実施する必要があります。
予防接種
MPA による治療中はワクチン接種の効果が低下する可能性があり、弱毒生微生物ワクチンの使用は避けるべきであることを患者に知らせるべきです。インフルエンザの予防接種は重要かもしれません。処方者は、インフルエンザワクチン接種に関する国のガイドラインを参照する必要があります。
胃腸障害
MPA 誘導体は、まれに胃腸管潰瘍、出血、穿孔などの消化器系への悪影響の発生率の増加と関連しているため、ミコフェノール酸ナトリウム (活性物質) は、消化器系に重篤な活動性障害のある患者には注意して投与する必要があります。システム。
他のエージェントとの組み合わせ
ミコフェノール酸ナトリウム(活性物質)は、臨床研究において次の薬剤と組み合わせて投与されています:抗胸腺細胞グロブリン、バシリキシマブ、マイクロエマルジョン用シクロスポリンおよびコルチコステロイド。ミコフェノール酸ナトリウム (活性物質) を他の免疫抑制剤と併用する場合の有効性と安全性は研究されていません。
妊娠と授乳
出産適齢期の女性
ミコフェノール酸ナトリウム(活性物質)による治療は、妊娠検査結果が陰性になるまで開始しないでください。
出産可能年齢の女性は、ミコフェノール酸ナトリウム (活性物質) による治療を開始する前、治療中、およびミコフェノール酸ナトリウム (活性物質) の最後の投与後 6 週間は、非常に効果的な避妊方法を使用しなければなりません。
妊娠
妊娠中のミコフェノール酸ナトリウム(活性物質)の使用は、先天奇形のリスク増加と関連しています。ミコフェノール酸ナトリウム(活性物質)については、妊婦を対象に実施された適切かつ十分に管理された研究はありませんが、米国国家移植妊娠登録簿(NTPR)のデータに基づくと、妊娠中のミコフェノール酸モフェチルと他の免疫抑制剤の併用は関連性が示されています。 RNTGの移植患者で観察された先天奇形の割合が4~5%であったのと比較して、先天奇形の割合は22%増加(曝露された生児出産18例中4例)した。
ミコフェノール酸モフェチルで報告されている先天奇形には、外耳や、先天性口唇口蓋裂、先天性横隔膜ヘルニア、遠位四肢の異常、心臓、食道、腎臓などのその他の顔面異常が含まれます。妊娠中のミコフェノール酸モフェチルの使用も、流産のリスク増加と関連しています。
MMF は経口または静脈内投与後に MPA に変換されるため、ミコフェノール酸ナトリウム(有効成分)についても上記のリスクを考慮する必要があります。 MPA の催奇形性の可能性は動物実験で観察されています。
ミコフェノール酸ナトリウム(活性物質)は、潜在的な利益が胎児への潜在的なリスクを上回る場合にのみ妊婦に使用されるべきです。妊娠している場合は、直ちに医師に相談するよう患者に指示する必要があります。
この薬は妊娠中のリスクカテゴリーDに属します。
この薬は医師のアドバイスなしに妊婦が使用しないでください。妊娠が疑われる場合は、すぐに医師に知らせてください。
授乳期
MPA が母乳中に排泄されるかどうかは不明です。
ミコフェノール酸ナトリウム(活性物質)は授乳中に使用しないでください。
多くの薬剤は母乳中に排泄され、授乳中の乳児には重篤な副作用が起こる可能性があるため、治療中および治療中止後 6 週間は授乳を控えるか、薬剤の使用を控えるかを決定する必要があります。母親にとっての薬の重要性を考慮して。
男性患者
性的に活動的な男性には、治療中、およびミコフェノール酸ナトリウム(活性物質)の最後の投与後合計 13 週間はコンドームの使用が推奨されます。さらに、治療中およびミコフェノール酸ナトリウム(活性物質)の最後の投与後合計 13 週間は、パートナーが非常に効果的な避妊法を使用することをお勧めします。
車両の運転および/または機械の操作能力への影響
機械を運転したり操作したりする能力に関する研究は行われていない。作用機序、薬力学的プロファイル、および報告された副作用は、この効果が一般的ではないことを示しています。
免疫抑制剤は結核の原発巣を活性化する可能性があります。免疫抑制下の患者を監視する医師は、活動性疾患が出現する可能性に注意を払い、早期診断と治療のためにあらゆる予防措置を講じる必要があります。
ミコフェノール酸ナトリウムの作用
有効性の結果
臨床研究
成人におけるミコフェノール酸ナトリウム(活性物質)(MPA)の承認には、2 つの重要な多施設共同ランダム化二重盲検研究が使用されました。どちらも市販の Cellcept (MMF) を比較対照として使用したランドマーク療法の対照臨床研究でした。どちらもMMFと同等の有効性と安全性を示しました。最初の研究には新規腎移植(ERLB301)を受けた成人 423 人が含まれており、MPA の有効性は MMF と同等であり、同等の安全性プロファイルを有することが実証されました。 2番目の研究は322人の維持腎移植レシピエント(ERLB302)を対象に実施され、免疫抑制維持療法としてMMFを受けている腎移植患者が有効性を損なうことなくMPAを安全に使用できることが実証されました。
成人新規腎移植患者(ERLB301 試験) 新規無作為化二重盲検二重プラセボ試験(ERLB301)は、年齢 18 ~ 75 歳の腎移植患者 423 名(MPA = 213、MMF = 210)を対象に実施されました。有効性の欠如(すなわち、生検で証明された急性拒絶反応(RACB)、移植片喪失、死亡、または最初の6か月以内の追跡不能)の発生率の尺度として、MPAとMMFの治療上の同等性を前向きに試験するために設計された。治療期間(主目的)と死亡、移植片喪失、または12ヵ月後の追跡対象喪失の発生率(副主目的)。
患者には、シクロスポリンおよびコルチコステロイドと併用して、移植後48時間以内にMPA 1.44 g/日またはMMF 2 g/日を12か月間投与した。 MPA 群と MMF 群では、それぞれ 39.4% と 42.9% が導入療法として抗体療法を受けました。
6か月後の有効性欠如の発生率(MPA 25.8% vs MMF 26.2%、95% CI: [-8.7、+8.0])に基づいて、治療上の同等性が実証されました。 12か月時点で、RACB、移植片喪失、死亡の発生率は、MPAとMMFでそれぞれ26.3%と28.1%、孤立したRACBの発生率は22.5%と24.3%であった。 RACB患者における重度の急性拒絶反応の発生率は、MPAでは2.1%、MMFでは9.8%でした(p = ns)。
表 3: 6 か月後および 12 か月後の主要有効性評価項目とその構成要素の分析 (ERLB301 試験)
|
MPA |
MMF |
95%CI |
|
|
6ヶ月 |
n (%) | n (%) | |
| 生検で証明された急性拒絶反応、移植片喪失、死亡、または追跡不能のエピソード | 55(25.8) | 55(26.2) | (-8.7、8.0) |
| 生検で証明された急性拒絶反応のエピソード | 46(21.6) | 48(22.9) | (-9.2、6.7) |
| 移植片の喪失または死亡 | 8 (3.8) | 11 (5.2) | (-5.4、2.5) |
| 移植片喪失 | 7 (3.3) | 9 (4.3) | (-4.6、2.6) |
| 死 | 1(0.5) | 2(1.0) | |
| 追跡の喪失* | 3 (1.4) | 0 | |
|
12ヶ月 |
|||
| 生検で証明された急性拒絶反応、移植片喪失、死亡、または追跡不能のエピソード | 60(28.2) | 59(28.1) | (-8.5、8.6) |
| 生検で証明された急性拒絶反応のエピソード | 48(22.5) | 51(24.3) | (-9.8、6.3) |
| 移植片の喪失または死亡 | 10 (4.7) | 14 (6.7) | (-6.4、2.4) |
| 移植片喪失 | 8 (3.8) | 9 (4.3) | (-4.3、3.2) |
| 死 | 2 (0.9) | 5(2.4) | |
| 追跡の喪失* | 5(2.3) | 0 |
*
追跡不能とは、事前の生検で急性拒絶反応、移植片喪失、死亡が証明されずに追跡不能となった患者を示します。治療上の同等性の基準は満たされました。主要変数(RACB、移植片喪失、死亡または6ヵ月目のフォローアップ喪失)の発生率の差の95%CIは完全に範囲内(12%、12%)に維持されました。 )。
全体的な安全性と血液学的プロファイルは、2 つの治療グループ間で同様でした。薬物有害事象の疑いは、MPA対MMF でそれぞれ 51.1% と 60.5% でした。全体的な感染発生率に差は観察されませんでした。重篤な感染症の全体的な発生率は、MPA グループで 22.1%、MMF グループで 27.1% でした。重度の肺炎の発生率は MPA グループの方が低かった (0.5% vs 4.3%、p = 0.01)。消化管有害事象の全体的な発生率に差は観察されませんでした(80.8%対80.8%)。 それぞれ 80%、p = ns、MPA対MMF)。
成人維持腎移植患者(ERLB302試験)
この維持研究は、18歳から75歳までの腎移植患者322人(MPA = 159、MMF = 163)を対象に実施され、移植後少なくとも6ヶ月間、MMF 2 g/日をシクロスポリンと併用して、または投与せずに投与されました。研究に参加する前に少なくとも4週間コルチコステロイドを服用していること。患者は、12か月間MPA 1.44 g/日またはMMF 2 g/日の投与群に1:1で無作為に割り付けられた。
有効性パラメーターは、6 か月目および 12 か月目での有効性の欠如 (例、RACB、移植片喪失、または死亡) の発生率でした。 12ヵ月後、同様の割合で有効性の欠如(MPA 2.5%; MMF 6.1%; p = ns)、生検で証明された急性拒絶反応(MPA 1.3%; MMF 3.1%; p = ns)、および生検で証明された慢性拒絶反応(MPA) 3.8%、MMF 4.9%、p = ns) が両方のグループで観察されました。
表 4: 副次的有効性評価項目(ERLB302 試験)
|
ミコフェノール酸ナトリウム(有効成分) 1.44 g/日 (n = 159) |
MMF 2 g/日 (n = 163) |
(IC 95%) ミコフェノール酸ナトリウム (有効成分) MMF |
|
|
6ヶ月 |
n (%) | n (%) | |
| 生検で証明された急性拒絶反応、移植片喪失、死亡、または追跡不能のエピソード | 6 (3.8) | 10 (6.1) | (-7.1、2.4) |
| 生検で証明された急性拒絶反応、生検で証明された慢性拒絶反応、移植片喪失、死亡、または追跡不能のエピソード | 9 (5.7) | 11 (6.7) | (-6.4、4.2) |
| 急性拒絶反応 | 2(1.3) | 3 (1.8) | (-10.9、5.5) |
| 生検で証明された急性拒絶反応 | 2(1.3) | 2 (1,2) | – |
| 生検で証明された慢性拒絶反応 | 4(2.5) | 4(2.5) | – |
| 追跡の喪失* | 4(2.5) | 6 (3.7) | – |
| 移植片の喪失または死亡 | 0 | 2 (1,2) | – |
|
12ヶ月 |
n (%) n =110 | n (%) n = 113 | – |
| 生検で証明された急性拒絶反応、移植片喪失、死亡または追跡不能のエピソード) | 10 (9.1) | 14 (12.4) | – |
| 生検で証明された急性拒絶反応、生検で証明された慢性拒絶反応、移植片喪失、死亡、または追跡不能のエピソード | 13(11.8) | 15(13.3) | – |
| 追跡の喪失* | 7 (6.4) | 8 (7.1) | |
| 移植片の喪失または死亡 | 1 (0.9) | 4 (3.5) |
*
追跡不能とは、RACB、移植片喪失、または死亡なしで追跡不能となった患者を示します。
維持試験でも、重篤な感染症の発生率(8.8 vs 16%、p <0.05、MPA vs MMF)を除いて、同様の全体的な安全性プロファイルが実証されました。全体の感染率は各グループで 59% でした。 MPA グループ (1.9%) では MMF グループ (4.9%) よりも肺炎が観察されましたが、統計的に有意ではありませんでした。全体的な消化管有害事象の同様の発生率が観察された(69.2対61.8%、MPA対MMF)が、「あらゆる消化管有害事象」は、MPA で最長 12 ヶ月治療された患者の方が数値的に高かった(月内 29.6%対24.5%) 12)、MPA を使用している患者では消化管重症度の増加が低い傾向がありました。

薬理的特性
薬力学
薬物療法グループ: 免疫抑制剤 (ATC コード L04 A A06)。
作用機序
プリン経路を利用できる他の細胞種とは対照的に、リンパ球の増殖はプリン合成のデノボ経路に大きく依存しているため、MPA は他の細胞よりも強力に T および B リンパ球の増殖を阻害します。したがって、作用機序はサイトカインの転写を妨害し、T リンパ球を温存するカルシニューリン阻害剤と相補的です。
薬物動態
吸収
経口投与後、ミコフェノール酸ナトリウム(活性物質)はほとんど吸収されます。胃耐性コーティングによると、MPA 濃度が最大になるまでの時間は約 1.5 ~ 2 時間でした。インビトロ研究では、ミコフェノール酸ナトリウム(活性物質)の胃炎防止コーティングの製剤が、胃内のような酸性条件下での MPa の放出を防ぐことが示されています。
マイクロエマルジョンに対するシクロスポリン免疫抑制下の安定した腎移植の患者の受容体では、MPa の胃腸吸収は 93%、絶対バイオアベイラビリティは 72% でした。
ミコフェノール酸ナトリウムの薬物動態 (活性物質) は用量に比例し、180 ~ 2,160 mg の範囲で研究された用量では直線的です。絶食時と比較して、高脂血症の食事(脂肪55g、1,000カロリー)とともにミコフェノール酸ナトリウム(活性物質)720mgを投与しても、有効性に関連する最も重要な薬物動態パラメータであるMPaへの全身曝露(AUC)には影響がなかった。しかしながら、最大MPa(C max )濃度は33%減少した。用量 MPa 間の吸収のばらつきを避けるために、ミコフェノール酸ナトリウム (活性物質) は空腹時に摂取する必要があります。
分布
平衡状態でのMPA分配量は50リットルです。ミコフェノール酸とグルクロニド ミコフェノール酸は、それぞれ 97% と 82% という高いタンパク質関連性を持っています。遊離 MPa の濃度は、タンパク質結合部位が減少した状態 (尿毒症、肝不全、低アルブミン血症、高タンパク質関連薬剤の併用) で増加する可能性があります。これにより、患者は MPA 有害反応のリスクが高まる可能性があります。
生体内変換・代謝
MPA半減期は11.7時間、クリアランス(クリアランス)は8.6L/hです。 MPa は主にグルクロニルトランスフェラーゼによって代謝されて、MPa のフェノール性グルクロニド、グルクロニド ミコフェノール酸 (MPAG) を形成します。 MPAG は MPA の主な代謝産物であり、生物活性を示しません。
マイクロエマルジョンに対するマイクロスポリン免疫抑制下で腎移植を受ける安定した患者では、経口ミコフェノール酸ナトリウムの約 28% が全身性前代謝によって MPAG に変換されます。 MPAGの半減期はMPaよりも長く約15.7時間、クリアランス(クリアランス)は0.45L/hです。
排除
尿中には最小限の MPa が存在しますが (LT; 1.0%)、ほとんどの MPA は MPAG として尿から除去されます。胆汁から分泌される MPag は、腸内細菌叢による不信感に利用可能です。この分離により得られる MPa は再吸収されます。ミコフェノール酸ナトリウム(活性物質)の投与後約 6 ~ 8 時間で、不信任 MPa 再吸収に従って MPa 濃度の 2 番目のピークを測定できます。
マイクロエマルジョン用シクロスポリンによる免疫抑制下で腎移植を受ける患者における薬物動態
マイコフェノール酸ナトリウム(活性物質)の投与後のMPAの主要な薬物動態パラメーターを表5に示します。マイコフェノール酸ナトリウム(活性物質)の単一投与薬物動態学は、マルチロスの薬物動態とマイコフェノール酸ナトリウム(活性物質)の慢性投与を予測します。最初の移植後の期間では、平均MPAおよびメインMPA MPA AUCは、移植後6ヶ月の約半分でした。
表5:マイクロエマルジョンのシクロスポリンとの免疫抑制下で腎移植を受けている患者の経口マイコフェノール酸ナトリウム投与(活性物質)の後のメイン(DP)MPA薬物動態パラメーター。
特別人口
腎不全
MPAの薬物動態は、機能がないまで正常な腎機能の変動の下で変更されていないようです。対照的に、MPAG暴露は腎機能を低減することで増加し、MPAG暴露は肛門で約8倍高くなりました。クリアランス








-1024x576.jpg?resize=1024,576&ssl=1)


