- 利尿(排尿)の促進。
- 心臓血管手術中および/または外傷後の急性腎不全(腎不全)の予防。
- 頭蓋内(脳)圧の軽減と脳浮腫の治療。
- 他の手段で下げることができない場合の高い眼圧の低下。
- 緑内障の発作。
- 有害物質の尿中排泄の促進。
- 心臓(心臓)および腎臓(腎臓)起源の脳浮腫。
マンニトールはどのように作用しますか?
20% マンニトール溶液は尿の生成を著しく増加させます。マンニトールは浸透圧利尿薬であり、腎臓によって排泄されます。マンニトールは、腎臓によって排泄される浸透圧利尿薬です。この作用は、頭蓋内圧 (脳内の液体の圧力)、頭蓋内浮腫 (脳内の圧力の上昇)、および眼圧の上昇を低下させるマンニトールの役割の基礎となっています。
マンニトール 20% の禁忌 – Eurofarma
マンニトール溶液は、全無尿(尿生成の欠如)、重度の心臓代償不全(心臓の問題)、活動性頭蓋内出血(脳への血液の流出)、重度の脱水症(体液喪失)および肺水腫の患者には使用すべきではありません。
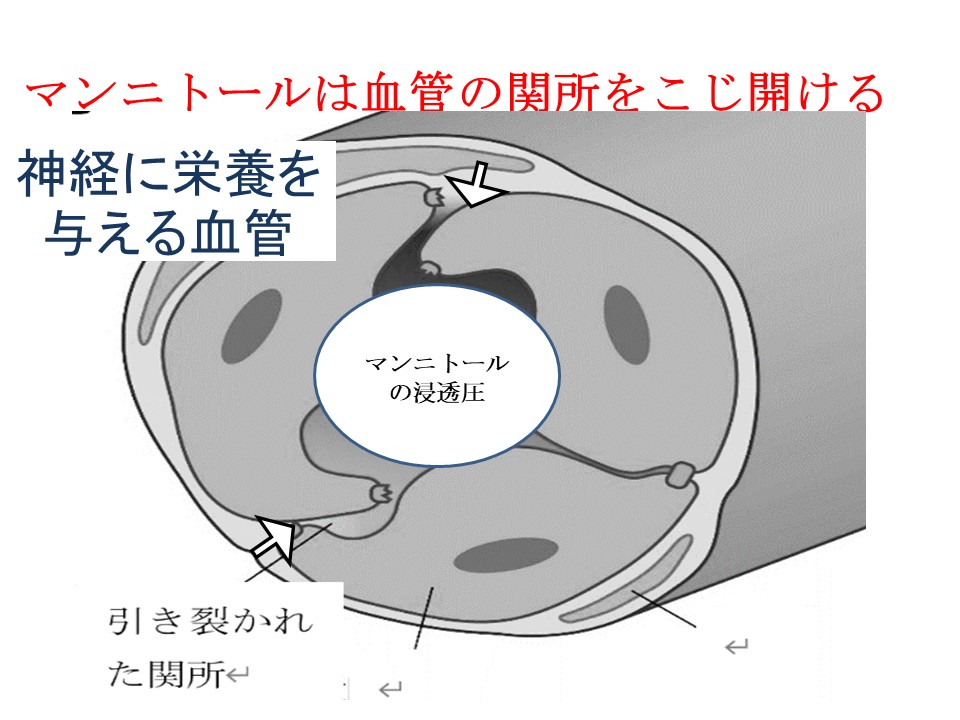
マンニトール溶液は輸血用に全血に添加したり、輸血に使用するのと同じ装置で投与したりしないでください。
マンニトール 20% の使用方法 – Eurofarma
この溶液は静脈内に単独でのみ使用してください。投与量は医師が決定する必要があり、患者の年齢、体重、臨床状態、溶液で希釈した薬、および実験室での測定によって異なります。
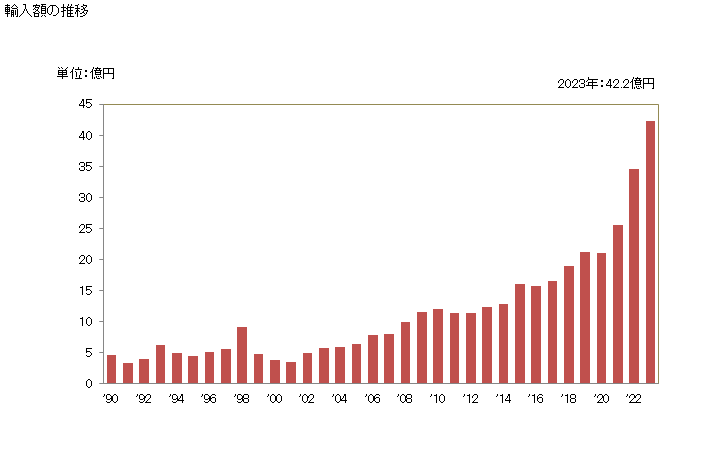
非経口溶液は、投与前に目視検査して、粒子の存在、溶液の濁り、亀裂、および一次包装の違反を観察する必要があります。
溶液は袋に包装されています
閉鎖系
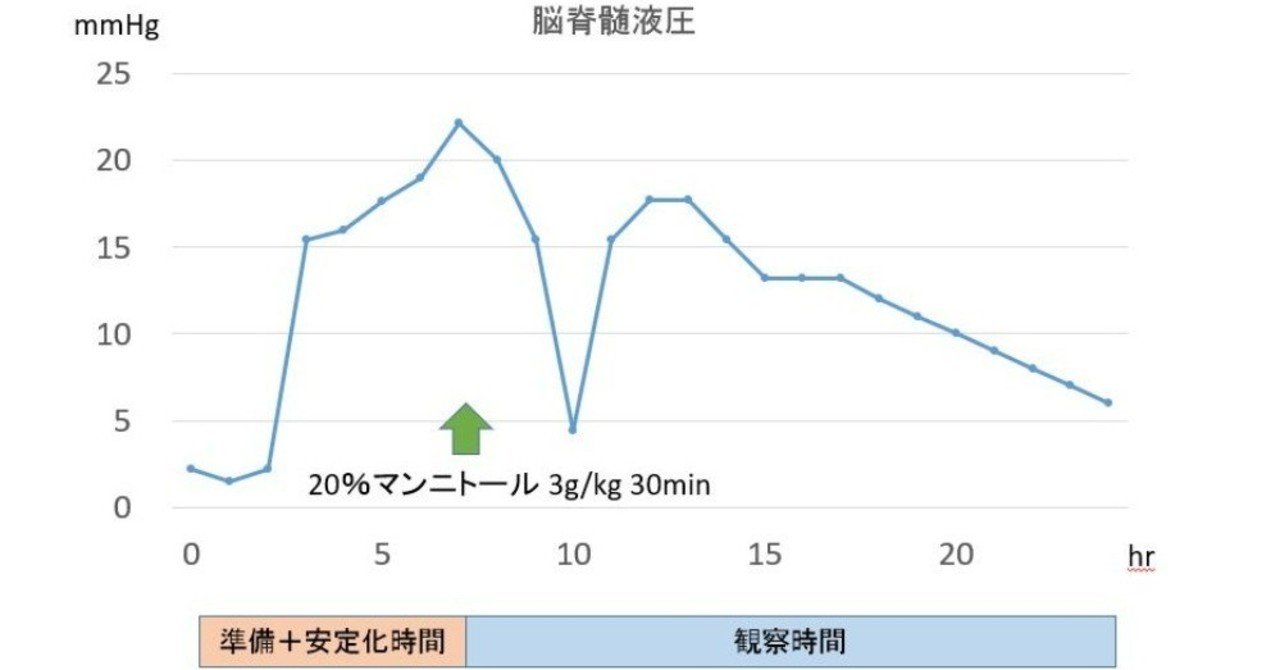
無菌器具を使用した静脈内投与用。
注意:
直列接続では一次パッケージを使用しないでください。このような処置は、第2のパッケージからの流体の投与が完了する前に、第1のパッケージから吸引された残留空気により空気塞栓症を引き起こす可能性がある。

製品の無菌性が損なわれ、汚染の危険があるため、パッケージに穴を開けないでください。
開くには:
Istarbag (PVC) 袋の場合は、薬剤を使用する際に保護包装紙を取り外してください。一次包装をしっかりと絞って、最小限の漏れがないか確認してください。溶液の漏れが観察された場合は、無菌性が損なわれる可能性があるため、包装を廃棄してください。

追加の薬剤が必要な場合は、投与用の溶液を準備する前に以下の指示に従ってください。
非経口溶液 (SP) を準備および投与する場合、以下に関する医療サービスにおける感染制御委員会の推奨事項に従う必要があります。
- 環境と表面の消毒。手の消毒。 PPEの使用。
- バッグ、薬剤追加ポイント、輸液ライン接続部の消毒。
- パッケージの底部にある溶液出口チューブからプラスチック製のプロテクターを取り外します。
- 70% アルコールを使用して一次パッケージを清掃します。
- サポートストラップでパッケージを吊り下げます。
- 溶液注入装置を接続します。機器の使用説明書を参照してください。
- 医師の処方箋に従って、持続点滴によって溶液を投与します。
薬を追加するには:
注意: 薬と溶液の間に不適合性があるかどうか、また該当する場合は薬間に不適合性があるかどうかを確認してください。

非経口溶液に医薬品を追加できるのは、機器用と医薬品投与用の 2 つの場所があるパッケージのみです。
非経口溶液の投与前の薬物投与の場合:
- 注射部位を無菌的に準備します。
- 滅菌針の付いた注射器を使用して、薬物投与に適した部位に穴をあけ、薬物を非経口溶液に注入します。
- 薬剤を非経口溶液に完全に混合します。
- 凍結乾燥粉末は、非経口溶液に添加する前に、適切な滅菌発熱性希釈剤で再構成/懸濁する必要があります。
非経口溶液投与中の薬物投与の場合:
- 輸液セットのクランプを閉じます。
- 無菌処理を実行して、薬剤投与に適切な部位を準備します。
- 滅菌針の付いた注射器を使用して部位に穴をあけ、非経口溶液に薬を加えます。
- 薬剤を非経口溶液に完全に混合します。
- 投与を継続します。
Istarbag バッグの場合、バッグとオーバーバッグの間に小さな水滴が存在する場合がありますが、これは製品および製造プロセスの特徴です。滅菌プロセスにより、パウチのプラスチックに多少の不透明さが見られる場合があります。これは正常なことであり、ソリューションの品質や安全性には影響しません。不透明度は徐々に減少します。
20% マンニトール溶液は低温にさらされると結晶化する可能性があります。投与前に結晶を検査してください。結晶の存在が観察された場合は投与しないでください。
このような結晶化が発生した場合、推奨される再可溶化手順は、定期的に激しく撹拌しながら加熱することです (無傷の軟質プラスチック包装の場合は 60 ~ 80 ℃ )。溶液を室温または体温まで冷却し、使用前に溶液に結晶が存在していないか再度検査してください。濾過装置を使用して管理します。
非経口溶液の調製および投与は、処方箋に従わなければなりません。その前に、その成分間で発生する可能性のある物理化学的適合性および薬物相互作用について薬剤師が注意深く評価する必要があります。
総投与量と投与速度は、治療対象の状態の性質と重症度、水分要求量、および尿量によって決定されなければなりません。約 200mg/kg 体重の 20% マンニトールの試験用量 (これは約 75mL の非経口溶液を意味します) を 3 ~ 5 分間かけて注入し、次の 2 ~ 3 分間少なくとも 30 ~ 50mL/時間の尿流量を生成します。何時間も。
小児の場合、用量は 200mg/kg、または体の面積 1 平方メートルあたり 6 グラムを 5 分間かけて投与します。尿流量が増加しない場合は、2 回目の試験用量を投与できます。反応が不十分な場合は、患者を再評価する必要があります。
眼圧および頭蓋内圧を低下させるには、20% 溶液 (7.5 ~ 10 mL/kg) を 1.5 ~ 2.0 g/kg の用量で 30 ~ 60 分間かけて投与すると、即時かつ最大の効果が得られます。通常、成人の頭蓋内圧の最大低下は、0.25g/kg の用量を 6 ~ 8 時間ごとの頻度で投与することで達成できます。
血液と脳脊髄液の間の浸透圧勾配が約 10 mOsmol であれば、頭蓋内圧は十分に低下します。脳脊髄液圧および眼内液圧の低下は、マンニトール注入の開始から 15 分で起こり、注入終了後も 3 ~ 8 時間続きます。
補助的な添加剤の使用は推奨されません。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
マンニトール 20% を使い忘れた場合はどうすればよいですか?
この薬の使用は病院環境で行われ、専門家によって指導および実施され、患者の行動には依存しません。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
マンニトール 20% に関する注意事項 – Eurofarma
マンニトールは細胞の外に残ります。血清中に高濃度のマンニトールが存在する場合、または患者がアシドーシス(血中pHが非常に低い)である場合、マンニトールが血液脳関門を通過して逆効果を引き起こし、頭蓋内圧を上昇させる可能性があります。
細胞外液の突然の膨張は劇症性うっ血性心不全を引き起こす可能性があるため、マンニトールを急速に投与する前に患者の心血管の状態を注意深く評価する必要があります。
マンニトール注入後のナトリウムを含まない細胞内液の細胞外コンパートメントへの移動により、血清ナトリウム濃度が低下し、既存の低ナトリウム血症が悪化する可能性があります(ナトリウム濃度の低下)。利尿(尿生成)を維持するためにマンニトールを投与すると、不十分な水分補給や血液量減少が隠蔽され、さらに悪化する可能性があります。
電解質を含まないマンニトール注射は血液と一緒に投与しないでください。血中ナトリウムおよびカリウム濃度の適切なモニタリング。血液濃縮(血液濃度)または血液希釈(血液希釈)の程度(ある場合)。腎臓(腎臓)、心臓(心臓)、肺機能の指標は、体液や電解質の過剰な排出を避けるために不可欠です。
実質的に高張の溶液(約600mOms/L)の投与は、静脈に損傷を引き起こす可能性がある。
マンニトール 20% の副作用 – Eurofarma
高用量で投与される 20% マンニトール溶液は、マンニトールを細胞の内側から外側に除去し、過剰な血管拡張を引き起こし、組織の脱水、うっ血性心不全(心不全)、脳の脱水(特に以下の患者の場合)を引き起こす可能性があります。心不全)、腎臓)および肺水腫。 20% マンニトールの急速投与は、開頭術 (脳手術) を受ける患者に低血圧を引き起こしました。マンニトール 20% 溶液は、頭蓋内圧亢進症の治療のためにマンニトールを投与されている患者において乏尿性腎不全 (尿量の減少を伴う腎不全) を引き起こす可能性があります。血液透析技術によりマンニトールが除去され、水分と浸透圧のバランスが再確立されます。
マンニトールの静脈内投与は、吐き気、嘔吐、口渇、頭痛、めまい、震え、発熱、頻脈(心臓の鼓動)、胸痛、高ナトリウム血症(血液中の過剰なナトリウム濃度)、脱水症状、目のかすみ、蕁麻疹(かゆみ)または高血圧(血圧の上昇)。過敏症(アレルギー)反応も報告されています。
溶液の血管外漏出は、浮腫(腫れ)や皮膚壊死を引き起こす可能性があります。血栓静脈炎(静脈の血栓形成と炎症)が発生することもあります。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。また、顧客サービスを通じて会社に通知してください。
マンニトール特別人口 20% – Eurofarma
妊娠
この薬は、医師または歯科外科医のアドバイスなしに妊娠中の女性が使用すべきではありません。
子供、高齢者、またはその他のリスクグループでの使用
マンニトール 20% 溶液の静脈内投与が高齢者、子供、授乳中の女性に禁忌や副作用を引き起こすという報告はありません。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
マンニトール 20% の組成 – Eurofarma
溶液の各 mL には以下が含まれます。
| マンニトール | 200mg |
| 注射用水 適量 | 1mL |
カロリー内容:
0.8Kcal/L。
浸透圧:
1098mOsm/L。
pH:
4.5~7.0。
マンニトール 20% の過剰摂取 – Eurofarma
20% マンニトール溶液の過剰摂取は、心臓の過負荷、急性肺の腫れ、体液と電解質のバランスの変化を引き起こす可能性があります。関連する症状には、吐き気、嘔吐、頭痛、震え、胸痛などがあります。過剰摂取の場合は投与を中止してください。血液透析技術によりマンニトールが除去され、水分と浸透圧のバランスが再確立されます。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。
中毒の場合、対処方法についてさらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
マンニトール 20% の薬物相互作用 – Eurofarma
マンニトール溶液 (活性物質) および他の薬剤との相互作用は、これまでのところ知られていません。医療用媒体として使用しないでください。
ジギタリス配糖体によるジギタリス毒性の可能性が高まる可能性があります。また、他の利尿薬の利尿作用や眼圧降下作用を高める可能性もあります。
リスクカテゴリー C: この薬は、医師または歯科外科医のアドバイスなしに妊婦が使用すべきではありません。
物質マンニトール 20% の作用 – Eurofarma
薬理学的特徴
マンニトール溶液(活性物質)は浸透圧効果を発揮し、顕著な利尿を誘発します。マンニトール (活性物質) は浸透圧利尿薬であり、腎臓から排泄されます。
マンニトール (活性物質) は、尿細管による水の吸収を防ぎ、ナトリウムと塩化物の排泄を改善し、それによって糸球体濾液の浸透圧を高めます。マンニトール(活性物質)の静脈内投与によって引き起こされる細胞外浸透圧の増加は、細胞内水の細胞外および血管空間への移動を誘発します。この作用は、頭蓋内圧、頭蓋内浮腫、および眼圧上昇の低下におけるマンニトール(活性物質)の役割の基礎となります。血液脳関門を通過したり、目に入ることはありません。
脳脊髄圧および眼圧の低下は、注入開始後 15 分以内に起こります。マンニトール (活性物質) を静脈内注射すると、肝臓での重要な代謝が起こる前に、腎臓から急速に排泄されます。マンニトール(活性物質)の排泄半減期は約 100 分(急性腎不全の場合は最大 36 時間延長可能)で、1 ~ 3 時間の注入後に利尿効果が観察されます。マンニトール溶液(活性物質)は、血管浸透圧を上昇させることにより、循環血管への液体の供給を増加します。
マンニトール 20% ストレージケア – Eurofarma
製品は、光や湿気を避け、15 ℃ ~30 ℃の温度で保管する必要があります。
有効期限
製造日から24ヶ月。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。
薬の特徴
液体、透明、低張性、無菌、非発熱性。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観の変化(結晶化を除く、6項参照)に気づいた場合は、使用の可否について医師または薬剤師に相談してください。
すべての薬は子供の手の届かないところに保管してください。
マンニトール 20% の法的声明 – Eurofarma
使用は病院に限定されます。
医師の処方箋に基づいて販売します。
MS 登録番号: 1.0311.0071
返事。コーチ: ヴィヴィアン・デジデリ – CRF-GO nº 2362。








-1024x576.jpg?resize=1024,576&ssl=1)


