出典:Zofran Medication Professional 情報シート。

オンダンセトロン塩酸塩の禁忌 – Isofarma
オンダンセトロン塩酸塩二水和物(活性物質)は、配合成分のいずれかに対して過敏症があることがわかっている患者には禁忌です。
オンダンセトロン塩酸塩二水和物(有効成分)を塩酸アポモルヒネと併用した場合に重度の低血圧および意識喪失が生じたという報告に基づき、これらの物質の併用は禁忌です。
出典:Zofran Medication Professional 情報シート。
オンダンセトロン塩酸塩の使い方 – Isofarma
静脈内または筋肉内。
オンダンセトロン塩酸塩二水和物(活性物質)注射液は、他の薬剤と同じ注射器または点滴で投与しないでください。
オンダンセトロン塩酸塩二水和物(有効成分)の注射液は1回限りの使用とし、開封後は直ちに注射または希釈してください。残った溶液はすべて廃棄する必要があります。アンプルはオートクレーブ滅菌しないでください。
PVC バッグと機器を使用して互換性研究が実施されました。ペットバッグまたはタイプ 1 ガラス瓶を使用して安定性をチェックします。
0.9% w/v NaCl 溶液または 5% w/v グルコース溶液でのオンダンセトロンの希釈は、ポリプロピレン製注射器中で安定であることが実証されました。
したがって、以下で推奨する適合性輸液で希釈したオンダンセトロンは、ポリプロピレン製注射器中で安定である可能性があると考えられます。
医薬品の適正管理に従って、静脈内溶液は注入時に適切な無菌条件下で調製されなければなりません。
静脈内輸液との適合性
注射用オンダンセトロン塩酸塩二水和物(有効成分)は、推奨される輸液とのみ混合してください。適合性研究により、注射可能なオンダンセトロン塩酸塩二水和物 (活性物質) 溶液は、以下の静脈内輸液を使用した場合、25°C 以下の温度、蛍光灯下または冷蔵庫内で 7 日間安定であることが実証されています。
- 静脈内塩化ナトリウム溶液 0.9% w/v;
- 静脈内ブドウ糖溶液 5% w/v;
- マンニトール静脈内溶液 10% w/v;
- リンゲル点滴静注液。
- 0.3% w/v 塩化カリウム + 0.9% w/v 塩化ナトリウムの静脈内溶液。
- 塩化カリウム溶液 0.3% w/v + グルコース 5% w/v の静脈内投与。
他の薬剤との適合性
注射用オンダンセトロン塩酸塩・二水和物(有効成分)は、例えば輸液ボトルや輸液ポンプを用いて1mg/時間の量で静脈内投与することができる。以下の薬物は、オンダンセトロンとともに、Y 装置を通じて 16 ~ 160 μg/mL (たとえば、それぞれ 8 mg/500 mL および 8 mg/50 mL) の濃度で投与できます。
シスプラチン
最大 0.48 mg/mL (たとえば、500 mL 中に 240 mg) の濃度を 1 ~ 8 時間かけて投与します。
フルオロウラシル
最大 0.8 mg/mL の濃度(たとえば、3 リットルで 2.4 g、または 500 mL で 400 mg)を、少なくとも 20 mL/h(24 時間あたり 500 mL)の速度で投与します。高濃度の 5-フルオロウラシルはオンダンセトロンの沈殿を引き起こす可能性があります。 5-フルオロウラシル点滴には、適合性が示されている他の賦形剤に加えて、最大 0.045% w/v の塩化マグネシウムが含まれる場合があります。
カルボプラチン
0.18 mg/mL ~ 9.9 mg/mL (たとえば、500 mL 中の 90 mg ~ 100 mL 中の 990 mg) の濃度を 10 分から 1 時間かけて投与します。
エトポシド
0.144 mg/mL ~ 0.25 mg/mL (たとえば、500 mL 中の 72 mg ~ 1,000 mL 中の 250 mg) の範囲の濃度を 30 分から 1 時間かけて投与します。
セフタジジム
250 mg ~ 2,000 mg の範囲の用量を、メーカーの推奨に従って注射用滅菌水で溶解し (たとえば、250 mg の場合は 2.5 mL、セフタジジム 2 g の場合は 10 mL)、静脈内ボーラス注射として約 1 分間投与します。 5分。

シクロホスファミド
メーカーの推奨に従って、注射用滅菌水で再構成した100 mg〜1 gの用量、シクロホスファミド100 mgあたり5 mL、シクロホスファミド100 mgあたり5 mLを、約5分間かけて静脈内ボーラス注射として投与した。
ドキソルビシン
メーカーの推奨に従って、注射用滅菌水でドキソルビシン 10 mg あたり 10 mg から 100 mg の範囲の用量、ドキソルビシン 10 mg あたり 5 mL を再構成し、静脈内ボーラス注射として約 5 分間投与しました。
デキサメタゾン
リン酸デキサメタゾンナトリウム 20 mg を、点滴 Y セットを介して 2 ~ 5 分間かけてゆっくりとした静脈内注射として投与でき、50 mL ~ 100 mL の互換性のある点滴液で希釈した 8 mg または 16 mg のオンダンセトロンを約 15 分間放出します。 。リン酸デキサメタゾンナトリウムとオンダンセトロンの適合性は、同じ装置を介してこれらの薬物を投与することで実証され、その結果、リン酸デキサメタゾンナトリウムは 32 μg ~ 2.5 mg/mL の範囲、デキサメタゾン ナトリウム 1 mg/mL では 8 μg の濃度となりました。オンダンセトロン。
オンダンセトロン塩酸塩二水和物の用量
化学療法および放射線療法によって引き起こされる吐き気と嘔吐
がん治療における催吐性の可能性は、使用される化学療法と放射線療法の用量と組み合わせによって異なります。用量レジメンの選択は、嘔吐の重症度によって決定する必要があります。
大人
推奨される静脈内または筋肉内用量は 8 mg で、治療直前に投与されます。
催吐性の高い化学療法の場合、最大初回静脈用量 16 mg のオンダンセトロンを 15 分間かけて注入することができます。 16 mg を超える単回静脈内投与は行わないでください。
催吐性の高い化学療法におけるオンダンセトロン塩酸塩二水和物(活性物質)の有効性は、化学療法前にデキサメタゾンリン酸ナトリウム 20 mg を単回静脈内投与することで増強できます。最初の 24 時間以降の長期または遅発性嘔吐を防ぐために、経口治療が推奨されます。
8 mg を超え最大 16 mg までの静脈内用量の場合は、投与前に 50 mL ~ 100 mL の 0.9% 塩化ナトリウム注射剤または 5% ブドウ糖注射剤で希釈し、15 分以上注入する必要があります(使用方法を参照)。 )。オンダンセトロン塩酸塩二水和物(活性物質)の用量が 8 mg 以下の場合、希釈する必要はなく、30 秒以上かけてゆっくりとした筋肉内または静脈内注射として投与する必要があります。
オンダンセトロン塩酸塩二水和物(活性物質)の初回用量の後には、2 時間または 4 時間間隔で 8 mg を 2 回筋肉内または静脈内投与するか、または 1 mg/h を最長 24 時間持続的に注入する必要があります。
小児および青少年(生後6か月から17歳まで)
化学療法誘発性の悪心および嘔吐の場合の用量は、体表面積または体重に基づいて計算できます。小児の臨床研究では、オンダンセトロンは、25 ~ 50 mL の生理食塩水またはその他の適合する輸液で希釈し、15 分以上かけて静脈内注入によって投与されました。
体表面積に基づく投与量
オンダンセトロン塩酸塩二水和物(活性物質)は、化学療法の直前に 5 mg/m2 の用量で単回静脈内投与する必要があります。静脈内投与量は 8 mg を超えてはなりません。経口投与は 12 時間後に開始し、最長 5 日間継続することができます (表 1)。成人用量を超えてはなりません。
表 1: 化学療法誘発性の悪心および嘔吐に対する体表面積に基づく用量 (2 ~ 17 歳)
|
体表面積 |
1日目 |
2日目~6日目 |
|
?0.6m2~?1.2m2 |
5 mg/ m2 を静脈内投与、さらに 12 時間後に 4 mg を経口投与 |
12時間ごとに4mg経口投与 |
|
gt; 1.2㎡ |
5 または 8 mg/m 2 を静脈内投与、さらに 12 時間後に 8 mg を経口投与 |
12時間ごとに8mgを経口投与 |
体重に基づいた投与量
オンダンセトロン塩酸塩二水和物(活性物質)は、化学療法の直前に 0.15 mg/kg の単回静脈内投与が必要です。静脈内投与量は 8 mg を超えてはなりません。 1日目には、4時間間隔でさらに2回の静脈内投与を行うことができます。経口投与は 12 時間後に開始でき、最長 5 日間継続できます (表 2)。成人用量を超えてはなりません。
表 2: 化学療法誘発性の吐き気および嘔吐に対する体重に基づく投与量 (2 ~ 17 歳)
|
体重 |
1日目 |
2日目~6日目 |
|
gt; 10kg |
0.15 mg/kg を 4 時間ごとに最大 3 回静脈内投与 |
12時間ごとに4mg経口投与 |
お年寄り
65 歳以上の患者の場合、静脈内投与はすべて希釈して 15 分かけて注入する必要があり、繰り返す場合は 4 時間以上の間隔をあけるべきです。
65~74歳の患者では、オンダンセトロン塩酸塩二水和物(活性物質)8 mgまたは16 mgを15分間かけて初回静脈内投与し、その後、15分間かけて8 mgを2回点滴し、間隔をあけて投与する必要があります。 4時間未満。
75 歳以上の患者の場合、オンダンセトロン塩酸塩二水和物 (活性物質) の初回静脈内用量は 15 分間かけて 8 mg を超えてはなりません。初回用量 8 mg の後に、4 時間以上の間隔をあけて、15 分間かけて 8 mg を 2 回注入する必要があります。
腎不全患者
投与経路、1日の投与量、または投与頻度を変更する必要はありません。
肝不全患者
中等度または重度の肝不全患者では、オンダンセトロン塩酸塩二水和物(活性物質)のクリアランスが大幅に減少し、血漿半減期が大幅に延長されます。これらの患者の場合、静脈内または経口での 1 日の総用量は 8 mg を超えてはなりません。
スパルテイン/デブリソキン代謝不全患者
オンダンセトロンの排出半減期は、スパルテインおよびデブリソキン代謝欠損症の人では変化しません。
したがって、そのような患者では、反復投与によって一般集団で発生するものと異なるレベルの薬物曝露が引き起こされることはありません。
1日の投与量や投与頻度を変更する必要はありません。
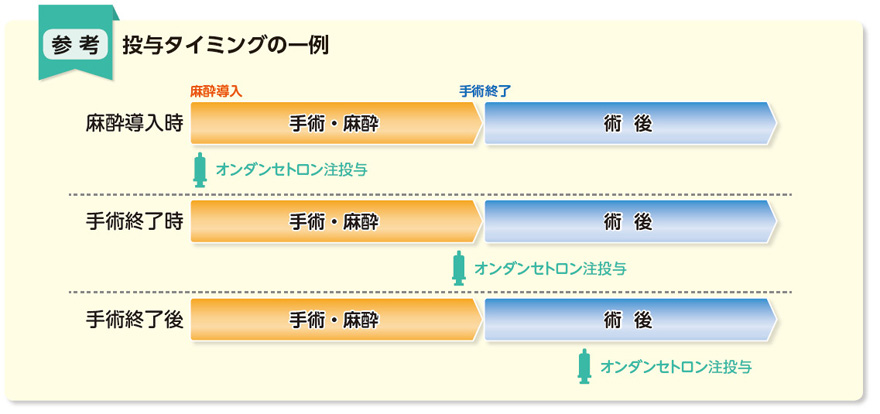
術後の吐き気と嘔吐
大人
術後の吐き気や嘔吐を防ぐために、オンダンセトロン塩酸塩二水和物(有効成分)を単回 4 mg で使用することが推奨されており、麻酔導入時に筋肉内またはゆっくりとした静脈内注射で投与できます。
確立された術後の悪心および嘔吐の治療には、4 mg の単回投与をゆっくりとした筋肉内または静脈内注射によって投与することが推奨されます。
小児および青少年(生後1か月から17歳まで)
全身麻酔下で手術を受ける小児患者の術後の吐き気と嘔吐の予防と治療のために、オンダンセトロンは、導入前、導入中、導入後に、0.1 mg/kg、最大 4 mg の用量でゆっくりとした静脈内注射によって投与できます。麻酔中または手術後。
お年寄り
高齢者の術後の吐き気や嘔吐の予防と治療にオンダンセトロン塩酸塩二水和物(活性物質)を使用した研究はほとんどありませんが、オンダンセトロン塩酸塩二水和物(活性物質)は化学療法を受けている65歳以上の患者に十分に忍容性があります。 。
腎不全患者
投与経路、1日の投与量、または投与頻度を変更する必要はありません。
肝不全患者
中等度または重度の肝不全患者では、オンダンセトロン塩酸塩二水和物(活性物質)のクリアランスが大幅に減少し、血漿半減期が大幅に延長されます。これらの患者の場合、静脈内または経口での 1 日の総用量は 8 mg を超えてはなりません。したがって、非経口または経口投与が推奨されます。
スパルテイン/デブリソキン代謝不全患者
オンダンセトロンの排出半減期は、スパルテインおよびデブリソキン代謝欠損症の人では変化しません。
したがって、そのような患者では、反復投与によって一般集団で発生するものと異なるレベルの薬物曝露が引き起こされることはありません。
1日の投与量や投与頻度を変更する必要はありません。
出典:Zofran Medication Professional 情報シート。
オンダンセトロン塩酸塩の使用上の注意 – Isofarma
他の選択的 5-HT3 受容体拮抗薬に対してすでにこの種の反応を示した患者における過敏症反応の報告があります。
さらに、オンダンセトロンは用量依存的に QT 間隔を延長します。トルサード ド ポワントの市販後の症例がオンダンセトロンを使用した患者で報告されています。先天性 QT 延長症候群の患者に対するオンダンセトロンの使用は避けてください。オンダンセトロン塩酸塩二水和物(活性物質)は、QTc 延長を有する患者、または QTc 延長を発症する可能性のある患者には注意して投与する必要があります。これらの症状には、電解質障害のある患者、先天性 QT 延長症候群のある患者、または QT 延長または電解質障害を引き起こす他の薬剤を服用している患者が含まれます。 。
オンダンセトロンを投与する前に、低カリウム血症と低マグネシウム血症を改善する必要があります。
オンダンセトロン塩酸塩二水和物(活性物質)と他のセロトニン作動薬の併用後にセロトニン症候群が報告されています。
オンダンセトロン塩酸塩二水和物(活性物質)と他のセロトニン作動薬との併用治療が臨床的に正当である場合、患者の適切な観察が推奨されます。
オンダンセトロンは大腸内の通過時間を延長するため、亜急性腸閉塞の兆候がある患者は投与後に監視する必要があります。
注射用オンダンセトロンは、同じ注射器で投与したり、他の薬剤と注入したりしないでください。
オンダンセトロン注射剤は、推奨される輸液のみを使用して投与してください。
車両の運転や機械の操作能力への影響
精神運動検査では、オンダンセトロン塩酸塩二水和物(活性物質)は、これらの活動における患者のパフォーマンスを損なうことはなく、また鎮静を引き起こすこともありませんでした。オンダンセトロン塩酸塩二水和物(活性物質)の薬理により、これらの各活動において悪影響は予想されません。
妊娠
リスクの概要
妊婦に対するオンダンセトロンの使用の安全性はまだ確立されていません。ラットとウサギを用いた生殖研究では、オンダンセトロンが器官形成中に体表面積に基づく最大推奨経口用量24 mg/日の約6倍と24倍でそれぞれ投与された場合、胎児に害を及ぼす証拠は示されなかった。ただし、動物実験は常に人間の反応を予測できるわけではないため、妊娠中のオンダンセトロンの使用は推奨されません。
妊娠中のオンダンセトロンの安全性データは限られており、入手可能な薬物疫学研究の結果には一貫性がありません。
製造販売後の報告では、妊娠中の塩酸オンダンセトロン二水和物(原体)の使用による先天奇形の症例が報告されていますが、因果関係を確立するには不十分な報告です。
動物データ
ラットとウサギの胚・胎児発育研究では、器官形成期に妊娠雌にそれぞれ最大 15 mg/kg/日および 30 mg/kg/日のオンダンセトロンを経口投与しました。ウサギの母親の体重増加がわずかに減少したことを除いて、母親動物や子供の発育に対するオンダンセトロンの有意な影響はありませんでした。ラットで 15 mg/kg/日、ウサギで 30 mg/kg/日の用量では、母親の用量は、体表面積に基づいて、それぞれヒトの最大推奨経口用量 24 mg/日の約 6 倍と 24 倍でした。 。出生前および出生後の発生毒性研究では、妊娠 17 日目から出産 21 日目まで、妊娠中のラットに 15 mg/kg/日までのオンダンセトロンを経口投与しました。母親の体重増加がわずかに減少したことを除いて、妊娠したラットや、交配した F1 世代の生殖能力を含む、その子の出生前および出生後の発育には影響はありませんでした。雌ラットにおける 15 mg/kg/日の用量では、母親の用量は、体表面積に基づくヒトの最大推奨経口用量 24 mg/日の約 6 倍でした。
授乳中
リスクの概要
オンダンセトロン塩酸塩二水和物(有効成分)が母乳に移行するかどうかは不明です。母乳育児中の小児に対するオンダンセトロン塩酸塩二水和物(活性物質)の影響、または乳生産に対するオンダンセトロン塩酸塩二水和物(活性物質)の影響に関するデータはありません。しかし、オンダンセトロンは動物の乳中に排泄されることが示されています。このため、オンダンセトロンによる治療を受けている授乳中の女性は授乳しないことが推奨されます。
生殖能力のある女性と男性
妊娠検査薬
生殖能力のある女性については、オンダンセトロン塩酸塩二水和物(有効成分)による治療を開始する前に、妊娠の状態を確認する必要があります。
避妊
生殖能力のある女性は、オンダンセトロン塩酸塩二水和物(活性物質)が発育中の胎児に害を及ぼす可能性について警告する必要があります。生殖能力のある性的に活動的な女性は、オンダンセトロン塩酸塩二水和物(活性物質)による治療中および治療中止後2日間、効果的な避妊法(妊娠率が1%未満となる方法)を使用することが推奨されます。
不妊
オンダンセトロン塩酸塩二水和物(有効成分)は生殖能力に影響を及ぼしません。
妊娠リスクカテゴリーB
この薬は、医師または歯科医の指導なしに妊娠中の女性が使用しないでください。
出典:Zofran Medication Professional 情報シート。
オンダンセトロン塩酸塩の副作用 – Isofarma
非常に一般的なイベント、一般的なイベント、および珍しいイベントは、通常、臨床研究データから決定されます。プラセボ群の発生率が考慮されました。まれなイベントおよび非常にまれなイベントは、自発的な市販後のデータから決定されます。以下の頻度は、適応症および処方に応じたオンダンセトロン塩酸塩二水和物(有効成分)の推奨標準用量で推定されます。
非常に一般的な反応 (gt; 1/10)
頭痛。
一般的な反応 (>1/100 および <1/10)
- 熱感または紅潮感;
- 便秘;
- 静脈注射部位での反応。
異常な反応 (>1/1,000 および <1/100)
- けいれん;
- 運動障害(臨床的後遺症の持続に関する決定的な証拠なしに観察される、眼科発作、ジストニー反応、ジスキネジアなどの錐体外路障害を含む)
- 不整脈;
- ST セグメントの低下の有無にかかわらず、胸痛。
- 徐脈;
- 低血圧;
- しゃっくり。
- 肝機能検査の無症候性の増加(これらの反応は、シスプラチンによる化学療法を受けている患者で観察されています)。
まれな反応 (>1/10,000 および <1/1,000)
アナフィラキシーを含む、即時型の、時には重度の過敏反応。急速な静脈内投与中に主にめまいが起こる。主に静脈内投与中の一時的な視覚障害(かすみ目など)。 QT間隔の延長(トルサード・ド・ポワントを含む)。
非常にまれな反応 (lt; 1/10,000)
一時的な失明、主に静脈内投与時の失明。有毒な表皮壊死融解症を含む有毒な発疹。
報告された失明症例のほとんどは 20 分以内に解決しました。ほとんどの患者はシスプラチンなどの化学療法剤を受けました。一過性の失明の一部の症例は皮質起源であると報告されています。
有害事象が発生した場合は、健康監視通知システム – NOTIVISA (http://portal.anvisa.gov.br/notivisa で利用可能)、または州または地方自治体の健康監視に通知してください。
出典:Zofran Medication Professional 情報シート。
オンダンセトロン塩酸塩の薬物相互作用 – Isofarma
特定の研究では、オンダンセトロンをアルコール、テマゼパム、フロセミド、トラマドール、またはプロポフォールと一緒に投与した場合、薬物動態学的相互作用がないことが実証されています。
オンダンセトロンは、複数のシトクロム P450 肝酵素 CYP3A4、CYP2D6、CYP1A2 によって代謝されます。オンダンセトロンを代謝できる酵素は多数あるため、これらの酵素のうちの 1 つの活性の阻害または低下(遺伝的 CYP2D6 欠損など)は通常、他の酵素によって補われ、オンダンセトロンのクリアランスにほとんど変化が生じず、用量調整が必要になります。 。
オンダンセトロンを QT 間隔を延長したり、電解質障害を引き起こす薬剤と併用する場合は注意が必要です。
アポモルヒネ
ゾフランによる重度の低血圧と意識喪失の報告に基づいていますか?塩酸アポモルヒネとの併用は禁忌です。
フェニトイン、カルバマゼピン、リファンピシン
フェニトイン、カルバマゼピン、リファンピシンなどの強力な CYP3A4 誘導剤で治療された患者では、オンダンセトロンの経口クリアランスが増加し、血漿濃度が減少しました。
セロトニン作動薬
ゾフランとの併用により、セロトニン症候群(精神状態の変化、自律神経の不安定、神経筋の異常を含む)が報告されていますか?選択的セロトニン再取り込み阻害剤 (SSRI) やセロトニンおよびノルエピネフリン再取り込み阻害剤 (SNRI) を含むその他のセロトニン作動薬。
トラマドール
小規模な研究からのデータは、オンダンセトロンがトラマドールの鎮痛効果を軽減する可能性があることを示しています。
出典:Zofran Medication Professional 情報シート。
物質オンダンセトロン塩酸塩の作用 – Isofarma
有効性の結果
オンダンセトロン塩酸塩二水和物(活性物質)は、シスプラチン化学療法を受けた患者の 75% において、吐き気と嘔吐を制御する効果を実証しました。 1
参考文献
1 MARTY M. et al .シスプラチン誘発性嘔吐の制御における、5-ヒドロキシトリプタミン3 (セロトニン) アンタゴニストであるオンダンセトロン (GR 38032F) と高用量メトクロプラミドとの比較。 N Engl J Med、32;322(12): 816-21、1990。
薬理学的特徴
薬力学特性
作用機序
オンダンセトロン塩酸塩二水和物(活性物質)の活性物質であるオンダンセトロンは、5-HT3 受容体の強力で高度に選択的なアンタゴニストです。吐き気と嘔吐の制御におけるその作用機序はまだよく知られていません。
化学療法剤および放射線療法は、小腸で 5-HT の放出を引き起こし、5-HT3 受容体で迷走神経求心性神経を活性化することによって咽頭反射を開始する可能性があります。オンダンセトロンは、この反射の開始をブロックします。
迷走神経の求心性神経の活性化により、第 4 脳室の床にある極端な領域で 5-HT の放出が引き起こされることもあり、これにより中枢機構を通じて嘔吐が促進されることもあります。したがって、細胞傷害性化学療法および放射線療法によって引き起こされる吐き気および嘔吐の制御におけるオンダンセトロンの効果は、末梢神経系および中枢神経系のニューロンの 5-HT3 受容体に対する薬剤の拮抗作用によるものです。
術後の吐き気と嘔吐の作用機序は不明ですが、その経路は細胞毒性物質によって引き起こされる吐き気と嘔吐の経路と共通しているはずです。
注射用オンダンセトロン塩酸塩・二水和物(有効成分)は、作用発現が早いため、必要に応じて麻酔導入時や化学療法・放射線療法の直前に投与できます。
薬力学的効果
オンダンセトロンは血漿プロラクチン濃度を変化させません。
QT間隔の延長
QTc 間隔に対するオンダンセトロンの効果は、58 人の健康な成人 (男性および女性) を対象とした二重盲検、ランダム化、プラセボ対照、陽性対照 (モキシフロキサシン) クロスオーバー研究で評価されました。オンダンセトロンの用量は 8 mg および 32 mg の静脈内注入でした。 15分以上。試験した最高用量の 32 mg では、ベースライン補正後のプラセボと比較した QTcF 間隔の平均最大差 (90% CI の上限) は 19.6 (21.5) ミリ秒でした。試験した最低用量である 8 mg では、ベースライン補正後のプラセボとの平均最大差 (90% CI 上限) は 5.8 (7.8) ミリ秒でした。この研究では、480 ミリ秒を超える QTcF 間隔の測定はなく、60 ミリ秒を超える QTcF 間隔の延長もありませんでした。
薬物動態学的特性
オンダンセトロンの薬物動態学的特性は、繰り返し投与しても変化しません。
吸収
オンダンセトロンの筋肉内および静脈内投与後には、同等の全身曝露が観察されました。
分布
血漿タンパク質への結合は約 70% ~ 76% です。成人の場合、経口投与後のオンダンセトロンの利用可能性は、静脈内または筋肉内投与後に観察されるものと同様です。分配量は定常状態で約 140 L です。
代謝
オンダンセトロンは、主に肝臓代謝によって、いくつかの酵素経路を介して体循環から除去されます。 CYP2D6 酵素 (デブリソキン多型) が存在しなくても、オンダンセトロンの薬物動態には影響しません。
排除
オンダンセトロンは、主に肝臓の代謝によって全身循環から除去されます。吸収された線量の 5% 未満が変化せずに尿中に排泄されます。経口投与後のオンダンセトロンの利用可能性は、静脈内または筋肉内投与後に観察されるものと同様です。最終除去半減期は約 3 時間です。
特殊な患者集団
セックス
経口投与後、女性の方が吸収速度と吸収範囲が大きく、全身クリアランスと分布量が減少することが実証されています。
小児および青少年(生後1か月から17歳まで)
手術を受けた生後 1 ~ 4 か月の小児患者 (n=19)のクリアランスは、生後 5 ~ 24 か月の患者 (n=22) よりも約 30% 低かったが、これは 3 ~ 12 歳の患者と同等であった。体重に対して正規化したときの年齢。生後1~4か月の患者の半減期は平均6.7時間であったのに対し、生後5~24か月および3~12歳の患者では2.9時間でした。生後 1 ~ 4 か月の集団における薬物動態パラメーターの違いは、新生児と乳児の体内水分の割合が高いこと、およびオンダンセトロンなどの水溶性薬物の流通量が多いことによって部分的に説明できます。全身麻酔で待機的手術を受ける3歳から12歳の小児患者では、成人患者の値と比較して、オンダンセトロンのクリアランスの絶対値と分布量の減少が見られました。両方のパラメータは体重とともに直線的に増加し、12歳以降、値は若年成人で得られる値に近づきました。クリアランスと分布容積を体重に従って正規化すると、これらのパラメーターの値は異なる年齢グループで同様でした。
体重に合わせて調整された用量の使用は、加齢に伴う変化を補い、小児患者の全身曝露を正常化するのに効果的です。
オンダンセトロンの薬物動態の分析は、オンダンセトロンの静脈内投与後1か月から44歳までの428人(がん患者、手術中の患者、健康なボランティア)を対象に実施されました。この分析に基づくと、小児および青少年における経口または静脈内投与後のオンダンセトロンの全身曝露(AUC)は、生後1~4か月の乳児を除いて成人と同等でした。分布量は年齢に関連しており、乳児や小児よりも成人の方が低かった。クリアランスは、生後 1 ~ 4 か月の乳児を除いて、年齢ではなく体重に関連していました。生後 1 か月から 4 か月の乳児のクリアランスに年齢に関連したさらなる減少があったのか、それともこの年齢グループで研究された個体数が少ないためにこのグループに単にばらつきがあったのかどうかを結論付けるのは困難です。生後6か月未満の患者は、術後の吐き気や嘔吐の場合に単回投与のみであることを考慮すると、クリアランスの減少は臨床的には関連しない可能性があります。
お年寄り
健康な高齢者ボランティアを対象とした初期の第I相試験では、加齢に伴うクリアランスのわずかな減少とオンダンセトロンの半減期の増加が示されました。しかし、個人間のばらつきが大きいため、若年者(65歳未満)と高齢者(65歳未満)の間で薬物動態パラメータにかなりの重複が生じ、若年者と高齢者の乳がん患者の間で安全性と有効性の差異は観察されなかった。高齢者向けに異なる推奨用量をサポートするために、吐き気と嘔吐の臨床試験に参加している高齢者を対象としています。最新の血漿中濃度および曝露反応モデルに基づいて、若年成人と比較した場合、75 歳以上の患者では QTcF に対する影響がより大きいと予測されます。静脈内投与の具体的な用量情報は、65 歳以上および 75 歳以上の患者に提供されます(「用量と投与 – 化学療法および放射線療法によって誘発される悪心および嘔吐 – 高齢者」を参照)。
腎機能障害のある患者さん
中等度の腎機能障害(クレアチニンクリアランスが 15 ~ 60 mL/min)の患者では、オンダンセトロンの静脈内投与後に全身クリアランスと分布量の両方が減少し、排出半減期がわずかに臨床的に有意ではありませんでした(5.4 時間)。 )。定期的な血液透析(透析の合間に研究)を必要とする重度の腎機能障害を持つ患者において、オンダンセトロンは静脈内投与後も本質的に変化しない薬物動態プロファイルを示しました。
肝機能障害のある患者
重度の肝機能障害を有する患者では、オンダンセトロンの全身クリアランスが著しく低下し、排出半減期が延長され(15~32時間)、全身前代謝の低下により経口バイオアベイラビリティが約100%となった。
出典:Zofran Medication Professional 情報シート。








-1024x576.jpg?resize=1024,576&ssl=1)


