すべてのリソソーム遺伝子変化と同様、特に重度の MPS VI の場合、不可逆的な臨床症状が現れる前にできるだけ早く治療を開始することが非常に重要です。
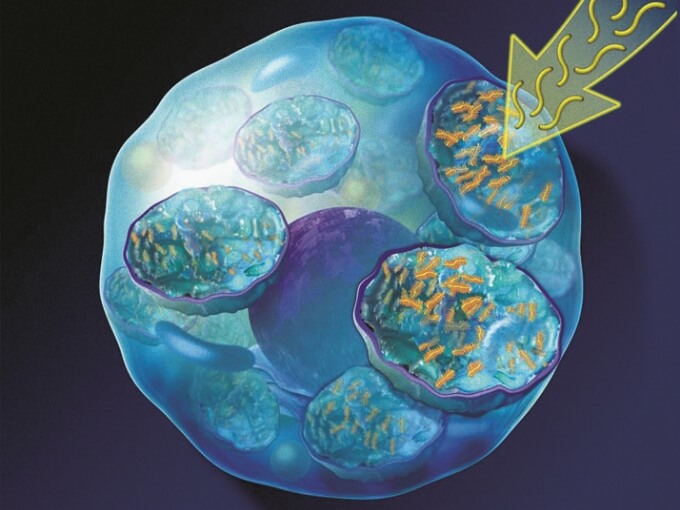
ナグラザイムはどのように作用するのでしょうか?
ナグラザイムは、生産が不足している酵素を患者に提供する酵素補充療法です。
Naglazyme の有効成分であるガルスルファーゼは、ヒトの酵素 N-アセチルガラクトサミン 4-スルファターゼのコピーです。ナグラザイムは、グリコサミノグリカン (GAG) の分解を助け、細胞内での蓄積を防ぎます。この作用により、患者の運動能力など、VI 型ムコ多糖症 (MPS VI) の症状が改善されます。
ガルスルファーゼは、「組換えDNA技術」と呼ばれる方法によって生産されます。つまり、ガルスルファーゼは、酵素を生産できるようにする遺伝子(DNA)を受け取った細胞によって生産されます。
ナグラザイムの禁忌
ナグラザイムは、薬剤または配合成分のいずれかに対して過敏症 (アレルギー) がある場合には禁忌です。
ナグラザイムの使い方
医師または看護師がナグラザイムを投与します。
ナグラザイムの投与量
あなたが受け取る用量はあなたの体重に基づいています。
推奨用量は体重1kgあたり1mgで、週に1回静脈内に点滴(静注)して投与します。各点滴は約 4 時間持続します。最初の 1 時間は注入速度が遅く (溶液全体の約 2.5%)、残りの溶液量 (約 97.5%) が次の 3 時間かけて投与されます。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
ナグラザイムを使い忘れた場合はどうすればよいですか?
ナグラザイムの点滴を忘れた場合は、医師に連絡してください。
この薬の使用について質問がある場合は、医師に相談してください
疑問がある場合は、薬剤師、医師、または歯科外科医にアドバイスを求めてください。
ナグラザイムの予防措置
- ナグラザイム (ガルスルファーゼ) で治療されている場合、注入に関連した反応が発生する可能性があります。注入関連反応は、注入中または注入日の終わりまでに発生する副作用です。このような反応が生じた場合は、直ちに医師に連絡してください。
- アレルギー反応がある場合、医師は点滴量を減らすか中止することがあります。医師はアレルギー反応を制御するために他の薬を投与することもあります。
- 発熱がある場合、またはこの薬を投与する前に呼吸困難がある場合は、ナグラザイム点滴を延期する必要があるかどうかを医師が判断するため、医師に相談してください。
- ナグラザイムは、腎臓や肝臓に問題がある患者を対象として研究されていません。腎不全または肝不全がある場合は医師に伝えてください。
- 筋肉痛、腕や脚のしびれ、または腸や膀胱の問題を経験した場合は、これらの反応は脊髄への圧力によって引き起こされる可能性があるため、医師に相談してください。
妊娠と授乳
ナグラザイムは、明らかに必要な場合を除き、妊娠中に投与すべきではありません。薬を使用する前に医師に相談してください。
ガルスルファーゼが乳中に排泄されるかどうかは不明です。したがって、ナグラザイムによる治療中は授乳を中止する必要があります。薬を使用する前に医師に相談してください。
この薬は、医師または歯科外科医のアドバイスなしに妊娠中の女性が使用すべきではありません。
小児用

ナグラザイムを小児集団に投与する場合に特別な配慮が必要であるという証拠はありません。
重要な問題の1つは、この病気の重篤な形態に苦しむ5歳未満の小児の治療であるが、5歳未満の患者は主な第3相試験には含まれていなかった。
1 歳未満の患者が利用できる選択肢は限られています。
高齢者向けの使用
ナグラザイムを用いて実施された臨床研究には、29歳以上の患者は含まれていませんでした。高齢の患者が同じ反応を示すかどうかは不明です。
車両の運転や機械の操作能力への影響
車両の運転や機械の操作能力に対するナグラザイムの影響に関する研究は行われていません。
ナグラザイムの副作用
すべての薬と同様に、ナグラザイムは副作用を引き起こす可能性がありますが、誰もが副作用を起こすわけではありません。
副作用は主に患者への薬剤投与中または注入直後(「注入反応」)に観察されました。
最も重篤な副作用は次のとおりです。
- 顔の腫れと発熱(非常に一般的)。
- 無呼吸(異常な呼吸間隔)、呼吸困難、喘息、蕁麻疹(一般的)。
- 舌や喉の腫れ、薬に対する重度のアレルギー反応(頻度は不明)。
これらの反応のいずれかが発生した場合は、すぐに医師に知らせてください。アレルギー反応を防ぐため(例:抗ヒスタミン薬やコルチコステロイド)、または熱を下げるため(解熱薬)、他の薬剤の使用が必要な場合があります。これらの薬剤は、ナグラザイムの次の点滴を開始する 30 ~ 60 分前に投与する必要があります。
インフュージョンリアクションの最も一般的な症状は次のとおりです。
- 熱;
- 寒気;
- 発疹;
- 蕁麻疹;
- 息切れ。
最も一般的な副作用 (この薬を使用している患者の 10% 以上で発生) は次のとおりです。
- 喉の痛み;
- 胃腸炎;
- 反射神経が悪い。
- 頭痛;
- 目の炎症(結膜炎);
- かすみ目;
- 聴覚障害;
- 高血圧(高血圧);
- 鼻づまり;
- 突出したへそ。
- 嘔吐;
- 吐き気;
- かゆみ;
- 痛み(耳、腹部、関節、胸の痛みを含む);
- 倦怠感。
一般的な副作用 (この薬を使用している患者の 1% ~ 10% で発生) は次のとおりです。
- 振戦;
- 低血圧(低血圧);
- 咳;
- あえぐ。
- 皮膚の赤み。
頻度が不明な他の反応は次のとおりです。
- ショック;
- チクチク;
- 心拍数の低下;
- 心拍数の増加。
- 青みがかった肌。
- 皮膚の青白さ。
- 血液酸素化の低下。
- 呼吸が速い。
これらの症状、またはこのリーフレットに記載されていないその他の症状が発生した場合は、直ちに医師に連絡してください。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。
また、顧客サービスを通じて会社に通知してください。
ナグラザイムの構成
プレゼンテーション
注射可能な溶液
5 ml の無色ガラスバイアル。5 ml あたり 5 mg のガルスルファーゼ [タンパク質含有量で表す] を含み、ボール紙包装で梱包されています。
小児および成人向け。

静脈内注入としてのみ使用してください。
構成
ガルスルファーゼの公称濃度は 1 mg/mL (タンパク質濃度として表す) です。
賦形剤:
塩化ナトリウム;一塩基性リン酸ナトリウム一水和物;二塩基性リン酸ナトリウム七水和物。ポリソルベート 80、注射用水。
正味量:
5mL。
ナグラザイムの過剰摂取
ナグラザイムは看護師または医師の監督下で投与され、正しい用量が投与されたことを確認し、必要に応じて措置を講じます。
ナグラザイムの使用による過剰摂取に関する文書はありません。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。
さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
ナグラザイムの薬物相互作用
市販薬を含む他の薬を使用しているか、最近使用したことがある場合は、医師に伝えてください。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
ナグラザイムという物質の働き
有効性の結果
臨床研究

5つの研究が完了しました。 5歳から29歳までの合計56人のMPS VI患者が4つの臨床研究に登録された。 1歳未満のMPS VI患者4人を対象に、ランダム化第4相試験も実施された。患者の大部分は重篤な症状を呈しており、これは身体的抵抗試験における不満足な成績によって証明されている。
このランダム化二重盲検多施設プラセボ対照臨床研究では、MPS VI 患者 38 人にガルスルファーゼ (活性物質) 1 mg/kg またはプラセボを週に 1 回、24 週間投与しました。患者の年齢は 5 歳から 29 歳の間で変化し、患者の年齢の中央値は 12 歳でした。対象は、12分間の歩行で5〜400メートルの距離をカバーした患者に限定された。すべての患者は、各点滴の前に抗ヒスタミン薬を投与されました。
ガルスルファーゼ(有効成分)を使用したグループは、3 分間の階段昇降テストにおいて、12 分間に歩行した距離の平均増加(12 分間歩行テスト、12-MWT)および段差を上る速度の増加を示しました。プラセボを使用したグループとの比較 (以下の表 1)。
24週間のプラセボ対照研究期間の後、38人の患者が研究の開始相でさらに72週間ガルスルファーゼ(活性物質)を投与された。ガルスルファーゼ(活性物質)を投与するために最初に無作為に割り付けられ、72週間(合計96週間)治療を受け続けた19人の患者の間で、12分間の歩行テスト(12MWT)での走行距離と登坂速度の増加が観察されました。開相の開始時と比較した階段の距離 (平均 [±SD] 変化): それぞれ 72 ± 116 メートルおよび 5.6 ± 10.6 ステップ/分)。
最初に 24 週間プラセボを投与するよう無作為に割り付けられ、その後ガルスルファーゼの使用に割り当てられた 19 人の患者のうち、非盲検試験期間の開始時と比較して、ガルスルファーゼの 72 週間使用後の増加 (平均 [± SD]変化)は、12分間のテスト(12MWT)および階段昇降速度で、それぞれ118±127メートルおよび11.1±10.0ステップ/分でした。
尿中 GAG 濃度を使用して生物活性を評価しました。全体として、患者の 95% が、ガルスルファーゼ (活性物質) を 72 週間使用した後、尿中 GAG レベルの少なくとも 50% の減少を示しました。ガルスルファーゼ (活性物質) を投与された患者で、尿中 GAG レベルが正常範囲に達した患者はいませんでした。
非盲検試験後に実施された延長試験では、ガルスルファーゼ(活性物質)を投与された患者は、抵抗力の最初の改善を約 240 週間維持しました。
2つの異なる用量を用いたランダム化研究の第4相では、1歳未満のMPS VI患者4人が1または2 mg/kg/週で53~153週間治療された。
対象となる患者数が少ないため限定的ではありますが、この研究から次の結論が得られます。
ガルスルファーゼ(活性物質)による治療により、顔面異形症の改善または安定化が実証されました。
骨格異形成の進行やヘルニアの発症は阻止できず、角膜混濁の進行も阻止できませんでした。限られた追跡期間中、成長率は正常のままでした。参加者4人全員の少なくとも片耳で聴力の改善が観察されました。尿中 GAG レベルは 70% 以上減少し、高齢患者の結果と一致しました。
乳児における安全性の結果は、5 歳から 29 歳までの患者で観察された結果と一致していました。
表 1: プラセボ対照臨床研究の結果
薬理学的特徴
作用機序
ムコ多糖類蓄積症は、グリコサミノグリカン (GAG) の異化に必要な特定のリソソーム酵素の欠乏によって引き起こされます。ムコ多糖症 VI 型(MPS VI、マロートー・ラミー症候群)は、N-アセチルガラクトサミン 4-スルファターゼ(アリールスルファターゼ B、ASB)の活性が欠如しているか、活性が著しく低下していることを特徴としています。
スルファターゼ活性が欠損すると、GAG基質であるデルマタン硫酸が体中に蓄積します。この蓄積は、広範な細胞、組織、器質的な機能障害を引き起こします。ガルスルファーゼ (活性物質) は、リソソームに捕捉された外因性酵素で構成され、GAG を異化します。細胞によるガルスルファーゼの取り込みおよびリソソームへのその侵入は、ガルスルファーゼのマンノース-6-リン酸末端オリゴ糖鎖と特定のマンノース-6-リン酸受容体との結合によって媒介される可能性が最も高い。
薬力学特性
尿中 GAG 濃度とガルスルファーゼ (活性物質) の異なる用量との関係は不明です。尿中 GAG 濃度と臨床反応との関係は確立されていません。抗体の発生と尿中 GAG レベルとの間に関連性は観察されませんでした。
薬物動態学的特性
ガルスルファーゼの薬物動態パラメータは、24 週間毎週 4 時間の点滴で 1 mg/kg のガルスルファーゼ (活性物質) を投与された MPS VI 患者 13 名で評価されました。
1週目と24週目の薬物動態パラメータを表2に示します。
表 2: 薬物動態パラメータ (中央値、範囲)
|
薬物動態パラメータ |
1週目 |
第24週 |
|
C max (mcg/mL) |
0.8(0.4~1.3) |
1.5(0.2~5.5) |
|
AUC 0-t (h-mcg/mL) a |
2.3(1.0~3.5) |
4.3(0.3~14.2) |
|
Vz (mL/kg) |
103 (56 ~ 323) |
69 (59 ~ 2,799) |
|
CL (mL/kg/分) |
7.2(4.7~10.5) |
3.7(1.1~55.9) |
|
半減期 (分) |
9 (6 ~ 21) |
26(8~40) |
C max – 最大血漿濃度。
AUC 0-t – 注入開始から注入後 60 分までの時間曲線下面積 x ガルスルファーゼの血漿濃度。
V z – 配布量。
CL-血漿クリアランス。
表 2 にリストされているガルスルファーゼの薬物動態パラメータは、試験のばらつきが大きいため、注意深い解釈が必要です。抗ガルスルファーゼ抗体の開発はガルスルファーゼの薬物動態に影響を与えているようですが、データは限られています。
免疫原性の可能性
ガルスルファーゼ (活性物質) で治療され、抗ガルスルファーゼ抗体の存在について評価を受けた患者の 98 パーセント (53/54) が、治療の 4 週間から 8 週間の間に IgG 抗ガルスルファーゼ抗体を発現しました (4 つの臨床研究において)。プラセボ対照臨床研究でガルスルファーゼ (活性物質) を使用した 19 人の患者において、抗ガルスルファーゼ抗体の発現と臨床転帰との間の潜在的な関係を検証するために血清サンプルが評価されました。
ガルスルファーゼ (活性物質) を使用した 19 人の患者全員が、ガルスルファーゼに対する特異的な抗体を発現しました。しかし、分析では、総抗体、中和抗体、または IgG 力価と、輸液関連反応、尿中グリコサミノグリカン (GAG) レベル、または身体持久力テストの結果との間に一貫した予測可能な関係は示されませんでした。抗体は、酵素活性を阻害する能力に関連して評価されましたが、細胞取り込み能力に関連して評価されたわけではありません。
データは、所定のアッセイを使用した検査結果が抗ガルスルファーゼ抗体陽性であることが判明した患者の割合を反映しています。このため、結果はこのアッセイの感度と特異性に大きく依存します。
さらに、アッセイにおける抗体の発生率の観察は、サンプルの取り扱いなどのいくつかの要因によって影響を受ける可能性があります。サンプル収集時間。併用薬と基礎疾患。これらの理由により、抗ガルスルファーゼ抗体の発生率と他の製品に対する抗体の発生率との比較は誤解を招く可能性があります。
非臨床毒性学
発がん性;突然変異誘発と生殖能力の低下。
ガルスルファーゼの発がん性および変異原性の可能性を評価するための長期研究は行われていません。
最大 3.0 mg/kg (体表面積に基づくヒトの推奨用量 1 mg/kg の約 0.5 倍) の静脈内用量でのガルスルファーゼの使用は、雄ラットと雌の生殖能力と生殖に影響を与えませんでした。
ナグラザイムストレージケア
ナグラザイムは冷蔵(2°C ~ 8°C)で保存する必要があります。この薬を凍らせたり、振ったりしないでください。光から守ります。
ナグラザイムはパッケージに記載されている使用期限を過ぎた後は使用しないでください。この製品には防腐剤は含まれておりません。希釈した溶液はすぐに使用する必要があります。すぐに使用できない場合は、希釈した溶液を 2°C ~ 8°C で保存してください。
希釈後の保管は、調製時から投与終了まで 48 時間を超えてはなりません。希釈液は点滴時以外は室温で保管しないでください。
調製後、希釈溶液を 2°C から 8°C の間に最長 48 時間保ちます。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。
身体的特徴
ナグラザイムをバイアルから取り出す前に、粒子状物質や色の変化がないか目視で検査してください。ナグラザイム溶液は、透明からわずかに乳白色で、無色から淡黄色でなければなりません。半透明の粒子が含まれる場合があります。溶液の色の変化が見られる場合、または粒子状物質が存在する場合は、溶液を使用しないでください。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かないところに保管してください。
ナグラザイムの法的声明
MS 登録: 1.7333.0001
担当薬剤師:
アナ・ルシア・ドミンゲス・ヴェローゾ
CRF-SP No.23562
製造元:
バイオマリン製薬株式会社
カリフォルニア州ノバト
アメリカ合衆国
製造元(一次包装):
歓喜のホリスターシュティア ラボラトリーズ LLC
ワシントン州スポケーン
アメリカ合衆国
または
Vetter Pharma-Fertigung GmbH amp;株式会社KG
ランゲナルゲン
ドイツ
梱包方法(二次梱包):
AndersonBrecon Inc. イリノイ州ロックフォード
アメリカ合衆国

または
バイオマリン・インターナショナル・リミテッド
シャンバリー、リンガスキディ、コーク州
アイルランド
輸入者:
BioMarin Brasil Farmacêutica LTDA.
ジェームス ジュール ストリート No. 92;参照: 42
サンパウロ、サンパウロ
郵便番号: 04576-080
CNPJ: 08.002.360/0001-34
顧客サービス
電話:0800-722-0350
医師の処方箋に基づいて販売します。








-1024x576.jpg?resize=1024,576&ssl=1)


