ミコフェノール酸モフェチルは、移植臓器の拒絶反応を予防し、腎臓、心臓、または肝臓の移植を受けた成人患者の通常の治療では反応しない拒絶反応の治療に適応されます。ミコフェノール酸モフェチルは、シクロスポリン A およびコルチコステロイドと併用する必要があります。

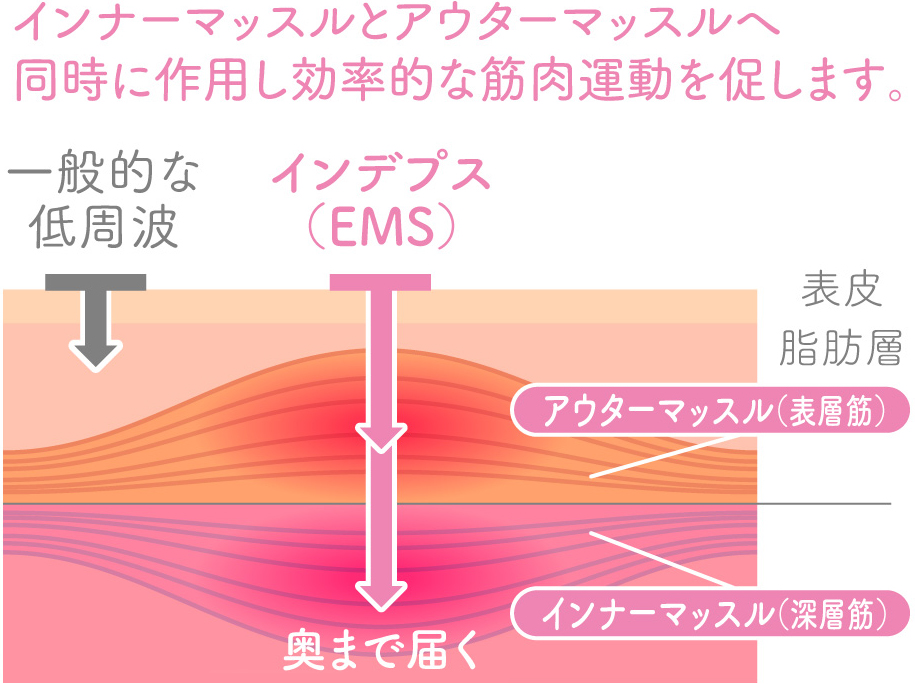
ミコフェノール酸モフェチル – EMS はどのように機能しますか?
ミコフェノール酸モフェチルは、移植の場合の臓器拒絶反応のプロセスに関与する主要細胞の 1 つであるリンパ球の増殖と分化を担う酵素 IMPDH の強力な阻害剤です。血液中のリンパ球が少なくなると、拒絶反応の可能性も低くなります。拒絶反応を避けるためには、移植後すぐにミコフェノール酸モフェチルの服用を開始する必要があります。
ミコフェノール酸モフェチルの禁忌 – EMS
ミコフェノール酸モフェチルにアレルギーがある場合、または他のアレルギー疾患がある場合は、医師に伝えてください。
ミコフェノール酸モフェチルは、ミコフェノール酸モフェチルまたはミコフェノール酸に対するアレルギーのある患者には禁忌です。
潰瘍などの胃の問題がある場合、または過去にあった場合は、医師に伝えてください。この場合、より注意深く監視する必要があります。
妊娠と授乳
この薬は、妊娠している女性、または治療中に妊娠する可能性のある女性は使用しないでください。
ミコフェノール酸モフェチルは胎児の発育に変化を引き起こすため、妊娠中は禁忌です。
ミコフェノール酸モフェチルは、非常に効果的な避妊法を使用していない出産適齢期の女性には禁忌です。
ミコフェノール酸モフェチルは授乳中の女性には禁忌です。
ミコフェノール酸モフェチルの使い方 – EMS
ミコフェノール酸モフェチル錠剤は医師の処方どおりに使用してください。

他の薬を服用する前に医師に相談してください。自分で薬を使用したり、混ぜたりしないでください。
取り扱いと応用
ミコフェノール酸モフェチル錠剤は少量の水と一緒に服用してください。錠剤は丸ごと飲み込む必要があり、吸入したり、皮膚や粘膜と直接接触したりしないように、割ったり、砕いたり、砕いたり、噛んだりしてはなりません。割れた錠剤を摂取しないでください。
ミコフェノール酸モフェチルが皮膚や粘膜に付着した場合は、多量の石鹸と水で洗ってください。目に入った場合は、大量の水で洗ってください。
ミコフェノール酸モフェチル錠剤は経口投与する必要があります。
ミコフェノール酸モフェチルの投与量 – EMS
移植臓器が良好に機能し続けるようにするには、ミコフェノール酸モフェチルを毎日服用することが重要です。医師から使用中止のアドバイスを受けるまで、ミコフェノール酸モフェチルの服用を続けてください。
ミコフェノール酸モフェチルの通常の用量は、1日2回1g(2錠)~1.5g(3錠)を適宜服用します。医師は、あなたの症例に適切な用量を計算する方法を知っており、また、特定の副作用が存在する場合に用量を減らす必要性を評価します。
腎臓拒絶反応を防ぐための標準用量
1.0gを1日2回投与します(1日量2g)。 1.5gを1日2回(1日量3g)の用量が臨床研究で使用され、有効性と安全性が示されていますが、腎移植患者に対する有効性の点では利点はありません。 2g/日のミコフェノール酸モフェチルを投与された患者は、3g/日のミコフェノール酸モフェチルを投与された患者と比較して、全体的な安全性プロファイルが良好であることが示されました。
心臓拒絶反応を避けるための標準用量
1.5gを1日2回投与します(1日量3g)。
肝拒絶反応を防ぐための標準用量
1.5gを1日2回投与します(1日量3g)。
通常の治療では反応しない初回拒絶反応および腎拒絶反応の治療用投与量
1.5gを1日2回投与します(1日量3g)。
経口投与
ミコフェノール酸モフェチルの初回用量は、腎臓、心臓、または肝臓の移植後できるだけ早く投与する必要があります。
特別な投与量の指示
好中球減少症(主に細菌と戦う役割を担う白血球の一種である好中球の減少)の患者
好中球減少症を発症した患者の場合、ミコフェノール酸モフェチルによる治療を中止するか、用量を減らす必要があります。
重度の腎機能障害
重度および慢性腎機能障害のある腎移植患者の場合、移植直後または急性または難治性拒絶反応の治療後以外の期間は、1日2回1gを超える用量を避けてください。移植臓器の機能が遅れている患者の場合、用量調整は推奨されませんが、患者の状態を注意深く監視する必要があります。
重度の腎機能障害を伴い心臓移植または肝臓移植を受けた患者
利用可能なデータはありません。
重度の肝機能障害
重度の肝実質疾患を有する腎移植患者には用量調整は必要ありません。重度の肝実質疾患を有する心臓移植患者に関する利用可能なデータはない。
高齢者(65歳以上)
用量調整は推奨されません。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
この薬は割ったり噛んだりしないでください。
ミコフェノール酸モフェチル – EMS の使用を忘れた場合はどうすればよいですか?
医師が指示した日と時間に薬を服用するためにできる限りのことを行う必要があります。何らかの理由で飲み忘れて、次の服用時間が近づいた場合は、忘れた分は飲まずに、次の通常どおり服用してください。
何らかの理由で飲み忘れてしまい、次の服用時間が離れてしまった場合は、思い出した時点ですぐに服用し、次の服用量も通常通り服用してください。
飲み忘れた場合は、決して次の倍量を服用しないでください。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
ミコフェノール酸モフェチルの注意事項 – EMS

次の場合は、薬を使用する前に医師に伝えてください。
- これまでに結核に罹患したことがあるか、結核患者と接触したことがありますか。
- 消化器系の病気がある。
- レシュ・ナイハン症候群やケリー・シーグミラー症候群など、まれに遺伝性ヒポキサンチン・グアニン・ホスホリボシル・トランスフェラーゼ(HGPRT)欠損症がある。
次の状況では、医師に直ちに通知する必要があります。
- 説明のつかない紫色の斑点や出血の兆候が現れた場合、日和見感染、致死感染、全身感染などの感染症、B型肝炎やC型肝炎の再活性化などの潜在的なウイルスの再活性化、またはポリオーマウイルスによる感染症、および以下の症状に関連する進行性多巣性白質脳症(PML)がある場合は、 JCウイルス、中枢神経系の深刻な変化。
- 腎移植後にBKウイルスに関連する腎症(腎臓損傷)がある場合。
- 純粋赤血球形成不全 (APSV) の場合は、骨髄が赤血球の産生を停止する状況です。
- 潰瘍、出血、消化管穿孔がある場合。
ミコフェノール酸モフェチルは体の防御機構を低下させます。このため、ある種の悪性腫瘍、特に皮膚腫瘍が発生するリスクが高くなります。したがって、適切な衣服と保護係数の高い日焼け止めを使用して、日光や紫外線への曝露を制限する必要があります。
セベラマーやその他のカルシウムを含まないリン酸塩結合剤を使用している場合は、ミコフェノール酸モフェチルを使用してから 2 時間後にこれらの薬を服用してください。
骨髄抑制が起こる可能性があり、併用投与は研究されていないため、ミコフェノール酸モフェチルとアザチオプリンの併用は避けてください。
免疫抑制剤は結核の原発巣を活性化する可能性があります。
免疫抑制下の患者を監視する医師は、活動性疾患が出現する可能性に注意を払い、早期診断と治療のためにあらゆる予防措置を講じる必要があります。
献血
治療中およびミコフェノール酸モフェチルの使用中止後少なくとも 6 週間は献血しないでください。
予防接種
ミコフェノール酸モフェチルによる治療中はワクチンの効果が低下する可能性があるため、ワクチンを受ける前に医師に相談してください。弱毒生ワクチンの使用は避けてください。
精液の寄付
男性は、治療中およびミコフェノール酸モフェチルの使用終了後少なくとも90日間は精液を提供すべきではありません。
研究室のモニタリング

医師は、実施する血液検査と採取の頻度について通知します。
男性の生殖能力
動物実験では、ミコフェノール酸モフェチルで治療された動物の子孫に奇形が観察されました。ミコフェノール酸モフェチルで治療した動物の生殖能力に対する影響は観察されませんでした。
避妊
女性
ミコフェノール酸モフェチルは、非常に効果的な避妊法を使用していない出産適齢期の女性には禁忌です。
ミコフェノール酸モフェチルによる治療を開始する前に、医師は流産や先天奇形のリスクの増加についてアドバイスし、あなたが出産可能年齢にある場合は妊娠の予防と計画についてアドバイスする必要があります。
治療中およびミコフェノール酸モフェチルの服用を中止してから最大6週間は、すでに子宮を摘出しているか性交をしていない場合を除き、2つの信頼できる避妊法を同時に使用する必要があり、そのうちの1つは非常に効果的です。
男性
父親の治療中または治療直後に妊娠した胎児への危害のリスクを排除する十分なデータがない場合は、次の予防措置が推奨されます: 性的に活発な男性患者および/またはそのパートナーは、父親の治療中に効果的な避妊薬を使用すること。男性患者であり、治療終了後少なくとも90日間。
薬物乱用と依存症
CellCept が乱用や中毒の可能性があることを証明するデータはありません。

現在までのところ、ミコフェノール酸モフェチルがドーピングを引き起こす可能性があるという情報はありません。疑問がある場合は、医師に相談してください。
ミコフェノール酸モフェチルの副作用 – EMS
ミコフェノール酸モフェチルは、免疫反応を低下させ、移植臓器を体が拒絶するのを防ぐように設計された他の薬剤とともに常に投与されるため、どの副作用がこの薬剤によるもので、どの副作用が基礎疾患や他の薬剤によるものであるかを区別するのは困難です。使用中。
ミコフェノール酸モフェチルを服用している患者に現れる最も一般的な問題は次のとおりです。
下痢、嘔吐、胃の不調、血液中の白血球数の減少、血液中の赤血球数の減少、全身感染症、およびサイトメガロウイルス病、カンジダ症、単純ヘルペスなどの他の種類の感染症。また、主に皮膚、血液、リンパ器官に良性または悪性の腫瘍(がん)が発生する可能性も高くなります。不快な反応や皮膚病変があった場合は医師に報告してください。
高齢患者(~65歳)
高齢患者、特に免疫抑制レジメンの一環としてミコフェノール酸モフェチルを受けている患者は、若い患者と比較した場合、特定の感染症(浸潤性サイトメガロウイルス疾患を含む)のリスクが高く、胃や腸での出血や肺での体液の蓄積の可能性が高い可能性があります。 。
経口投与におけるミコフェノール酸モフェチルの安全性プロファイル
?で報告された有害事象lt で 10% および 3%。臨床研究において、シクロスポリンAおよびコルチコステロイドを伴うミコフェノール酸モフェチルによる治療を受けた成人患者の10%:
*合計 n = 1,483。
**合計 n = 578。
***合計 n = 564。
腎移植拒絶反応を予防するための 3 件の対照研究では、ミコフェノール酸モフェチルを 2 g/日投与された患者の方が、3 g/日投与された患者より副作用が少なかった。
市販後の経験
感染症
髄膜炎や心臓の最内層の炎症、結核、結核菌に似た他の細菌である非定型マイコバクテリアによる感染など、死亡の危険をもたらす感染症ですが、通常、免疫力が低下している人にのみ影響を及ぼします。
ミコフェノール酸モフェチルで治療を受けた患者において、進行性多巣性白質脳症(PML)(脳白質の変性疾患)を発症し、場合によっては死に至るケースが報告されています。報告された症例には一般に、免疫抑制療法や免疫系機能不全などのPMLの危険因子が存在していました。
BKウイルスに関連した腎臓損傷が、ミコフェノール酸モフェチルで治療された患者で観察されています。この感染症は重篤な結果を引き起こす可能性があり、腎移植片の喪失につながる場合もあります。
血液と免疫システム
ミコフェノール酸モフェチルを併用治療された患者において、純赤血球形成不全(APSV)(白血球と血小板は正常に形成されるが、骨髄における赤血球形成が欠如している)および低ガンマグロブリン血症(まれなタイプの免疫不全)の症例が報告されている。他の免疫抑制剤と併用してください。
先天性疾患
妊娠中に他の免疫抑制剤と組み合わせてミコフェノール酸モフェチルに曝露された女性患者の子供で先天奇形が報告されています。
妊娠、産後、周産期の状態
主に妊娠の第一期にミコフェノール酸モフェチルに曝露された患者における自然流産の症例が報告されています。
胃腸
腸(サイトメガロウイルスによって引き起こされることもある)および膵臓の炎症、腸絨毛の顕著な減少を伴う孤立したケース。
ミコフェノール酸モフェチルの市販後のその他の副作用は、腎臓、心臓、肝臓の移植対照研究で観察されたものと同様です。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。
また、顧客サービスを通じて会社に通知してください。
ミコフェノール酸モフェチルの特別集団 – EMS
妊娠
ミコフェノール酸モフェチルは胎児の発育に変化を引き起こすため、妊娠中は禁忌です。
ミコフェノール酸モフェチルは自然流産のリスクを高め(特に妊娠初期)、妊娠中に母親が暴露した場合には先天奇形のリスクを高めます。
以下の奇形は、妊娠中に他の免疫抑制剤と組み合わせてミコフェノール酸モフェチルに曝露された患者の小児において、市販後期間に最も頻繁に報告されています。
- 顔の奇形。
- 耳と目の異常。
- 指の奇形。
- 心臓の異常;
- 食道の奇形;
- 神経系の奇形。
労働と出産
分娩中および分娩中のミコフェノール酸モフェチルの安全な使用は確立されていません。
授乳中
ミコフェノール酸モフェチルは、お子様に重篤な副作用を引き起こす可能性があるため、授乳中は禁忌です。
女性の生殖能力
ミコフェノール酸モフェチルは、非常に効果的な避妊法を使用していない出産適齢期の女性には禁忌です。
妊娠検査薬
ミコフェノール酸モフェチルによる治療を開始する前に、医師は妊娠検査を受けるように指示します。 2 回目の検査は 8 ~ 10 日後に行う必要があります。治療中に妊娠した場合、または治療終了後 6 週間以内に妊娠した場合は、直ちに医師に報告する必要があります。
高齢者(65歳以上)の使用
高齢の患者は、若い患者と比較した場合、特定の感染症(浸潤性サイトメガロウイルス疾患を含む)や胃や腸の出血、肺への体液の蓄積などの有害事象のリスクがより高い可能性があります。
小児用(18歳以上)
小児患者における心臓移植または肝臓移植について利用可能なデータはありません。
機械を運転および操作する能力への影響
機械を運転および操作する能力に対するミコフェノール酸モフェチルの影響に関する研究は行われていません。
ミコフェノール酸モフェチルの組成 – EMS
各コーティング錠には次のものが含まれます。
|
ミコフェノール酸モフェチル |
500mg |
|
賦形剤* |
コーティング錠 1 錠 |
*微結晶セルロース、ポビドン、クロスカルメロースナトリウム、二酸化ケイ素、ステアリン酸マグネシウム、ヒプロメロース、ヒプロロース、マクロゴール、二酸化チタン、アルミニウム染料ブルーラックn°2、黄色酸化鉄、赤色酸化鉄。
ミコフェノール酸モフェチルのプレゼンテーション – EMS
500mgのコーティング錠。パッケージ内容: 10、20、30、40、50 ** 、60 * 、90 *および 500 ** 。
*分割包装。
**病院の包装。
口頭で。
大人用。
ミコフェノール酸モフェチルの過剰摂取 – EMS
医師が推奨する用量を超える用量を投与した場合、下痢、嘔吐、白血球数の減少、感染症など、その薬に特徴的な副作用が現れることがあります。
ミコフェノール酸モフェチルの過剰摂取は、免疫系の顕著な抑制、感染症や骨髄抑制に対する感受性の増加を引き起こす可能性があると予想されます。
ミコフェノール酸モフェチルは血液透析では除去できません。ただし、血漿濃度が高い場合(>100 mcg/mL)、薬物の一部が除去される可能性があります。コレスチラミンなどの胆汁酸封鎖剤は、この薬の排泄を増加させる可能性があります。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。
さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
ミコフェノール酸モフェチルの薬物相互作用 – EMS
複数の薬剤を同時に使用すると、薬剤の効果が増減する可能性があるため、ミコフェノール酸モフェチルによる治療を開始する前または治療中に、使用している薬剤について医師に伝えてください。
アシクロビル、制酸薬(水酸化アルミニウムや水酸化マグネシウムなど)、プロトンポンプ阻害薬(オメプラゾール、ランソプラゾール、パントプラゾールなど)、抗生物質、カルシウムなどの他の薬(医師が処方していない薬を含む)を服用している場合は医師に伝えてください。 -遊離リン酸塩結合剤、コレスチラミン、シクロスポリン A、テルミサルタン、ガンシクロビル、リファンピシン、プロベネシド、セベラマー、生ウイルスワクチン、タクロリムス、ノルフロキサシンとメトロニダゾールの組み合わせ、およびミコフェノール酸の代謝に影響を与えるもの(イサブコナゾールなど)。予防接種を受ける前に必ず医師に相談してください。
経口避妊薬
ミコフェノール酸モフェチルは経口避妊薬の有効性に影響を与えないようです。ただし、ミコフェノール酸モフェチルによる治療中に妊娠しないようにするため(胎児の発育に異常を引き起こす可能性があります)、すでに子宮を摘出しているか、性行為をしていない場合を除き、2つの避妊方法を同時に使用する必要があります。性的な。
抗生物質
β-グルクロニダーゼを産生する腸内細菌を排除する抗生物質(アミノグリコシド、セファロスポリン、フルオロキノロン、ペニシリン系抗生物質など)は、体内のミコフェノール酸モフェチルの濃度を下げることができます。
以下の抗生物質に関する情報が入手可能です。
クラブラン酸に関連するシプロフロキサシンまたはアモキシシリン:
これらの抗生物質と一緒に投与すると、体内のミコフェノール酸モフェチルの量が減少します。しかし、その効果は時間の経過とともに減少する傾向があり、臨床的重要性はまだ確立されていません。
ノルフロキサシンとメトロニダゾール:
ノルフロキサシンとメトロニダゾールの併用により、ミコフェノール酸モフェチルの単回投与後の血流中の薬物濃度が減少しました。この効果は、これらの抗生物質を別々に投与した場合にはどちらの抗生物質でも発生しませんでした。
トリメトプリム/スルファメトキサゾール:
トリメトプリム/スルファメトキサゾールの組み合わせでは、血流中のミコフェノール酸モフェチルの濃度に対する影響は観察されませんでした。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
ミコフェノール酸モフェチルの食品との相互作用 – EMS
腎臓移植患者に1.5gを1日2回投与した場合、食物はミコフェノール酸モフェチルの吸収の程度(MPA AUC)に影響を与えなかった。ただし、MPA の C max は、食物の存在下では 40% 減少しました。
ミコフェノール酸モフェチルという物質の作用 – EMS
効果の結果
効果
ミコフェノール酸モフェチルは、臨床研究において、腎臓、心臓、肝臓移植における拒絶反応の予防のために、抗胸腺細胞免疫グロブリン、OKT3、シクロスポリン A、コルチコステロイドと併用して投与されました。ミコフェノール酸モフェチルは、腎移植における難治性拒絶反応エピソードの治療に、シクロスポリン A およびコルチコステロイドと併用して使用されました。ミコフェノール酸モフェチルによる治療前に、患者は抗リンパ球免疫グロブリン、抗胸腺細胞免疫グロブリンおよびOKT3の投与を受けていた可能性もあります。さらに、ミコフェノール酸モフェチルは、ダクリズマブおよびタクロリムスに関連する臨床研究で使用されました。
臓器拒絶反応の防止
大人:
移植片拒絶反応の予防における、コルチコステロイドおよびシクロスポリン A と併用したミコフェノール酸モフェチルの安全性と有効性が、腎移植レシピエントを対象とした 3 件の多施設共同無作為化二重盲検試験で評価されました。心臓移植レシピエントを対象とした盲検試験と、肝臓移植レシピエントを対象とした多施設無作為化二重盲検試験です。
腎臓移植
大人:
3件の研究では、急性拒絶反応の発症を防ぐために、経口ミコフェノール酸モフェチルの2用量(1gを1日2回、1.5gを1日2回)と、シクロスポリンAおよびコルチコステロイドを併用したアザチオプリン(2件の研究)またはプラセボ(1件の研究)を比較した。 。
主要有効性アウトカムは、移植後の最初の6か月以内に治療失敗(生検で証明された急性拒絶反応、または死亡、移植片喪失、または研究からの早期離脱の発生として定義される)を経験した各治療群の患者の割合であった。生検で証明された拒絶反応以外の理由)。ミコフェノール酸モフェチルは、3 つの治療レジメンで評価されました:(1)抗胸腺細胞免疫グロブリン/MMF またはアザチオプリン/シクロスポリン A/コルチコステロイドによる導入、(2)MMF またはアザチオプリン/シクロスポリン A/コルチコステロイド、および(3)MMF またはプラセボ/シクロスポリン A/コルチコステロイド。
ミコフェノール酸モフェチルは、コルチコステロイドおよびシクロスポリン A と併用すると、移植後最初の 6 か月間で治療失敗の発生率を減少させました (p lt; 0.05)。以下の表は、これらの研究結果をまとめたものです。治療を途中で中止した患者は、死亡または移植片喪失の発生について監視され、これら 2 つの事象の累積発生率は個別に記載されています。治療を途中で中止した患者は、完了後の急性拒絶反応の発生について監視されなかった。対照群と比較すると、ミコフェノール酸モフェチル群では治療を中止した患者(生検で証明された拒絶反応、死亡、移植片喪失がなかった)の数が多く、ミコフェノール酸モフェチル3g/日群が最も高かった。しかし、急性拒絶反応率は、特にミコフェノール酸モフェチル 3 g/日のグループでは過小評価される可能性があります。
腎移植研究
治療失敗の発生率(生検で証明された拒絶反応または何らかの理由による早期終了)
*抗胸腺細胞免疫グロブリン/MMFまたはアザチオプリン/シクロスポリンA/コルチコステロイドによる誘導。
*MMF またはアザチオプリン/シクロスポリン A/コルチコステロイド。
*MMF またはプラセボ/シクロスポリン A/コルチコステロイド。
**早期終了の理由として、死亡または移植片喪失は含まれません。
12か月時点での移植片喪失および患者死亡の累積発生率を以下に示します。移植片喪失および患者の死亡に関してミコフェノール酸モフェチルの優位性は確立されていません。数値的には、3 つの研究において、ミコフェノール酸モフェチルを 2 g/日および 3 g/日投与された患者は、対照群の患者よりも良い結果を示しました。 3つの研究のうち2つにおいて、ミコフェノール酸モフェチルを1日2g投与した患者は、3g/日を投与した患者よりも良好な結果を示した。すべての治療群において、治療を途中で終了した患者は、移植片喪失および1年後の患者死亡に関してより悪い転帰を示した。
腎移植研究
12か月以内の移植片喪失および患者死亡の累積発生率
心臓移植
多施設共同、並行群間、無作為化比較二重盲検研究が、一次心臓移植レシピエントを対象に実施されました。 650人の患者が関与した。 72人には治験薬が投与されず、578人には治験薬が投与された。
患者は、免疫抑制維持療法として、ミコフェノール酸モフェチル 1.5 g を 1 日 2 回 (n = 289)、またはアザチオプリン 1.5 ~ 3 mg/kg/日 (n = 289) を、シクロスポリン A およびコルチコステロイドと組み合わせて投与されました。 2 つの主な有効性パラメータは次のとおりです:(1)移植後、心筋内膜生検で証明された拒絶反応、血行力学的低下のエピソードが少なくとも 1 回あった患者、または最初の 6 か月以内に再移植されたか死亡した患者の割合、および(2)移植後最初の 12 か月以内に死亡または再移植された患者の割合。治療を途中で中止した患者は、移植片拒絶反応の発生について最長 6 か月間、死亡の発生について 1 年間モニタリングされました。
拒絶:
以下に示すように、生検で証明された血行動態の低下を伴う拒絶反応に関して、ミコフェノール酸モフェチルとアザチオプリンとの間に差異は確立されていない。
半年で拒否?
*血行動態の低下は、以下の基準が満たされた場合に発生しました:肺毛細管圧勾配 20 mm または 25% の増加。心指数lt; 2.0 L/min/m 2または 25% の減少。駆出率 30%;肺動脈酸素飽和度 60% または 25% の減少。 B3によるギャロップリズムの存在。端数制限 20% または 25% の減少。臨床状態を制御するための変力サポートの必要性。
生存:
この研究に参加した患者では、ミコフェノール酸モフェチル群に無作為化された患者とアザチオプリン群の患者との間に死亡と再移植に関して統計的に有意な差はなかった。治験薬を投与された患者では、死亡と再移植の間の差の信頼区間の97.5%下限は1年目で0.9であり、以下に示すように、これらの患者においてミコフェノール酸モフェチルがアザチオプリンよりも優れていることを示している。
1年以内の死亡または再移植
肝臓移植
一次肝移植レシピエントを対象とした多施設並行無作為比較二重盲検研究が、米国の16施設、カナダの2施設、ヨーロッパの4施設、オーストラリアの1施設で実施された。関与した患者の総数は565人で、そのうち564人が治験薬の投与を受けた。患者は、ミコフェノール酸モフェチル1gを1日2回、IVで14日間投与され、その後ミコフェノール酸モフェチル1.5gが1日2回経口投与されるか、アザチオプリン1~2mg/kg/日IV、その後アザチオプリン1~2mg/kgが投与された。免疫抑制療法としてシクロスポリン A およびコルチコステロイドと併用して / 日経口投与。有効性の 2 つの主な尺度は次のとおりです: (1) 移植後最初の 6 か月以内に、生検または死亡/再移植によって証明された治療による拒絶反応を 1 回以上経験した患者の割合、および (2)は、移植後最初の 12 か月で移植片喪失 (死亡/再移植) を示しました。治療を途中で中止した患者は、移植片拒絶の発生および移植片喪失(死亡/再移植)の発生について1年間監視されました。
結果:
一次解析(治療意図)では、シクロスポリンAおよびコルチコステロイドと併用したミコフェノール酸モフェチルは、急性拒絶反応の予防においてアザチオプリンより優れており(p = 0.025)、生存期間の点ではアザチオプリンと同等でした。
半年以内に拒絶反応、1年以内に死亡または再移植
| アザ N = 287 | ミコフェノール酸モフェチル N = 278 | |
| 生検により6か月以内に治療されたことが証明された拒絶反応 | 137 (47.7%) | 107 (38.5%) |
| 1年以内の死亡または再移植 | 42名(14.6%) | 41 (14.7%) |
難治性拒絶反応の治療
急性難治性移植片拒絶反応を患う腎臓移植レシピエント150人を対象に、MMF 3 g/日と静脈内コルチコステロイドの無作為化非盲検比較研究が行われた。主なパラメーターは、研究開始後 6 か月後に生存し、移植片が機能していた患者の割合でした。
結果:
対照群では移植片喪失の発生率が予想外に低く、逐次確率率検定に基づく一次解析では、MMF 群の移植片生着率が高くなる傾向が示されました (p = 0.081)。コクラン・マンテル・ヘンゼル検定(逐次モニタリング用に調整されていない)を使用した二次解析では、研究開始から6か月後のMMFグループにおける移植片喪失または死亡の発生率が45%減少することが示唆されました(p = 0.062)。
移植片の喪失または6か月以内の死亡
| IVコルチコステロイド N = 73 | ミコフェノール酸モフェチル N = 77 | |
| 移植片の喪失または6か月以内の死亡 | 19名(26.0%) | 11 (14.3 |
薬理学的特徴
薬力学
ミコフェノール酸モフェチル (MMF) は、ミコフェノール酸 (MPA) の 2-モルホリノエチル エステルです。 MPA は、イノシン一リン酸デヒドロゲナーゼ (IMPDH) の強力、選択的、非競合的、可逆的阻害剤であるため、DNA に取り込まれることなくグアノシン ヌクレオチド合成の de novo 経路を阻害します。 MPA が IMPDH の酵素活性を阻害するメカニズムは、ニコチンアミドアデニン ジヌクレオチド補因子と触媒水分子の両方を構造的に模倣する MPA の能力に関連していると思われます。これにより、グアノシン ヌクレオチドの新規合成における基本的なステップである、IMP のキサントース-5′-一リン酸への酸化が防止されます。 MPA は、他の細胞よりもリンパ球に対して大きな細胞増殖抑制効果を持っています。これは、T および B リンパ球がその増殖において de novo プリン合成経路に非常に依存している一方で、他の細胞は別の経路を使用できるためです。
薬物動態
MMF の薬物動態は、腎臓、心臓、肝臓移植患者を対象に研究されています。一般に、MPA の薬物動態プロファイルは腎臓移植患者と心臓移植患者で類似しています。肝移植の初期には、1.5 g の経口または静脈内 MMF を投与された患者の MPA レベルは、1 g の経口または静脈内 MMF を投与された腎臓移植レシピエントと同様でした。
吸収
経口投与後、ミコフェノール酸モフェチルは急速かつ広範に吸収され、その活性代謝物である MPA に完全に代謝されます。 MPA の AUC に基づく経口ミコフェノール酸モフェチルの平均バイオアベイラビリティは、IV ミコフェノール酸モフェチルの平均バイオアベイラビリティと 94% 相関しています。
ミコフェノール酸モフェチルは、静脈内注入中に全身的に測定できます。ただし、経口投与後、ミコフェノール酸モフェチルは定量限界 (0.4 mcg/mL) を下回ります。
最近の移植後期間 (LT; 40 日) では、腎臓、心臓、および肝臓の移植を受けた患者は、移植後期間後期と比較して MPA AUC が平均約 30% 減少し、C MAXが約 40% 減少しました ( 3〜6か月)。
腎移植を受ける患者に推奨される注入指数では、1 g を 1 日 2 回投与した後の移植直後段階の MPA AUC 値は、経口投与後に観察される値と同等です。肝移植を受ける患者において、1gを1日2回静脈内投与し、その後1.5gを1日2回経口投与すると、MPA AUC値は、1gを1日2回ミコフェノール酸投与を受けた腎臓移植を受けた患者で見られるものと同様の結果となった。モフェティラから。
経口製剤の同等性
ミコフェノール酸モフェチルの生物学的同等性を評価しました。 500 mg 錠剤 2 個は、250 mg カプセル 4 個に相当します。
分布
腸肝再循環の結果、通常、用量投与後約 6 ~ 12 時間で MPA の血漿 MPa 濃度の二次的増加が観察されます。 MPA の曲線下面積 (AUC) の約 40% の減少は、コレスチラミンの同時投与 (4 g を 1 日 3 回) に関連しており、腸肝再循環の中断があることを示しています。 MPA は、臨床的に適切な濃度で、血漿アルブミンに対して 97% です。
代謝
MPA は主にグルコロニルトランスフェラーゼ (ISOFRAFEFORE UGT1A9) によって代謝されます。生体内で不活性フェノール性グルコロニド (MPAG) を形成するために、MPAG は腸肝再循環を通じて遊離 MPa に再度変換されます。より小さいアシルグルコニド (acmpag) も形成されます。 Acmpag は薬理学的に活性があり、MMF のいくつかの副作用 (下痢、白血球減少症) の原因であると疑われています。
排除
薬物の卑劣な部分は MPA (LT; 用量の 1%) として尿中に排泄されます。放射性ミコフェノール酸モフェチルを経口投与すると完全に回収され、用量の 93% が尿中に、6% が便中に回収されました。投与量のほとんど (約 87%) が MPAG の形で尿中に排泄されました。
通常の臨床濃度では、MPa と MPAG は血液透析によって除去されません。ただし、MPAG 濃度が高い場合 (GT; 100 mcg/ml)、少量が除去されます。コレスチラミンなどの胆汁酸誘拐物質は薬物の腸肝循環を妨げるため、MPa AUC を低下させます。
MPa の配置は複数のキャリアに依存します。有機陰イオン(OATP)と複数の耐性タンパク質2型(MRP2)のポリペプチド輸送体がMPAの配置に関与しています。 OATP、MRP2および乳がんタンパク質(BCRP)等角は、グルコロン酸胆汁排泄に関連するキャリアです。複数の薬剤耐性タンパク質(MDR1)もMPAを輸送することができますが、その寄与は吸収プロセスに限定されているようです。腎臓では、MPAとその代謝産物は潜在的に腎有機陰イオンコンベアと相互作用する可能性があります。
特殊な臨床状況における薬物動態
重度の腎障害のある患者
単一の用量研究(グループあたり6人の患者)では、重度の慢性腎機能障害(糸球体ろ過率LT; 25 mL/min/1.73 m 2 )の個人で観察された平均血漿MPA ACSは、正常な健康で観察されるよりも28-75高かった腎障害の低いボランティアまたは個人。単回投与のMPAG AUCは、腎機能障害が中程度の腎機能障害または健康な正常な個人と比較して、重度の腎機能障害のある人で3〜6倍高く、MPAGの既知の腎除去に同意しました。マイコフェノール酸モフェチルの複数回投与の効果は、重度の慢性腎機能障害の患者では研究されていません。
腎移植の機能が遅れている患者
移植後の腎移植後遅延の患者では、AUC0-12の平均MPAは、移植後の腎移植片機能の問題なく移植された患者で観察された患者に匹敵しました。移植片機能が遅れている患者には、遊離画分と血漿MPA濃度が一時的に増加するはずです。モフェチルのマイコフェノール酸塩の調整は必要ないようです。平均血漿MPAG AUC0-12は、移植後の腎移植片の機能に遅滞なく患者よりも2〜3倍高かった。
腎臓移植後の移植片機能が一次遅れた患者では、血漿MPAG濃度が蓄積しました。 MPAの蓄積があったとしても、非常に少なかった。
肝障害のある患者さん
MPAGおよびMPAの薬物動態は、相対的な用語では、経口または静脈内マイコフェノレートで治療されたアルコール性肝硬変のボランティアの肝実質疾患によって影響を受けませんでした。これらのプロセスに対する肝疾患の影響は、おそらく特定の疾患に依存します。しかし、原発性胆道肝硬変など、主に胆管損傷を伴う肝疾患は異なる効果をもたらす可能性があります。
高齢者(GT; 65歳)
高齢者におけるモフェチルマイコフェノール酸の挙動は、正式に評価されていません。
前臨床安全性データ
実験モデルでは、モフェチルマイコフェノール酸は腫瘍形成性ではありませんでした。動物の発がん性研究でテストされた最高の用量は、推奨される臨床用量2 g/日および全身暴露(AUC曝露)で腎移植患者で観察される約2〜3倍の全身曝露(AUCまたはC Max )を観察しました(AUCまたはC Max )は、推奨される3 g/日の臨床用量で心臓移植患者で観察されました。 2つの遺伝毒性試験(ラットにおけるリンパ腫/チミジンキナーゼ試験とラットの微生核異常試験)は、非常に毒性レベルの投与量の染色体不安定性を引き起こすモフチルミコフェノール酸の可能性を示しました。他の遺伝毒性試験(細菌変異試験、酵母または中国のハムスター卵巣細胞の染色体異常検査の有糸分裂遺伝的変換の検査)は変異原性活性を示さなかった。
モフェチルマイコフェノール酸は、最大20 mg/kg/日の経口投与における雄ラットの肥沃度に影響を与えませんでした。この用量への全身曝露は、腎臓移植患者で2 g/日の推奨用量で2〜3倍の臨床暴露、および3 g/日の推奨臨床用量で心臓移植患者における1.3〜2倍の全身暴露を表します。雌の動物の繁殖と肥沃度の研究では、4.5 mg/kg/日の経口投与は、母体毒性の非存在下で第1世代の子犬に奇形(角膜症、アグナティア、ハイドロセファルスを含む)を引き起こしました。この用量への全身曝露は、腎移植患者に2 g/日の推奨用量で約0.5時間の臨床暴露、心臓移植患者の推奨3 g/日用量で約0.3時間の臨床曝露でした。若い世代またはその後の世代の女性では、肥沃度または生殖パラメーターに影響が観察されていません。
ラットとウサギの催奇形性研究では、ラットでは胎児の再吸収と奇形が6 mg/kg/日の用量(角膜症、アグナティア、水頭症を含む)および90 mg/kg/kg/日の用量でウサギを含むラビット(心臓の原性および腎腎を含むウサギが発生しました。母体の毒性がない場合、コードや腎臓の異型、および横隔膜および臍ヘルニアなどの異常。これらのレベルへの全身曝露は、腎臓移植患者に2 g/日の推奨用量での臨床暴露、および心臓移植患者の推奨3 g/日用量展示での約0.3時間の臨床暴露に相当します。
血液系およびリンパ系は、マウス、マウス、犬、猿のマコフェノール酸モフェチルを使用して実施された毒物学的研究に最初にコミットしました。これらの効果は、腎臓移植患者の2 g/日の推奨用量で臨床暴露よりも低い全身曝露のレベルで発生しました。胃腸の影響は、暴露レベルの犬で観察されました








-1024x576.jpg?resize=1024,576&ssl=1)


