- 胃食道逆流症(胃から食道への逆流)(GERD)。
- びらん性逆流性食道炎(食道の炎症)の治療。
- 食道炎の再発を防ぐ維持療法。
- 胸やけ/胸やけ(胸焼け)、胃酸逆流、心窩部痛などの胃食道逆流症の症状の治療。
- 非ステロイド性抗炎症薬(NSAID)による継続的な治療が必要な患者。
- 抗炎症療法に関連する上部胃腸症状の治療。
- 「COX-2選択的」クラスの新しい抗炎症薬を含む抗炎症薬による治療に関連する胃潰瘍の治癒。
- 追加のリスクがある患者における、選択的 COX-2 などの抗炎症薬による治療に関連する胃潰瘍および十二指腸潰瘍の予防。
- ヘリコバクター・ピロリ菌に関連する十二指腸潰瘍の治療。
- 適切な抗菌治療と併用したヘリコバクター・ピロリ菌の除菌。
- ゾリンジャー・エリソン症候群(過剰な塩酸産生)および特発性過剰分泌を含む過剰分泌の病理学的状態。
- エソメプラゾールナトリウムの静注による治療後の胃潰瘍および十二指腸潰瘍の止血の維持と再出血の予防。
エソメプラゾールマグネシウム – EMSはどのように機能しますか?
エソメプラゾールマグネシウムは、プロトンポンプ阻害という特定の作用機序を通じて胃内の酸の生成を減少させます。
経口投与後、1時間以内に効果が現れます。
エソメプラゾールマグネシウムの禁忌 – EMS
エソメプラゾール、他のベンズイミダゾール(ベンズイミダゾール駆虫薬 – 寄生虫の侵入を治療する薬)、または配合成分のいずれかにアレルギーがある場合は、エソメプラゾール マグネシウムを使用しないでください。
エソメプラゾールマグネシウムの使い方 – EMS
エソメプラゾールマグネシウム錠剤は、液体と一緒に丸ごと経口投与する必要があります。
この薬は壊したり噛んだりすることはできません。
エソメプラゾールマグネシウムの投与量 – EMS
大人
胃食道逆流症(GERD)
- びらん性逆流性食道炎の治療: 40 mg を 1 日 1 回、4 週間投与します。食道炎が治癒していない患者、または症状が持続する患者には、さらに 4 週間の治療が推奨されます。
- 食道炎患者の再発を防ぐための維持療法、20 mgを1日1回。
- 胸やけ/胸焼け(胸焼け)、胃酸逆流、心窩部痛などの胃食道逆流症の症状の治療。食道炎を患っていない患者には、1日1回20 mgを投与します。 4 週間経過しても症状のコントロールが達成できない場合は、患者を検査する必要があります。胃食道逆流症の症状が治まれば、必要に応じてエソメプラゾールマグネシウムを 1 日あたり 20 mg の用量で使用して症状をコントロールできます。
抗炎症薬で治療を受けている高リスク患者の場合、オンデマンド治療で症状をコントロールすることは推奨されません。
継続的な抗炎症療法が必要な患者
- 抗炎症薬による治療に伴う上部胃腸症状の治療。抗炎症薬の服用を継続する必要がある患者には、1日1回20 mgを投与します。 4週間経っても症状がコントロールできない場合は、患者を検査する必要があります。
- 抗炎症薬による治療に伴う胃潰瘍の治癒には、通常、20 mg を 1 日 1 回、4 ~ 8 週間服用します。患者によっては、1 日 1 回 40 mg を 4 ~ 8 週間投与する必要がある場合があります。
- リスクのある患者における抗炎症薬による治療に伴う胃潰瘍および十二指腸潰瘍の予防、1日1回20 mg。
ヘリコバクター ピロリ/ヘリコバクター ピロリの除菌に関連する十二指腸潰瘍の治療: エソメプラゾール マグネシウム 20 mg とアモキシシリン 1 g およびクラリスロマイシン 500 mg を 1 日 2 回、7 日間投与
潰瘍の症状の治癒と解消のために抗分泌薬による治療を続ける必要はありません。
- ゾリンジャー・エリソン症候群および特発性過剰分泌を含む分泌過剰の病理学的状態では、推奨される開始用量はエソメプラゾールマグネシウム40 mgを1日2回です。用量調整は個別に行われ、臨床的に指示された期間、治療を継続する必要があります。最大 120 mg の用量が 1 日 2 回投与されています。
- エソメプラゾールナトリウム40mgを1日1回4週間静注した後の胃潰瘍および十二指腸潰瘍の止血の維持と再出血の予防。経口治療期間の前に、エソメプラゾールナトリウム 80 mg を 30 分間のボーラス注入で投与する酸抑制療法を実施し、その後 8 mg/h の持続静脈内注入を 3 日間かけて行う必要があります。
12~18歳の子供
胃食道逆流症(GERD)
- びらん性逆流性食道炎の治療。40 mg を 1 日 1 回、4 週間投与します。治癒していない食道炎の患者、または症状が持続する患者には、さらに 4 週間の治療が推奨されます。
- 胃食道逆流症の症状の治療。食道炎のない患者には 1 日 1 回 20 mg を投与します。 4 週間経過しても症状のコントロールが達成できない場合は、患者を検査する必要があります。胃食道逆流症の症状が解消したら、医師の監督下でエソメプラゾールマグネシウムを1日20mgの用量で使用できます。
- 小児(12~18歳)に対するエソメプラゾールマグネシウムによる治療は8週間に限定する必要があります。
子供たち
データがないため、エソメプラゾール マグネシウムは 12 歳未満の小児には使用しないでください。
腎不全
腎不全患者には用量調整は必要ありません。重度の腎障害のある患者に対する経験は限られているため、これらの患者は慎重に治療する必要があります。
肝不全
軽度から中等度の肝障害のある患者には用量調整は必要ありません。重度の肝障害のある患者の場合、エソメプラゾールマグネシウムの1日最大用量20 mgを超えてはなりません。
お年寄り
高齢者には用量調整の必要はありません。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
エソメプラゾールマグネシウム – EMS の使用を忘れた場合はどうすればよいですか?
エソメプラゾールマグネシウムの服用を忘れた場合は、思い出したらすぐに服用する必要がありますが、次の服用時間が近い場合は、忘れた分を服用する必要はありません。次はいつも通りの時間に服用してください。忘れた分を補うために2回分を服用しないでください。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
エソメプラゾールマグネシウムの注意事項 – EMS
エソメプラゾールマグネシウムによる治療中に、食事のない体重減少、嘔吐、食べ物を飲み込むのが困難、明るい血や黒い便(コーヒーかすなど)が出る場合、また、潰瘍が疑われるか存在する場合は、エソメプラゾールマグネシウムによる治療によって次のような症状が生じる可能性があるため、医師に伝えてください。これらの症状を軽減し、診断を遅らせます。
アタザナビルやネルフィナビルなどの抗レトロウイルス薬(特定の種類のウイルスに対する)を服用しているかどうかもお知らせください。まれにフルクトース不耐症、グルコース-ガラクトース吸収不良、スクラーゼ-イソマルターゼ機能不全などの遺伝性の問題がある場合は、この薬を服用しないでください。
いくつかの研究では、エソメプラゾール系の薬剤による治療は、骨粗鬆症(骨の密度と質量が減少する病気)に関連する骨折のリスクがわずかに増加する可能性があることを示唆しています。しかし、他の同様の研究では、リスクの増加は証明されませんでした。
骨粗鬆症または骨粗鬆症に関連する骨折を発症するリスクがある患者には、適切な医学的モニタリングを受けることが推奨されます。
エソメプラゾールマグネシウムは、機械の運転や操作能力に影響を与えることはないと考えられています。
エソメプラゾールマグネシウムの副作用 – EMS
一般的な反応 (この薬を使用している患者の 1% ~ 10% で発生)
頭痛、腹痛、下痢、ガス、吐き気、嘔吐、便秘。
異常な反応 (この薬を使用している患者の 0.1% ~ 1% の間で発生します)
周囲の腫れ、睡眠困難、めまい、皮膚の灼熱感/しびれ、眠気、めまい、口渇、肝酵素量の増加(この効果は血液検査を行った場合にのみ確認できます)、皮膚反応(皮膚炎、かゆみ、じんましんや皮膚の発疹)。
まれな反応(この薬を使用している患者の 0.01% ~ 0.1% で発生します)
白血球の減少(白血球減少症)、血液凝固細胞の減少(血小板減少症)、薬に対する過敏症(アレルギー)反応(腫れ、アナフィラキシー反応/ショック)、血中のナトリウムの減少(低ナトリウム血症)、興奮、混乱、うつ病、味覚障害、かすみ目、気管支けいれん、口の内層の炎症(口内炎)、胃腸の真菌感染症(胃腸カンジダ症)、黄疸(皮膚や目が黄色くなる)を伴うまたは伴わない肝臓の炎症(肝炎)、脱毛、光に対する皮膚の過敏症(光線過敏症)、関節痛、筋肉痛、倦怠感、発汗の増加、発熱。
非常にまれな反応(この薬を使用している患者の 0.01% 未満で発生します)
血液中の白血球顆粒球の欠如または不十分な数(無顆粒球症)、血球の減少(汎血球減少症)、攻撃性、幻覚、肝機能障害、肝性脳症、重度の皮膚障害(多形紅斑、スティーブンス・ジョンソン症候群および中毒性表皮壊死融解症) )、筋力低下、腎臓の炎症、男性の胸の肥大、血中のマグネシウムの減少(低マグネシウム血症)、重度の低マグネシウム血症は血中のカルシウムの減少(低カルシウム血症)を引き起こす可能性があり、低マグネシウム血症は低カリウム血症(血中の低濃度カリウム)も引き起こす可能性があります)および腸の炎症(顕微鏡的大腸炎)。
注意:
本製品は国内で新たな適応症を取得した医薬品であり、研究により許容できる有効性と安全性が示されていますが、たとえ正しく適応・使用されたとしても、予測できない、または未知の有害事象が発生する可能性があります。この場合は医師に知らせてください。
エソメプラゾールマグネシウムの特別集団 – EMS
子供たち
12 歳未満の小児に対する臨床経験は限られています。医師の判断により、この年齢層にのみ使用してください。
妊娠と授乳
この薬は、医師または歯科外科医のアドバイスなしに妊婦が使用しないでください。
エソメプラゾールの母乳中への排泄に関するデータはないため、授乳中には使用しないでください。
腎臓または肝臓疾患のある患者
エソメプラゾールマグネシウムは、肝臓や腎臓に重篤な問題がある患者には注意して使用する必要があります。
エソメプラゾールマグネシウムの組成 – EMS
各遅延放出フィルムコーティング錠には次のものが含まれます。
20mg
| エソメプラゾールマグネシウム三水和物 |
22.3mg(エソメプラゾール20mgに相当) |
|
賦形剤* |
遅延放出コーティング錠 1 錠 |
40mg
|
エソメプラゾールマグネシウム三水和物 |
44.5mg(エソメプラゾール40mgに相当) |
|
賦形剤* |
遅延放出コーティング錠 1 錠 |
*乳糖、結晶セルロース、クロスポビドン、アルファ化コーンスターチ、コロイド状二酸化ケイ素、ステアリン酸マグネシウム、ヒプロメロース+トリアセチン+二酸化チタン、ベンガラ、ポリメタクリル酸エチル+ポリアクリル酸エチル+タルク+二酸化ケイ素+炭酸水素ナトリウム+ラウリル硫酸ナトリウム、マクロゴール、シメチコン、精製水。
エソメプラゾールマグネシウムのプレゼンテーション – EMS
エソメプラゾールマグネシウム20mgと40mg。 7、14、28、56 * のコーティング錠が含まれています。
*病院用パッケージ。
経口使用。
大人および小児は12歳からご使用いただけます。
エソメプラゾールマグネシウムの過剰摂取 – EMS
エソメプラゾールマグネシウムの過剰摂取に対する特異的な治療法は知られていません。 80 mg のエソメプラゾール マグネシウムの投与では、いかなる合併症も発生しませんでした。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
エソメプラゾールマグネシウムの薬物相互作用 – EMS
以下の薬を服用している場合は、エソメプラゾールマグネシウムを注意して使用する必要があります。
真菌感染症の治療(ケトコナゾール、イトラコナゾール、エルロチニブ)、ジゴキシン、不安症(ジアゼパム)、てんかん(フェニトイン)、血液凝固(ワルファリンまたはクロピドグレル)、胃の運動促進(シサプリド)、メトトレキサート、エイズの治療(アタザナビル、ネルフィナビル)およびサキナビル)、アモキシシリン、キニジン、ナプロキセン、ロフェコキシブ、クラリトマイシン、ボリコナゾール、リファンピシンおよびセントジョーンズワート(オトギリソウ)による治療。これらの薬剤はエソメプラゾールマグネシウムの併用により効果が変化する可能性があるため。
エソメプラゾールとクロピドグレルの併用は避けてください。
エソメプラゾールの同時投与は、タクロリムスの血中濃度の上昇に関連しています。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
エソメプラゾールマグネシウムという物質の作用 – EMS
有効性の結果
胃酸分泌への影響
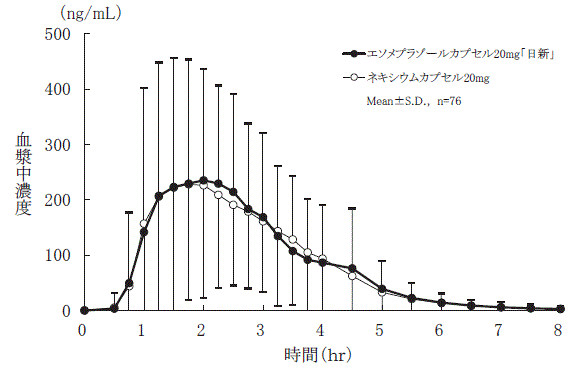
エソメプラゾールマグネシウム (活性物質) 20 mg および 40 mg を経口投与すると、1 時間以内に効果が始まります。 20 mg のエソメプラゾール マグネシウム (活性物質) を 1 日 1 回、5 日間繰り返し投与した後、5 回目の投与の 6 ~ 7 時間後に測定すると、ペンタガストリン刺激後の酸生成の平均ピークが 90% 減少します。 (Andersson T et al . Aliment Pharmacol Ther 2001; 15(10): 1563-9)。
症状のある患者において、20 mg および 40 mg のエソメプラゾールマグネシウム (活性物質) を 5 日間経口投与した後、24 時間で平均してそれぞれ 13 時間および 17 時間、4 を超える胃内 pH が維持されました。逆流性食道炎。 20mgのエソメプラゾールマグネシウム(活性物質)により、胃内pHを少なくとも8時間、12時間、16時間以上維持した患者の割合は、それぞれ76%、54%、24%でした。 40 mg のエソメプラゾール マグネシウム (活性物質) の対応する割合は、97%、92%、および 56% でした。
血漿濃度の代理パラメータとしてAUC(曲線下面積)を使用すると、酸分泌の阻害と曝露との関係が示されている(Lind T et al. Aliment Pharmacol Ther 2000;14:861-7)。
酸阻害の治療効果
40 mg のエソメプラゾール マグネシウム (活性物質) による逆流性食道炎の治癒は、患者の約 78% で 4 週間後に起こり、93% では 8 週間後に起こります (Richter JE et al. Am J Gastroenterol 2001; 96(3): 656 – 65)。
1日2回20mgのエソメプラゾールマグネシウム(活性物質)と適切な抗生物質による1週間の治療により、約90%の患者でヘリコバクター・ピロリの除菌が成功した(Nader F et al . GED 2005; 24(1) : 21-9 )。
1週間の除菌治療の後、潰瘍を効果的に治癒し、合併症のない十二指腸潰瘍の症状を消失させるために、その後の抗分泌薬による単独療法は必要ない(Tulassay Z et al . Eur J Gastroenterol Hepatol 2001; 13:1457-65)。
無作為化二重盲検プラセボ対照臨床研究では、764 人の患者がエソメプラゾールナトリウム 80 mg を 71.5 時間連続静脈内ボーラス注入され、その後エソメプラゾールマグネシウム (活性物質) 40 mg を経口的に 27 時間連続静脈内投与されました。日々。治療後7日目および30日目における再出血の発生率は、それぞれ治療群で7.2%対プラセボ群で12.9%、7.7%対13.6%でした(Sung JJ et al . Ann Intern Med 2009)。
酸阻害に関連するその他の効果
抗分泌物質による治療中、酸分泌の減少に反応して血清ガストリンが増加します。また、胃酸度の低下によりクロモグラニン A (CgA) も増加します。 CgA レベルの増加は、神経内分泌腫瘍の研究を妨げる可能性があります。文献の報告では、プロトンポンプ阻害剤による治療は CgA 測定の 5 ~ 14 日前に中断する必要があることが示されています。この期間内にレベルが正規化されない場合は、測定を繰り返す必要があります。
エソメプラゾールマグネシウム(活性物質)による長期治療中に、おそらく血清ガストリンレベルの上昇に関連する腸クロム親和性細胞の数の増加が小児および成人で観察されています。この所見は臨床的関連性があるとは考えられていません。抗分泌薬による長期治療中に、比較的高い頻度で胃腺嚢胞が発生したことが報告されています。これらの変化は、酸分泌の顕著な阻害の生理学的結果であり、良性であり、可逆的であると思われる(Maton P et al . Gastroenterology 2000; 118(4): A19 Abs337; Genta RM et al. Gastroenterology 2000; 118(4): A16 Abs326)。
プロトンポンプ阻害剤を含め、胃の酸性度が低下すると、胃腸管に通常存在する細菌の数が増加します。プロトンポンプ阻害剤による治療は、サルモネラ菌やカンピロバクターなどの胃腸感染症のリスクをわずかに増加させる可能性があります (Dial S et al . CMAJ 2004; 171(1):33-8; Dial S et al . JAMA 2005; 294 ( 23): 2989-95)。入院患者では、クロストリジウム・ディフィシルに関しても同じことが起こる可能性があります。
比較臨床研究
5件のクロスオーバー研究において、症候性胃食道逆流症患者24人において、エソメプラゾールマグネシウム(活性物質)40mg経口、ランソプラゾール30mg、オメプラゾール20mg、パントプラゾール40mg、ラベプラゾール20mgを1回投与した後、24時間の胃内pHプロファイルが評価された。 1日1回。 5日目、胃内pHは、エソメプラゾールマグネシウム(活性物質)で平均15.3時間、ラベプラゾールで13.3時間、オメプラゾールで12.9時間、ランソプラゾールで12.7時間、パントプラゾールで11.2時間、平均4.0以上に維持された(p≠0.001)。エソメプラゾールマグネシウム(活性物質)と他のすべての比較したものとの違い)。エソメプラゾール マグネシウム (活性物質) は、他のプロトン ポンプ阻害剤と比較して、12 時間以上胃内 pH が 4.0 を超える患者の割合の大幅な増加にもつながりました (p lt; 0.05) (Miner P Jr et al . Am J Gastroenterol) 2003年;
非ステロイド性抗炎症薬(NSAID)による継続的な治療が必要な患者
非ステロイド性抗炎症薬(NSAID)治療に伴う上部胃腸症状の治療
エソメプラゾール マグネシウム (活性物質) は、非選択的または COX-2 選択的 NSAID を使用している患者の上部胃腸症状の治療において、プラセボよりも有意に優れていました (Hawkey CJ et al . Gut 2003; 52(Suppl 6): A226, Abs WED -G) -253)。
非ステロイド性抗炎症薬(NSAID)による治療に伴う胃潰瘍の治癒
エソメプラゾールマグネシウム(活性物質)は、COX-2選択的NSAIDを含むNSAIDを使用している患者の胃潰瘍の治癒においてラニチジンよりも有意に良好でした(Goldstein JL et al. Gastroenterology 2004; 126(4 suppl 2): A610、Abs W1310)。
リスクのある患者における非ステロイド性抗炎症薬(NSAID)療法に関連する胃潰瘍および十二指腸潰瘍の予防
エソメプラゾールマグネシウム (活性物質) は、COX-2 選択的治療を含む NSAID による過去または現在の治療に関連する胃潰瘍および十二指腸潰瘍の予防においてプラセボよりも有意に優れていました (Yeomans ND et al. Gastroenterology 2004; 126(4 suppl 2): A604 Abs) W1278)。
薬理学的特徴
錠剤は胃内で分散しますが、微顆粒の胃耐性コーティングにより、エソメプラゾール マグネシウム (有効成分) は小腸に到達して吸収されるまで確実に保護されます。
薬力学特性
エソメプラゾール マグネシウム (活性物質) はオメプラゾールの S 異性体であり、特異的かつ標的を絞った作用機序を通じて胃酸分泌を減少させます。これは、壁細胞のプロトンポンプの特異的阻害剤です。オメプラゾールの S 異性体と R 異性体は同様の薬力学的活性を持っています。
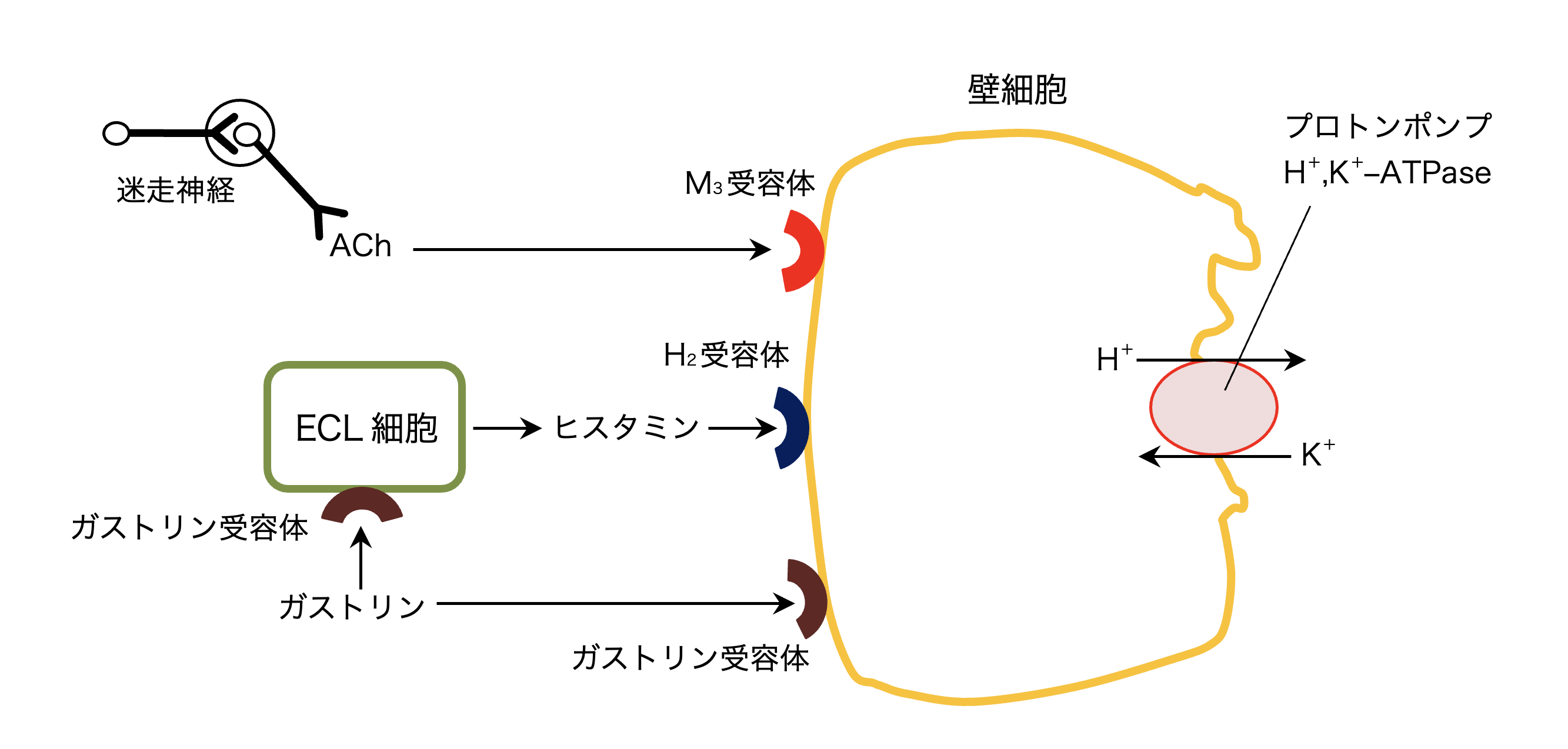
作用部位と作用機序
エソメプラゾールマグネシウム(活性物質)は弱塩基であり、壁細胞の分泌小管の強酸性環境で濃縮されて活性型に変換され、プロトンポンプである酵素H + K + -ATPaseを阻害します。基礎酸と刺激酸の分泌。
薬物動態学的特性
吸収と分配
エソメプラゾールマグネシウム(活性物質)は酸性環境では不安定であり、腸溶性コーティング顆粒として経口投与されます。インビボでの R 異性体への変換は無視できます。エソメプラゾールマグネシウム(活性物質)の吸収は速く、血漿濃度のピークは投与後約 1 ~ 2 時間で発生します。絶対バイオアベイラビリティは、40 mg の単回投与後に 64% であり、1 日 1 回の反復投与後には 89% に増加します。エソメプラゾールマグネシウム(活性物質)20mgの場合、対応する値はそれぞれ50%と68%です。健康な人における定常状態での見かけの分布体積は、体重 1 kg あたり約 0.22 L です。エソメプラゾールマグネシウム(有効成分)の血漿タンパク質結合率は97%です。
食物摂取はエソメプラゾール マグネシウム (活性物質) の吸収を遅らせ、減少させますが、胃内酸性度に対するエソメプラゾール マグネシウム (活性物質) の効果には大きな影響を与えません。
代謝と排泄
エソメプラゾールマグネシウム (活性物質) は、シトクロム P450 (CYP) システムによって完全に代謝されます。その代謝の主要部分は、エソメプラゾール マグネシウム (活性物質) の代謝産物であるヒドロキシとデメチルの形成に関与する多型 CYP2C19 に依存しています。残りの部分は、血漿中の主な代謝産物であるエソメプラゾール マグネシウム スルホン (活性物質) の形成に関与する、別の特定のアイソフォーム CYP3A4 に依存しています。
以下のパラメーターは主に、機能的な CYP2C19 酵素、つまり代謝が盛んな被験者の薬物動態を反映しています。
総血漿クリアランスは、単回投与後は約 17 L/h、反復投与後は約 9 L/h です。 1 日 1 回の反復投与後の血漿除去半減期は約 1.3 時間です。血漿中濃度対時間曲線下面積 (AUC) は、エソメプラゾール マグネシウム (活性物質) を繰り返し投与すると増加します。

この増加は用量依存性であり、繰り返し投与すると用量と AUC の関係が非線形になります。この時間と用量への依存性は、おそらくエソメプラゾールマグネシウム(活性物質)および/またはそのスルホン代謝物によるCYP2C19酵素の阻害によって引き起こされる初回通過代謝と全身性クリアランスの減少によるものです。エソメプラゾール マグネシウム (活性物質) は、投与間の血漿から完全に除去され、1 日 1 回の投与中に蓄積する傾向はありません。
エソメプラゾールマグネシウム(活性物質)の主な代謝物は胃酸分泌に影響を与えません。
エソメプラゾールマグネシウム(活性物質)の経口投与量の約 80% が代謝産物として尿中に排泄され、残りは糞便中に排泄されます。未変化の薬物が尿中に検出されるのは 1% 未満です。
特殊な患者集団
人口の約 3% は機能的な CYP2C19 酵素を持たず、代謝不良者と呼ばれています。これらの個人では、エソメプラゾール マグネシウム (活性物質) の代謝はおそらく主に CYP3A4 によって触媒されています。 40 mg のエソメプラゾール マグネシウム (活性物質) を 1 日 1 回繰り返し投与した後、平均 AUC は、機能的な CYP2C19 酵素を有する個人 (代謝の高い人) よりも代謝の悪い人の方が約 100% 高かった。平均ピーク血漿濃度 (C max ) は約 60% の増加を示しました。
これらの発見は、エソメプラゾール マグネシウム (活性物質) の投与量には影響しません。
エソメプラゾールマグネシウム(活性物質)の代謝は、高齢者(71~80歳)でも大きく変化しません。 40 mg のエソメプラゾール マグネシウム (活性物質) を単回投与した後、平均 AUC は女性の方が男性よりも約 30% 高くなります。 1日1回の反復投与では、男性と女性の間で差は観察されません。これらの発見は、エソメプラゾール マグネシウム (活性物質) の投与量には影響しません。
軽度から中等度の肝不全患者では、エソメプラゾールマグネシウム(活性物質)の代謝が損なわれる可能性があります。重度の肝不全患者では代謝率が低下し、その結果、エソメプラゾールマグネシウム(活性物質)のAUCが2倍になります。したがって、重度の肝障害のある患者では最大 20 mg を超えてはなりません。エソメプラゾール マグネシウム (活性物質) またはその主な代謝産物は、1 日 1 回の投与では蓄積する傾向を示しません。
腎機能が低下した患者を対象とした研究は行われていません。腎臓はエソメプラゾール マグネシウム (活性物質) の代謝産物の排泄を担当しますが、未変化化合物の排泄は担当しないことを考慮すると、腎不全の患者ではエソメプラゾール マグネシウム (活性物質) の代謝が変化するとは予想されません。関数。
12~18歳の患者におけるエソメプラゾールマグネシウム(活性物質)20mgおよび40mgの反復投与後の総曝露量(AUC)および薬物の最大血漿濃度に達するまでの時間(tmax)を測定した。エソメプラゾールマグネシウム(活性物質)の両方の用量については成人と同様です。
前臨床安全性データ
前臨床研究では、反復投与毒性、遺伝毒性、生殖毒性に関する従来の研究に基づいて、ヒトに対する特別な危険性は明らかにされていません。ラセミ混合物を用いたラットでの発がん性研究では、胃の腸クロム親和性細胞とカルチノイドの過形成が示されました。ラットにおけるこれらの胃への影響は、胃酸産生の低下に続発する顕著かつ持続的な高ガストリン血症の結果であり、プロトンポンプ阻害剤によるラットの長期治療後に観察されます。
ラットまたはイヌにおけるエソメプラゾールマグネシウム(活性物質)による治療後、新生児期から授乳中および離乳後まで、成体動物で以前に観察されたものと比較して、毒性および/またはその他の予期せぬ効果は見られませんでした。また、新生児/幼年期の動物がエソメプラゾール マグネシウム (活性物質) による治療後に胃粘膜の増殖性変化を受けやすいことを示す出来事もありません。したがって、これらの青少年毒性研究には、小児集団における特定のリスクを示す証拠はありませんでした。
出典:Esoneo Medication Professional の添付文書。
エソメプラゾールマグネシウム保管ケア – EMS
室温(15℃~30℃)で保管してください。
光を避け、乾燥した場所に保管してください。バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。
身体的特徴
ベージュ色の円形、両凸の滑らかな錠剤。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かない場所に保管する必要があります。
エソメプラゾールマグネシウムに関する法的声明 – EMS
MS登録番号1.0235.1079
農場。答え:
ロノエル・カザ・デ・ディオ博士
CRF – SP番号 19,710
EMS S/A
ロドビア ジョルナリスタ フランシスコ アギーレ プロエンサ、s/n°、Km 08
チャカラ アッセイ – ホルトランディア – SP
CEP 13186-901
CNPJ: 57.507.378/0003-65
ブラジルの産業
医師の処方箋に基づいて販売します。








-1024x576.jpg?resize=1024,576&ssl=1)


