RotateQはどのように機能しますか?
RotateQ®は、ロタウイルス感染によって引き起こされる胃腸炎(下痢および嘔吐)から子供を保護するのに役立つウイルスワクチンです。

ワクチンは、最も一般的なタイプまたはロタウイルスの「株」に対する身体が自然な防御を開発するのを支援することで機能します。
親/保護者のための情報
ロタウイルス胃腸炎とは何ですか?
ロタウイルス胃腸炎は、発熱、嘔吐、下痢を引き起こす可能性があります。これらの症状は、体液の喪失(脱水)や死に至る可能性があります。
これは、世界中の赤ちゃんや幼い子供の間で重度の脱水下痢の主な原因です。ワクチンを使用する前に、ウイルスは年間約2,500万人の医師の訪問の原因でした。この病気は、世界中で年間210万人の入院と352,000〜592,000人の死亡の原因となりました。
ロタウイルスは小腸に感染し、臨床像は通常、発熱と嘔吐から始まり、下痢が続きます。下痢は軽度から重度であり、通常は3〜9日間続きます。重度の嘔吐と下痢(1日5回以上)は平均3〜6日間続きます。 5歳までに、ほとんどすべての子供が少なくとも一度はロタウイルスに感染しています。これは、衛生基準が高い場合でも発生します。
rotateq禁忌
子供は次の場合にワクチンを受け取ってはいけません。
- ワクチンの用量を受け取った後、アレルギー反応を起こします。
- あなたはワクチンのいずれかの成分にアレルギーがあります。このリーフレットの最初に材料のリストがあります。
- 重度の組み合わせ免疫不全(SCID)があります。
rotateqの使用方法
RotateQ®は、医療専門家によってのみ管理されます。
ワクチンは、一連の3回の用量で経口投与されます。最初の用量は、6週齢で投与されます。他の2つの用量は、1〜2か月間隔で与えられます。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。医師の知識なしに治療を中止しないでください。
RotateQの使用を忘れたときはどうすればよいですか?
子供は3回のワクチンを必要とします。その後の用量を受け取るために、子供が医療の任命に戻ったことに関する医師の指示に従うことが重要です。予定されているすべての任命に出席することが重要です。忘れてしまった場合、または予定されている時間に任命のために戻ってくることができない場合は、子供の医師からアドバイスを求めてください。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
Rotateqの注意事項
あなたの子供がワクチンを受け取る前にあなたの医師が知っておくべきことがあります。
あなたはあなたの子供かどうか医師に伝えるべきです:
- 発熱して病気にかかっています。軽度の発熱または軽度の上気道感染症(寒い)だけでは、ワクチン接種を遅らせる理由ではありません。
- 下痢または嘔吐がある;
- あなたは体重を増やしていません。
- 期待どおりに成長していません。
- 血液障害があります。
- 何らかの癌があります。
- 病気(HIV感染またはエイズを含む)のために免疫系が弱くなっています。
- 免疫系を弱める可能性のある治療または薬を受けています。
- 胃腸の問題で生まれた、または腸の閉塞または腹部手術を受けた。
- 免疫系が弱い家族や介護者、たとえば癌の人や免疫系を弱める可能性のある薬を服用している人と定期的に密接に接触してください。
他のワクチンと同様に、RotateQ®はそれを受け取ったすべての子供を完全に保護しない場合があります。一部の子供はすでにウイルスを持っているかもしれませんが、まだ病気の兆候を示していません。これらの場合、ワクチンは病気を予防しない可能性があります。
RotateQ®は、ロタウイルスによって引き起こされた場合にのみ、下痢と嘔吐から保護するのに役立ちます。ワクチンは、他の理由によって引き起こされた場合、これらの症状に対する保護を提供しません。ワクチンウイルスの拡散を防ぐために、おむつを交換した後に手を洗うことをお勧めします。
機械の運転または操作
RotateQ®は、成人での使用には示されていません。
糖尿病の方は注意:砂糖が含まれています。
回転qの副作用
すべての薬と同様に、RotateQ®は副作用を提示することができます。
rotateq®の副作用は一般に軽度で一時的なものです。さらに、これらの副作用は、プラセボの投与(活性成分のない経口溶液)の投与と比較して、はるかに頻繁に報告されませんでした。
RotateQ®の使用で報告された副作用は次のとおりです。
非常に一般的な反応(この薬を使用している患者の 10% 以上で発生します)
下痢、嘔吐、発熱。
異常な反応 (この薬を使用している患者の 0.1% ~ 1% の間で発生します)
鼻の点滴、喉の痛み、耳の感染。
まれな反応(この薬を使用している患者の 0.01% ~ 0.1% で発生します)
喘鳴と咳。
未知の頻度反応
重度の可能性のあるアレルギー反応(アナフィラキシー)、アレルギー腫脹、じんましん、および腸重積(あるセグメントが別のセグメントに囲まれる腸閉塞の形式)。 、腹部と発熱。
これらは、 rotateq®のすべての考えられる副作用ではありません。より完全なリストを医師から取得できます。
このリーフレットで言及されていない副作用に気付いた場合は、医師または医療専門家に知らせてください。
状態が持続または悪化した場合は、医師の診察を求めてください。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。また、顧客サービスを通じて会社に通知してください。
Rotateq特別人口
妊娠と授乳
RotateQ®は、成人には示されていない小児ワクチンであり、妊娠中または母乳育児の女性に投与すべきではありません。人間の妊娠または授乳中に使用するデータはありません。
この薬は、医師または歯科外科医のアドバイスなしに妊婦が使用しないでください。
子供たち
ROTATEQ®は、6〜32週齢の乳児に投与された場合、一般的に忍容性が高く、ロタウイルス胃腸炎の予防に非常に効果的であることが示されています。安全性と有効性は、6週齢未満の新生児ではまだ確立されていません。
rotateqの構成
各2 mLの用量には、次のヒト/ウシロタウイルスの再配列が含まれています。
G1、G2、G3、G4およびP1A [8]。
再配置の最小レベルは次のとおりです。
|
G1 |
2.2 x 10 6感染ユニット |
|
G2 |
2.8 x 10 6感染ユニット |
|
G3 |
2.2 x 10 6感染ユニット |
|
G4 |
2.0 x 10 6感染ユニット |
|
P1A [8] |
2.3 x 10 6感染ユニット |
賦形剤:
スクロース、クエン酸ナトリウムジヒド酸ナトリウム、リン酸ナトリウム単菌一水和物、水酸化ナトリウム80、培地および胎児ウシ血清の痕跡。ソリューションには、防腐剤やチメロサルは含まれていません。
RotateQプレゼンテーション
RotateQ®は、2 mLで満たされたツイストキャップを備えた1つのプラスチックチューブを含むカートリッジに提示される単一用量経口溶液です。
経口使用。
小児用途(6〜32週齢)。
回転qの過剰摂取
RotateQ®の推奨よりも高い用量の投与の報告があります。一般に、過剰摂取で報告された有害事象のプロファイルは、 RotateQ®の推奨用量で観察されたものと同等でした。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
rotateq薬物相互作用
子供は他のワクチンと同時にRotateQ®を受け取ることができますが、ワクチンは他のワクチンや溶液と混合されるべきではありません。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。

物質回転qの作用
有効性の結果
ヒトロタウイルス血清型(G1、G2、G3、G4およびP1A [8])は、ヒト/ウシのロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質)に対して選択されました。北米、ヨーロッパ、オーストラリアのロタウイルス疾患の症例の90%、および1973年から2003年の間に世界中のロタウイルス疾患の症例の88%以上。
効果
ヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(活性物質)の保護効果を2つの方法で評価しました。
- ロタウイルス胃腸炎を予防するためのヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](活性物質)の有効性は、ワクチンを受けた6,983人の乳児(n = 3,484)またはプラセボ(n = n = 3,484)または2つの研究でのプラセボ(n = 3,499):ロタウイルス有効性と安全試験 – 休憩と研究007。
- 入院や緊急治療室への訪問を含むロタウイルス胃腸炎による医療の減少は、残りの研究で68,038人の乳児の間で評価され、残りのフィンランドの延長研究から20,736人の乳児のサブグループで評価されました。休息中のワクチン接種後最大2年間乳児を追跡し、フィンランドの休憩延長研究の乳児はワクチン接種後最大3年間続き続けました。拡張調査中に安全データは収集されませんでした。乳児の親/保護者による仕事による日常的な医療任命と不在の減少も、残りの研究で評価されました。
ワクチンまたはプラセボの3回目の用量は、最大32週齢まで乳児に投与されました。
すべての第III相の研究では、ポリオワクチン1、2、3(減衰)を除き、他の認可された小児ワクチンの付随する投与が許可されました。
ワクチンに含まれる血清型G(G1-G4)の自然ロタウイルス感染によって引き起こされる重症度の胃腸炎に対する有効性は73.8%であり、重度のロタウイルス胃腸炎に対する有効性は、最初のロタウイルスシーズン中に発生した98.2%でした。予防接種。ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質)は、ワクチンに含まれていないG血清型に対する保護も提供しました。限られたデータに基づいて、ワクチンに含まれていない血清型(G9)によって引き起こされる重症度の胃腸炎に対する有効性は74.1%でした。ヒト/ウシのロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(活性物質)の有効性は、重症度のロタウイルス胃腸炎に対するワクチン接種の終了後の2つのロタウイルスシーズン中に発生しました。
ヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(活性物質)(アクティブな物質)入院率、緊急治療室訪問、オフィス訪問、および子供の保護者による就業日の紛失を減らしました。
静止と拡張の研究における血清型G1-G4によって引き起こされる医療訪問(入院と緊急治療室への訪問)の減少率は次のとおりでした。
- 入院および緊急治療室の訪問のための94.4%(ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質)n = 34,035幼児、プラセボn = 34,003乳児;
- 入院のための94.3%、および;
- 緊急治療室の相談のための94.4%。
3年間(ヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(活性物質)n = 3,112乳児、パースボn = 3,126乳児)ワクチンのグループとプラセボ群では1回(タイプ不可能な)訪問しかありませんでした。子どもの両親/保護者による非緊急医療の任命と勤務日の逃した日は、残りの研究でワクチン接種後最大2年間評価されました。削減率は次のとおりでした:
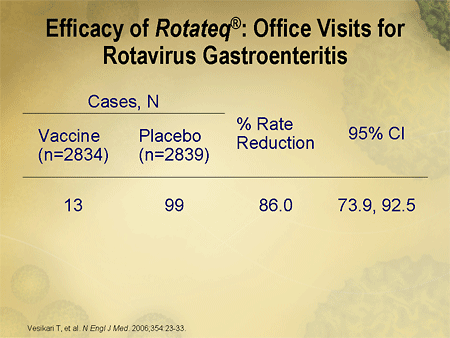
- 非緊急医療相談の場合は86.0%(ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質)n = 2,834乳児、プラセボn = 2,839乳児)、および;
- 両親/法的保護者による失われた就業日の86.6%(ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質)n = 34,035乳児、プラセボN = 34,003乳児)。
ヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(活性物質)の最初のフルロタウイルスシーズンを通して、ロタウイルス胃腸炎(活性物質)の完全なワクチン接種と、入院とロタビルスの訪問の減少と救急室の訪問の減少胃腸炎後の最大3年後のGワクチン接種を表1から3に示します。
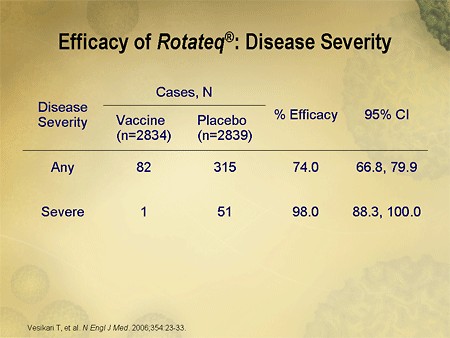
表1ヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(活性物質)の重症度と重度のロタウイルス胃腸炎G1-G4の最初のバクシネーション後のロタビロスシーズン中の胃腸炎に対する胃腸炎に対する表
|
予防接種済み |
プロトコルによる |
itt † |
||
|
ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質) |
プラセボ |
ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質) |
プラセボ |
|
|
2,834 |
2,839 | 2,834 |
2,839 |
|
|
胃腸炎の症例 |
||||
|
重大度 |
82 | 315 | 150 | 371 |
|
深刻な* |
1 | 51 | 2 | 55 |
|
有効性の推定(%)および(95%信頼区間) |
||||
|
重大度 |
74.0(66.8; 79.9) | 60.0(51.5; 67.1) | ||
|
重度の胃腸炎* |
98.0(88.3; 100.0) |
96.4(86.2; 99.6) |
||
*発熱、嘔吐、下痢から行動の変化までの症状の強度と期間に基づいた臨床スコアリングシステムによって定義された重度の胃腸炎。
† ITT分析には、少なくとも1回のワクチン(ITT – 治療意図)を受けた有効性コホートのすべての乳児が含まれます。
表2ヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰物)(活性物質)の有効性は、安静時のロタウイルスG1-G4による胃腸炎の入院を減らしました。
|
– |
プロトコルによる |
itt* |
||
|
ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質) |
プラセボ |
ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質) |
プラセボ |
|
|
予防接種済み |
34,035 | 34,003 | 34,035 |
34,003 |
|
入院数 |
6 | 144 | 10 | 187 |
|
有効性の推定(%)、および(95%信頼区間) |
95.8 (90.5; 98.2) |
94.7 (89.3; 97.3) |
||
*ITT分析には、少なくとも1回のワクチンを受けたすべての乳児が含まれます。
表3ヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(活性物質)の重症度および重度のロタウイルス胃腸炎G1-G4の胃腸炎に対する胃腸炎(活性物質) 007
|
プロトコルによる |
itt † |
|||
|
ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質) |
プラセボ |
ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質) |
プラセボ |
|
|
予防接種済み |
650 | 660 | 650 |
660 |
|
胃腸炎の症例 |
||||
|
重大度 |
15 | 54 | 27 | 64 |
|
深刻な* |
0 | 6 | 0 | 7 |
|
有効性の推定(%)および(95%信頼区間) |
||||
|
重大度 |
72.5 (50.6; 85.6) |
58.4 (33.8; 74.5) |
||
|
深刻な* |
100.0 (13.0; 100.0) |
100.0 (30.2; 100.0 |
||
*発熱、嘔吐、下痢から行動の変化までの症状の強度と期間に基づいた臨床スコアリングシステムによって定義された重度の胃腸炎。
† ITT分析には、少なくとも1回のワクチンを受けた有効性コホートのすべての乳児が含まれます。
また、ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質)の有効性を評価するために分析も実施しました。ワクチンの少なくとも1回の用量(ITT – 治療意図)を受けた乳児の間で、ワクチン接種後の最初のロタウイルスシーズンまでの最初の用量。
REST研究では、ワクチン接種後の最初のロタウイルスシーズンまでの天然に発生する血清型G1、G2、G3、またはG4によって引き起こされるロタウイルス胃腸炎の重症度の主要な有効性は74.0%(95%CI:66.8〜79.9)およびITT有効性は60.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0.0. %(95%CI:51.5〜67.1)。
ワクチン接種後の最初のロタウイルスシーズンまでの天然に発生する血清型G1、G2、G3、またはG4によって引き起こされる重度のロタウイルス胃腸炎に対する主要な有効性は98.0%(95%CI:88.3〜100.0)であり、ITT有効性は96.4%(95%CI)でした。 :86.2〜99.6)。
重度の疾患に対するヒト/ウシのロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](活性物質)の有効性は、REST研究のすべての参加者間のロタウイルス胃腸炎の入院の減少によっても実証されました。
ヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(活性物質)95.888888888の3回目の用量後の最初の2年間の血清型G1、G2、G3、G4によって引き起こされるロタウイルス胃腸炎の入院の減少%(95%CI:90.5〜98.2)。
入院の減少におけるITTの有効性は94.7%でした(95%CI:89.3〜97.3)。 In study 007, the primary efficacy of any severity of rotavirus gastroenteritis caused by naturally occurring serotypes G1, G2, G3 or G4 through the first rotavirus season after vaccination was 72.5% (95% CI: 50.6 to 85.6) and ITT efficacy was 58.4% (95%CI:33.8〜74.5)。
研究007では、ワクチン接種後の最初のロタウイルスシーズンを通じて天然に発生する血清型G1、G2、G3、またはG4によって引き起こされる重度のロタウイルス胃腸炎に対する主要な有効性は100%(95%CI:13.0〜100。0)および重度のロタビルスに対するITT有効性でした。疾患は100%でした(95%CI:30.2〜100.0)。
血清型に依存しないロタウイルス胃腸炎
RESTおよび研究007の有効性サブグループで特定されたロタウイルス血清型は、G1P1Aでした[8]。 G2P1 [4]; G3P1A [8]; G4 P1A [8];およびG9P1A [8]。
休息では、ヒト/ウシのロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質)の有効性は、あらゆる重症度のある天然ロタウイルス胃腸炎に対する、血清型に関係なく71.8%でした(95%でしたCI:64.5〜77.8)および重度のロタウイルス疾患に対する有効性は98.0%でした(95%CI:88.3〜99.9)。用量1からのITTの有効性は、重症度のあるロタウイルス疾患の場合は51.0%(95%CI:41.7〜58.9)でした。
研究007では、ヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(活性物質)の主要な有効性は、あらゆる重症度、血清型に関係なく、72.7%でした(955%でした。 %CI:51.9〜85.4)および重度のロタウイルス疾患に対する有効性は100%でした(95%CI:12.7〜100)。用量1からのITTの有効性は、重症度のあるロタウイルス疾患の場合は48.0%(95%CI:21.6〜66.1)でした。
未熟児の有効性と安全性
In a placebo-controlled study, Human/Bovine Rotavirus Vaccine G1, G2, G3, G4 and P1 [8] (Attenuated) (active substance) or placebo were administered to 2,070 premature infants (25 to 36 weeks of gestational age), withその1,007は、年齢に応じて、ヒト/ウシのロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(活性物質)を受け取りました。すべての副作用に対して追跡された308人の早産児のサブセットのうち、安全性プロファイルは、一般的にヒト/ウシのロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(活性物質)を投与しているグループで、それらと比較して類似していました。プラセボを受け取った人。発熱、嘔吐、下痢、または過敏性の発生率は、一般的にワクチンを受けた人とプラセボを受けた人との間で類似していた。
204人のワクチン接種乳児(ワクチン群で99)のサブグループでは、3回目の用量のワクチンの少なくとも14日後に発生したワクチン血清型G1-G4の重症度の重症度の重症度の発生率の減少によって測定される保護効果ワクチン接種後の最初のフルロタウイルスシーズン中、それは70.3%でした[95%CI:LT; 0〜94.7]。
残りの研究では、2,070人のワクチン接種乳児(ワクチン群で1,007)で、入院率の低下と緊急治療室への訪問率の低下により保護効果が測定され、3回目の用量後14日から2年後の血清型G1-G4によって引き起こされるロタウイルス胃腸炎が原因で測定されます。 100%[95%CI:74〜100]でした。
同様に、3回目の用量が100%であった14日から2年後の期間の血清型によって引き起こされるロタウイルス胃腸炎による入院率と緊急治療室への訪問率を減らす際に測定された保護効果は[95%CI:82から100]。
効果
表4に示されている3つの市場後のワクチンの有効性研究の結果は、入院、緊急治療室またはオフィス訪問の大幅かつ一貫した減少または全死因胃腸炎を示しています。米国とフランスのこれらのワクチンの有効性データは、ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質)がG12P [8]株および持続的な保護に対して特定の効果を持っていることを示しました。ロタウイルス関連の入院と、生涯の7年目までの子供の緊急治療室への訪問に対して。
Tabela 4 Estudos pós-comercialização demonstrando a efetividade de Vacina Rotavírus Humano/Bovino G1, G2, G3, G4 e P1 [8] (Atenuada) (substância ativa) na prevenção de gastroenterite
|
研究デザイン(地域) |
研究集団 |
研究の結果 |
有効性%[95%CI] |
ロタウイルスの季節 |
|
健康保険請求データベースの分析(米国) |
33,140ワクチン接種26,167ワクチン接種年齢? 7か月は3回の投与を受けました | GERによる入院と緊急治療室の訪問 | 100%[87,100] |
2007-2008 |
| GER†による相談 | 96%[76,100] | |||
| 胃腸炎のすべての原因のための入院と緊急治療室の訪問 | 59%[47.68] | |||
|
コホート研究(フランス)‡ |
1,895は3回の投与量でワクチン接種しました2,102はワクチン接種されていない年齢LT。 2年 | GERによる入院 | 98%[83,100] |
2007-2008 |
|
2008-2009 |
||||
|
ケースコントロール研究(米国)§ |
402ケース2,559コントロール¶年齢LT; 8歳は3回投与されました | GERによる入院と緊急治療室の訪問† | 80%[74.84] |
2011-2012 2012-2013 |
|
ひずみ固有 |
||||
|
G1P [8] |
89%[55.97] |
|||
|
G2P [4] |
87%[65.95] |
|||
|
G3P [8] |
80%[64.89] |
|||
|
G12P [8] |
78%[71.84] |
|||
|
年齢固有 |
||||
|
人生の1年目 |
91%[78.96] |
|||
|
人生の2年目 |
82% [69,89] |
|||
|
3º ano de vida |
88% [78,93] |
|||
|
4º ano de vida |
76% [51,88] |
|||
|
5º ano de vida |
60% [16,81] |
|||
|
6º ao 7º ano de vida |
69% [43,84] |
|||
*Wang ft、 et al 。米国の胃腸炎を予防する際の五日のロタウイルスワクチンの有効性。 Pediatrics.125 (e208). 2009-1246. 2010年。
†ger =ロタウイルス胃腸炎
‡ Gagneur, A, et al.ロタウイルス下痢の入院に対するロタウイルスワクチン接種の影響:イヴァンホー研究。 Vaccine. (29)。 3753- 3759. 2011.
§ Payne DC, et al.ロタウイルスワクチン保護における長期一貫性:RV5およびRV1ワクチンの有効性米国の子供、2012-2013。 Clin Infect dis.1-7。 2015年。
¶ロタウイルス陰性の急性胃腸炎でコントロールします。
他のワクチンとの研究
ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1の免疫原性[8](弱毒化)(活性物質)および吸着型ジフテリア、破傷風および百日咳ワクチン(無細胞および後耳ワクチン(DTPA)、ポリオワクチン1、3、3、3、3、3、3、3 (不活性化)(IPV)、ヘモフィルスインフルエンザB(HIB)コンジュゲートワクチン、B型肝炎ワクチン(組換え)および肺炎球菌ワクチン(コンジュゲート)は、1,358人の乳児で評価されました。特定のワクチンに対する免疫応答は、ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質)の影響を受けませんでした。さらに、研究により、これらのワクチンで投与された場合、ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](活性物質)(89.5%)の有効性が実証されています。
ポリオワクチン1、2、3(減衰物)(OPV)を使用したヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1(減衰)(活性物質)の付随する投与は、抗原に対する免疫応答に影響を与えませんでした。 735人のワクチン接種乳児を含む対照研究のポリオ。 OPVの付随する投与は、ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質)に対する免疫学的反応の一部を減少させましたが、血清学的反応率(上昇?ベースラインと比較して3倍)血清抗ロタウイルスIgAの場合はGTでした。 93%。重度のロタウイルス胃腸炎に対する高レベルの有効性の維持の証拠がありました。ヒト/ウシのロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)に対する免疫応答は、OPVがヒト/ウシロータウイルスワクチンG1、G2、G3、G4の2週間後に投与された場合、影響を受けませんでした。およびP1 [8](減衰)(活性物質)。
発熱、嘔吐、下痢、および過敏性の発生率を含む安全性プロファイルは、一般に、ヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(減衰)と同時に特定のワクチンを投与された乳児の間で類似していました。活性物質)およびプラセボと同時に特定のワクチンを受けた乳児。
1つの研究では、7,367人の乳児が六量体ワクチン(DTPA、IPV、HIB、およびB型肝炎)を投与されました。因果関係に関係なく、深刻な副作用(SAE)の総頻度は、ヒト/ウシのロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質)および3.2を投与された人では2.9%でした。プラセボを受けた人の%。より詳細な安全情報は、ヒト/ウシのロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(活性物質)を六角形のワクチンで投与された638人の乳児のサブグループの間で評価されました。発熱、嘔吐、下痢、および過敏性の発生率を含む安全性プロファイルは、一般に、ヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(減衰)を含む六バレンワクチンを投与された乳児の間で類似していました。活性物質)およびプラセボで六量体ワクチンを受けた乳児。
403人の健康な乳児を対象とした、その後の多施設、無作為化、二重盲検プラセボ対照安全性および免疫原性研究で、ヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(薬物活性)の併用投与)六量体ワクチンでは、六角形のワクチンまたはヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1に存在する抗原に対する血清抗体応答や血清保護率を妨害しませんでした[8](活性物質) )。ヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(活性物質)の付随する投与および六価ワクチンは十分に許容されました。
ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](活性物質)(活性物質)および髄膜炎菌ワクチンC(結合)の付随的な使用に関する多施設、無作為化、オープン、免疫原性研究が行われました。 246人の健康な乳児。付随する投与は、ワクチンに対する免疫応答に影響を与えず、両方のワクチンは十分に許容されていました。
免疫原性
ヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(活性物質)がロタウイルス胃腸炎から保護する免疫学的メカニズムは不明です。ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質)に対する抗体反応と、ロタウイルス胃腸炎に対する保護との関係は確立されていません。しかし、ヒト/ウシロタウイルスワクチンG1、G2、G3、G4、およびP1 [8](減衰)(活性物質)は、血清型G1、G2、G3、G3、G4およびP1Aを中和する抗体を誘導します[8]。第III相試験では、ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1のレシピエントの92.9%から100%[8](減衰)(活性物質)は、3回後に血清抗ロタウイルスIgAの有意な増加を達成しました。 – 用量スケジュール。
出典:RotateQ投薬プロフェッショナルインサート。
薬理学的特徴
ロタウイルスは、先進国および発展途上国の幼児や幼児の重度の急性胃腸炎の主な原因です。ロタウイルス胃腸炎は、社会経済的状態や環境条件に関係なく、5歳までの乳児や幼児の95%以上に影響を与える普遍的な疾患です。世界中で、1億3,800万人の子供が毎年ロタウイルス胃腸炎を発症し、2,500万人の医療訪問、210万人の入院、352,000〜592,000人の死亡をもたらすと推定されています。米国では、推定350万人の子供が毎年ロタウイルス胃腸炎を発症し、500,000件の医療訪問、55,000の入院、20〜102人の死亡をもたらしました。米国では、8人に1人の子供が医療を求め、73人に1人が5歳までにロタウイルス胃腸炎のために入院します。入院の最も高い割合は、6〜24ヶ月の乳児と幼児の間で発生します。適切な経口または静脈内液投与で治療されない場合、ロタウイルス胃腸炎は致命的な脱水を引き起こす可能性があります。
ロタウイルス胃腸炎は温帯気候の季節疾患であり、冬の数ヶ月で流行が発生します。ロタウイルス胃腸炎は、一般的に熱帯および亜熱帯気候の領域で風土病です。ロタウイルスは、地理的地域や季節に関係なく、世界中の下痢のすべての入院の約28%から71%の原因です。ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質)は、小腸で複製し、免疫を誘発する生の減衰ウイルスワクチンです。
作用機序
A proteção contra a infecção natural pelo rotavírus é amplamente sorotipo-específica.ヒトロタウイルス血清型(G1、G2、G3、G4およびP1A [8])は、ヒト/ウシロタウイルスワクチンG1、G2、G3、G4およびP1 [8](減衰)(活性物質)に対して選択されました。 1996年から1999年までの米国のロタウイルス疾患の%および1973年から2003年までの世界中のロタウイルス疾患の88%以上。 ) (active substance) protects against rotavirus gastroenteritis is unknown. Estudos sugerem que uma combinação de fatores é importante na imunidade contra rotavírus, incluindo anticorpos neutralizantes contra as proteínas G do capsídeo externo, IgA sérica e secretória e outras respostas locais da mucosa.
出典:RotateQ投薬プロフェッショナルインサート。
RotateQストレージケア
Conservar e transportar sob refrigeração (2°C a 8°C).光から守ります。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。
外観
RotaTeq ® é um líquido amarelado claro a amarelado rosado.
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かないところに保管してください。
RotateQの法的声明
MS 1.0029.0175
農場。答え:
フェルナンド・C・レモス
CRF-SP番号16,243
/arc-anglerfish-tgam-prod-tgam.s3.amazonaws.com/public/7YJQO5KQDNF5NJFEUQWK6TM4YY)
登録およびインポート:
メルクシャープアンプ; Dohme Farmaceutica Ltda.
Rua 13 De Maio、815
Sousas, Campinas/SP
CNPJ:45.987.013/0001-34 – ブラジルMSD
On Line 0800-0122232
製造元:
メルクシャープアンプ; Dohme Corp.
ウエストポイント、米国








-1024x576.jpg?resize=1024,576&ssl=1)


