ベンセラジド塩酸塩 + レボドパはどのように作用しますか?

パーキンソン病の症状は、中枢神経系(CNS)におけるドーパミンの欠乏によるものです。ドーパミンは細胞間のコミュニケーションを助ける物質です。この病気の治療は、ドーパミンの前駆体であるレボドパと、レボドパを放出しないように機能する酵素である塩酸ベンセラジドという2つの物質の会合である、この薬物の投与によって行われるドーパミンの置換に基づいています。 CNSに入る前にドーパミンに変換され、レボドパの副作用が軽減されます。
したがって、レボドパ + 塩酸ベンセラジドを投与すると、脳内でドーパミンに変換されるドーパミン前駆体が投与され、パーキンソン病の症状の原因となるメカニズムであるドーパミンの欠乏によって引き起こされる症状が改善されます。
この薬を空腹時に服用した場合、この薬の治療作用が始まるまでの推定平均時間は約 25 分です。
ベンセラジド塩酸塩 + レボドパの禁忌 – Aché
この薬剤は、レボドパ、ベンセラジド、または製剤のその他の成分に対して過敏症があることがわかっている患者には投与すべきではありません。
この薬は、非選択的モノアミンオキシダーゼ阻害剤 (MAOI) クラスの抗うつ薬と併用しないでください。
ただし、セレギリンやラサギリンなどの選択的 MAO-B 阻害剤、またはモクロベミドなどの選択的 MAO-A 阻害剤は禁忌ではありません。 MAO-A 阻害剤と MAO-B 阻害剤の組み合わせは非選択的 MAOI と同等であるため、レボドパ + 塩酸ベンセラジドと同時に投与すべきではありません。
この薬は、内分泌(ホルモン産生)腺、腎臓、肝臓、心臓の制御不能な疾患のある患者、閉塞隅角緑内障(眼圧の上昇)のある患者、または精神疾患の病歴のある患者には投与しないでください。精神病的な要素。
この薬は、適切な避妊方法がない場合、妊婦または出産可能年齢の女性による使用は禁忌です。レボドパ + 塩酸ベンセラジドによる治療中に妊娠した場合は、医師の指示に従って薬の使用を中止する必要があります。
レボドパ + 塩酸ベンセラジドによる治療を受けている母親は母乳育児をすべきではありません。
この薬は25歳未満の子供には禁忌です(骨の発育が完了している必要があります)。
この薬は、医師または歯科外科医のアドバイスなしに妊婦が使用しないでください。
ベンセラジド塩酸塩 + レボドパの使用方法 – Aché
この薬は経口投与する必要があります。可能な限り、レボドパ + 塩酸ベンセラジドは、食事の少なくとも 30 分前または食後 1 時間以内に服用する必要があります。胃腸への悪影響は、主に治療の初期段階で発生する可能性がありますが、この薬を小さなスナック(クッキーなど)や液体と一緒に服用するか、徐々に用量を増やすことによって、ほとんど制御できます。
レボドパ + 塩酸ベンセラジド錠剤は噛まずに飲み込む必要があります。飲み込みやすくするために割ることもできます。
投与量
通常の投与量:
レボドパ + 塩酸ベンセラジドによる治療は徐々に開始し、効果が最適化されるまで用量を徐々に増加する必要があります。
初期治療:
パーキンソン病の初期段階では、レボドパ 1/4 錠 + 塩酸ベンセラジド 250 mg (62.5 mg) を 1 日 3 ~ 4 回投与して治療を開始することが推奨されます。
効果の最適化は、通常、レボドパ + 塩酸ベンセラジドの 1 日量 (レボドパ 300 ~ 800 mg + ベンセラジド 75 ~ 200 mg の範囲に相当) を 3 回以上に分けて行うことで達成されます。理想的な効果が得られるまでには 4 ~ 6 週間かかる場合があります。
メンテナンス治療:
平均維持量は、レボドパ 1/2 錠 + 塩酸ベンセラジド 250 mg (125 mg) を 1 日 3 ~ 6 回、つまり 1 日あたりレボドパ 300 mg ~ 600 mg です。
特別な投与方法:
医師は、レボドパ + 塩酸ベンセラジド、または併用する他の薬剤の用量を調整する必要性について指示します。
患者は、望ましくない精神症状の可能性がないか注意深く観察する必要があります。
腎不全患者への使用:
軽度または中等度の腎不全の場合、用量を減らす必要はありません。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。医師の知識なしに治療を中止しないでください。
ベンセラジド塩酸塩+レボドパを使い忘れた場合はどうすればよいですか?
この薬の服用を忘れた場合は、思い出したらすぐに服用し、通常の治療スケジュールに戻ってください。ただし、次の服用時間が近い場合は、忘れた分は飲まずに次の通常の時間に飲んでください。忘れた分を補うために2回分を服用しないでください。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
ベンセラジド塩酸塩 + レボドパの注意事項 – Aché
処方箋と医師の監督なしにこの薬を使用しないでください。あなたの場合、レボドパ + 塩酸ベンセラジドが適応とならない可能性がありますが、それを判断できるのは医師だけです。同様の理由で、この薬を譲ったり、他の人に勧めたりしないでください。敏感な人には過敏反応が起こる可能性があります。
この薬を服用する前に、次のことを医師に伝えてください。 開放隅角緑内障 (眼圧の上昇、通常は無症状) がある場合。手術を受けなければならず、全身麻酔が必要な場合。
レボドパ + 塩酸ベンセラジドの使用を突然中止すべきではありません。突然の中断は、非常に高い発熱(40度以上)、自律神経の不安定(心拍数、血圧、発汗など、神経系によって制御される器質的機能の変動)を特徴とする神経弛緩性悪性症候群に似た状態を引き起こす可能性があります。 .)、顕著な筋肉の硬直および精神障害(せん妄など)があり、クレアチンホスホキナーゼ(CPK、筋肉損傷を示す酵素)の増加などの検査室の変化を伴う可能性があり、致命的になる可能性があります。
モニタリングのために臨床検査が必要かどうかを医師が通知します。
ドーパミン作動薬(神経伝達物質ドーパミンの活性を妨げます)
ドーパミン作動薬(脳内のドーパミン受容体に作用する薬)で治療を受けたパーキンソン病患者では、ギャンブル依存症、性欲の増大、性的過剰などが報告されています。ドーパミン作動薬ではないこの薬剤とこれらの出来事との間に因果関係は確立されていません。ただし、レボドパ + 塩酸ベンセラジドはドーパミン作動薬であるため、注意が必要です。
薬物依存または乱用の可能性
パーキンソン病患者の小さなサブグループは、認知障害(たとえば、記憶喪失が特徴)と行動の変化を示しており、これらは、摂取する市販薬の量の増加と、症状を治療するために必要な用量の増加に直接起因する可能性があります。運動障害。
現在までに、レボドパと塩酸ベンセラジドの組み合わせがドーピングを引き起こす可能性があるという情報はありません。疑問がある場合は、医師に相談してください。
腎不全および肝不全の患者
腎障害または肝障害のある患者におけるレボドパの薬物動態データは入手できません。
レボドパ + 塩酸ベンセラジドは、血液透析を受けている尿毒症患者(腎不全により血液中に過剰な尿素が存在する)において忍容性が良好です。
薬物相互作用およびその他の形態の相互作用
食物との相互作用:
レボドパ + 塩酸ベンセラジドをタンパク質が豊富な食事と一緒に摂取すると、効果の減少が観察されます。
薬物動態学的相互作用:
レボドパ + 塩酸ベンセラジドを服用する前に、以下を服用しているかどうかを医師に伝えてください。

抗コリン作用のあるトリヘキシフェニジル(抗パーキンソン病)、硫酸第一鉄、メトクロプラミド(胃腸運動障害の治療に使用)。
薬力学的相互作用:
レボドパ + 塩酸ベンセラジドを服用する前に、神経弛緩薬(幻覚や妄想などの精神病の陽性症状の治療に使用される物質)、オピオイド(鎮痛作用のある物質)、レセルピンを含む降圧薬、米国の抗うつ薬を服用しているかどうかを医師に知らせてください。非選択的MAO酵素阻害剤(MAOI)のクラス、アドレナリン、ノルアドレナリン、イソプロテレノール、アンフェタミンなどの交感神経興奮性化合物(交感神経系を刺激し、ストレスの多い状況に身体が反応できるようにする作用に関連する)、その他の抗パーキンソン病薬、手術を受けなければならず、ハロセンによる全身麻酔が必要な場合。
レボドパは、カテコールアミン (アドレナリン、ノルアドレナリン、ドーパミンなどの化合物)、クレアチニン (腎機能の指標)、尿酸、およびグルコース (糖) の臨床検査の結果に影響を与える可能性があります。
クームス試験(新生児の自己免疫疾患および溶血性疾患の診断に使用される)の結果は、レボドパ + 塩酸ベンセラジドで治療を受けている患者において偽陽性を示す可能性があります。
他の薬を服用している場合は、医師または歯科医に伝えてください。医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
ベンセラジド塩酸塩 + レボドパの副作用 – Aché
この薬は一般に忍容性が良好ですが、不随意運動、精神病症状、狭心症(心臓由来の胸痛)、便秘、体重減少、息切れなどの望ましくない影響が発生する可能性があります。
市販後
血液およびリンパ系の障害:
溶血性貧血(赤血球の破壊による細胞の酸素化を維持するためのヘモグロビン不足)、一過性白血球減少症(白血球の減少)、血小板減少症(凝固に重要な血液要素である血小板の減少)がまれに報告されています。
栄養障害および代謝障害:
食欲不振(食欲の低下または喪失)が報告されています。
精神障害:
うつ病はパーキンソン病患者の臨床像の一部である可能性があり、レボドパ + 塩酸ベンセラジドで治療されている患者にも発生する可能性があります。興奮、不安、不眠症、幻覚、妄想、一時的な見当識障害は、特に高齢の患者や精神病歴のある患者に発生することがあります。
神経系障害:
味覚障害または味覚障害(味覚の変化)の単独の症例が報告されています。治療の後期段階では、ジスキネジア(不随意の舞踏病様運動、ジストニア性またはアテトーゼ性運動)が発生することがあります。治療が長期に及ぶと、無動(可動性の低下)、歩行のすくみ、投与終了時の悪化、「オンオフ」効果(オンオフ現象)などの治療反応の変動が生じる可能性があります。レボドパ + 塩酸ベンセラジドの使用は眠気を引き起こす可能性があり、日中の過度の眠気や突然の睡眠エピソードを伴うことは非常にまれです。
心臓障害:
心臓不整脈(心拍のリズムの変化)が時々発生することがあります。
血管障害:
起立性低血圧(立ち上がると血圧が低下する)がまれに発生することがあります。胃腸障害:レボドパおよび塩酸ベンセラジドでは、吐き気、嘔吐、下痢が報告されています。
皮下組織および皮膚の疾患:
まれにかゆみ、発疹、潮紅(赤み)などのアレルギー反応が起こる場合があります。
調査:
トランスアミナーゼおよびアルカリホスファターゼ(肝臓関与の指標)の一時的な増加が発生する場合があります。レボドパと塩酸ベンセラジドの組み合わせを使用すると、ガンマ-グルタミルトランスフェラーゼ (肝臓関与のもう 1 つの指標) と血中尿素レベル (腎臓関与の指標) の増加が観察されました。

尿の色が変化する場合があり、一般的には赤みがかった色に変化し、しばらく休むと暗くなることがあります。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。また、顧客サービスを通じて会社に通知してください。
ベンセラジド塩酸塩 + レボドパの特別集団 – Aché
車両の運転や機械の操作能力への影響
レボドパは、眠気や突然始まる睡眠エピソードと関連しており、これらは日常生活中に非常にまれに、場合によっては患者の警告や認識なしに発生します。レボドパによる治療を受けており、眠気や突然の睡眠エピソードを経験している患者には、乗り物の運転や、不注意によって自分や他人が重傷を負ったり死亡したりする可能性のある活動(例:機械の操作)を避けるよう警告されるべきである。これらの繰り返しのエピソードと眠気が解消されるまで。
妊娠と授乳
この薬は、適切な避妊方法がない場合、妊婦または出産可能年齢の女性による使用は禁忌です。
ベンセラジドの母乳中への移行は不明であるため、子供の骨の発達に変化が生じる可能性を排除できないため、この薬による治療を受けている母親は母乳育児をすべきではありません。
この薬は、医師または歯科外科医のアドバイスなしに妊婦が使用しないでください。
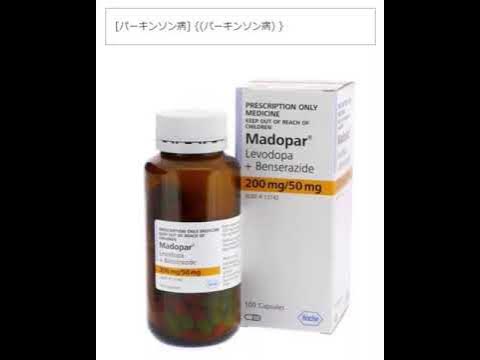
ベンセラジド塩酸塩 + レボドパの組成 – Aché
各タブレットには次のものが含まれています。
|
レボドパ |
200mg |
|
ベンセラジド塩酸塩 |
57 mg (ベンセラジド 50 mg に相当) |
賦形剤:
マンニトール、微結晶セルロース、第二リン酸カルシウム二水和物、クロスポビドン、ポビドン、二酸化ケイ素、ドキュセートナトリウム、ステアリン酸マグネシウムおよびベンガラ。
ベンセラジド塩酸塩 + レボドパの過剰摂取 – 痛み
過剰摂取の兆候と症状は、治療用量のレボドパ + 塩酸ベンセラジドの副作用と本質的に似ていますが、より重篤になる可能性があります。過剰摂取は、心臓血管への悪影響(不整脈 – 心拍の周波数やリズムの変化など)、精神障害(錯乱や不眠症など)、胃腸への影響(吐き気や嘔吐など)、および異常な不随意運動を引き起こす可能性があります。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
ベンセラジド塩酸塩 + レボドパの薬物相互作用 – Aché
薬物動態学的相互作用
抗コリン作用のあるトリヘキシフェニジルとレボドパ錠 + 塩酸ベンセラジド (活性物質) の組み合わせにより、レボドパの吸収速度は低下しますが、程度は低下しません。
硫酸第一鉄は、レボドパの最大血漿濃度と曲線下面積を 30 ~ 50% 減少させます。硫酸第一鉄の同時投与中に観察される薬物動態の変化は、すべての患者ではなく一部の患者において臨床的に重大であると考えられます。
メトクロプラミドはレボドパの吸収速度を高めます。
ドンペリドンは、胃内容排出を刺激することにより、レボドパの生物学的利用能を高める可能性があります。
薬力学的相互作用
レセルピンを含む神経弛緩薬、オピオイドおよび降圧薬は、レボドパ + 塩酸ベンセラジド(活性物質)の作用を阻害します。
この薬剤は、非選択的モノアミンオキシダーゼ阻害剤 (MAOI) と併用すべきではありません。不可逆的な非選択的 MAOI を使用している患者にレボドパ + 塩酸ベンセラジド (活性物質) を投与する場合、MAOI の中止とレボドパによる治療の開始の間には、最低 2 週間の間隔をあけなければなりません。そうしないと、高血圧クリーゼなどの副作用が発生する可能性があります。セレギリンやラサギリンなどの選択的 B-MAOI、およびモクロベミドなどの選択的 A-MAOI は、レボドパ + 塩酸ベンセラジド (活性物質) による治療を受けている患者に処方できます。忍容性と有効性の観点から、患者の個々のニーズに応じてレボドパの用量を再調整することが推奨されます。選択的 MAO-A 阻害剤と MAO-B 阻害剤の組み合わせは非選択的 MAOI の使用と同等であり、レボドパ + 塩酸ベンセラジド (活性物質) と一緒に投与すべきではありません。
レボドパはその作用を増強する可能性があるため、この薬は交感神経興奮薬(交感神経系を刺激するエピネフリン、ノルエピネフリン、イソプロテレノール、アンフェタミンなど)と同時に投与しないでください。併用投与が必要な場合は、心血管系の厳密なモニタリングが不可欠であり、交感神経刺激薬の用量の減量が必要になる場合があります。
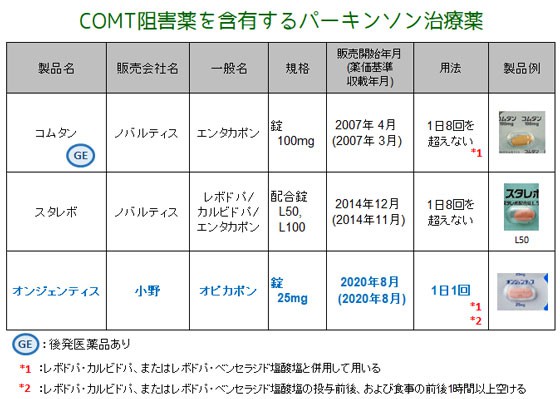
抗コリン薬、アマンタジン、セレギリン、ブロモクリプチン、ドーパミン作動薬などの他の製品との併用は許可されています。ただし、望ましい効果と悪影響の両方が強化される可能性があります。レボドパまたは他の抗パーキンソン病薬の用量を減らす必要がある場合があります。 COMT 阻害剤による補助治療を開始する場合、レボドパ + 塩酸ベンセラジド (活性物質) の用量を減らす必要がある場合があります。レボドパの効果は即時ではないため、レボドパ + 塩酸ベンセラジド (活性物質) による治療を開始する場合、抗コリン薬を突然中止すべきではありません。
レボドパは、カテコールアミン、クレアチニン、尿酸、ブドウ糖の臨床検査結果を変える可能性があります。
レボドパ + 塩酸ベンセラジド (活性物質) で治療されている患者では、クームズ検査の結果が偽陽性となる可能性があります。
ハロタンによる全身麻酔では、血圧の変動や不整脈が発生する可能性があるため、レボドパ + 塩酸ベンセラジド (活性物質) の使用は外科的介入の 12 ~ 48 時間前に中止する必要があります。この薬物による治療は、手術後に徐々に再開し、以前の用量レベルまで用量を増やして再開できます。
レボドパ + 塩酸ベンセラジド (活性物質) をタンパク質が豊富な食事と一緒に摂取すると、効果の低下が観察されます。
物質ベンセラジド塩酸塩 + レボドパの作用 – Aché
効果の結果
レボドパ + 塩酸ベンセラジド (有効成分) は、パーキンソン病のすべての段階に対する確立された治療法であり、運動症状と患者の生活の質の大幅な改善を促進します。
この薬は、2 つの物質 (レボドパ + 塩酸ベンセラジド (有効成分) およびベンセラジド) を 4:1 の比率で組み合わせたもので、この比率は臨床試験で理想的であることが実証され、その後の経験によって確認されています。
レボドパ + 塩酸ベンセラジド (活性物質) + 塩酸ベンセラジド (活性物質) は、パーキンソン病に見られる線条体のドーパミンの減少を補うために 1970 年に導入されました。近年、レボドパ + 塩酸ベンセラジド (活性物質) + 塩酸ベンセラジドの組み合わせをこの疾患の標準治療法として確認し確立するために、かなりの数の臨床研究が行われましたが、その後、多くの補助療法が導入されました。最近のコクランレビューでは、レボドパ + 塩酸ベンセラジド (活性物質) を用いた研究に含まれる 29 の研究、合計 5,200 人以上の患者から結果を収集しており、その大部分はレボドパ + 塩酸ベンセラジド (活性物質) + 塩酸ベンセラジドについて言及しています。
近年、Katzenschlagerらは、は、英国のパーキンソン病研究グループで多施設、3 群、非盲検、実用的な臨床試験を実施しました。 1985年から1990年の間に、782人の患者が、レボドパ+塩酸ベンセラジド(活性物質)/デカルボキシラーゼ阻害剤、レボドパ+塩酸ベンセラジド(活性物質)/デカルボキシラーゼ阻害剤+セレギリン、またはブロモクリプチンのいずれかに無作為に割り付けられた。最終結果は死亡率、障害、運動合併症でした。健康関連の生活の質と精神機能も評価されました。
最終評価時の追跡調査期間の中央値は、連絡が取れた生存患者のうち166人(21%)で14年であった。ベースライン特性の調整後、障害スコアはブロモクリプチン群よりもレボドパ+塩酸ベンセラジド群の方が良好でした(ウェブスター: 16.6 vs 19.8; p = 0.03; Northwestern University Disability: 34.3 vs 30.0, p = 0.05)。健康生活の質調査の 36 項目における身体機能 (差 20.8; 95% CI 10.0, 31.6; p lt; 0.001) および要約身体スコア (差 5.2; 95% CI 0.7, 9.7; p = 0.03) を評価短縮形では、レボドパ + 塩酸ベンセラジド (有効成分) の方が高かった。死亡率、ジスキネジアの有病率、運動能力の変動、認知症の差異はグループ間で有意な差はなかった。
著者らは、ドーパミン作動薬であるブロモクリプチンによる初期治療では死亡率や運動障害は減少せず、運動合併症の頻度の初期減少は時間の経過とともに維持されないと結論付けた。彼らは、ドーパミン作動薬による初期治療による長期的な利益や臨床的に関連する疾患修飾効果の証拠は見つからず、レボドパとベンセラジド塩酸塩(活性物質)とベンセラジドの併用が依然としてドーパミン病の第一選択治療であると結論付けた。 。
薬理的特性
薬力学特性
脳内で神経伝達物質として作用するドーパミンは、パーキンソン病患者の大脳基底核に十分な量が存在しません。レボドパ + 塩酸ベンセラジド (活性物質) または L-ドーパ (3,4-ジヒドロキシ L-フェニルアラニン) は、ドーパミンの生合成の中間体です。レボドパ + 塩酸ベンセラジド (活性物質) (ドーパミンの前駆体) は、ドーパミンは血液脳関門を通過できますが、ドーパミンは通過できないため、ドーパミンレベルを上昇させるプロドラッグとして使用されます。中枢神経系 (CNS) に入ると、レボドパ + 塩酸ベンセラジド (活性物質) は、L-芳香族アミノ酸脱炭酸酵素によってドーパミンに代謝されます。
レボドパ + 塩酸ベンセラジド (活性物質) は、投与後、脳外および脳組織の両方で急速に脱炭酸されてドーパミンになります。したがって、投与されたレボドパ+塩酸ベンセラジド(活性物質)のほとんどは大脳基底核に利用できず、末梢で産生されたドーパミンが副作用を引き起こすことが多い。したがって、レボドパ+塩酸ベンセラジド(活性物質)の脳外脱炭酸を阻害することが特に望ましい。これは、レボドパ + 塩酸ベンセラジド (活性物質) と末梢脱炭酸酵素阻害剤であるベンセラジドを同時に投与することで達成できます。
レボドパ + 塩酸ベンセラジド (有効成分) + 塩酸ベンセラジドの治療作用が現れるまでの推定平均時間は、空腹時に薬を摂取した場合、約 25 分です。
薬物動態学的特性
吸収
レボドパ + 塩酸ベンセラジド (有効成分) は主に小腸の上部で吸収され、吸収は場所に依存しません。最大血漿濃度は、レボドパ + 塩酸ベンセラジド (活性物質) + 塩酸ベンセラジドの摂取後約 1 時間で到達します。
レボドパ + 塩酸ベンセラジド (活性物質) の最大血漿濃度 (C max ) および吸収の程度 (曲線下面積) は、用量 (レボドパ + 塩酸ベンセラジド (活性物質) 50 ~ 200 mg) に比例して増加します。
食物摂取により、レボドパ + 塩酸ベンセラジド (活性物質) の吸収速度と吸収範囲が減少します。レボドパ + 塩酸ベンセラジド (活性物質) + 塩酸ベンセラジド錠剤を標準的な食事の後に投与すると、最大血漿濃度は 30% 低くなり、到達までに時間がかかります。レボドパ + ベンセラジド塩酸塩 (活性物質) の吸収の程度は 15% 減少します。
分布
レボドパ + 塩酸ベンセラジド (活性物質) は、飽和輸送系を介して血液脳関門を通過します。血漿タンパク質には結合せず、その分布量は 57 リットルです。 CSF中のレボドパ+塩酸ベンセラジド(活性物質)の曲線下面積は、血漿中の曲線下面積の12%である。
レボドパ + 塩酸ベンセラジド (活性物質) とは異なり、治療用量のベンセラジドは血液脳関門を通過せず、主に腎臓、肺、小腸、肝臓に集中します。
生体内変換
レボドパ + 塩酸ベンセラジド (活性物質) は、2 つの主な代謝経路 (脱炭酸および O-メチル化) と 2 つの副経路 (アミノ基転移および酸化) によって生体内変換され、芳香族アミノ酸脱炭酸酵素はレボドパ + 塩酸ベンセラジド (活性物質) をドーパミンに変換します。この経路の主な最終生成物は、ホモバニリン酸とジヒドロキシフェニル酢酸です。
カテコール-O-メチルトランスフェラーゼは、レボドパ+塩酸ベンセラジド(活性物質)をメチル化し、3-O-メチルドーパに変換します。この主要な血漿代謝産物は 15 時間の排出半減期を持ち、治療用量のレボドパ + 塩酸ベンセラジド (活性物質) + 塩酸ベンセラジド錠剤を投与されている患者に蓄積します。
レボドパ + 塩酸ベンセラジド (活性物質) の末梢脱炭酸の減少は、ベンセラジドと組み合わせて投与した場合、レボドパ + 塩酸ベンセラジド (活性物質) および 3-O-メチルドーパの血漿レベルの上昇と、カテコールアミン (ドーパミン) のレベルの低下に反映されます。およびノルアドレナリン)およびフェノールカルボン酸(ホモバニリン酸、ジヒドロキシフェニル酢酸)。
ベンセラジドは、腸粘膜および肝臓でヒドロキシル化されてトリヒドロキシベンジルヒドラジンになります。この代謝産物は、芳香族アミノ酸デカルボキシラーゼの強力な阻害剤です。
排除
レボドパ + 塩酸ベンセラジド (活性物質) による末梢阻害型デカルボキシラーゼの存在下では、レボドパ + 塩酸ベンセラジド (活性物質) の消失半減期は約 1.5 時間です。パーキンソン病の高齢患者(65 ~ 78 歳)では、排出半減期がわずかに長くなります(約 25%)。
レボドパ + ベンセラジド塩酸塩 (活性物質) の血漿クリアランスは約 430 mL/min です。
ベンセラジドは生体内変換によりほぼ完全に除去されます。代謝産物は主に尿中に排泄され (64%)、程度は低いですが糞便中に排泄されます (24%)。
特殊集団における薬物動態
尿毒症患者および肝不全患者における薬物動態データは入手できない。
腎不全の場合に使用する
この薬剤は広範囲に代謝され、レボドパ + 塩酸ベンセラジド (活性物質) の 10% 未満が変化せずに腎臓から排泄されます。腎不全患者におけるレボドパ + 塩酸ベンセラジド (有効成分) の薬物動態データは入手できません。
レボドパ + 塩酸ベンセラジド (活性物質) + 塩酸ベンセラジドの組み合わせは、血液透析を受けている尿毒症患者の忍容性が良好です。
肝不全の場合の使用
レボドパ+塩酸ベンセラジド(有効成分)は、主に腸管、腎臓、心臓、肝臓に豊富に存在する脱炭酸酵素(芳香族アミノ酸)によって代謝されます。
肝障害患者におけるレボドパ + 塩酸ベンセラジド (有効成分) の薬物動態に関するデータは入手できません。
レボドパ+塩酸ベンセラジド(有効成分)の薬物動態に及ぼす年齢の影響
高齢のパーキンソン病患者 (65 ~ 78 歳) では、レボドパ + 塩酸ベンセラジド (活性物質) の排出半減期と曲線下面積 (AUC) の両方が、若い患者で観察された値よりも約 25% 高くなります (34 – 64 歳)。
年齢の影響は統計的には有意ですが、臨床的には無視できる程度であり、用量スケジュールとの関連性はそれほど高くありません。
前臨床研究
発がん性
レボドパ+塩酸ベンセラジド(有効成分)+塩酸ベンセラジドについては発がん性試験は実施されていません。
変異原性
レボドパ+塩酸ベンセラジド(有効成分)及び塩酸ベンセラジドの組み合わせには、エームス試験により変異原性は認められなかった。追加のデータはありません。
生殖能力
レボドパと塩酸ベンセラジド(活性物質)および塩酸ベンセラジドの組み合わせが動物の生殖能力に及ぼす影響に関する研究は行われていません。
催奇形性
マウス (400 mg/Kg)、ラット (600 mg/Kg および 250 mg/Kg)、ウサギ (120 mg/Kg および 150 mg/Kg) の骨格発達に対して催奇形性の影響は示されませんでした。
母体毒性の用量を適用すると、ウサギでは子宮内死亡の増加が観察され、ラットでは胎児体重の減少が観察されました。
その他
ラットにおける一般的な毒物学的研究により、骨格の発達に障害が発生する可能性が実証されています。
ベンセラジド塩酸塩 + レボドパの保管管理 – Aché
室温(15~30℃)で保管してください。光や湿気から守ります。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。
身体的特徴
レボドパ + ベンセラジド塩酸塩の錠剤は、ピンク色の円形の一部分の十字型です。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かないところに保管してください。
ベンセラジド塩酸塩 + レボドパに関する法的声明 – Aché
MS 1.0573.0444
担当薬剤師:
ガブリエラ・マルマン – CRF-SP 番号 30,138
アシェ ラボラトリオス ファーマセウティコス SA
ヴィア・ドゥトラ、km 222.2
グアルーリョス – SP
CNPJ 60.659.463/0001-91
ブラジルの産業
医師の処方箋に基づいて販売します。
嚢: 0800 701 6900








-1024x576.jpg?resize=1024,576&ssl=1)


