Nulojix はどのように機能しますか?

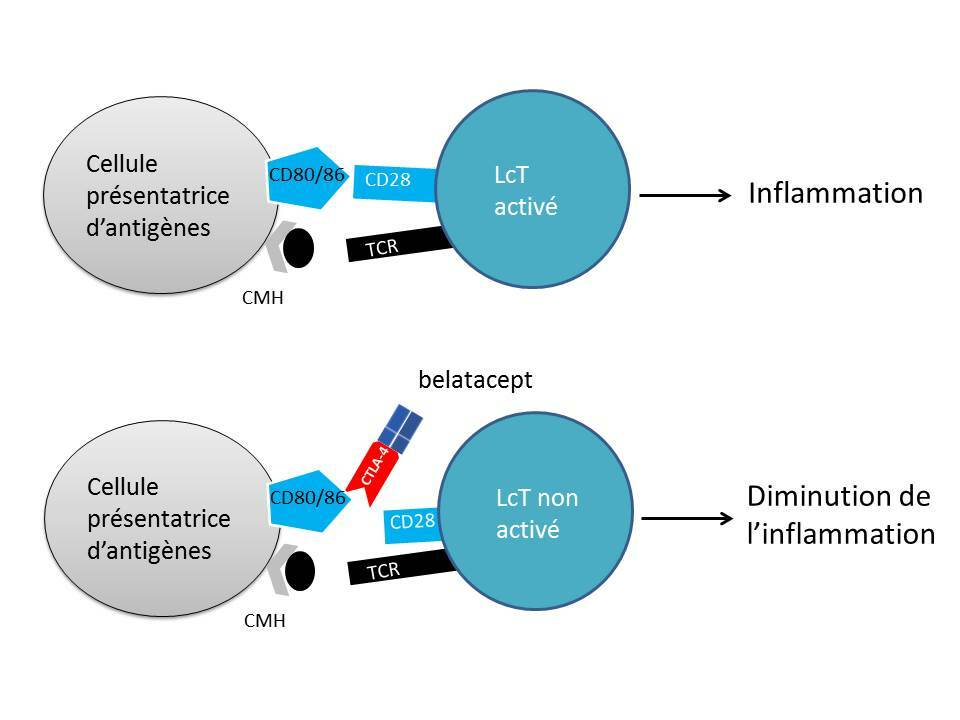
体内では、ベラタセプトは抗原提示細胞上の CD80 および CD86 受容体に結合します。これらの細胞は免疫システムにとって重要です。その結果、ベラタセプトは CD28 への結合によって媒介される T 細胞の共刺激をブロックし、これらの細胞の活性化を阻害します。
活性化された T 細胞は、移植された腎臓「に対する」免疫応答の主要なメディエーターです。 CTLA4-Ig の修飾型である Belatacept は、由来する CTLA4-Ig 前駆体分子よりも強く CD80 および CD86 に結合します。この増大した力は、免疫系によって誘発された場合の同種移植片の失敗や機能喪失を防ぐために必要なレベルの免疫抑制を提供します。
腎臓および膵島移植の霊長類モデルでは、ベラタセプトを単剤として、または他の標準的な抗拒絶療法と組み合わせて使用すると、プラセボと比較して移植片の生着が有意に延長され、抗ドナー抗体の産生が阻害されました。
インビトロで、ベラタセプトは、T細胞の増殖と、サイトカインであるインターロイキン-2、インターフェロン-α、インターロイキン-4、TNFαなどのいくつかの炎症メディエーターの産生をブロックします。同種抗原(移植された腎臓に由来する)に対する T 細胞応答を阻害することは、固形臓器移植後の移植片拒絶反応を防ぐために重要です。
Nulojix の禁忌
Nulojix は使用しないでください。
- エプスタイン・バーウイルス(EBV)に感染したことがない、または感染したかどうかわからない場合。
- ベラタセプトまたは Nulojix の他の成分に対してアレルギー (過敏症) がある場合。
Nulojixの使用方法
Nulojix は医療専門家によって投与されます。
これは、約 30 分間かけて静脈の 1 本に注入 (「点滴」として) 投与されます。
推奨用量は体重 (kg) に基づいており、医療専門家によって計算されます。治療の用量と頻度を表 1 に示します。
表 1: 腎移植レシピエントに対する Nulojix の投与量
|
初期段階の線量 |
用量 |
|
移植当日、移植前(1日目) |
10mg/kg |
|
5日目、14日目、28日目(移植後4週間) |
10mg/kg |
|
移植後8週目の終わりと12週目 |
10mg/kg |
|
維持期の線量 |
用量 |
|
移植後 16 週目の終わりから開始し、4 週間ごと (± 3 日) |
5mg/kg |
推奨されない投与経路による使用のリスク
非推奨の経路で投与される IV 点滴用の Nulojix 凍結乾燥粉末の効果に関する研究はありません。したがって、このプレゼンテーションの安全性と有効性を考慮すると、投与は静脈内のみである必要があります。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
Nulojix の使用を忘れた場合はどうすればよいですか?
Nulojix を受け取るには、すべての予約に出席することが非常に重要です。 Nulojix を受け取るべき用量を受け取らなかった場合は、次の用量をいつ服用すべきかを医師に相談してください。
ご質問がある場合は、薬剤師または医師に相談してください。
Nulojix の予防措置
移植後リンパ増殖性障害 (PTLD)
Nulojix による治療は、移植後リンパ増殖性障害 (PTLD) と呼ばれる種類のがんにかかるリスクを高めます。 Nulojix 治療では、PTLD が脳内でより頻繁に発症し、死に至る可能性があります。
以下の場合、患者は PTLD を発症するリスクが高くなります。
- 移植前にEBVに曝露されていない場合。
- サイトメガロウイルス(CMV)と呼ばれるウイルスに感染している場合。
- 急性拒絶反応の治療に使用される可能性のあるT細胞除去療法(抗胸腺細胞グロブリンなど)を受けている場合。
これらの症状について不明な点がある場合は、医師に相談してください。
重篤な感染症
Nulojix 治療では重篤な感染症が発生し、死に至る可能性があります。
Nulojix は、感染症と戦う体の能力を弱めます。重篤な感染症には次のようなものがあります。
- 結核。
- サイトメガロウイルス (CMV) は、血液や組織に重篤な感染症を引き起こす可能性のあるウイルスです。
- 帯状疱疹およびその他のヘルペスウイルス感染症。
進行性多巣性白質脳症(PML)
Nulojix の投与を受けている患者に、進行性多巣性白質脳症 (PML) と呼ばれるまれなタイプの脳感染症が発生したとの報告があります。 PML は重度の障害や死につながることがよくあります。
家族やあなたの世話を担当する人に、あなたの治療について伝えてください。自分では気づかない症状が発生する場合があり、PML、PTLD、またはその他の感染症を除外するために医師の調査が必要になる場合があります。
悪性腫瘍
Nulojix を服用している間は、日光や紫外線への曝露を制限してください。保護指数の高い保護服と日焼け止めを着用してください。 Nulojix を服用する人は、特定の種類のがん、特に皮膚がんのリスクが高くなります。
移植片血栓症
拡張基準ドナー同種移植片のレシピエントでは、移植後期間に移植片血栓症の発生率の増加が観察されています。
アレルギー反応
推奨用量でベラタセプトを投与されている患者において、注入関連反応が報告されています。現在までに、この薬に対するアナフィラキシーや過敏症の報告はありません。
予防接種
生ウイルスワクチンの使用は避けるべきです。ワクチン接種が必要な場合は医師に伝えてください。医師が今後の進め方について指導します。
肝移植での使用
肝移植を受けた場合、Nulojix の使用は推奨されません。
コルチコステロイドの用量の減少
Nulojix を使用している患者におけるコルチコステロイドの用量の減量は、特にヒト白血球抗原 4 ~ 6 (HLA) 不適合のある患者では、慎重に行う必要があります。商業試験では、バシリキシマブ、ミコフェノール酸モフェチルの導入と、移植後 6 週目にコルチコステロイドの投与量を 5 mg/日まで減量した Nulojix の併用は、急性拒絶反応、特にグレード III の拒絶反応率の増加と関連していました。これらのグレード III の拒絶反応は、HLA 4 ~ 6 の不適合を有する患者で発生しました。
小児および青少年への使用
Nulojix は 18 歳未満の患者を対象とした研究は行われていないため、これらの患者には Nulojix は推奨されません。
運転と機械の使用

Nulojix の投与後に疲労や体調不良を感じた場合は、車の運転や機械の操作を行わないでください。 Nulojix が機械の運転や使用に影響を与えるかどうかは不明です。
妊娠と授乳
妊娠中の女性に対する Nulojix の影響は不明であるため、医師が特に推奨しない限り、妊娠している場合は Nulojix を使用しないでください。 Nulojix の使用中は妊娠を避けてください。 Nulojix の使用中に妊娠した場合は、医師に知らせてください。
活性物質であるベラタセプトが母乳中に排泄されるかどうかは不明です。 Nulojix による治療を受けている場合は、授乳を中止する必要があります。
この薬は医師のアドバイスなしに妊婦が使用しないでください。
他の薬の使用
処方箋なしで入手した薬を含め、他の薬を服用している場合、または最近服用した場合は、医師または薬剤師に伝えてください。
Nulojix の使用中に他の薬を服用する前に、医師または薬剤師に相談してください。
糖尿病の方は注意してください:
砂糖が含まれています。
他の薬を服用している場合は医師に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
Nulojix の副作用
すべての薬と同様に、Nulojix は副作用を引き起こす可能性がありますが、誰もが副作用を経験するわけではありません。 Nulojix は、治療が必要な重篤な副作用を引き起こす可能性があります。
ベラタセプトで報告された最も一般的な (? 2%) 重篤な副作用は次のとおりです。
尿路感染症、CMV感染症、発熱、血清クレアチニン上昇、腎盂腎炎、下痢、胃腸炎、移植された腎臓の機能の問題、白血球の減少、肺炎、基底細胞癌、貧血、脱水症。
ベラタセプトで治療された患者の間で最も一般的に報告される副作用 (? 20%) は次のとおりです。
下痢、貧血、尿路感染症、手足の腫れ、便秘、高血圧、発熱、吐き気、移植腎臓の機能障害、咳、嘔吐、白血球の減少、血液中のリン酸塩レベルの低下、頭痛。
ベラタセプトの中断または中止を引き起こす副作用?患者の 1% は次のとおりでした。
腎静脈血栓症(閉塞)およびCMV感染。

表 2 は、臨床研究で 3 年目まで累積的に報告され、両方の belatacept レジメン (MI – より強度が高く、LI – 強度が低い) でグループ化された、少なくとも 1 つの因果関係が疑われる有害反応を、系統臓器分類および頻度カテゴリー別に示しています。
頻度カテゴリは次のように定義されます。
非常に一般的 (? 1/10)。一般的 (? 1/100 ~ lt; 1/10);そして珍しい(? 1/1,000 から lt; 1/100)。
各カテゴリ内で、望ましくない影響が重大度の順に示されています。
臨床研究における望ましくない影響
感染症と蔓延
|
非常に一般的な |
尿路感染症、上気道感染症、 |
|
一般 |
全身感染症、肺炎、インフルエンザ、胃腸炎、帯状疱疹、 |
|
普通でない |
PML、真菌性脳感染症、CMV大腸炎、腎症(炎症) |
良性、悪性および不特定のがん(嚢胞およびポリープを含む)
|
一般 |
皮膚の扁平上皮癌、基底細胞癌、 |
|
普通でない |
エプスタイン・バーウイルス**に関連するリンパ増殖性疾患、乳がん |
血液およびリンパ系の障害
|
非常に一般的な |
貧血、白血球減少症(白血球の減少) |
|
一般 |
血小板減少症(凝固因子の減少)、好中球減少症 |
|
普通でない |
単球減少症(白血球の減少)、純粋な無形成 |
免疫系障害
|
一般 |
血中免疫グロブリンG(IgG防御タンパク質)の減少 |
|
普通でない |
低ガンマグロブリン血症(免疫防御タンパク質の減少) |
内分泌疾患
|
一般 |
クッシンイド |
|
普通でない |
副腎不全 |
代謝と栄養障害
|
非常に一般的な |
低リン血症(血中リン酸濃度の低下)、 |
|
一般 |
体重増加、糖尿病、脱水症、体重減少、 |
|
普通でない |
糖尿病性ケトアシドーシス(糖尿病性ケトアシドーシスと同様の血液酸性度の変化) |
精神障害
|
非常に一般的な |
不眠症、不安症 |
|
一般 |
うつ |
|
普通でない |
異常な夢、気分の変化、注意欠陥/ |
神経系障害
|
非常に一般的な |
頭痛(頭痛) |
|
一般 |
振戦、感覚異常(チクチク感)、脳卒中 |
|
普通でない |
脳炎(中枢神経系の炎症)、 |
目の病気
|
一般 |
白内障、目の充血(充血)、かすみ目 |
|
普通でない |
網膜炎、結膜炎、目の炎症、角膜炎、羞明、まぶたの浮腫(腫れ) |
耳と迷路の障害
|
一般 |
めまい、耳痛、耳鳴り |
|
普通でない |
聴覚低下(聴力の低下) |
心臓障害
|
一般 |
頻脈(心拍数が速くなる)、徐脈 |
|
普通でない |
急性冠症候群、二次房室ブロック |
血管障害
|
非常に一般的な |
呼吸困難(息切れ)、咳 |
|
一般 |
肺水腫(肺の腫れ)、喘鳴、 |
|
普通でない |
急性呼吸窮迫症候群、肺高血圧症、 |
胃腸障害
|
非常に一般的な |
下痢、便秘、吐き気、嘔吐、腹痛 |
|
一般 |
消化不良(胸やけ)、アフタ性口内炎、腹部ヘルニア |
|
普通でない |
胃腸障害(腸リズムの変化)、膵炎、 |
肝胆道障害
|
一般 |
細胞溶解性肝炎(肝臓の炎症)、肝機能検査異常 |
|
普通でない |
胆石症、肝嚢胞、脂肪肝(肝臓への脂肪の蓄積) |
皮膚および皮下組織の疾患
|
一般 |
にきび、そう痒症(かゆみ)、脱毛症(脱毛)、皮膚病変、 |
|
普通でない |
乾癬、異常な発毛、脆い爪、 |
筋骨格疾患および結合組織疾患
|
非常に一般的な |
腰痛(背中の痛み)、関節痛(関節痛)、背中の痛み |
|
一般 |
筋肉痛(筋肉痛)、筋力低下、骨の痛み、腫れ |
|
普通でない |
骨代謝障害、骨炎、骨溶解症、滑膜炎 |
腎臓および泌尿器疾患
|
非常に一般的な |
血中クレアチニンの上昇、タンパク尿(尿中のタンパク質の損失)、 |
|
一般 |
腎尿細管壊死、腎静脈の血栓(閉塞)*、狭窄 |
|
普通でない |
腎動脈の血栓症(閉塞)*、腎炎、腎硬化症、萎縮 |
乳房および生殖器系の疾患
|
普通でない |
精巣上体炎(精巣上体の炎症)、持続勃起症(陰茎の勃起) |
先天性、家族性、遺伝性疾患
|
一般 |
水腫 |
|
普通でない |
低ホスファターゼ症 |
管理現場における一般的な混乱と状況
|
非常に一般的な |
末梢浮腫(手足のむくみ)、発熱(発熱) |
|
一般 |
倦怠感(倦怠感)、胸痛、倦怠感、瘢痕化 |
|
普通でない |
輸液関連反応*、過敏症、線維化、炎症、 |
臨床検査
|
一般 |
C反応性タンパク質の上昇、副甲状腺ホルモンの増加 |
|
普通でない |
膵臓酵素の増加、トロポニンの増加、 |
怪我、中毒、処置上の合併症
|
非常に一般的な |
移植片機能不全(移植された腎臓の機能喪失) |
|
一般 |
慢性同種移植腎症(腎機能の進行性喪失) |
|
普通でない |
移植失敗、輸血反応、創傷裂開、 |
*「選択された副作用の説明」を参照してください。
** 第 3 相研究では中央値 3.3 年、第 2 相研究では中央値約 7 年にわたって報告されたすべてのイベントが含まれます。
選択された副作用の説明
がんと移植後リンパ増殖性障害(PTLD)
PTLDは、シクロスポリンと比較して、両ベラタセプト治療群でより高い割合で発生しました。非黒色腫皮膚がんの発生頻度は、推奨用量のベラタセプトレジメンではシクロスポリンレジメンよりも低かった。
感染症
結核および非重篤なヘルペスウイルス感染症の全体的な発生率は、シクロスポリンレジメンよりもベラタセプトレジメンの方が数値的に高かった。結核症例の大部分は、結核の蔓延率が高い国に現在居住している、または以前に居住していた患者で発生しました。ポリオーマウイルス感染症および真菌感染症の全体的な発生率は、シクロスポリン群と比較して、推奨用量のベラタセプト群の方が数値的に低かった。 belatacept の臨床プログラム内で、PML と診断された患者が 2 人いました。
CNSに関与する感染症は、Belatacept LI群およびシクロスポリン群よりもBelatacept MI群でより頻繁でした。最も一般的なCNS感染症はクリプトコッカス髄膜炎でした。
移植片血栓症
拡張基準のドナー腎臓のレシピエントを対象とした第3相試験(研究2)では、移植片血栓症はベラタセプト群でより頻繁に発生しました(MIレジメンとLIレジメンではそれぞれ4.3%と5.1%)、シクロスポリンでは2.2%でした。標準基準による生体ドナーおよび死亡ドナーの腎臓のレシピエントを対象とした別の第 3 相試験では、移植片血栓症の発生率は、MI レジメンと LI レジメンでそれぞれ 2.3% と 0.4% であったのに対し、シクロスポリンでは 1.8% でした。第 2 相試験では、移植片血栓症の症例が 2 例あり、各レジメンで 1 例であったのに対し、シクロスポリン群では 0 例でした。一般に、これらの事象は早期に発生し、ほとんどが移植片喪失につながりました。
輸液関連の反応
3 年目までは、アナフィラキシー (重度のアレルギー反応) や薬剤に対する過敏症の報告はありませんでした。
ベラタセプト併用療法で最も頻繁に報告された急性点滴関連反応は、低血圧(低血圧)、高血圧(高血圧)、紅潮(皮膚の発赤)、および頭痛(頭痛)でした。ほとんどのイベントは重篤ではなく、程度は軽度から中等度であり、再発はありませんでした。ベラタセプトとプラセボ点滴を比較したところ、事象発生率に差はありませんでした。
家族やあなたの世話をする人にあなたの治療について伝えてください。自分では気づかない症状が現れることもあります。あなたまたはあなたの家族が上記の症状に気づいた場合は、すぐに医師に相談してください。
これらの副作用のいずれかが重篤になった場合、またはこの説明書に記載されていない副作用に気付いた場合は、医師または薬剤師に相談してください。
薬の使用により望ましくない反応が現れた場合は、医師または薬剤師に知らせてください。また、顧客サービスを通じて会社に通知してください。
注意:
この製品は新薬であり、研究により許容できる有効性と安全性が示されていますが、たとえ正しく指示され使用されたとしても、予測できないまたは未知の有害事象が発生する可能性があります。この場合は医師に知らせてください。
Nulojix の組成
Nulojix の各バイアルには次のものが含まれています。
ベラタセプト250mg。
不活性成分:
スクロース、リン酸一ナトリウム一水和物、塩化ナトリウム、水酸化ナトリウムおよび塩酸。
Nulojixの過剰摂取
必要以上に Nulojix を投与された場合、医師は副作用の兆候や症状を監視し、必要に応じてこれらの症状を治療します。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。
さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
Nulojix の薬物相互作用
処方箋なしで入手した薬を含め、他の薬を服用している場合、または最近服用した場合は、医師または薬剤師に伝えてください。
この薬を使用中に他の薬を服用する前に、医師または薬剤師に相談してください。
Nulojix 食品との相互作用
糖尿病の方は注意
砂糖が含まれています
他の薬を服用している場合は医師に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
Nulojix ストレージ ケア
IV 点滴用の Nulojix (belatacept) 凍結乾燥粉末は、2°C ~ 8°C で冷蔵保存する必要があります。 Nulojix は使用するまで元のパッケージに保管し、光から保護してください。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。

再構成後、溶液をバイアルから静脈内容器に直ちに移すことをお勧めします。
希釈後、Nulojix の注入は粉末の再構成から 24 時間以内に完了する必要があります。すぐに使用しない場合、輸液は 2°C ~ 8°C で 24 時間まで冷蔵保存する必要があります (この 24 時間のうち最大 4 時間は 20°C ~ 25°C の制御された温度で保存できます)。環境光)。
物理的および感覚的特性
粉末は全体または断片化されたケーキで、色は白からほぼ白です。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かないところに保管してください。
Nulojix のクールな名言
登録 MS – 1.0180.0401
技術責任者:
エリザベス M. オリベイラ博士 – CRF-SP 番号 12,529
製造元:
ブリストル・マイヤーズ スクイブ ホールディングス ファーマ株式会社
ボ ティエラス ヌエバス Rt. 686 Km 2.3
マナティ – プエルトリコ
輸入者:
ブリストル・マイヤーズ スクイブ ファーマシューティカ SA
Rua Carlos Gomes, 924 – サント アマロ – サンパウロ – SP CNPJ 56.998.982/0001-07
医師の処方箋に基づいて販売します。
使用は病院に限定されます。








-1024x576.jpg?resize=1024,576&ssl=1)


