Starlix は単独で使用することも、相補的な作用機序を持つメトホルミンなどの他の経口抗糖尿病薬と組み合わせて使用することもできます。

スターリックスはどのように機能しますか?
スターリックスは初期のインスリン分泌を回復し、食後の血糖値(血中のブドウ糖の存在)と糖化ヘモグロビン(HbA1c)を減少させます。ナテグリニドはアミノ酸フェニルアラニンの誘導体であり、他の抗糖尿病薬とは化学的および薬理学的に異なります。 。
インスリン(膵臓と呼ばれる器官によって生成される)は、特に食後の血糖値を下げるのに役立つ物質です。 2 型糖尿病患者では、体がインスリンにうまく反応せず、食後すぐにインスリンの産生が開始されない可能性があります。スターリックスは膵臓を刺激してインスリンをより早く生成し、食後の血糖値を制御します。
インスリンレベルは 3 ~ 4 時間以内にベースラインに戻り、食後の高インスリン濃度が低下します。この高濃度は遅発性低血糖症 (低血糖) と関連しています。スターリックスは、食事前に経口的に素早く吸収されます。ナテグリニドの平均最大濃度は通常 1 時間未満で発生します。
ナテグリニドとその代謝物は迅速かつ完全に排泄され、そのほとんどは尿中に、10% は糞便中に排泄されます。
これらの薬だけでは血糖値をコントロールするのに十分でない場合、医師はスターリックスを他の経口抗糖尿病薬とともに処方します。糖尿病治療薬の使用を始めたばかりの場合でも、推奨された食事療法や運動を継続することが重要です。
医師はあなたが定期的にスターリックスをどのくらい服用しているかを確認することができます。彼はあなたのニーズに応じて投与量を調整できます。 Starlix について、またはこの薬が処方された理由についてご質問がある場合は、医師にお尋ねください。
スターリックスの禁忌
スターリックスを服用する前に、医師の指示に従ってください。このリーフレットに記載されている情報と異なる場合があります。
Starlix は使用しないでください。
- 上記の有効成分または配合成分に対してアレルギー(過敏症)がある場合。
- 1 型糖尿病 (インスリン依存性糖尿病、つまり、体がインスリンを生成しない) の場合。
- 授乳中の場合;
- 高血糖(非常に高い血糖および/または糖尿病性ケトアシドーシス – 高血糖の結果、体内でケトンと呼ばれる有毒な酸が高レベルで生成される場合)の症状(過度の喉の渇き、頻尿、脱力感、疲労など)がある場合は、吐き気、息切れ、混乱。
- 発汗、震え、不安、集中力の低下、衰弱、混乱、失神などの低血糖(低血糖)の症状がある場合。
これらのいずれかに該当する場合は、医師に相談し、Starlix を使用しないでください。アレルギーがあると思われる場合は、医師に相談してください。
この薬は小児による使用は禁忌です。
この薬は、医師または歯科外科医のアドバイスなしに妊娠中の女性が使用すべきではありません。
スターリックスの使い方
この説明書に記載されている指示と異なる場合でも、医師や薬剤師の指示には注意深く従ってください。推奨用量を超えないようにしてください。
スターリックスの投与量
スターリックスは、すぐに(1分)、または主な食事(朝食、昼食、夕食)の30分前までに服用する必要があります。
主な食事を抜く必要がある場合は、対応する用量のスターリックスを服用しないでください。
薬は水と一緒に服用する必要があります。

単剤療法(単独療法)
通常、食前に120mgを服用してください。
用量の調整は、グリコシル化ヘモグロビン (HbA1c) の定期的な測定に基づいて行う必要があります。 Starlix の主な治療効果は食後の血糖値を下げることであるため、Starlix に対する治療反応は食後 1 ~ 2 時間の血糖値で監視することもできます。
併用療法
スターリックスのみを使用していて追加の治療が必要な場合、医師は維持用量にメトホルミンを追加することがあります。
メトホルミンを単独で使用していて追加の治療が必要な場合、医師は食前に通常のスターリックス用量 120 mg を追加することがあります。
高齢の患者さん
高齢の患者には特別な用量調整は必要ありません。
肝不全患者
軽度から中等度の肝臓病の患者には用量調整は必要ありません。スターリックスは、重度の肝疾患のある患者には注意して使用する必要があります。
腎不全患者
腎不全患者では用量調整は必要ありません。
医師の推奨に従って、スターリックスを毎日主食の前に服用してください。医師の指示に従ってスターリックスの服用を続けてください。
スターリックスをどのくらいの期間服用すべきかについて質問がある場合は、医師または薬剤師に相談してください。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
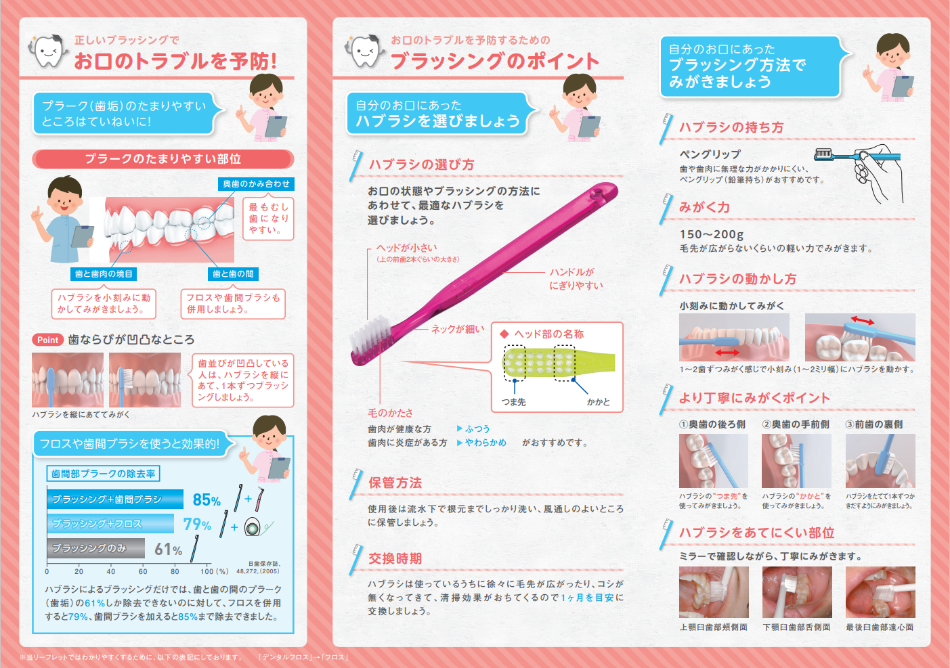
この薬は割ったり、開けたり、噛んだりしないでください。
Starlix の使用を忘れた場合はどうすればよいですか?
食事時にスターリックスを飲み忘れた場合は、次の食事時に 1 錠服用してください。飲み忘れた分を補うために倍量を服用してはいけません。
スターリックスの服用をやめたら
医師の指示がない限り、スターリックスの服用を中止しないでください。服用を中止すると、高血糖値は制御されなくなります。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
スターリックスの予防措置
Starlix については特に注意してください。
- 重度の肝臓疾患がある場合。
- 深刻な腎臓の問題がある場合。
- これらのいずれかに該当する場合は、Starlix を服用する前に医師に相談してください。
糖尿病患者は、低血糖(低血糖とも呼ばれます)に関連した症状を発症することがあります。
スターリックスなどの経口糖尿病薬も低血糖の症状を引き起こす可能性があります。一部の患者は、他の患者よりも抗糖尿病治療のこの効果に敏感です。これらには、通常より激しい運動をしている患者やアルコールを飲んでいる患者、高齢者や栄養失調の人、他の経口抗糖尿病薬を服用している患者、または低血糖を引き起こす可能性のある別の疾患(下垂体や副腎の活動低下など)を患っている患者が含まれます。
これらの症状のいずれかに該当する場合は、医師に相談してください。血糖値をより注意深く監視する必要があります。
発熱、外傷、感染症などの症状に苦しんでいる場合、または手術を受けなければならない場合、医師は一定の期間で抗糖尿病薬を変更することがあります。
Starlix の一部の成分に関する情報
Starlix 錠剤には乳糖 (牛乳に含まれる糖) が含まれています。重度の乳糖不耐症がある場合は、スターリックスを服用する前に医師に相談してください。
この薬には乳糖が含まれています。
スターリックスの副作用
すべての薬と同様、スターリックスを服用している患者は、他の人が経験していなくても、望ましくない反応を経験する可能性があります。
スターリックス治療中の副作用は通常、軽度から中等度です。

一般的な反応 (この薬を使用している患者の 1% ~ 10% で発生します)
低血糖(低血糖)の症状は通常は軽いです。
これらの症状には次のようなものがあります。
発汗、めまい、震え、脱力感、空腹感、動悸(顕著で速い心拍)、疲労感、吐き気。また、食事の不足や、服用している抗糖尿病薬の用量が多すぎることによって引き起こされることもあります。低血糖の症状が現れた場合は、砂糖を含むものを食べたり飲んだりする必要があります。
まれな反応(この薬を使用している患者の 0.01% ~ 0.1% で発生します)
- 肝機能検査の異常;
- 発疹、かゆみなどのアレルギー(過敏症)。
その他の望ましくない反応
頭痛、腹痛、胃腸障害、下痢。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。
また、顧客サービスを通じて会社に通知してください。
スターリックス特別集団
お年寄り
スターリックスは高齢の患者でも使用できます。
子供と青少年
小児におけるスターリックスの使用は研究されていないため、推奨されません。
妊娠
治療中に妊娠した場合は、できるだけ早く医師に相談してください。
妊娠している場合はスターリックスを服用しないでください。妊娠中にスターリックスを服用することによる潜在的なリスクについて医師があなたと話し合うでしょう。

妊娠中に薬を服用する前に、医師または薬剤師に相談してください。
授乳
スターリックスによる治療中は授乳しないでください。
薬を服用する前に医師または薬剤師に相談してください。
車両の運転および/または機械の操作能力への影響
運転するすべての糖尿病患者は低血糖に特に注意する必要があります。
これらの症状のいずれかが発生した場合は、車を運転したり機械を操作したりしないでください。
スターリックスの構成
プレゼンテーション
コーティング錠
120 mg のコーティング錠剤を 24 個、48 個、または 84 個パックします。
口頭で。
大人用。
構成
各コーティング錠には次のものが含まれます。
ナテグリニド120mg。

賦形剤:
乳糖一水和物、微結晶セルロース、ポビドン、クロスカルメロースナトリウム、ステアリン酸マグネシウム、黄色酸化第二鉄、ヒプロメロース、二酸化チタン、タルク、マクロゴール、二酸化ケイ素。
スターリックスの過剰摂取
誤って錠剤を多量に摂取した場合は医師に相談してください。低血糖の症状が現れた場合、たとえば、めまい、ふらつき、空腹感、神経質で震え、眠気、混乱、汗だくなどの症状がある場合は、砂糖を含むものを食べたり飲んだりする必要があります。
重度の低血糖症状 (発作、意識喪失) が起こりそうな場合は、救急医療機関に電話するか、誰かに代わってもらってください。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。
さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
スターリックスの薬物相互作用
食べ物や飲み物と一緒にスターリックスを摂取する
スターリックスは食前に服用してください。食中や食後に服用すると効果が遅れる可能性があります。
アルコールは血糖コントロールを乱す可能性がありますので、この問題については医師に相談することをお勧めします。
他の薬を服用している
処方箋なしで購入したものも含め、他の薬を服用している場合、または最近服用した場合は、医師または薬剤師に伝えてください。
他の薬がスターリックスの作用に影響を与える可能性があり、逆にスターリックスが他の薬の作用に影響を与える可能性があります。これにより、血糖値が上昇または低下する可能性があります。
以下の薬を服用している場合は、医師または薬剤師に伝えることが特に重要です。
- 抗炎症剤(例えば、筋肉痛や関節痛の治療に使用されます)。
- アスピリンなどのサリチル酸塩(鎮痛剤として使用)。
- モノアミンオキシダーゼ阻害剤(うつ病の治療に使用)。
- ベータ遮断薬(高血圧や心臓病の治療などに使用されます)。
- チアジド系薬剤(高血圧の治療に使用)。
- プレドニゾンやコルチゾンなどのコルチコステロイド(炎症性疾患の治療に使用されます)。
- 甲状腺薬(甲状腺ホルモン産生が低下している患者の治療に使用されます)。
- 交感神経興奮薬(喘息の治療などに使用されます)。
- スルフィネピラゾン(慢性痛風の治療に使用されます)。
- ゲムフィブロジル(高血中脂質レベルを下げるために使用されます)。
- フルコナゾール(真菌感染症の治療に使用されます)。
- アナボリック ホルモン (メタンドロステノロンなど、筋肉の成長を促進するために使用されます)。
- グアネチジン、ギムネマシルベスタ、チオクト酸、グルコマンナン、セントジョーンズワート(食品、栄養補助食品、または薬草)。
- ソマトロピン(成長ホルモン)。
- ソマトスタチン類似体(ランレオチド、オクトレオチドなど、カルチノイド症候群に関連するホルモンを阻害するために使用されます)。
- リファンピシン(結核の治療などに使用されます)。
- フェニトイン (発作の治療などに使用されます)。
- 医師はこれらの薬の投与量を調整する必要があるかもしれません。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしにこの薬を使用しないでください。健康に危険を及ぼす可能性があります。
物質スターリックスの作用
効果の結果
合計 3,566 人の患者が、ナテグリニド (活性物質) の安全性と有効性を評価するために、8 ~ 24 週間続く 9 つの二重盲検、プラセボ、または実薬対照研究に無作為に被験者されました。これらの患者のうち、3,118 人はベースラインを超える有効性値を示しました。これらの研究では、ナテグリニド(活性物質)が毎日 3 回の食事のそれぞれの最大 30 分前に投与されました。
ナテグリニド単剤療法(有効成分)とプラセボの比較
24 週間の無作為化二重盲検プラセボ対照研究で、HbA 1Cを有する 2 型糖尿病患者が対象となりました。食事療法のみで治療を受けた6.8%は、ナテグリニド(活性物質)(60mgまたは120mg、食前に1日3回)またはプラセボを投与される群に無作為に割り付けられた。
ベースライン HbA 1C は7.9% ~ 8.1% の範囲であり、77.8% の患者はこれまでに経口抗糖尿病療法による治療を受けていませんでした。以前に抗糖尿病薬で治療を受けていた患者には、無作為化前に少なくとも2か月間この薬の投与を中止するよう求めた。食前にナテグリニドを追加すると、プラセボと比較して、平均HbA 1Cおよび平均空腹時血漿グルコース(FPG)が統計的に有意に減少しました(表1を参照)。 HbA 1Cと FPG の減少は、これまでに抗糖尿病薬による治療を受けていない(未治療)患者と、以前にこれらの薬にさらされた患者でも同様でした。
この研究では、ナテグリニド(活性物質)120 mgを1日3回食前に投与された患者において、重度の低血糖症(血漿グルコース<36 mg/dL)のエピソードが報告されました。低血糖症に陥った患者で第三者の援助を必要とした患者はいなかった。
ナテグリニド (活性物質) で治療された患者は、プラセボと比較して平均体重が統計的に有意に増加しました (表 1 を参照)。
別の無作為二重盲検24週間実薬プラセボ対照研究では、2型糖尿病患者を無作為にナテグリニド(活性物質)(120mgを1日3回、食前)、メトホルミン500mg(3回)を投与する群に割り付けた。ナテグリニド(活性物質)120 mg(1日3回、食前)とメトホルミン500 mg(1日3回)の組み合わせ、またはプラセボ。ベースライン HbA1C は 8.3% ~ 8.4% の範囲でした。
患者の 57% (57%) はこれまでに経口抗糖尿病薬による治療を受けていませんでした。ナテグリニド単独療法は、プラセボと比較して平均HbA 1Cおよび平均FPGの有意な減少をもたらし、これは上記で報告された研究の結果と同様であった(表2を参照)。
表 1: ナテグリニド単剤療法 (活性物質)、確立された用量を用いた 24 週間の研究の最終結果
p値 = 0.004
ナテグリニド単剤療法(活性物質)と他の経口抗糖尿病薬との比較
グリブリド
24 週間の二重盲検実薬対照試験で、2 型糖尿病患者がスルホニル尿素で少なくとも 3 か月間コントロールされ、ベースライン HbA 1Cを有していた患者は誰でしたか? 6.5%は、ナテグリニド(活性物質)(食前に1日3回60mgまたは120mg)を投与されるか、または1日1回グリブリド10mgを投与されるように無作為に割り付けられた。ナテグリニド(活性物質)に無作為化された患者は、グリブリドに無作為化された患者と比較して、エンドポイントで平均HbA 1Cおよび平均FPGが有意に増加しました。
メトホルミン
別の24週間の無作為化二重盲検実薬およびプラセボ対照研究では、2型糖尿病患者が無作為にナテグリニド(活性物質)(120mgを食前に1日3回)、メトホルミン500mg(1日3回)を投与される群に割り付けられた。 、ナテグリニド(有効成分)120 mg(1日3回、食前)とメトホルミン500 mg(1日3回)の組み合わせ、またはプラセボ。ベースライン HbA 1C は8.3% ~ 8.4% の範囲でした。患者の 57% (57%) はこれまでに経口抗糖尿病療法による治療を受けていませんでした。メトホルミン単独療法によるエンドポイントでの平均HbA 1Cおよび平均FPGの減少は、ナテグリニド(活性物質)単独療法によるこれらの変数の減少よりも有意に大きかった(表2を参照)。プラセボとの関連で、ナテグリニド単独療法(活性物質)は平均体重の有意な増加と関連し、一方、メトホルミン単独療法は平均体重の有意な減少と関連した。
抗糖尿病治療を受けていない(ナイーブ)患者のサブセットでは、ナテグリニド単独療法の平均HbA 1Cおよび平均FPGの減少は、メトホルミン単独療法の場合と同様でした(表2を参照)。他の抗糖尿病薬、主にグリブリドで以前に治療を受けた患者のサブセットでは、ナテグリニド単独療法群の HbA 1Cはベースラインからわずかに増加しましたが、メトホルミン単独療法群では HbA 1Cが減少しました(表 2 を参照)。
ナテグリニド併用療法(有効成分)
メトホルミン
別の24週間の無作為化二重盲検実薬およびプラセボ対照研究では、2型糖尿病患者が無作為にナテグリニド(活性物質)(120mgを食前に1日3回)、メトホルミン500mg(1日3回)を投与される群に割り付けられた。 、ナテグリニド(有効成分)120 mg(1日3回、食前)とメトホルミン500 mg(1日3回)の組み合わせ、またはプラセボ。ベースライン HbA 1C は8.3% ~ 8.4% の範囲でした。患者の 57% (57%) はこれまでに経口抗糖尿病療法による治療を受けていませんでした。以前に抗糖尿病薬で治療を受けていた患者には、ランダム化の前に少なくとも2か月間薬を中止するよう求めた。ナテグリニド(活性物質)とメトホルミンの併用は、ナテグリニド(活性物質)単独療法またはメトホルミン単独療法と比較して、HbA 1Cおよび FPG の統計的に有意な大幅な減少をもたらしました(表 2 を参照)。
ナテグリニド(活性物質)は、単独またはメトホルミンと組み合わせて、プラセボおよびメトホルミン単独と比較して、食前から食後2時間までの食時血糖値の上昇を有意に減少させました。
この研究では、ナテグリニド(活性物質)とメトホルミンの併用療法を受けた患者で重度の低血糖症(血漿グルコース = 36 mg/dL)が 1 回報告され、メトホルミン治療群の 1 人の患者で重度の低血糖症が 4 回報告されました。低血糖症状を起こした患者で第三者の援助を必要とした患者はいなかった。
プラセボと比較して、ナテグリニド単独療法では体重の有意な増加が見られましたが、ナテグリニドとメトホルミンの併用療法では体重の有意な変化は観察されませんでした(表2を参照)。別の24週間の二重盲検プラセボ対照研究では、メトホルミンによる治療(=1ヶ月間毎日1500mg)後のHbA 1C = 6.8%の2型糖尿病患者に、まずメトホルミン単独療法を4週間受けさせた( 1日2000 mg)を投与し、メトホルミンに加えてナテグリニド(活性物質)(60 mgまたは120 mgを1日3回、食前)またはプラセボを投与する群に無作為に割り付けられました。ナテグリニド(活性物質)とメトホルミンの併用療法は、メトホルミン単独療法と比較して、統計的に有意なHbA 1Cのより大きな減少と関連していました(ナテグリニド(活性物質)60 mgおよびナテグリニド(活性物質)60 mgおよびナテグリニドでは-0.4%および-0.6%)それぞれ、(活性物質)60 mgおよびナテグリニド(活性物質)120 mgとメトホルミン)。
表 2: ナテグリニド単独療法とメトホルミン併用療法の 24 週間の研究の最終結果
p値? 0.05 vs.プラセボ。
b p値? 0.03 vs.メトホルミン。
cp値? 0.05 vs.組み合わせ。
※メトホルミンは1日3回投与します。
ロシグリタゾン
ロシグリタゾン 8 mg/日の単独療法では適切にコントロールできなかった 2 型糖尿病患者を対象に、24 週間の二重盲検多施設プラセボ対照研究が実施されました。ナテグリニドの追加(120 mgを1日3回、食事とともに)は、ロシグリタゾン単独療法と比較して統計的に有意なHbA 1Cの減少と関連していました。 24 週間ではその差は -0.77 でした。ベースラインと比較した主な体重変化は、ナテグリニド(活性物質)とロシグリタゾンで治療された患者では約 +3 kg であったのに対し、プラセボとロシグリタゾンで治療された患者では約 +1 kg でした。
グリブリド
グリブリド10mgを1日1回投与してもコントロールが不十分な2型糖尿病患者を対象とした12週間の研究では、ナテグリニドを追加(食前に60mgまたは120mgを1日3回)しても追加の効果は得られませんでした。
薬理学的特徴
薬物療法グループ:
その他の経口血糖降下薬。
ATCコード:
A10BX03。
薬力学
ナテグリニド (有効成分) はアミノ酸フェニルアラニンの誘導体であり、他の抗糖尿病薬とは化学的および薬理学的に異なります。ナテグリニド (活性物質) は初期のインスリン分泌を回復させ、食後血糖と HbA 1Cを減少させます。
早期のインスリン分泌は、正常な血糖コントロールを維持するために不可欠なメカニズムです。ナテグリニド (活性物質) は、食前に摂取すると、2 型糖尿病患者で失われたインスリン分泌の初期段階を再確立します。この作用は、インスリン K + ATPチャネルとの急速かつ一時的な相互作用によって媒介されます。膵臓のベータ細胞で。電気生理学的研究により、ナテグリニド (活性物質) は心血管 K + ATPチャネルと比較して膵臓ベータ細胞に対して 300 倍高い選択性を持っていることが実証されました。
他の経口抗糖尿病薬とは異なり、ナテグリニド (活性物質) は食後の最初の 15 分間に顕著なインスリン分泌を誘導します。これにより、食後の血糖値の上昇が軽減されます。インスリンレベルは 3 ~ 4 時間以内にベースラインに戻り、遅発性低血糖症と関連する食後の高インスリン血症が軽減されます。ナテグリニド(有効成分)はすぐに消失します。
ナテグリニド(活性物質)によって誘導される膵臓ベータ細胞によるインスリン分泌はグルコースに敏感であり、グルコースレベルが低下すると分泌されるインスリンは少なくなります。逆に、食物またはブドウ糖点滴の同時投与は、インスリン分泌の明らかな増加をもたらします。低グルコース濃度の環境では、ナテグリニド(活性物質)がインスリン分泌を刺激する可能性が低下するため、食事を抜いた場合などの低血糖に対する追加の保護が提供されます。
臨床研究では、ナテグリニド(活性物質)による単独療法治療により、HbA 1Cおよび食後血糖値によって測定される血糖コントロールが改善されました。主に空腹時血糖に影響を与えるメトホルミンとの併用では、物質の相補的な作用機序により、いずれかの薬剤単独と比較して、HbA 1Cに対する効果は相乗的でした。
インスリン抵抗性改善薬トログリタゾンとの併用研究では、ナテグリニドとトログリタゾンの併用治療を受けた患者において、ナテグリニド単独およびトログリタゾン単独と比較して、統計的に有意なHbA 1Cの改善が観察されました。
24週間の研究では、少なくとも3か月間、高用量のスルホニルウレア剤で安定しており、ナテグリニド(活性物質)の単独療法に直接切り替えた患者は、空腹時血糖値とHbAの増加によって証明されるように、血糖コントロールの低下を示しました。 1C 。
薬物動態
吸収
ナテグリニド (活性物質) は、食前にナテグリニド (活性物質) 錠剤を経口投与すると急速に吸収され、ナテグリニド (活性物質) の平均最大濃度は通常 1 時間未満で生じます。ナテグリニド (活性物質) は、経口溶液から急速かつほぼ完全に (= 90%) 吸収されます。絶対的な経口バイオアベイラビリティは 72% と推定されます。 2 型糖尿病患者に、ナテグリニド (活性物質) を毎日 3 食前に 60 ~ 240 mg の用量範囲で 1 週間投与したところ、ナテグリニド (活性物質) は AUC と C max .eot maxの両方で線形の薬物動態を示しました。 。用量非依存性であった。
分布
静脈内データに基づく定常状態でのナテグリニド (活性物質) の分布量は約 10 リットルと推定されます。 in vitro研究では、ナテグリニド (活性物質) が血清タンパク質、主に血清アルブミン、そして程度は低いですが、α-1 酸性糖タンパク質に広範囲 (97 ~ 99%) 結合していることが示されています。血清タンパク質への結合の程度は、0.1 ~ 10 mcg/mL ナテグリニド (活性物質) の試験範囲では薬物濃度に依存しません。
代謝
ナテグリニド (活性物質) は、混合機能オキシダーゼ システムによって広範囲に代謝されてから除去されます。ヒトで見られる主な代謝産物は、イソプロピル側鎖のメチル炭素またはメチル基の 1 つにおける水酸化によって生じます。主要な代謝産物の活性は、それぞれ、ナテグリニド (活性物質) の活性よりも約 5 ~ 6 倍、および 3 分の 1 です。同定された微量代謝物は、ナテグリニド(活性物質)のジオール、イソプロペンおよびアシルグルクロニドでした。微量代謝物のイソプロペンのみが活性を持ち、その活性はナテグリニド(活性物質)とほぼ同じ強力です。
インビトロおよびインビボ実験から入手可能なデータは、ナテグリニド(活性物質)が主にチトクロム P450 酵素 CYP 2C9 (70%) によって代謝され、程度は低いですが CYP 3A4 (30%) によって代謝されることを示しています。
排除
ナテグリニド(活性物質)とその代謝物は迅速かつ完全に除去されます。投与されたナテグリニド (活性物質) [ 14 C] の約 75% は、投与後 6 時間以内に尿中に回収されます。ナテグリニド (活性物質) [ 14 C] の大部分 (83%) は尿中に排泄され、さらに 10% が糞便中に排泄されます。
投与量の約 6 ~ 16% が未変化の薬物として尿中に排泄されました。血漿中濃度は急速に減少し、ボランティアおよび 2 型糖尿病患者を対象としたナテグリニド (活性物質) のすべての研究において、ナテグリニド (活性物質) の排出半減期は平均 1.5 時間であり、ナテグリニドの明らかな蓄積はありません。活性物質)を 1 日 3 回、最大 240 mg の複数回投与します。
特別な集団
高齢者患者(65歳以上の患者)
年齢はナテグリニド(活性物質)の薬物動態特性に影響を与えませんでした。
腎不全
糖尿病(1型)患者の中等度/重度腎不全における平均曝露[AUC (0-24)]、ピーク血漿濃度(C max )および見かけの体内クリアランス(クレアチニンクリアランス15-50 ml/分/1.73 m 2 ) 2) 健康な人と比較した。血液透析を受けている患者におけるナテグリニド(活性物質)の曝露には大きな変化はありませんでしたが、最大血漿濃度(C max )は 49% 減少しました。中等度/重度の腎不全患者におけるナテグリニド(活性物質)の曝露とクレアチニンクリアランス(CrCL)で測定した腎機能との間に相関関係は見出されませんでした。
肝不全
軽度/中等度の肝不全患者におけるナテグリニド(活性物質)の曝露は肝不全の程度と相関しなかったが、健常者と比較してAUC(0-24)の平均増加は30%、C max は37%でした。 。見かけのボディクリアランスは 8% 減少しました。これらの違いは統計的に有意ではありませんでした。ナテグリニド(有効成分)については、重度の肝機能障害のある患者では薬物動態が評価されていないため、これらの患者にはナテグリニド(有効成分)の使用は推奨されません。
食事の影響
食後に投与した場合、ナテグリニド(活性物質)の吸収の程度(AUC)は変化しません。しかしながら、C maxの減少および最大血漿濃度(t max )に達する時間の遅延によって特徴付けられる吸収速度の遅延が存在する。ナテグリニド(有効成分)は食前に投与することをお勧めします。通常は食事の1分前にすぐに服用しますが、食事の30分前までに服用することもできます。
セックス
ナテグリニド(活性物質)の薬物動態において、男性と女性の間で臨床的に有意な差は観察されませんでした。
前臨床安全性データ
前臨床データは、安全性薬理、反復投与毒性、遺伝毒性、発癌性、生殖能力への影響に関する従来の研究に基づくと、人体に対する特別な危険性を明らかにしていません。
変異原性
ナテグリニド(活性物質)は、インビトロエームス試験、ラットのリンパ腫含有量、チャイニーズハムスター肺細胞の染色体異常含有量、またはインビボラット小核アッセイにおいて、遺伝毒性を示さなかった。
発がん性
ナテグリニドを最大約400 mg/kg/日の用量でラットに104週間投与した場合、または最大900 mg/kg/日の用量でラットに投与した場合、腫瘍形成反応の証拠は観察されなかった[75]。
生殖毒性
「警告と予防措置 – 妊娠、授乳、生殖能力のある女性および男性」を参照してください。
生殖能力
生殖能力は、ラットにおけるナテグリニド (活性物質) の最大 600 mg/kg/日の投与によって影響を受けました。
スターリックス ストレージ ケア
スターリックスは室温 (15 ~ 30°C) で保管する必要があります。
バッチ番号と製造日および有効期限: パッケージを参照してください。
使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。
身体的特徴
黄色の楕円形の錠剤。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かないところに保管してください。
スターリックスのクールな名言
登録 MS – 1.0068.0153
農場。答え:
フラビア・レジーナ・ペゴラー
CRF-SP 18.150
輸入者:
ノバルティス バイオシエンシアス SA
教授ビセンテ・ラオ、90歳
サンパウロ – SP
CNPJ: 56.994.502/0001-30
ブラジルの産業。
製造元:
ノバルティス ファルマ SpA
トッレ アヌンツィアータ (NA)、イタリア。
梱包業者:
Anovis Industrial Farmacêutica Ltda.
タボアン・ダ・セラ、SP
医師の処方箋に基づいて販売します。

-ナテグリニド-120mg-錠-(ノバルティス社.jpg?resize=1200,779&ssl=1)






-1024x576.jpg?resize=1024,576&ssl=1)


