パラセタモール 500 mg + コデインリン酸塩 30 mg は、外傷(捻挫、脱臼、打撲、挫傷、骨折)、術後、抜歯後、神経痛、腰痛などに起因する中等度から重度の痛みの軽減に適応されます。痛み、関節痛、および同様の症状。

パラセタモール + コデインリン酸 – EMS はどのように機能しますか?
パラセタモール + リン酸コデインは、コデインとパラセタモールという 2 つの鎮痛薬の組み合わせで、軽度から重度の痛みを軽減します。
パラセタモール + コデインリン酸塩の禁忌 – EMS
パラセタモール、リン酸コデイン、または薬の他の成分に対してアレルギーがあることがわかっている場合は、パラセタモール + リン酸コデインを使用しないでください。
コデインは、12 歳未満の子供の痛みには禁忌です。
コデインは、扁桃摘出術やアデノイド切除術を受けた小児の術後疼痛の治療には禁忌です。
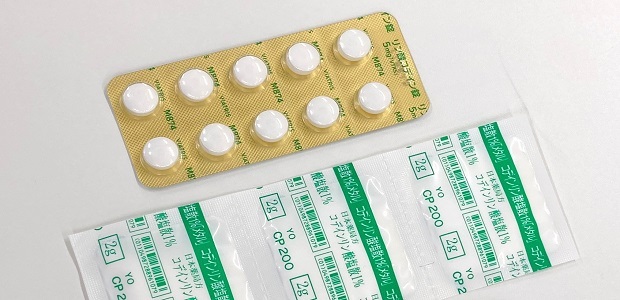
パラセタモール + リン酸コデインは、コデインを他の人よりも完全かつ迅速に活性代謝物に変換する CYP2D6 の超急速代謝者には禁忌です。これらの人は、極度の眠気、錯乱、浅い呼吸などの症状を含む過剰摂取/中毒の兆候を示す可能性があり、これは致命的となる可能性があります。
パラセタモール + コデインリン酸塩は母乳で育てられている母親には禁忌です。
パラセタモール + コデインリン酸塩の使い方 – EMS
投与量は、痛みの強さと患者の反応に応じて調整する必要があります。
一般に、痛みを伴うプロセスに応じて、次のことが推奨されます。
パラセタモール 500mg + コデインリン酸 7.5 mg = 4 時間ごとに 1 錠。
パラセタモール 500mg + コデインリン酸塩 30 mg = 4 時間ごとに 1 錠。
成人の場合、より激しい痛み(特定の術後処置、重度の外傷、新生物に起因する痛みなど)の場合は、パラセタモール 500 mg + コデインリン酸塩 7.5 mg の最大 8 錠を超えず、6 時間ごとに 2 錠が推奨されます。 24時間でパラセタモール500mg+リン酸コデイン30mg。
成人の1日最大投与量は次のとおりです。
リン酸コデイン:
24時間ごとに240mg。
パラセタモール:
24時間ごとに4000mg。
この薬は割ったり噛んだりしないでください。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
パラセタモール + コデインリン酸塩 – EMS の使用を忘れた場合はどうすればよいですか?
使用説明書に従い、1日の推奨用量を超えない限り、思い出したらすぐにこの薬の用量を服用できます。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
パラセタモール + リン酸コデインの予防措置 – EMS
コデイン
超急速コデイン代謝者における死亡のリスク
これらの人々は、他の人々よりも完全かつ迅速に、コデインをその活性代謝物であるモルヒネに変換します。この急速な変換により、モルヒネの血中濃度が予想よりも高くなります。推奨用量であっても、代謝が非常に速い人は、致死的または生命を脅かす呼吸抑制を経験したり、過剰摂取の兆候(極度の眠気、混乱、浅い呼吸など)を示したりする可能性があります。
この製品は短期間の使用のみを目的としています。医師の監督なしに継続的に服用しないでください。
コデインはオピオイド剤であり、誤用や乱用の危険性があります。
コデインの長期使用および/または高用量により、耐性、心理的および/または身体的依存が発生する可能性があります。
コデインは、発作性疾患、頭部損傷のある患者、および頭蓋内圧が上昇している状態の患者には注意して使用する必要があります。
コデインは、気管支喘息、肺水腫、閉塞性気道疾患、急性呼吸抑制、重度の肺疾患、肥満、閉塞性睡眠時無呼吸症候群、閉塞性腸疾患などの呼吸機能が低下している患者、および次のようなリスクのある患者には注意して使用する必要があります。麻痺性イレウス。セロトニン作動薬を服用している場合は、アセトアミノフェン + コデインリン酸塩を使用する前に医師または薬剤師に相談してください。セロトニン作動薬を服用しているかどうかわからない場合は、医師または薬剤師に相談してください。
腹痛や呼吸困難の最初の兆候が現れたら、治療を中止する必要があります。
アルコールと一緒に使用しないでください。ベンゾジアゼピンまたは他の鎮静剤を服用している場合は、使用前に医師または薬剤師に相談してください。オピオイドとベンゾジアゼピンまたはアルコールを含む他の中枢神経系 (CNS) 抑制剤を併用すると、重度の鎮静、呼吸抑制、昏睡、および死に至る可能性があります。
オピオイドは次の症状と関連していると考えられています。
- 副腎不全、潜在的に致命的な状態。副腎不全は、吐き気、嘔吐、食欲不振、疲労、脱力感、めまい、低血圧などの非特異的な症状や徴候を示すことがありますが、これらは1か月使用した後により頻繁に報告されています。これらの症状のいずれかが発生した場合は、医師の診察を受けてください。
- アンドロゲン欠乏症。性欲低下、インポテンス、勃起不全、無月経、不妊症などの非特異的な症状や徴候が現れることがあります。これらの症状のいずれかがある場合は、医師の診察を受けてください。
- セロトニン症候群。セロトニン作動薬の併用によって生じる、まれではあるが致死的な症状の可能性があります。症状が現れた場合は直ちに医師の診察を受けてください。セロトニン作動薬を服用している場合、または服用する予定がある場合は、医師に伝えてください。
パラセタモール
パラセタモールの過剰摂取に関する警告: 推奨用量を超えて投与すると (過剰摂取)、肝障害を引き起こす可能性があります。過剰摂取の場合は、直ちに医師の診察を受けてください。兆候や症状に気づいていない場合でも、子供だけでなく大人にとっても迅速な治療が重要です。
アルコール摂取に関する警告
慢性的なアルコール使用者は、アセトアミノフェン、その他の鎮痛剤、または解熱剤(成人向け製品)を服用する必要があるかどうか、医師に相談してください。
アセトアミノフェンを使用しているため、肝疾患のある方は使用前に医師に相談してください。
アセトアミノフェンの投与を受けている患者において、急性汎発性発疹性膿疱症、スティーブンス・ジョンソン症候群、中毒性表皮壊死融解症などの重篤な皮膚反応が非常にまれに報告されています。患者には重篤な皮膚反応の兆候について説明する必要があり、皮膚の発疹やその他の過敏症の兆候が最初に現れた時点で薬の使用を中止する必要があります。
パラセタモールを含む他の製品は使用しないでください。
症状が持続または悪化する場合、または新たな症状が現れた場合は、使用を中止し、医師にご相談ください。
賦形剤として亜硫酸塩を含む製品の場合
この製品には亜硫酸塩が含まれており、特定の感受性のある人々にアナフィラキシー症状や生命を脅かす、またはそれほど重度ではない喘息エピソードを含むアレルギー型反応を引き起こす可能性があります。一般集団における亜硫酸塩過敏症の全体的な有病率は不明ですが、おそらく低いと考えられます。亜硫酸塩過敏症は、喘息のない人よりも喘息の人に多く見られます。
車両の運転や機械の操作能力への影響
自動車の運転や機械の操作には注意してください。
パラセタモール + コデインリン酸塩の副作用 – EMS
臨床研究データ
臨床研究データに基づくコデインとアセトアミノフェンの安全性は、歯科手術、一般外科、または関節リウマチに続発する疼痛の治療における 27 件の無作為化、プラセボ対照、単回投与または複数回投与の臨床研究のデータに基づいています。
次の表には、複数の事象が報告され、その発生率がプラセボおよび?で発生した場合に発生した有害事象が含まれています。患者の1%。ダッシュは lt の発生率を表します。 1%。
によって報告された副作用27件のランダム化プラセボ対照臨床試験において、コデイン/アセトアミノフェンで治療を受けた被験者の1%:
|
システム・オルガンクラス(希望学期) |
コデイン/パラセタモールの単回投与量 30/300 mg ~ 1000 mg (N=337) % (頻度) |
コデイン/パラセタモールの単回投与量 60 mg/600-1000 mg (N=965) % (頻度) |
30-60mg/300-1000mg のコデイン/パラセタモール複数回投与 (N=249) % (頻度) |
プラセボ (N=1017) % |
|
胃腸障害 |
||||
|
便秘 |
– | – | 7.2(共通) | – |
|
口渇 |
– | 1.0(共通) | – | – |
|
吐き気 |
12.8 (非常に一般的) | 11.3 (非常に一般的) | 16.5 (非常に一般的) | 7.8 |
|
嘔吐 |
8.3(共通) | 8.2(共通) | 8.8(共通) | 4.6 |
|
神経系疾患 |
||||
|
めまい |
5.6(共通) | 4.7(共通) | 9.6(共通) | 2.6 |
|
眠気 |
3.6(共通) | 7.5(共通) | 10.8 (非常に一般的) | 2.8 |
|
一般的な疾患と投与部位の状態 |
||||
|
多汗症(過度の発汗) |
– | 1.0(共通) | – | – |
市販後データ
コデイン、アセトアミノフェンの市販後経験中に特定された副作用(ADR)は、自発報告率から次の表に含まれています。
周波数は次の規則に従って提供されます。
- 非常に一般的な ?1/10。
- 一般的な ?1/100 および lt;1/10;
- 珍しい ?1/1,000 および lt;1/100。
- レア ?1/10,000 および lt;1/1,000。
- 非常にまれな lt;1/10,000。
- 不明 (入手可能なデータから推定できない)。
コデイン、アセトアミノフェン、またはその組み合わせを使用した市販後経験中に特定された副作用(自発報告率から推定された頻度カテゴリー別):
|
システム/臓器クラス – 周波数カテゴリ |
優先用語ごとの有害事象 |
|
胃腸障害 |
|
|
非常に珍しい |
腹痛 |
| 消化不良(消化困難) | |
|
免疫系疾患 |
|
|
非常に珍しい |
アナフィラキシー反応 |
| 過敏症(アレルギー反応) | |
|
調査 |
|
|
非常に珍しい |
トランスアミナーゼ(細胞内酵素)の増加 † |
| 神経系疾患 | |
|
非常に珍しい |
頭痛 |
| 鎮静 | |
|
精神障害 |
|
|
非常に珍しい |
不安 |
| 依存 | |
| 薬物離脱症候群 | |
| 多幸感 | |
|
呼吸器、胸部、縦隔の疾患 |
|
|
非常に珍しい |
気管支けいれん(気管支の筋肉の収縮) |
|
呼吸困難(息切れ) |
|
|
呼吸抑制 |
|
|
血管障害 |
|
|
非常に珍しい |
紅潮(皮膚が赤くなる) |
|
皮膚および皮下組織の疾患 |
|
|
非常に珍しい |
血管皮症 |
|
皮膚炎 |
|
|
固定された発疹(皮膚の赤みがかったまたは茶色がかった斑点) |
|
|
そう痒症(かゆみ) |
|
|
発疹 |
|
|
そう痒性発疹 |
|
|
蕁麻疹 |
|
†推奨用量のアセトアミノフェンを受けている一部の患者では、低レベルのトランスアミナーゼ上昇が発生する可能性があります。これらの上昇は肝不全を伴わず、通常は治療の継続またはアセトアミノフェンの中止で解決しました。
コデインはオピオイド剤です。オピオイドは以下の症状と関連しています。
- 鎮静;
- めまい;
- 気管支けいれん;
- 消化不良、吐き気、嘔吐、便秘などの胃腸障害。
- 陶酔的な気分。
- 高用量を長期間使用すると薬物依存が発生する可能性があります。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。
また、顧客サービスを通じて会社に通知してください。
パラセタモール + コデインリン酸塩の特別集団 – EMS
コデイン
子供たち

コデインは、12 歳から 18 歳の青少年の痛みには推奨されません。
扁桃摘出術やアデノイド切除術後の術後期間にコデインを投与され、超急速コデイン代謝者であるという証拠があった小児では、呼吸抑制と死亡が発生しています。
閉塞性睡眠時無呼吸症候群で、扁桃摘出術やアデノイド切除術後の痛みに対してコデインの治療を受けた場合にコデインの超急速代謝を行う小児は、コデインの呼吸抑制作用に特に敏感である可能性があります。コデインは、CYP2D6 の超急速代謝者には禁忌です。
腎臓および肝臓の障害
腎臓および肝臓に障害のある患者は、パラセタモール + コデインリン酸塩を使用する前に医師に相談してください。この薬剤の使用は、混乱、浅い呼吸、致命的となる可能性のある極度の眠気などの症状を含む、コデイン毒性の最初の兆候が現れた時点で中止する必要があります。
妊娠
コデインは胎盤を通過します。子宮内でコデインに曝露された新生児は、出生後に禁断症状(新生児禁欲症候群)を発症する可能性があります。これに関連して脳梗塞も報告されています。
授乳
推奨用量では、コデインとその活性代謝物は非常に低濃度で母乳中に存在します。
コデイン代謝が正常(CYP2D6 活性が正常)の女性では、母乳中に分泌されるコデインの量は少なく、用量に依存します。産後の痛みを治療するためにコデインを含む製品が一般的に使用されているにもかかわらず、乳児における有害事象の報告はまれです。しかし、女性の中にはコデインの代謝が非常に速い人もいます。これらの女性は、コデインの活性代謝物であるモルヒネの血清レベルが予想よりも高く、母乳中のモルヒネのレベルが予想よりも高くなり、母乳で育てられた乳児にとって潜在的に危険な高い血清モルヒネレベルにつながります。母親がコデインの超急速代謝者であったため、母乳中の高濃度のモルヒネにさらされた乳児の死亡例が報告されています。したがって、母親によるコデインの使用は、授乳中の乳児に死亡を含む重篤な副作用を引き起こす可能性があります。コデインは授乳中の女性には禁忌です。
パラセタモール
妊娠と授乳
妊娠中または授乳中の女性を対象とした、コデインとパラセタモールの併用に関する適切でよく管理された臨床研究はありません。
コデインとパラセタモールの併用は、母親に対する治療の潜在的な利益が発育中の胎児に対する潜在的なリスクを上回る場合を除き、妊娠中に使用すべきではありません。コデインとパラセタモールの組み合わせは、授乳中の女性には禁忌です。
妊娠中または授乳中の女性を対象とした、パラセタモールに関する適切でよく管理された臨床研究はありません。
推奨用量で母親に投与すると、パラセタモールは胎盤を通過し、摂取後 30 分以内に胎児循環に到達し、胎児硫酸塩との結合によって効果的に代謝されます。
アセトアミノフェンは、指示どおりに服用すれば、妊娠中の母親や胎児に悪影響を及ぼしません。
パラセタモールは、低濃度 (母親の摂取量の 0.1% ~ 1.85%) で母乳中に排泄されます。
母親がパラセタモールを推奨用量で摂取しても、乳児にリスクはありません。
母親に対する治療の潜在的な利益が発育中の胎児に対する潜在的なリスクを上回る場合を除き、この製品は妊娠中に使用すべきではありません。妊娠中の方は使用前に医師にご相談ください。
この薬は、医師または歯科外科医のアドバイスなしに妊婦が使用しないでください。
パラセタモール + コデインリン酸塩の組成 – EMS
パラセタモール 500 mg + リン酸コデイン 7.5 mg の各錠剤の含有量
|
パラセタモール |
500,000mg |
|
リン酸コデイン |
7.5mg |
|
賦形剤* 適量 |
1錠 |
*微結晶セルロース、メタ重亜硫酸ナトリウム、ドキュセートナトリウム、二酸化ケイ素、黄色酸化鉄、ステアリン酸マグネシウム。
パラセタモール 500 mg + リン酸コデイン 30 mg の各錠剤の含有量
|
パラセタモール |
500,000mg |
|
リン酸コデイン |
30mg |
|
賦形剤* 適量 |
1錠 |
*微結晶セルロース、メタ重亜硫酸ナトリウム、ドキュセートナトリウム、二酸化ケイ素、ステアリン酸マグネシウム。
パラセタモール + コデインリン酸塩のプレゼンテーション – EMS
500 mg パラセタモール + 7.5 または 30 mg コデイン リン酸塩の錠剤。12、20、24、30、36、60、および 480 錠 (病院) のパックに入っています。
経口使用。
成人および12歳以上の小児が使用できます。
パラセタモール + コデインリン酸塩の過剰摂取 – EMS
コデイン

コデインの過剰摂取のリスクには、心肺停止、脳浮腫、昏睡、錯乱状態、低血圧、低酸素症、麻痺性イレウス、縮瞳、腎不全、呼吸抑制および呼吸不全、嗜眠および嘔吐が含まれます。
特に、幼児では過剰摂取後に興奮やけいれんが起こることがあります。
パラセタモール
肝胆道疾患
徐放性アセトアミノフェン含有製品が含まれる場合、または正確な製剤が不明な場合は、最初のアセトアミノフェン濃度の 4 ~ 6 時間後に追加の血漿アセトアミノフェン濃度を取得することが推奨されます。これは、これらの血漿アセトアミノフェン濃度は徐放性により上昇し続けるためです。アセトアミノフェン製品の放出が延長され、治療の決定が変更される可能性があります。
成人および青年(12 歳以上)の場合、8 時間以内に 7.5 ~ 10 グラムを超えて摂取すると肝毒性が発生する可能性があります。死亡例はまれで(未治療の症例の 3 ~ 4% 未満)、15 グラム未満の過剰摂取ではほとんど報告されていません。小児(12 歳未満)の場合、150 mg/kg 未満の急性過剰摂取は肝毒性と関連しませんでした。肝毒性の可能性のある過剰摂取後の初期症状には、食欲不振、吐き気、嘔吐、発汗、顔面蒼白、全身倦怠感などが含まれる場合があります。
肝臓毒性の臨床的および実験室的証拠は、摂取後 48 ~ 72 時間まで明らかでない可能性があります。
おそらく、パラセタモールの代謝方法の違いのため、幼児における急性パラセタモール過剰摂取後の重篤な毒性や死亡は極めてまれでした。
パラセタモールの過剰摂取に関連する以下の臨床事象は、過剰摂取で観察された場合に予期されるものと考えられており、これには劇症肝不全またはその後遺症による致死的事象が含まれます。
パラセタモールの過剰摂取で特定された副作用
代謝障害および栄養障害:
食欲の低下。
胃腸障害:
嘔吐、吐き気、腹部不快感。
肝胆道疾患:
肝壊死、急性肝不全、黄疸、肝腫大、肝臓の不快感。
一般的な疾患と投与部位の状態:
蒼白、多汗症、倦怠感。
調査:
血清ビリルビンの増加、肝酵素の増加、国際正規化比(INR)比の増加、プロトロンビン時間の延長、血清リン酸の増加、血清乳酸の増加
以下の臨床事象は急性肝不全の後遺症であり、死に至る可能性があります。これらの事象がパラセタモールの過剰摂取(成人および青少年 12 歳以上 8 時間で 7.5 g 以上、12 歳未満の小児 8 時間で 150 mg/kg 以上)に関連した急性肝不全の状況で発生した場合、それらは考慮されます。期待される。
パラセタモールの過剰摂取に関連する急性肝不全の予想される後遺症
感染症と蔓延:
敗血症、真菌感染症、細菌感染症。
血液およびリンパ系の障害:
播種性血管内凝固症候群、凝固障害、血小板減少症。
代謝障害および栄養障害:
低血糖症、低リン酸血症、代謝性アシドーシス、乳酸アシドーシス。
神経系疾患:

昏睡(大量のパラセタモール過剰摂取または複数の薬物の過剰摂取を伴う)、脳症、脳浮腫。
心臓疾患:
心筋症。
血管障害:
低血圧。
呼吸器、胸部、縦隔の疾患:
呼吸不全。
胃腸障害:
膵炎、胃腸出血。
腎臓および泌尿器疾患:
急性腎不全。
一般的な疾患と投与部位の状態:
多臓器不全。
血液およびリンパ系の疾患:
溶血性貧血(グルコース-6-リン酸デヒドロゲナーゼ[G6PD]欠損症患者):
パラセタモールの過剰摂取により、G6PD 欠損症患者で溶血が報告されています。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。
さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
パラセタモール + コデインリン酸塩の薬物相互作用 – EMS
中枢神経系抑制剤
中枢神経系(CNS)抑制剤(例、バルビツレート系、抱水クロラール、ベンゾジアゼピン系、フェノチアジン系、アルコール、中枢作用性筋弛緩剤など)との併用は、相加的なCNS抑制剤および呼吸抑制を引き起こす可能性があります。
オピオイド鎮痛薬
他のオピオイド受容体アゴニストと併用すると、相加的な CNS 抑制、呼吸抑制、および降圧効果を引き起こす可能性があります。
CYP2D6阻害剤
コデイン鎮痛は、脱メチル化によって触媒されて活性代謝物モルヒネを形成するシトクロム P450 アイソザイム CYP2D6 に依存すると考えられていますが、他のメカニズムも言及されています。
キニジン、メタドン、およびパロキセチン (CYP2D6 阻害剤) との相互作用が報告されており、血漿モルヒネ濃度の低下につながり、コデイン鎮痛を低下させる可能性があります。
セロトニン作動薬
オピオイドと、選択的セロトニン再取り込み阻害剤 (SSRI)、選択的セロトニンおよびノルエピネフリン再取り込み阻害剤 (SNRI)、三環系抗うつ薬 (TCA)、トリプタン、5 受容体拮抗薬 -HT3 などのセロトニン作動性神経伝達物質系に影響を与える他の薬剤との併用セロトニン神経伝達物質系に影響を与えるもの(ミルタザピン、トラゾドン、トラマドールなど)、およびモノアミンオキシダーゼ(MAO)阻害剤(精神疾患やその他の疾患の治療に使用されるリネゾリドや静脈内メチレンブルーなど)は、セロトニンを引き起こす可能性があります。
ワルファリン様化合物

ほとんどの患者にとって、アセトアミノフェンの時折の使用は通常、慢性ワルファリン治療を受けている患者の国際正規化比 (INR) にほとんど、またはまったく影響しません。しかし、パラセタモールがワルファリンや他のクマリン誘導体の抗凝固作用を増強する可能性については議論があります。この薬を使用する前に、血液をサラサラにする薬ワルファリンまたは他のクマリン誘導体を使用しているかどうかを医師または薬剤師に相談してください。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
パラセタモールを含む他の製品を使用しないでください。
パラセタモール + コデインリン酸塩という物質の作用 – EMS
有効性の結果
公開臨床研究では、鎮痛を必要とする急性の関節および筋骨格損傷を負ったアスリート50人に、パラセタモール500mgとコデイン30mgの組み合わせを1錠投与し、4時間目以降は4錠間隔で1~2錠服用することが許可された。時間、24時間まで。各施設あたり 78 人 (78%) の研究者が、治療効果を優れた (46%) および良好 (32%) と評価しました。最初の痛みと比較した場合、30 分後の平均痛みの軽減 (ビジュアル アナログ スケールで評価) は 54% (plt;0.001)、治療 24 時間目では 84% でした。患者の 88% (88%) が、パラセタモール 500mg + コデイン 30mg の組み合わせによる治療の忍容性を、優れている (72%) および良い (16%) と評価しました。 1
二重盲検無作為化研究では、歯科手術による痛みに苦しむ120人の患者を単回のパラセタモール1000mg、コデイン60mg、パラセタモール1000mg+コデイン60mg、またはプラセボで治療した。要因分析により、1000 mg のパラセタモール + 60 mg のコデインが、さまざまな有効性測定を通じて評価された有意な鎮痛効果 (plt;0.05) を促進することが実証されました。有害事象の発生率は、プラセボ治療を含む治療間で差がないようでした。 2
参考文献:
1.ラスマーNP。スポーツ選手の急性関節および筋骨格損傷:パラセタモールとコデインの関連による鎮痛。臨床薬理学。 1988年。 97(4):277-82。
2. ベントレー KC、ヘッド T。歯痛に対するアセトアミノフェン 1000mg とコデイン 60mg の添加鎮痛剤。臨床薬理学amp;治療薬。 1987年; 42(6): 634-40。
出典: Tylex Medication Professional の添付文書。
薬理学的特徴
薬力学特性
コデイン
コデインはオピオイド鎮痛剤および鎮咳剤です。コデインは、主にその活性代謝産物であるモルヒネを介してα-オピオイド受容体に作用する鎮痛薬であり、モルヒネはほぼもっぱらシトクロム P450 の遺伝的多型酵素 2D6 (CYP2D6) によって形成されます。コデインは、鎮痛、縮瞳、鎮静を媒介するβ受容体にも弱く結合します。
コデインの主な影響は中枢神経系 (CNS) にあります。コデインはアヘン剤アゴニストですが、アヘン剤受容体に対する親和性は低いです。コデインは、鎮痛、鎮咳、下痢止め作用があるという点でモルヒネに似ています。
パラセタモール
パラセタモールは、中枢作用性、非サリチル酸塩、非オピオイド鎮痛薬です。パラセタモールは臨床的に証明された鎮痛/解熱薬であり、視床下部の熱調節中枢への作用により疼痛閾値を上昇させることにより鎮痛と解熱をもたらすと考えられています。発熱している子供にパラセタモールを単回投与(12.5 mg/kg)した研究では、15 ~ 30 分以内に解熱が始まることが示されました。
薬物動態学的特性
吸収
コデイン
コデインは、錠剤や液体を経口投与した後、50 ~ 80% の生物学的利用能で迅速かつよく吸収されます。コデインは、経口投与後 0.17 ~ 1 時間後に血漿中ですぐに検出されるようになります。コデイン 30 mg および 60 mg の Tmax は 0.75 ~ 1 時間および 0.61 ~ 1.3 時間で発生し、 Cmaxはそれぞれ 61 ~ 3 89.1 ng/mL および 122.8 ~ 214.2 ng/mL でした。 30 mg および 60 mg のコデインの AUC は、216 ~ 354.6 ng·h/·mL および 417 ~ 734 ng·h/·mL です。コデインは食物の有無にかかわらず投与できます。
コデイン 30 mg とアセトアミノフェン 1000 mg を一緒に投与した場合、コデインとアセトアミノフェンの間の薬物動態学的相互作用は証明されていません。
パラセタモール
経口パラセタモールは、胃腸管、主に小腸から急速かつほぼ完全に吸収されます。吸収は受動的輸送によって起こります。経口吸収速度は主に胃内容排出速度に依存します。
相対的なバイオアベイラビリティは 85% から 99% まで変化します。通常、最大血漿濃度は経口投与後約 30 ~ 60 分で到達します。
成人の場合、最大血漿濃度は摂取後 1 時間以内に生じ、1000 mg の単回投与量で 14.8 ~ 17.6μg/mL の範囲になります。 6 時間ごとに 1000 mg を投与した後の定常状態での最大血漿濃度は 17.6 ~ 18.2μg/mL の範囲です。生後6か月から11歳までの発熱性小児59名を対象とした5つの企業スポンサーによる研究からプールされた薬物動態データは、51±39分で最大平均濃度12.08±3.92μg/mLが得られたことを示した。 12.5 mg/kg の用量後 (中央値、35 分)。
パラセタモールのピーク濃度は食物と一緒に投与すると遅れますが、吸収の程度には影響しません。パラセタモールは食事時間に関係なく投与できます。
分布
コデイン
コデインはすぐに組織に入り、腎臓、肺、肝臓、脾臓に集中します。コデインは 10% 未満のタンパク質結合であり、分布容積 (Vd) は 3 ~ 4 L/kg です。
パラセタモール
アセトアミノフェンは、脂肪を除くほとんどの身体組織に広く分布しているようです。見かけの分布量は、小児および成人で 0.7 ~ 1 L/kg です。比較的小さな割合 (10% ~ 25%) のパラセタモールが血漿タンパク質に結合します。
代謝
コデイン
コデインは肝臓での O- および N- 脱メチル化によって代謝されて、モルヒネ、ノルコデイン、およびノルモルヒネやヒドロコドンなどの他の代謝産物になります。約50%は腸と肝臓で全身性代謝前に代謝されます。
モルヒネ代謝は、遺伝的多型を示すシトクロム P450 アイソザイム CYP2D6 によって媒介されます。代謝における遺伝的差異により、人口のかなりの割合がコデインの代謝が不十分または急速に行われます。結果として、それらはオピオイド鎮痛効果や予測不可能な有害事象を引き起こします。民族性は CYP2D6 変動性の発生の要因です。 CYP2D6 の代謝が不良(PM)である患者は、この酵素が欠損しているか、完全に欠如しているため、十分な効果が得られません。白人の約 7 ~ 10%、中国人、日本人、ヒスパニックの 0.5 ~ 1%、アラブ人の 1%、アフリカ系アメリカ人の 3% は代謝が不良です。
超高速メタボライザーは、コデインをより迅速かつ完全にモルヒネに変換します。超急速代謝者(UM)では、低用量でもオピオイド毒性の副作用が発生するリスクが高くなります。オピオイド毒性の一般的な症状には、精神状態の低下、換気低下、縮瞳、蠕動低下などが含まれます。この CYP2D6 遺伝子型の存在率はさまざまですが、アジア人では 0.5 ~ 2% と推定されています。白人では1~10%。アフリカ系アメリカ人では3~6.5%。北アフリカ人、エチオピア人、アラブ人では 16 ~ 29% です。
パラセタモール
パラセタモールは主に肝臓で代謝され、次の 3 つの主要な経路が関与します。
グルクロニドとの結合。硫酸塩共役。そしてシトクロム P450 酵素経路を介した酸化。酸化経路は、グルタチオンとの結合によって解毒される反応性中間体を形成し、不活性なシステインおよびメルカプツール酸代謝物を形成します。 in vivo で関与する主要なチトクロム P450 アイソザイムは CYP2E1 であると思われますが、CYP1A2 および CYP3A4 はin vitroミクロソーム データに基づいてマイナーな経路と考えられています。その後、CYP1A2 と CYP3A4 の両方がin vivo で無視できるほど寄与していることが示されました。
成人では、パラセタモールの多くはグルクロン酸と結合し、程度は低いですが硫酸塩と結合します。グルクロニド、硫酸塩、およびグルタチオンに由来する代謝物には生物活性がありません。未熟児、新生児、幼児では、硫酸抱合体が優勢です。さまざまな重症度や病因の肝機能障害を持つ成人において、パラセタモールの生体内変換は健康な成人と同様であるが、若干遅いことがいくつかの代謝研究で実証されています。
健康な成人および肝臓障害のある成人では、1 日あたり 4 g の連続投与によりグルクロン酸抱合 (非毒性経路) が誘導され、その結果、時間の経過とともに総パラセタモール クリアランスが増加し、血漿蓄積が制限されることを強調することが重要です。
排除
コデイン
コデインとモルヒネなどのその活性代謝物は、主にグルクロン酸との抱合体として、ほぼ完全に腎臓から排泄されます。コデインを単独で投与する場合でも、パラセタモールと併用する場合でも、投与されたコデインの用量のうち、代謝されずに尿中に排泄されるのはわずか 3% ~ 16% です。 30 mg および 60 mg のコデインの T1/2 は、それぞれ 1.5 ~ 2.2 時間および 2.1 ~ 4.5 時間です。パラセタモールと一緒に投与されたコデインの場合、T1/2 はコデイン単独の場合と同様です。しかし、血液透析患者を対象とした研究では、平均T 1/2 が13 ± 3.3 時間であったのに対し、研究の健常者ではT 1/2 が4.5 ± 0.8 時間でした。腎障害のある患者は、薬物や代謝産物が蓄積する可能性があるため、慎重に投与および漸増する必要があります。
コデインの全身クリアランスは 252 mL/min と報告されています。パラセタモールと併用した場合のクリアランスは 291 mL/分です。肝障害のある患者に対する具体的な投与推奨はありませんが、薬物の蓄積を避けるために、より少ない用量と長い投与間隔を考慮する必要があります。
パラセタモール
パラセタモールの排出半減期は約 1 ~ 3.5 時間です。新生児や肝硬変患者では約 1 時間長くなります。パラセタモールは、グルクロニド(45~60%)および硫酸塩(25~35%)結合体、システインやメルカプチュレート代謝物などのチオール(5~10%)、およびカテコール(3~6%)として体から排出されます。








-1024x576.jpg?resize=1024,576&ssl=1)


