- 先天性無ガンマグロブリン血症および低ガンマグロブリン血症。
- 一般的な可変免疫不全症。
- 重度の複合免疫不全症とウィスコット・アルドリッチ症候群。
- 再発性感染症を伴う IgG サブクラス欠損症。
重度の続発性低ガンマグロブリン血症および再発性感染症を伴う骨髄腫または慢性リンパ性白血病の患者におけるヒト免疫グロブリン補充療法。
ハイゼントラはどのように機能しますか?
Hizentra には主に免疫グロブリン G (IgG) が含まれており、感染症を引き起こす病原体に対する幅広い抗体が含まれています。この薬を適切な用量で服用すると、IgG 抗体レベルを正常範囲に戻すことができます。
ハイゼントラの禁忌
Hizentra は、Hizentra の有効成分または処方中の賦形剤に対する重度の全身性過敏症 (アレルギー) またはアナフィラキシー反応 (急性アレルギー反応) の病歴のある患者には禁忌です。
非常にまれな病気である I 型および II 型高プロリン血症 (血液中の過剰なプロリン) がある場合は、この薬を使用しないでください。この病気を患っている家族は世界中でわずか数家族だけが知られています。
ハイゼントラの使い方
ハイゼントラは皮下点滴専用です。血管内に注入しないでください。
Hizentra は、注入ポンプを使用して毎週または隔週 (2 週間ごと) に皮下投与することを目的としています。ハイゼントラは、腹部、太もも、上腕、および/または腰の側面に注入する必要があります。
注射部位
Hizentra は 1 回分の投与で複数の注射部位に注入できます。
毎週の投与の場合、注入ごとに最大 4 部位が同時に使用されるか、最大 12 部位が連続して使用されます。医療専門家が必要と判断した場合は、2 週間ごとの投与ごとに注射部位の数を増やす必要があります。注射部位は少なくとも 2 センチメートル離す必要があります。現在の注射部位は毎週の投与ごとに変更する必要があります。
音量
Hizentra の最初の注入は、注射部位あたり 15 mL を超えてはなりません。 4 回目の注入後、体積は 1 部位あたり 20 mL に増加し、その後許容範囲に応じて 1 部位あたり 25 mL に増加します。
レート
Hizentra の最初の注入では、推奨される流量は 15 mL/時間/部位です。その後の注入では、許容範囲に応じて流量を 25 mL/時間/部位まで増やすことができます。
医療従事者は以下の手順に従い、無菌技術を使用して Hizentra を投与します。
物資を集める
Hizentra ボトル、使い捨て材料 (Hizentra には付属しません)、および点滴に必要なその他のアイテム (輸液ポンプ、鋭利物またはその他の容器、患者の治療日記/記録簿)。
表面の掃除
平らな表面はアルコール綿を使用して徹底的に清掃されます。
手を洗う
手をよく洗い、乾燥させます。ハイゼントラを調製および投与する際の手袋の使用は任意です。
ボトルのチェック
ハイゼントラの各ボトルは注意深く検査されます。液体が透明でない場合、粒子が含まれている場合、変色している場合、保護キャップが紛失している場合、またはラベルの使用期限が過ぎている場合、ボトルは使用できません。
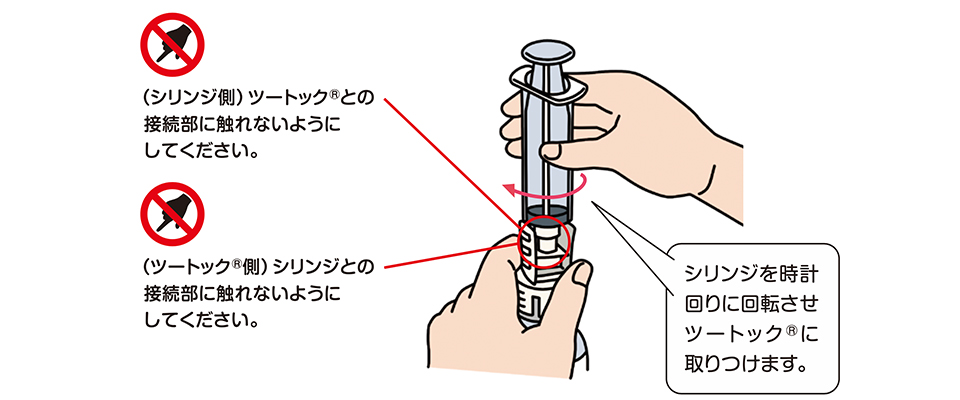
Hizentra をバイアルからシリンジに移す
- ボトルの保護キャップを外すと、ハイゼントラ ボトルのゴム栓の中央部分が露出します。
- コルクはアルコール綿で掃除し、乾燥させます。
- 転送デバイスを使用する場合は、デバイスの製造元が提供する指示に従う必要があります。
- Hizentra を移すために針と注射器を使用する場合は、以下の指示に従う必要があります。
- 滅菌移送針が滅菌注射器に取り付けられます。シリンジのプランジャーを引いて、シリンジ内の空気を抜き出す必要があります。この空気は、引き出されるハイゼントラの量と同じです。
- 移送針はボトルの栓の中心に挿入され、泡の形成を避けるために、空気をボトルの上部空間 (液体の中ではなく) に注入する必要があります。
- 必要な量の Hizentra を引き出す必要があります。
希望の用量を達成するために複数のバイアルを使用する場合は、この手順を繰り返す必要があります。
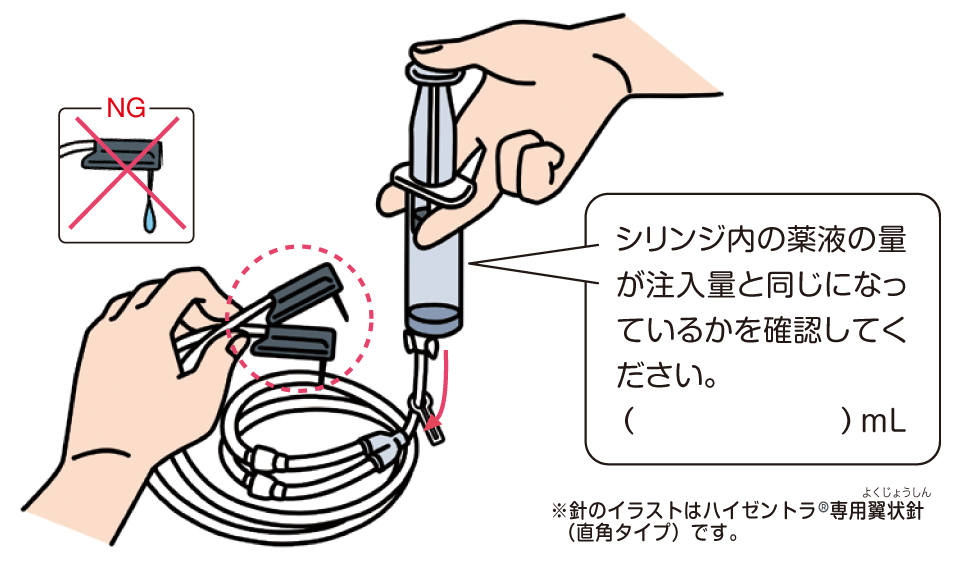
輸液ポンプとチューブの準備
製造業者の指示に従い、必要に応じて皮下投与セットおよびチューブを使用してポンプをプライミングする。医療従事者は、チューブ内に空気が入っていないことを確認するために、ハイゼントラを必ずチューブ内に入れます。
注射部位の準備
- 注射部位の数と位置は、総投与量によって異なります。 Hizentra は最大 4 か所に同時に注入されます。または最大 12 回の連続注入。注射部位は少なくとも 2 センチメートル離す必要があります。
- 皮膚用の消毒剤が使用され、各領域は中心から始めて円を描くように外側に向かって洗浄されます。先に進む前に、各スポットを乾燥させる必要があります。
針の挿入
- 皮膚を2本の指で挟み、針を皮下組織に挿入します。
- 必要に応じて、滅菌ガーゼとテープ、または透明な包帯を使用して針を所定の位置に保つことができます。
- 注入を開始する前に、準備した投与チューブの端に滅菌注射器を取り付け、血液がチューブに逆流しないようにプランジャーを引き戻す必要があります。
血液が付着した場合は、針とチューブを取り外して廃棄する必要があります。新しい針、新しい注入チューブ、および異なる注射部位を使用して、ステップ 6 (準備) から開始してこのプロセスを繰り返す必要があります。

点滴の開始
輸液ポンプをオンにするには、製造元の指示に従う必要があります。
治療の登録
使用した各ボトルのラベルを剥がし、患者の治療日誌/記録簿に貼り付ける必要があります。
クリーニング
投与終了後は、輸液ポンプを停止する必要があります。テープまたは包帯を取り除き、注入部位から針を取り外す必要があります。ポンプチューブが外れてしまいます。
未使用の製品およびすべての使用済みの使い捨て消耗品は、地域の要件に従って直ちに廃棄する必要があります。ポンプはメーカーの指示に従って洗浄および保管する必要があります。
非互換性
この薬は他の薬と混ぜてはいけません。
ハイゼントラの投与量
大人も子供も
以下の用法・用量は目安ですが、用量の決定(個別の場合もあります)は医師の責任となります。
皮下投与計画では、IgG 抗体の持続レベルを達成する必要があります。
少なくとも 0.2 ~ 0.5 g/kg 体重 (1.0 ~ 2.5 mL/kg) の初回投与量が必要な場合があり、数日に分けて投与する必要がある場合があります。安定した IgG レベルに達した後、月の累積投与量が体重 1kg あたり 0.4 ~ 0.8 g (2.0 ~ 4.0 mL/kg) 程度となるように、維持量を繰り返しの間隔で投与します。
静脈内治療から皮下治療に切り替える患者の場合、通常、毎月の用量を週ごとの用量に分割します。
血液中の抗体の量は、患者の臨床反応とともに測定する必要があります。臨床反応(感染率など)に応じて、トラフレベルを望ましいレベルまで上げるために、用量調整および/または投与間隔を考慮する必要があります。
子供と青少年
投与量は成人と同様に体重に相当します。ハイゼントラは、2~11歳の小児21名と12~16歳の青少年12名を対象とした2つの臨床研究で評価されました。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。医師の知識なしに治療を中止しないでください。
Hizentra の使用を忘れた場合はどうすればよいですか?
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
ハイゼントラの予防措置
ハイゼントラは皮下のみに使用し、血管内には投与しないでください。ハイゼントラを誤って血管(静脈または動脈)内に投与した場合、患者はショックを引き起こす可能性があります。
最初の数回の注入中は、医療専門家によって注意深く監視され、注入中または少なくとも注入後の最初の 20 分間に有害事象がないかチェックされます。
過敏症/アナフィラキシー
一部の副作用は、ヒト免疫グロブリンを初めて投与する患者、またはまれに患者がヒト免疫グロブリンによる治療を変更したとき、または治療が 8 週間以上中断された後により頻繁に発生することがあります。
真のアレルギー反応はまれです。
過敏症反応は、以前にヒト正常免疫グロブリンによる治療に耐えた患者でも発生する可能性があります。
特に、抗 IgA 抗体に対する既知のアレルギーを持つ患者では、重度の過敏症またはショックに至るアナフィラキシー反応が発生する可能性があります。抗 IgA 抗体を有し、皮下 IgG 製品による治療が唯一の治療選択肢である患者は、慎重な医師の監督下でのみ Hizentra を使用してください。
まれに、ヒト免疫グロブリンによる以前の治療に耐えていた患者であっても、ヒト免疫グロブリンはアナフィラキシー反応(急性アレルギー反応)を伴う血圧低下を引き起こすことがあります。
アレルギー症状(かゆみ、皮膚の発赤、息切れ、気分が悪くなるなど)に気づいた場合は、すぐに医師に伝えてください。彼はただちに注射を中止し、ショック状態に陥った場合にはこの場合の標準的な手順を実行する予定である。
医療専門家:
- 製品の最初の注射をゆっくりと注射することで、ヒト免疫グロブリンに対する感受性が低いことを確認します。
- 点滴中および薬の投与後少なくとも 20 分間は症状がないか観察します。ヒト免疫グロブリンの投与を受けたことがない場合、治療をハイゼントラの代替製品に置き換えた場合、または前回の投与から長期間が経過している場合は、特に最初の投与中と投与後の最初の 1 時間はモニタリングされます。最初の注入、有害事象の可能性のある兆候に備えて。
併発疾患
血栓塞栓症
動脈および静脈の血栓塞栓症イベントは、免疫グロブリンの使用に関連しています。
高齢、エストロゲンの使用、長期の血管カテーテルの使用、血管疾患や血栓エピソードの病歴、心臓血管の危険因子(アテローム性動脈硬化症の病歴や/遺伝性または後天性凝固亢進状態の患者、長期間の固定状態にある患者、重度の血液量減少患者、血液粘度を上昇させる疾患を患っている患者。患者は、息切れ、胸痛、手足の痛みや腫れ、局所的な神経障害などの血栓塞栓性イベントの初期症状について説明されるべきであり、症状が現れたら直ちに医師に連絡するようアドバイスされるべきです。 。 症状。患者は免疫グロブリンを使用する前に十分に水分補給する必要があります。
無菌性髄膜炎症候群 (SMA)
SMA は、静脈内または皮下の免疫グロブリンの使用によって報告されています。この症候群は通常、免疫グロブリン治療後数時間から 2 日以内に始まります。
SMA は次の徴候と症状によって特徴付けられます。
重度の頭痛、首のこわばり、眠気、発熱、羞明、吐き気、嘔吐。 SMA の兆候や症状を呈する患者は、髄膜炎の他の原因を除外するために、脳脊髄液検査を含む完全な神経学的検査を受ける必要があります。免疫グロブリン治療を中止すると、後遺症を残さずに数日以内に SMA が寛解する可能性があります。
ウイルスの安全性
人間の血液から調製された医薬品の使用による感染を防ぐために、次のようないくつかの対策が講じられています。感染マーカーについて寄付をスクリーニングする。ウイルスを不活化して除去するための製造ステップを含めること。
これらの対策にもかかわらず、ヒトの血液から調製された医薬品を投与する場合、感染性病原体が伝播する可能性を完全に排除することはできません。これは、未知または新興のウイルスやその他の病原体にも当てはまります。
ハイゼントラに関連したウイルス性疾患の伝播例は報告されていません。ハイゼントラによる感染伝播が疑われるすべての症例は、CSL ベーリング ファーマコビジランスに報告する必要があります。
これらの対策は、エイズウイルス、A型肝炎、B型肝炎、C型肝炎、パルボウイルスB19などのウイルスに対して効果的であると考えられています。
臨床経験では、免疫グロブリン (ハイゼントラクラスの薬剤) による A 型肝炎やパルボウイルス B19 感染の伝染は示されておらず、抗体含有量もウイルスの安全性に重要な貢献をしていると考えられています。
ハイゼントラを使用するたびに、薬の名前とバッチ番号を書き留めることをお勧めします。
受胎能力、妊娠、授乳
妊娠
妊婦に対するヒト免疫グロブリンの使用に関する前向き臨床試験のデータは限られています。したがって、ハイゼントラは妊娠中または授乳中の女性には注意して投与する必要があります。免疫グロブリンの臨床経験から、妊娠中や胎児や新生児への有害な影響は期待できないことが示唆されています。
新生児が適切な受動免疫を持って生まれるためには、妊婦の継続的な治療が重要です。
この薬は、医師または歯科外科医のアドバイスなしに妊娠中の女性が使用すべきではありません。
授乳期
免疫グロブリンは乳中に排泄され、新生児への防御抗体の伝達に寄与する可能性があります。
生殖能力
免疫グロブリンの臨床経験に基づいて、生殖能力に対する有害な影響は予想されないことが示唆されています。
車両の運転や機械の操作能力への影響

免疫グロブリンが機械の運転や操作の能力に影響を与えるという証拠はありません。
ハイゼントラの副作用
ヒト免疫グロブリンベースの薬剤に関連して、悪寒、頭痛、発熱、嘔吐、アレルギー反応、吐き気、関節痛、低血圧、中程度の背中の痛みなどの副作用が発生することがあります。
ヒト免疫グロブリンは、患者が以前の投与で過敏症(アレルギー)の兆候を示さなかった場合でも、まれに急激な血圧低下を引き起こし、場合によってはアナフィラキシーショック(急性アレルギー反応)を引き起こすことがあります。
注入部位では次の反応が起こる可能性があります。
腫れ、痛み、発赤、硬結、局所の熱感、そう痒症(かゆみ)、血腫、発疹。
臨床研究の経験
Hizentra を使用した以下の臨床研究から副作用が得られました。
健康な被験者(n = 28)を対象とした第 I 相試験が 1 件、原発性免疫不全患者(n = 100)を対象とした第 III 相試験が 2 件あります。
これら 3 つの臨床研究で報告された副作用は、以下に説明する MedDRA System Organ Class および頻度に従って要約および分類されています。
注入ごとの頻度は、次の基準を使用して分析されました。
- 非常に一般的です(この薬を使用している患者の 10% 以上で発生します)。
- 一般的(この薬を使用する患者の 1% から 10% の間で発生します)。
- まれです(この薬を使用している患者の 0.1% ~ 1% の間で発生します)。
- まれです (この薬を使用している患者の 0.01% ~ 0.1% で発生します)。
市販後の経験
Hizentra の市販後に以下の副作用が確認されています。
このリストには、Hizentra の臨床試験ですでに報告されている反応は含まれていません。
皮下免疫グロブリンのクラスに関連する副作用
注入部位反応以外は不明。
小児人口
Hizentra の臨床試験では、成人患者と小児患者において同様の全体的な安全性プロファイルが示されています。
高齢者人口
臨床試験から得られる情報は限られていますが、65 歳以上の患者とそれより若い患者では安全性プロファイルに違いはありません。
65 歳以上の患者に対する Hizentra の市販後の経験では、この年齢層と若い患者でも同様の安全性プロファイルが示されています。
注意:この製品は国内で新たな投与経路および新たな濃度が設定された医薬品であり、研究により許容できる有効性と安全性が示されていますが、たとえ正しく適応され使用されたとしても、予測できないまたは未知の有害事象が発生する可能性があります。この場合は医師に知らせてください。
ハイゼントラの構成
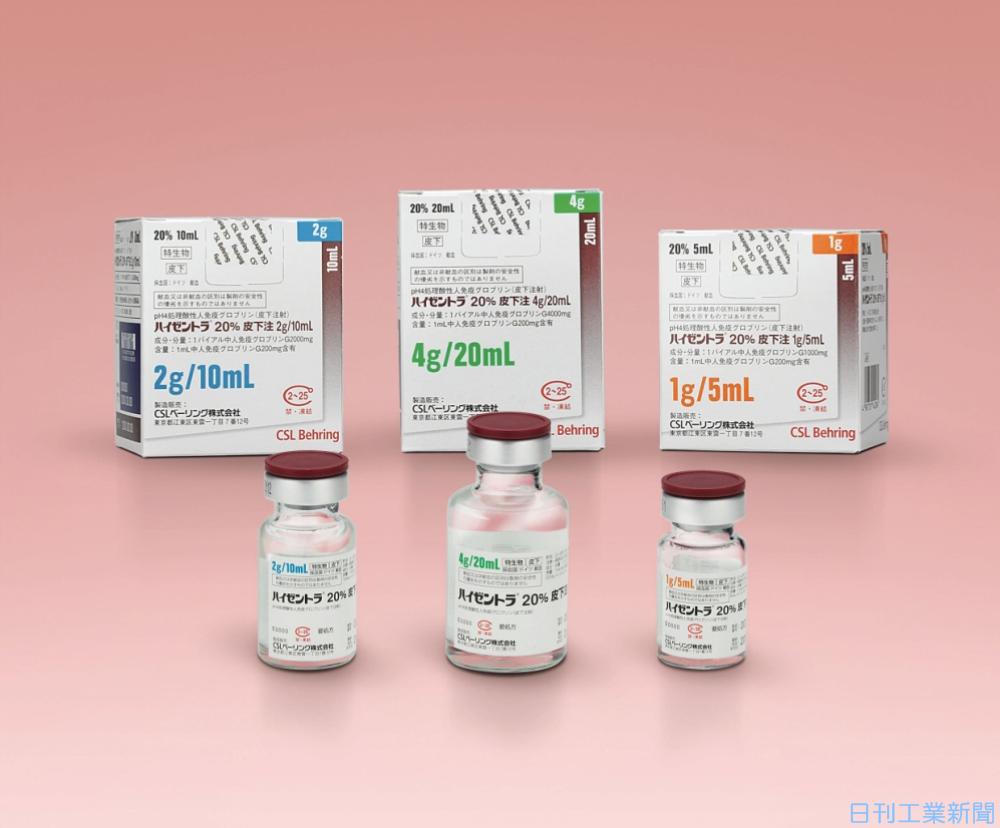
プレゼンテーション
ハイゼントラ 1g:
注入用の注射液 5 mL が入ったバイアル 1 個が入ったパッケージ。
ハイゼントラ 2g:
注入用の注射液 10 mL が入ったバイアル 1 個が入ったパッケージ。
ハイゼントラ 4g:
注入用の注射用溶液 20 mL が入ったバイアル 1 個が入ったパッケージ。
溶液の濃度は 200 mg/mL です。
皮下ルート。
小児および成人向け。
構成
ハイゼントラ 1 mL には次のものが含まれます。
ヒト免疫グロブリン 200 mg (少なくとも 98% IgG を含むヒト血漿タンパク質)。
賦形剤:
プロリン、ポリソルベート 80、注射用水。
IgG サブクラスのおおよその割合は次のとおりです。
IgG1 68%、IgG2 27%、IgG3 3%、IgG4 2%。
最大 IgA 含有量は 50 mg/L です。
製品の浸透圧は約 380 mOsmol/kg です。
ハイゼントラは基本的にナトリウムを含みません。
ハイゼントラの過剰摂取
過剰摂取の影響は不明です。過剰摂取の場合は、薬の副作用の発生を注意深く監視し、必要に応じて支援策を提供する必要があります。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
ハイゼントラの薬物相互作用
弱毒生ウイルスワクチン
免疫グロブリンの投与は、麻疹、風疹、おたふく風邪、水痘などの弱毒生ウイルスで作られたワクチンの効果を 6 週間から 3 か月間低下させる可能性があります。ハイゼントラを使用した後は、弱毒化生ウイルスワクチンの接種まで 3 か月の間隔をあけてください。麻疹の場合、効果の低下は最長 1 年間続く場合があります。したがって、麻疹のワクチン接種を受けている場合、医師は抗体レベルを検査します。
血清学的検査
免疫グロブリン注射後、ハイゼントラ点滴後に受け取った抗体により、一部の検査では偽陽性が示される場合があります。血液型に対する抗体の移入は、関連する検査 (クームス テスト、網赤血球数、ハプトグロビンなど) に干渉する可能性があります。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしにこの薬を使用しないでください。健康に危険を及ぼす可能性があります。
ハイゼントラ物質の作用
有効性と安全性の結果

前臨床研究
ヒト免疫グロブリン (活性物質) の安全性は、いくつかの前臨床研究で調査されています。賦形剤プロリンの調査に特に重点が置かれました。プロリンは生理学的非必須アミノ酸です。体重1kg当たり1450mgのプロリンを毎日投与して治療したラットで行われた研究では、催奇形性や胎児毒性の証拠は示されませんでした。プロリンの遺伝毒性研究では、病理学的所見は示されませんでした。
高プロリン血症に関する発表された研究では、1日高用量の長期使用が非常に若いラットの脳の発達に影響を与えることが示されています。しかし、ヒト免疫グロブリン(活性物質)の臨床使用を反映して用量が計画された研究では、胎児の脳の発達に対する影響は観察されませんでした。成体および幼若ラットにおけるプロリンの追加の安全性薬理学的研究では、行動障害の証拠は見つかりませんでした。
免疫グロブリンは人体の天然成分です。動物実験、免疫グロブリンの急性および慢性毒性、および胚胎児毒性からのデータは、異種種の免疫グロブリン間の相互作用および異種タンパク質に対する抗体の誘導のため、決定的なものではありません。ヒト免疫グロブリン (活性物質) を静脈内、傍静脈、動脈内および皮下に投与したウサギで行われた局所忍容性研究では、この製品は良好な忍容性を示しました。
臨床研究
ヒト免疫グロブリン(活性物質)の安全性と有効性は、ヨーロッパ(PTI および PDIC 研究)およびヨーロッパと米国(IDP 研究)で実施された 5 件の前向き、非盲検、単群、多施設研究で調査されました。追加の安全性および有効性データは、米国で実施された前向き、非盲検、単群、多施設拡張研究(IDP 拡張研究)で収集されました。
主な研究では、原発性免疫不全症(PID)を患う3~69歳の患者80人に、中央値200~888 mg/体重kgでヒト免疫グロブリン(活性物質)を3~4週間ごとに点滴投与した。最長1年間。この処理により、処理期間を通じて一定の最小 IgG 濃度が達成され、平均濃度は 8.84 g/L ~ 10.27 g/L でした。重篤な急性細菌感染症の発生率は、患者あたり年間 0.08 人でした (97.5% の上限信頼限界は 0.182 でした)。
IDP研究の延長研究では、主研究と同様に、ヒト免疫グロブリン(活性物質)の用量が55人の患者に投与された(そのうち45人が主研究に参加しており、10人が新規患者であった)。主な研究の結果は、平均 IgG トラフ濃度 (9.31g/L ~ 11.15g/L) および急性細菌感染率 (0.018/患者/年、上限 97.5% 信頼水準) についての延長研究によって確認されました。は0.098でした)。
2番目の研究には、慢性免疫性血小板減少性紫斑病(ITP)を患う15~69歳の患者57人が参加した。ベースラインでの血小板数は 20 x 109/L でした。ヒト免疫グロブリン(活性物質)を体重 1 kg あたり 1 g の用量で 2 日連続投与したところ、80.7 % の患者で、最初の注入から 7 日以内に血小板数が少なくとも 50 x 109/L まで上昇しました。患者の 43% で、この増加は 2 回目の注入前のわずか 1 日後に発生しました。この血小板数に達するまでの平均時間は 2.5 日でした。治療に反応した患者では、血小板数は変化しませんでした。 50×109/L、平均期間15.4日。
PRIMA (Privigen Impact on Mobility and Autonomy Study) と呼ばれるオープン多施設研究では、CIDP 患者 (静脈内免疫グロブリン前治療の有無にかかわらず) が、初回用量 2 g/kg 体重で 2 ~ 5 日間投与され、その後、 1 g/kg 体重の維持用量を 3 週間ごとに 1 ~ 2 日間かけて 6 回投与します。以前に治療を受けた患者は、INCAT(炎症性神経障害の原因と治療)表に基づいて臨床症状の悪化が確認されるまで、ヒト免疫グロブリン(活性物質)による治療を開始する前に免疫グロブリンの静脈内投与を受けました。 10ポイントに調整されたINCATスケールでは、ベースラインから治療25週目までに少なくとも1ポイントの改善が17/28患者で観察された(60.7%、95%信頼区間42.41、76.4)。治療のための初回導入用量の投与後に9人の患者が反応し、10週目には16人の患者が反応した。
薬理的特性
ヒト免疫グロブリン(活性物質)には、静脈内投与用のヒト免疫グロブリン(活性物質)が含まれています。
薬力学特性
ヒト免疫グロブリン (活性物質) の製造プロセスには、次のステップが含まれます: エタノール中で血漿から IgG 画分を沈殿させ、続いてオクタン酸中で分画し、pH 4 でインキュベートします。
次の精製プロセスには、濾過、クロマトグラフィー、および最大 20 ナノメートルの粒子を除去できる濾過ステップが含まれます。
ヒト免疫グロブリン (活性物質) には、主に免疫グロブリン G (IgG) が含まれており、感染性病原体に対する機能的に無傷な広範囲の抗体が含まれています。 IgG 分子の Fc 機能と Fab 機能は両方とも保存されます。 Fab 部分が抗原に結合する能力は、生化学的および生物学的方法によって実証されています。 Fc機能は、補体活性化およびFc受容体媒介白血球活性化を用いて試験された。免疫複合体によって誘発される補体活性化の阻害(「除去」、静脈内免疫グロブリンの抗炎症機能)は、ヒト免疫グロブリン(活性物質)に保存されています。
ヒト免疫グロブリン (活性物質) は、補体やプレカリクレイン系の非特異的活性化を引き起こしません。
ヒト免疫グロブリン (活性物質) には、平均的な集団に存在するすべての免疫グロブリン G 抗体が含まれています。少なくとも1000人のドナーの血漿から製造される。 IgG サブクラスの分布は、天然ヒト血漿の分布にほぼ対応します。適切な用量のヒト免疫グロブリン (活性物質) を投与すると、低い IgG レベルを正常に戻すことができます。
補充療法以外の適応における作用機序はまだ完全には解明されていませんが、免疫調節効果が含まれています。
薬物動態学的特性
静脈内投与後、すべての正常なヒト免疫グロブリン (活性物質) は、患者の血流中で即座かつ完全に生体利用可能になります。これは、血漿と血管外液との間に比較的迅速に分配される。血管内区画と血管外区画の間の平衡は、約 3 ~ 5 日後に達成されます。
ヒト免疫グロブリン (活性物質) の薬物動態パラメータは、原発性免疫不全疾患の患者を対象に実施された臨床研究で決定されました。主な研究では25人の患者(13歳から69歳)、この研究の延長研究では13人の患者(9歳から59歳)が薬物動態調査に参加した(下表を参照)。
主要研究における原発性免疫不全疾患患者の半減期は 36.6 日、延長研究では 31.1 日でした。この半減期は患者ごとに異なる場合があります。
原発性免疫不全疾患患者におけるヒト免疫グロブリン(活性物質)の薬物動態パラメータ:
|
パラメータ |
主な研究 (n=25) 中央値 (範囲) |
延長研究 (n=13) 中央値 (範囲) |
|
C max (最大濃度) |
23.4 g/L (10.4 – 34.6) | 26.3 (20.9-32.9) |
|
C min (最低濃度) |
10.2g/L(5.8~14.7) | 9.75 (5.72-18.01) |
| t1/2 (半減期) | 36.6 日 (20.6 – 96.6) | 31.1 (14.6-43.6) |
IgG および IgG 複合体は細網内皮系の細胞で分解されます。
ハイゼントラ ストレージ ケア
ハイゼントラは 25 °C 以下の温度で保管する必要があります。凍らせないでください。光から守ります。
賞味期限は製造日より30ヶ月です。
バッチ番号と製造日および有効期限: パッケージを参照してください。

使用期限を過ぎた医薬品は使用しないでください。元のパッケージに入れて保管してください。
開封後は、内容物を直ちに使用する必要があります。
Hizentra は 1 回のみの使用を目的としています。
ハイゼントラは、溶液には防腐剤が含まれていないため、バイアルを開けたらすぐに投与する必要があります。
薬の特徴
ハイゼントラは、半透明の淡黄色から淡褐色の溶液です。溶液が濁っていたり、粒子状物質が含まれている場合は製品を使用しないでください。未使用の製品または廃棄物は、地域の要件に従って処分する必要があります。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かないところに保管してください。
ハイゼントラの法律上の格言
登録 MS 1.0151.0126
農場。答え:
クリスティーナ・J・ナカイ
CRF-SP: 14,848
製造元:
CSL ベーリング AG
ベルン – スイス
輸入者:
CSL Behring Comércio de Produtos Farmacêuticos Ltda.
オリンピコス通り、134 – 9階
CEP: 04551-000 – サンパウロ – SP
CNPJ: 62.969.589/0001-98
[メールで保護されています]
医師の処方箋に基づいて販売します。
使用は病院に限定されます。


.jpg?ssl=1)







