レビトラはどのように作用するのでしょうか?
レビトラ® は、1 日 1 回、性行為の約 25 ~ 60 分前に服用してください。効果が現れるまでの時間は個人差がありますが、通常は投与後10~60分程度で現れます。実施された臨床研究では、バルデナフィルは性交の 4 ~ 5 時間前に投与すると効果的でした。ただし、治療に対する反応が得られるためには性的刺激が必要です。

レビトラの禁忌
この薬は次の場合には禁忌です。
- レビトラ®のいずれかの成分に対して既知のアレルギー(過敏症)がある患者。アレルギー反応の兆候には、発疹、かゆみ、顔や唇の腫れ、息切れ(息切れ)などが含まれる場合があります。
- 硝酸塩または一酸化窒素供与物質(硝酸プロパチル、ニトログリセリン、イソソルビドなど)を含む狭心症の薬剤による併用治療を受けている患者向け。これらの薬をレビトラ®と併用すると、血圧に重大な影響を与える可能性があります。
- リオシグアトの投与を受けており、肺動脈性肺高血圧症と呼ばれる疾患と診断されている患者。
- インジナビルまたはリトナビルなどでエイズの治療を受けている患者向け。
専用の口腔内治療可能なタブレット
- エリスロマイシン、クラリスロマイシン、その他のマクロライド系抗生物質による治療を受けている患者。
- ケトコナゾールまたはイトラコナゾール、抗真菌薬による治療を受けている患者。
レビトラの使い方
経口使用。
コーティング錠
レビトラ®コーティング錠は、食事と一緒に摂取しても、食事と一緒に摂取しなくても問題ありません。
口腔内崩壊錠
Levitra ® 10 mg 口腔内崩壊錠は、溶けるまで舌の上に置く必要があります。口腔内分散性錠剤は、水疱から錠剤を取り出した直後に、口の中に液体を入れずに使用する必要があります。
Levitra ® 10 mg 口腔内崩壊錠は、食後または空腹時に使用できます。
レビトラの投与量
用量レジメン
推奨される開始用量は、レビトラ® 10 mg フィルムコーティング錠 1 錠で、必要に応じて性行為の約 25 ~ 60 分前に投与されます。
コーティング錠
有効性と忍容性に応じて、用量はレビトラ® 20 mg フィルムコーティング錠 1 錠に増量されるか、レビトラ® 5 mg フィルムコーティング錠 1 錠に減量される場合があります。
推奨される 1 日の最大用量は、レビトラ® 20 mg フィルムコーティング錠 1 錠です。
推奨される最大投与頻度は 1 日 1 回です。
臨床研究では、レビトラ® は性行為の 4 ~ 5 時間前に投与すると効果があることが示されています。
治療に対する自然な反応を得るには性的刺激が必要です。
レビトラ® は口腔内分散錠の形でも入手できますが、レビトラ® (塩酸バルデナフィル) 口腔内分散錠とレビトラ® (塩酸バルデナフィル) コーティング錠には互換性がありません。
この薬は割ったり、開けたり、噛んだりしないでください。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
口腔内崩壊錠
推奨される開始用量は、レビトラ® 10 mg 口腔内崩壊錠 1 錠で、必要に応じて性行為の約 25 ~ 60 分前に投与されます。
推奨される 1 日の最大用量は、レビトラ® 10 mg 口腔内崩壊錠 1 錠です。
推奨される最大投与頻度は 1 日 1 回です。臨床研究では、レビトラ® は性行為の 4 ~ 5 時間前に投与すると効果があることが示されています。
治療に対する自然な反応を得るには性的刺激が必要です。
レビトラ® はコーティング錠の形でも入手できますが、レビトラ® (塩酸バルデナフィル) 口腔内分散錠とレビトラ® (塩酸バルデナフィル) コーティング錠には互換性がありません。
この薬は割ったり、開けたり、噛んだりしないでください。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
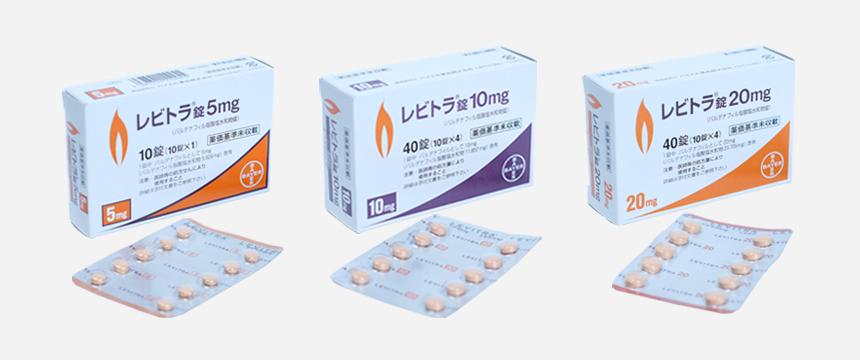
特殊な患者集団に関する追加情報
子供および青少年(18歳未満)
レビトラ® は小児への使用には適応されていません。
高齢の患者さん
高齢の患者には用量調整は必要ありません。
肝不全患者
軽度の肝障害のある患者では用量調整は必要ありません, Child-Pugh A.
独自のコーティング錠剤:
中等度の肝不全、チャイルド・ピューB の患者では、バルデナフィルの排出が減少します。したがって、初回用量のレビトラ® 5 mg コーティング錠 1 錠を使用することをお勧めしますが、後で医師がレビトラ® 10 mg コーティング錠 1 錠の最大用量まで増量することができます。
独自の口腔内崩壊性錠剤:
中等度の肝不全(チャイルド・ピューB)または重度の肝不全(チャイルド・ピューC)の患者は、レビトラ® 10 mg 口腔内崩壊錠を使用すべきではありません。
腎不全患者
軽度、中等度、または重度の腎障害のある患者では、用量を調整する必要はありません。
バルデナフィルの薬物動態は、透析を受けている患者では研究されていません。
性別
レビトラ® は女性への使用には適応されていません。
併用薬
コーティング錠:
α遮断薬とバルデナフィルには血管を拡張する作用があるため、併用すると血圧低下の症状が生じる場合があります。併用治療は、安定したα遮断薬治療を受けている場合にのみ開始してください。タムスロシンまたはアルフゾシンとともに、バルデナフィルはいつでも投与できます。バルデナフィルがテラゾシンおよび他のアルファブロッカーと同時に処方される場合、投与間の適切な間隔を考慮する必要があります。最適化された用量のレビトラ®コーティング錠剤による治療を既に行っている場合は、アルファ遮断薬療法を最小用量で開始する必要があります。アルファブロッカーの用量を徐々に増やすと、血圧がさらに低下する可能性があります。
いわゆる CYP3A4 阻害剤 (ケトコナゾール、イトラコナゾール、エリスロマイシン、クラリスロマイシン、リトナビル、インジナビルなど) を服用している場合は、レビトラ®の用量を調整する必要がある場合があります。
抗生物質エリスロマイシンまたはクラリスロマイシンの場合、レビトラ® 5 mg のコーティング錠 1 錠の最大用量を超えてはなりません。
ケトコナゾールまたはイトラコナゾール(抗真菌薬)と組み合わせて使用する場合、レビトラ® 5 mg のコーティング錠 1 錠の最大用量を超えてはならず、後者の用量は 200 mg を超えてはなりません。
HIV感染症の治療に使用されるインジナビルやリトナビルとの併用は禁忌です。
口腔内分散性錠剤:
Levitra ® 10 mg 口腔内崩壊錠は、中等度または強力な CYP3A4 阻害剤を投与されている患者には禁忌です。
α遮断薬とバルデナフィルには血管を拡張する作用があるため、併用すると血圧低下の症状が生じる場合があります。併用治療は、安定したα遮断薬治療を受けている場合にのみ開始してください。この場合、レビトラ®コーティング錠を使用して、推奨される最低用量で治療を開始する必要があります。アルファ遮断薬で治療されている患者は、初回用量としてレビトラ® 10 mg 口腔内分散錠を使用しないでください。タムスロシンまたはアルフゾシンとともに、バルデナフィルはいつでも投与できます。バルデナフィルが他のアルファ遮断薬と同時に処方される場合、投与間の適切な間隔を考慮する必要があります。すでにバルデナフィルの最適用量で治療を受けている場合は、アルファブロッカー療法を最小用量で開始する必要があります。アルファブロッカーの用量を徐々に増やすと、血圧がさらに低下する可能性があります。
レビトラを飲み忘れた場合はどうすればよいですか?
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
レビトラの注意事項
性行為には特定の心臓リスクが伴うため、医師はあなたの心臓血管の状態を評価する必要があります。

バルデナフィルには血管拡張作用があり、軽度かつ一時的な血圧低下を引き起こす可能性があります。血管の拡張は、一部の心臓弁疾患にも影響を与える可能性があります。関連使用は、患者がアルファブロッカー療法で安定している場合にのみ開始する必要があり、レビトラ®コーティング錠による治療は推奨最低用量で開始する必要があります。
レビトラ®の使用は、透析を必要とする肝臓、腎臓、心臓、循環器系の重篤な疾患のある患者、網膜色素変性症と呼ばれる遺伝性の眼疾患のある患者、および低血圧の患者(最高血圧 90 未満)には推奨されません。安静時 mmHg)、過去 6 か月以内に心臓発作または脳卒中を起こしたことがある。
心臓の機能に変化がある患者(先天性 QT 間隔延長)や、キニジン、プロカインアミド、アミオダロン、ソタロールなどの不整脈に対する薬を服用している患者は、バルデナフィルの服用を避けるべきです。
バルデナフィルは、慎重なリスク/ベネフィット評価の後、出血を引き起こす血液凝固の変化がある患者、または重大な活動性消化性潰瘍のある患者にのみ投与されるべきです。
一般に、勃起不全の治療薬は、陰茎の解剖学的変形のある患者や、鎌状赤血球貧血など、痛みを伴い持続する陰茎の不随意勃起(持続勃起症)を起こしやすい状態の患者には注意して使用する必要があります。多発性骨髄腫または白血病。
ヘパリンとバルデナフィルの関連性は、ラットの出血時間には影響しませんでしたが、この相互作用はヒトでは研究されていません。
レビトラ®コーティング錠など、レビトラ®と同じグループの他の薬剤の摂取に伴う血流低下による一時的な視力喪失や視神経損傷の報告があります。突然視力を失った場合は、レビトラ®の服用を中止し、直ちに医師の診察を受けてください。
車両を運転したり、機械を操作したりする能力
この薬が車の運転や機械の操作能力を変える可能性があるかどうかは不明です。したがって、患者は治療中に起こり得る影響を認識しておく必要があります(レビトラ®コーティング錠は、人によってはめまいを引き起こしたり、視力に影響を与える可能性があるため、これらの症状のいずれかを経験した場合は、車の運転や機械の操作を行わないでください)。
専用の口腔内崩壊錠
レビトラ® 10 mg 口腔内崩壊錠の安全性は、中等度または重度の肝障害、チャイルド ピューB またはチャイルド ピューC の患者では研究されていないため、これらの患者におけるレビトラ® 10 mg 口腔内崩壊錠の使用は推奨されません。
Levitra ® 10 mg 口腔分散錠には、フェニルケトン尿症の人に害を及ぼす可能性があるフェニルアラニンの供給源であるアスパルテーム 1.8 mg が含まれています。
フェニルケトン尿症に注意:フェニルアラニンが含まれています。
Levitra ® 10 mg 口腔内分散錠には、7.96 mg のソルビトールが含まれています。フルクトース不耐症というまれな遺伝性の問題を抱えている患者は、レビトラ® 10 mg 口腔内崩壊錠を服用すべきではありません。
レビトラの副作用
副作用の一覧表
レビトラ®で報告された副作用の頻度を以下の表にまとめます。各頻度グループ内で、副作用は重症度の降順に表示されます。頻度は、非常に一般的 (? 1/10)、一般的 (? 1/100 ~ lt; 1/10)、珍しい (? 1/1,000 ~ lt; 1/100)、まれな (? 1/10,000 ~ lt; 1/10) として定義されます。 ; 1/1,000)、非常にまれです (lt; 1/10,000)。
市販後の追跡調査中にのみ確認され、頻度が推定できない副作用は「不明」としてリストされます。
表 1: 世界中のすべての臨床研究において患者で報告された副作用のうち、報告され、その薬剤に関連した副作用。患者の0.1%、または稀であり、本質的に重篤であると考えられる
|
身体システムによる分類 |
非常に一般的な |
一般 |
普通でない |
レア |
|
感染症と蔓延 |
– | – | – | 結膜炎 |
|
免疫系の障害 |
– | – | アレルギー性浮腫および血管性浮腫 | アレルギー反応 |
|
精神障害 |
– | – | 睡眠障害 | – |
|
神経系障害 |
頭痛 | めまい | 主観的な皮膚感覚と感覚の変化、眠気 | 失神 記憶喪失、発作 |
|
眼疾患を含む関連調査 |
– | – | 視覚障害、目の充血、視覚的な色の歪み、目の不快感と目の痛み、光恐怖症 | 眼圧の上昇 |
|
耳と迷路の障害 |
– | – | 耳鳴り、めまい | – |
|
心臓疾患を含む関連調査 |
– | – | 動悸、頻脈 | 狭心症、心筋梗塞、心室性頻脈性不整脈 |
|
血管障害(以下を含む)関連調査 |
– | 血管拡張 | – | 低血圧 |
|
呼吸器、胸部、縦隔の疾患 |
– | 鼻づまり | 息切れ、正弦波のうっ血 | – |
|
胃腸障害など関連調査 |
– | 胃の不調 | 吐き気、腹部および胃腸の痛み、口渇、下痢、胃食道逆流症、胃炎、嘔吐 | – |
|
肝胆道系疾患 |
– | – | トランスアミナーゼ酵素の増加 | – |
|
皮膚および皮下の疾患 |
– | – | 発赤、発疹 | – |
|
筋骨格および結合組織の疾患(以下を含む)関連調査 |
– | – | 背中の痛み、クレアチンホスホキナーゼ酵素の増加、筋緊張とけいれんの増加、筋肉痛 | – |
|
生殖器系と乳房の疾患 |
– | – | 勃起力の増加 |
痛みを伴い持続する陰茎の不随意勃起 |
|
管理現場における一般的な混乱と状況 |
– | – | 倦怠感 |
胸痛 |
選択された副作用の説明
心筋梗塞、まれに非動脈炎性前部虚血性視神経障害(永久的な視力喪失を含む視力低下の原因)、(一時的または永久的な)視力喪失を含む視覚障害、突発性難聴や聴力損失のまれな報告があります。少数のケースでは。これらの報告された事象が、レビトラ® の使用、潜在的な危険因子、これらの因子の関連、または他の因子に直接関連しているかどうかを判断することはできません。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。
また、顧客サービスを通じて会社に通知してください。
レビトラ特別集団
妊娠・授乳期・小児
レビトラ® は、女性および子供 (18 歳未満) への使用には適応されていません。
レビトラの組成
コーティング錠
レビトラ® 5mg コーティング錠
各コーティング錠剤には次のものが含まれます。
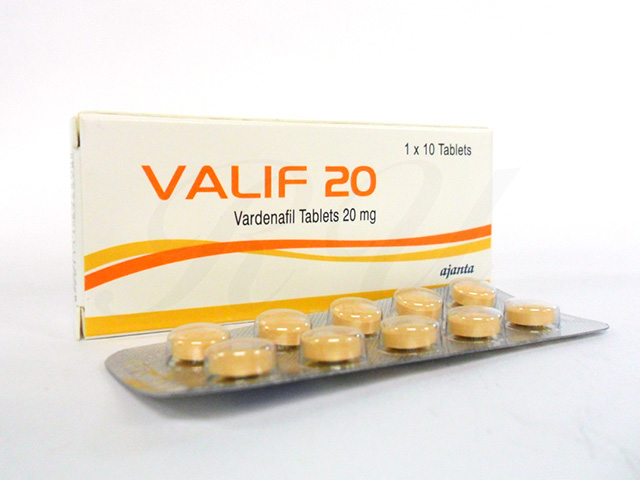
バルデナフィル 5 mg (バルデナフィル塩酸塩三水和物 5.926 mg)。
レビトラ® 10mg コーティング錠
各コーティング錠剤には次のものが含まれます。
バルデナフィル 10 mg (バルデナフィル塩酸塩三水和物 11.852 mg)。
レビトラ® 20mg コーティング錠
各コーティング錠剤には次のものが含まれます。
バルデナフィル 20 mg (バルデナフィル塩酸塩三水和物 23.705 mg)。
賦形剤:
クロスポビドン、ステアリン酸マグネシウム、微結晶セルロース、二酸化ケイ素、マクロゴール、ヒプロメロース、二酸化チタン、ベンガラ、黄色酸化鉄。
口腔内崩壊錠
各口腔内崩壊錠には次のものが含まれます。
バルデナフィル 10 mg (バルデナフィル塩酸塩三水和物 11.852 mg)。
賦形剤:
アスパルテーム、ミントフレーバー、ステアリン酸マグネシウム、ファーマバースト B2 (クロスポビドン、マンニトール、水和コロイダルシリカ、ソルビトール)。
レビトラのプレゼンテーション
コーティング錠
Levitra®は、5 mg、10 mg、20 mg の濃度のコーティング錠の形で提供されます。 5 mg の濃度が 4 錠入りのパックで提供されます。 10 mg 濃度は 1 錠のパッケージで提供され、20 mg 濃度は 2、4 または 8 錠のパッケージで提供されます。
経口使用。
大人用。
口腔内崩壊錠
Levitra ®は、2 錠または 4 錠のパックで 10 mg の濃度の口腔内崩壊錠の形で提供されます。
経口使用。
大人用。
レビトラの過剰摂取
バルデナフィルは、ボランティアを対象に実施された研究で、1日あたり最大120 mgの単回投与で評価されています。バルデナフィルを 1 日 1 回 4 週間投与した場合、最大 80 mg の単回投与および最大 40 mg の複数回投与は、重篤な副作用を引き起こすことなく耐容されました。
40 mg のバルデナフィルを 1 日 2 回投与すると、重度の腰痛が発生するケースがありました。筋肉毒性や神経毒性は観察されませんでした。
過剰摂取の場合は、必要に応じて一般的な補助措置を講じる必要があります。バルデナフィルは血漿タンパク質に強く結合しており、尿中に大幅には除去されないため、腎透析によってバルデナフィルのクリアランスが加速されるべきではありません。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。
さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
レビトラの薬物相互作用
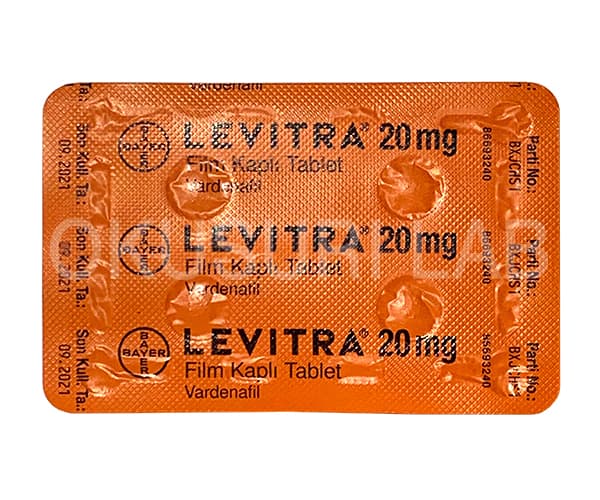
Levitra®は、タムスロシンまたはアルフゾシンと併用していつでも投与できます。レビトラ®フィルムコーティング錠をテラゾシンやその他のアルファ遮断薬と併用する場合は、適切な投与間隔を考慮する必要があります。
最適化された用量のレビトラ®コーティング錠剤ですでに治療を受けている患者では、アルファ遮断薬による治療を最小用量で開始する必要があります。レビトラ®コーティング錠などの PDE5 阻害剤で治療を受けている場合、α 遮断薬の用量を段階的に増やすと、血圧がさらに低下する可能性があります。
インジナビルまたはリトナビルとの併用は禁忌です。
レビトラ®と勃起不全の他の治療法を組み合わせた場合の安全性と有効性は研究されていません。したがって、これらの関連付けの使用はお勧めできません。
レビトラ® は、単独で投与しても、アセチルサリチル酸と組み合わせて投与しても、出血時間は変わりません。
CYP阻害剤
バルデナフィルは、主に肝酵素によって CYP3A4 を介して代謝されますが、CYP3A5 および CYP2C アイソフォームによる一定の寄与もあります。したがって、これらの酵素の阻害剤はバルデナフィルのクリアランスを減少させる可能性があります。
専用コーティング錠
ケトコナゾールやイトラコナゾール(真菌性疾患に使用)、インジナビルやリトナビル(HIV感染症の治療に使用)、クラリスロマイシンやエリスロマイシン(抗生物質)などの中程度または強力なCYP3A4阻害剤を併用すると、バルデナフィル血漿レベルが大幅に上昇する可能性があります。ケトコナゾールおよびイトラコナゾールと組み合わせて使用する場合、レビトラ® 5 mg フィルムコーティング錠 1 錠の最大用量を超えないようにしてください。 200 mg、およびエリスロマイシンまたはクラリスロマイシンと併用。レビトラ® は、 200 mg を超える用量のケトコナゾールまたはイトラコナゾールと一緒に投与しないでください。
インジナビルまたはリトナビルとの併用は禁忌です。
レビトラ® 20 mg コーティング錠と、胃炎および消化性潰瘍に使用される薬剤であるシメチジン (400 mg を 1 日 2 回) との間に相互作用はありませんでした。
専用の口腔内崩壊錠
レビトラ®口腔内分散性錠剤の使用は、エリスロマイシン、ケトコナゾール、イトラコナゾール、クラリスロマイシン、インジナビル、またはリトナビルによる治療を受けている患者には禁忌です。
硝酸塩および一酸化窒素供与体
健康な男性を対象とした研究では、レビトラ® 10 mg コーティング錠をニトログリセリンの 24 時間から 1 時間までの様々な間隔で投与した後、ニトログリセリン 0.4 mg の舌下投与による血圧降下効果の増加は観察されませんでした。
健康な中年者において、レビトラ® 20 の摂取後 1 時間および 4 時間後に硝酸塩舌下 0.4 mg(狭心症や心筋梗塞の場合に心臓の動脈を拡張する薬)を投与すると、血圧降下効果が増加しました。 mgコーティング錠。これらの効果は、ニトログリセリンの 24 時間前に Levitra® 20 mg コーティング錠を摂取した場合には観察されませんでした。
バルデナフィルと硝酸塩の併用は禁忌です。ニコランジル(抗不整脈薬および高血圧症に使用される)は、バルデナフィルと深刻な相互作用を引き起こす可能性があります。
専用の口腔内崩壊錠
ニコランジル(抗不整脈薬および高血圧症に使用される)は、バルデナフィルと深刻な相互作用を引き起こす可能性があります。
アルファブロッカー
研究は、α遮断薬を短期間使用した後の正常血圧のボランティアと、前立腺肥大を治療するためにα遮断薬による安定した治療を受けている患者を対象に実施され、併用治療は患者が次のような場合にのみ開始されるべきであると結論づけられた。アルファブロッカー療法で安定している。アルファブロッカー療法が安定している場合は、レビトラ® を推奨最小用量で開始する必要があります。
テラゾシンやその他のα遮断薬を使用する場合、レビトラ®を投与する際には、適切な投与間隔を考慮する必要があります。タムスロシンまたはアルフゾシンの場合、投与間に間隔を置く必要はありません。
すでに最適用量のレビトラ®コーティング錠剤による治療を受けている場合、医師は最低用量のアルファブロッカーによる治療を開始する必要があります。バルデナフィルなどの PDE5 阻害剤で治療を受けている場合、α 遮断薬の用量を段階的に増やすと、血圧がさらに低下する可能性があります。
専用の口腔内崩壊錠
アルファ遮断薬による治療を受けている患者は、初回用量として Levitra ® 10 mg 口腔内崩壊錠を使用しないでください。
リオシグアテ
リオシグアトは、心臓から肺に血液を運ぶ動脈の高血圧の治療に使用される薬剤の一種で、患者の血圧に深刻な影響を与える可能性があります。動物モデルでは、シルデナフィルまたはバルデナフィルをリオシグアトと組み合わせると、全身血圧を下げる相加効果が実証されました。シルデナフィルまたはバルデナフィルの用量を増やすと、場合によっては全身血圧が比例以上に低下しました。
探索的研究では、シルデナフィルで治療を受けた肺動脈性肺高血圧症(PAH)患者にリオシグアトを単回投与すると、相加的な血行動態効果が実証されました。シルデナフィル単独で治療した患者と比較して、シルデナフィルとリオシグアトの併用で治療したPAH患者では、主に低血圧による高い中止率が観察されました。
レビトラ®と GC 刺激薬であるリオシグアトの併用は禁忌です。

その他
14 日間、レビトラ® 20 mg コーティング錠剤と 0.375 mg のジゴキシン (心不全治療薬) を 1 日おきに同時投与した場合、相互作用はありませんでした。
制酸薬の単回投与。水酸化マグネシウム/水酸化アルミニウムは、バルデナフィルの AUC または C maxに影響を与えませんでした。
Levitra ® 20 mg コーティング錠のバイオアベイラビリティは、胃炎や消化性潰瘍に使用されるラニチジン 150 mg を 1 日 2 回の併用投与によって影響を受けませんでした。
レビトラ® 10 mg および 20 mg コーティング錠は、単独で投与した場合、または心筋梗塞や脳卒中を予防するために使用される低用量のアセチルサリチル酸 (81 mg 錠 2 個) と併用して投与した場合、出血時間に影響を与えませんでした。
Levitra® 20 mg コーティング錠は、アルコール (0.5 g/kg 体重) の降圧効果を増加させませんでした。
薬物動態調査データでは、アセチルサリチル酸、アンジオテンシン変換酵素 (ACE) 阻害剤、β 遮断薬、弱 CYP3A4 阻害剤、利尿薬 (動脈性高血圧の制御に最も一般的に使用される薬剤)、および治療薬の間の相互作用に起因する有意な効果は示されませんでした。バルデナフィルの薬物動態に関するスルホニルウレア剤やメトホルミンなどの糖尿病の治療。
糖尿病の治療に使用されるレビトラ® 20 mg コーティング錠剤とグリベンクラミドの同時投与は、グリベンクラミドの相対的な生物学的利用能やバルデナフィルの薬物動態に影響を与えませんでした。
レビトラ® 20 mg コーティング錠と抗凝固剤として使用されるワルファリン 25 mg の間には、プロトロンビン時間や凝固因子 II、VII、X などの薬理学的相互作用は観察されませんでした。バルデナフィルの薬物動態は、ワルファリンの同時投与によって影響を受けませんでした。
レビトラ® 20 mg コーティング錠とニフェジピン 30 mg または 60 mg を併用投与した場合にも、関連する薬物動態学的および薬力学的相互作用は示されませんでした。ニフェジピンは高血圧の治療および冠状動脈拡張薬として使用されます。レビトラ®コーティング錠は、プラセボと比較して、さらなる平均血圧低下をもたらしました。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
専用コーティング錠
ケトコナゾール、イトラコナゾール、エリスロマイシン、クラリスロマイシン、インジナビル、リトナビルなどの中度または強力なシトクロム CYP3A4 阻害剤を併用すると、バルデナフィル血漿レベルが大幅に増加する可能性があります。
レビトラ® 5 mg フィルムコーティング錠の最大用量は、ケトコナゾールまたはイトラコナゾールの用量と組み合わせて使用する場合、超えてはなりません。 200 mg、エリスロマイシンまたはクラリスロマイシン。
レビトラ® は、ケトコナゾールまたはイトラコナゾールを 200 mg を超える用量で服用している患者には投与しないでください。
レビトラという物質の作用
有効性の結果
バルデナフィルは、特殊集団を含むすべての主要な臨床有効性研究において、プラセボと比較して臨床的および統計的に勃起機能の有意な改善を実証しました。
臨床研究では、勃起不全(ED)を患う1万7000人以上の男性にバルデナフィルが投与され、その多くは他の複数の病状を抱えていた。 2,500人以上の患者がバルデナフィルによる6か月以上の治療を受けています。これら 2,500 人の患者のうち、900 人が 1 年以上治療を受けました。
Global Assessment Questionnaire (GAQ) に基づくランダム化二重盲検プラセボ対照固定用量研究では、バルデナフィル 5 mg、10 mg、20 mg を投与した患者の 65%、80%、85% で勃起が改善しました。バルデナフィルはそれぞれ6ヵ月時点で、プラセボの28%と比較した。
バルデナフィル塩酸塩(活性物質)口腔内分散錠の有効性と安全性は、最長 12 週間治療を受けた勃起不全患者 701 人を含む 2 件の研究で幅広い集団で実証されました。事前に定義されたサブグループへの患者の分布には、高齢患者 (51.3%)、糖尿病の病歴を持つ患者 (28.7%)、脂質異常症 (39.2%)、高血圧 (39.7%) が含まれていました。
塩酸バルデナフィル(活性物質)口腔内分散性錠剤を用いた 2 件の研究の統合データでは、報告されたすべての性行為の試みのうち 71.3% が浸透に成功しましたが、プラセボ群ではすべての試みの 43.9% が成功しました。これらの結果は、高齢患者(66.9%)、糖尿病の病歴のある患者(63.4%)、脂質異常症の病歴のある患者(66.4%)、高血圧症の病歴のある患者(69.7%)のサブグループにも反映されていた。報告されたすべての性的試みのうち、挿入に成功したのは。
バルデナフィル塩酸塩(活性物質)口腔内崩壊錠で報告されたすべての性的試みの約62.7%が勃起維持の点で成功しましたが、プラセボではすべての性的試みの約26.0%が成功しました。事前に定義されたサブグループでは、報告されたすべての患者の 56.7% (高齢患者)、56% (糖尿病の病歴のある患者)、59% (脂質異常症の病歴のある患者)、および 60% (高血圧の病歴のある患者)バルデナフィル塩酸塩(有効成分)口腔内崩壊錠を用いた試みは、勃起維持の点で成功しました。
塩酸バルデナフィル(活性物質)口腔内崩壊錠の有効性は、勃起不全のベースライン重症度、病因(器質性、心因性、およびその両方)、勃起不全の期間、民族および年齢を考慮せずに実証されました。
特別集団での研究を含む主要な臨床研究から得られた統合データでは、最初の投与量の治療に成功した患者は、プラセボ群で37%、バルデナフィル10mgで68%、バルデナフィル20mgで70%でした。最初の用量の浸透に成功した患者については、平均して、バルデナフィル 10mg および 20mg を投与された患者は、3 か月の研究期間後、その後のすべての試みのそれぞれ 86% および 90% で成功しました。バルデナフィルは、ベースラインの重症度、病因(器質性、心因性、およびその両方)、EDの期間、サブグループ分析の決定要因として民族性および年齢を考慮することなく、患者に有効でした。
薬理的特性
薬力学特性
陰茎の勃起は、海綿体とその細動脈の平滑筋の弛緩に基づく血行力学的プロセスです。性的刺激中、海綿体の神経終末は一酸化窒素 (NO) を放出し、酵素グアニル酸シクラーゼを活性化します。その結果、海綿体内の環状グアノシン一リン酸 (cGMP) のレベルが増加します。これにより、平滑筋の弛緩が引き起こされ、陰茎への血流が増加します。
cGMP の有効レベルは、一方ではグアニル酸シクラーゼによる合成速度に依存し、他方では cGMP 加水分解ホスホジエステラーゼ (PDE) の分解速度に依存します。
ヒト海綿体における主な PDE は、cGMP に特異的なホスホジエステラーゼ 5 型 (PDE5) です。
バルデナフィルは、海綿体における cGMP の分解に関与する酵素である PDE5 を阻害することにより、性的刺激により海綿体で局所的に放出される内因性 NO の効果を潜在的に高める可能性があります。バルデナフィルによる PDE5 の阻害は、海綿体における cGMP レベルの増加をもたらし、平滑筋の弛緩と海綿体への血液流入をもたらします。
したがって、バルデナフィルは性的刺激に対する自然な反応を強化します。
精製酵素製剤に関する研究では、バルデナフィルが選択性が高く、非常に強力な PDE5 阻害剤であり、ヒト PDE5 に対する IC50 が 0.7 nM であることが示されています。
バルデナフィルの阻害効果は、他の既知のホスホジエステラーゼよりも PDE5 に対して強力です (PDE6 よりも 15 倍、PDE1 よりも 130 倍、PDE11 よりも 300 倍、PDE2、3、4、7 よりも 1,000 倍、 8、9、10)。インビトロでは、バルデナフィルは単離されたヒト海綿体において cGMP の上昇を引き起こし、筋肉の弛緩を引き起こします。
意識のあるウサギでは、バルデナフィルは内因性の一酸化窒素合成に依存して陰茎の勃起を引き起こし、一酸化窒素供与体によって増強されます。
作用機序
Rigiscan のプラセボ対照研究では、一部の男性では 20mg のバルデナフィルにより、早ければ 15 分で浸透に十分な勃起 (Rigiscan によると硬さが約 60%) が生じました。バルデナフィルに対するこれらの被験者の全体的な反応は、投与後 25 分でプラセボと比較して統計的に有意になりました。
勃起不全の男性を対象とした多施設無作為二重盲検プラセボ対照研究では、バルデナフィルの投与から挿入に十分と思われる勃起が得られ、性交が完了するまでの最短時間が評価されました。 10 または 20 mg のバルデナフィルの投与後に性交を正常に完了した男性の割合は、GT 作用が始まってプラセボと比較して高かった (PLT; 0.025)。 10分とGT。それぞれ11分。
薬物動態学的特性
吸収
経口投与後、バルデナフィルはすぐに吸収されます。 15 分後に AC Maxに到達できるようになりました。 90%の場合、空腹時経口投与後30~120分(平均60分)で最大値に達します。
初回通過効果が大きいため、平均経口バイオアベイラビリティは約 15% です。
バルデナフィルの経口投与後、AUC と C Max は推奨用量範囲 (5 ~ 20mg) にほぼ比例して増加します。バルデナフィラを脂っこい食事(57%脂肪を含む)と一緒に食べると、吸収率が低下し、60分間の中央値t -maxが増加し、C maxが平均20%減少します。バルデナフィル AC は影響を受けません。通常の食事(30%の脂肪を含む)の後では、バルデナフィルの薬物動態パラメータ(C max 、t maxおよびAUC)はいずれも影響を受けませんでした。
これらの結果を考慮すると、バルデナフィルは食事の有無にかかわらず摂取できます。
分布
バルデナフィルのバランスステータス (VSS) における平均分布量は 208 L であり、組織内での分布を示しています。
バルデナフィルとその主な循環代謝物 (M1) は、元の化合物または M1 化合物の約 95% である血漿タンパク質と高度に関連しています。このタンパク質結合は可逆的であり、化合物の総濃度には依存しません。
バルデナフィルの測定値は、投与90分後に健康な個人の精液中に検出されましたが、患者の精液中には投与量の0.00012%が現れる可能性があります。
代謝・生体内変化
バルデナフィルは主に CYP3A4 を介して肝酵素によって代謝されますが、CYP3A5 および CYP2C アイソフォームの寄与もあります


.jpg?ssl=1)







