静脈尿路造影(成人および小児患者)、逆行性尿道造影および上尿路造影、末梢静脈造影、従来の選択的冠動脈造影、インターベンショナル冠動脈造影、コンピュータ断層撮影(頭蓋骨および体)、海綿体造影、子宮卵管造影、胆管造影および内視鏡的逆行性胆管膵管造影、関節造影、瘻孔造影、乳汁造影、涙嚢造影、唾液造影、静脈内および動脈内のデジタルサブトラクション血管造影、従来の血管造影、心血管造影(成人および小児患者の場合)、椎間板造影および脊髄造影。
イオメプロール 816.5mg
静脈尿路造影(腎不全や糖尿病患者を含む成人患者)、コンピュータ断層撮影(身体)、従来の血管造影、静脈デジタルサブトラクション血管造影、心血管造影(成人および小児患者)、従来の選択的冠動脈造影、インターベンショナル冠動脈造影、瘻孔造影、乳汁造影、涙嚢造影および唾液造影。
この薬は診断目的のみに使用されます。
イオメロンの禁忌
尿路血管造影の使用には厳密かつ絶対的な禁忌はありませんが、ヴァルデンストレームマクログロブリン血症、多発性骨髄腫、重度の肝臓疾患や腎臓疾患の場合には使用を避けるべきです。
この薬は、イオメプロール、ヨウ素を含むその他の造影剤、またはその成分に対して過敏症のある患者による使用は禁忌です。
この薬は、妊娠中であるかどうかにかかわらず、妊娠中の女性生殖器の検査や急性炎症の場合にも禁忌です。
イオメロンの使い方
投与量を確認するには、.pdf のリーフレットをお読みください。
イオメロンの注意事項
すべての投与経路に対する警告と予防措置:
深刻な望ましくない影響の可能性を考慮すると、ヨード造影剤の使用は、造影を使用した検査が特に必要な場合に限定されるべきです。この必要性は、患者の臨床状態、特に心血管系、泌尿器系、肝胆道系の病状に応じて評価する必要があります。
心血管造影技術用の造影剤は、緊急時の集中治療を専門とする設備と人員を備えた病院または診療所で使用する必要があります。ヨウ素化造影剤を必要とする他のより一般的な診断技術に関して、これらの技術を実施するセンターは、すぐに使用できる機器と蘇生治療手段を常に備えていなければなりません。
特別な人々に対する警告と予防措置
新生児、授乳中の母親と子供たち
1 歳未満の乳児、特に新生児は、電解質の不均衡や血行動態の変化に特に敏感です。使用量、投与技術手順、患者の状態については特別な注意を払う必要があります。
高齢の患者さん
高齢者の場合、過剰な用量の造影剤の使用による反応のリスクが特に高くなります。これらの患者は、心筋虚血、重度の不整脈、期外収縮を呈する可能性が高くなります。神経学的変化と血管病理が頻繁に関連することが悪化要因となります。このような人では、急性腎不全の可能性も高くなります。特定の病理学的状態を持つ患者に対する警告と予防措置 ヨード造影剤に対する過敏症:ヨード造影剤に対する過敏症または以前の反応の存在も、非イオン性造影剤の使用によって重篤な反応が起こるリスクを高めます。
アレルギー体質
ヨード造影剤に対する副作用は、アレルギー、特に花粉症、蕁麻疹、食物アレルギーの病歴のある患者でより一般的であると考えられています。
喘息患者
喘息患者における気管支けいれん誘発反応のリスクは、造影剤の投与後に高くなります。甲状腺機能亢進症または結節性甲状腺腫:造影剤中に存在する可能性のある少量の遊離無機ヨウ素は、特に甲状腺機能亢進症または甲状腺腫の患者において、甲状腺機能に何らかの影響を与える可能性があります。イオン造影剤の投与後の甲状腺機能亢進症の発作が報告されています。
動脈内および静脈内投与経路に関する警告と注意事項
特定の病態を持つ患者に対する警告と予防措置
腎不全
腎機能障害があると、造影剤投与後に腎機能障害が起こりやすくなる可能性があります。予防策には、高リスク患者を特定すること、造影剤投与前に十分な水分補給を確保すること、できれば検査前および検査中および造影剤が腎臓から完全に排出されるまで血管内灌流を維持することが含まれます。可能な限り、造影剤が完全に除去されるまで、腎毒性薬の投与を避けたり、患者に大規模な手術や技術(腎血管形成術など)を受けさせたりしないでください。腎機能が検査前のレベルに戻るまで、造影剤を使用した新たな検査の実施を延期してください。イオメプロールなどの造影剤は透析可能なため、透析患者はイオメプロールなどの造影剤を受けることができます。
糖尿病
糖尿病患者における腎障害の存在は、造影剤投与後に腎不全を起こしやすくする要因の 1 つです。この不足により、ビグアナイド治療を受けた患者では乳酸アシドーシスが進行する可能性があります。予防策として、ビグアナイド薬による治療は検査の 48 時間前までに中断する必要があり、腎機能が完全に回復したことを管理によって確認した後に再開できます。
多発性骨髄腫とパラタンパク質血症
イオメプロールの使用は通常禁忌です。骨髄腫症またはパラプロテイン血症の存在は、造影剤の投与によって引き起こされる腎不全を起こしやすい状態であることを考慮する必要があります。造影処置を使用する利点と、起こり得るリスクを慎重に比較検討する必要があります。造影剤投与後は、適切な水分補給と患者の腎機能のモニタリングが推奨されます。
褐色細胞腫
これらの患者は、放射線検査中に静脈内造影剤を投与された後、重篤な高血圧症(まれに制御不能)を発症する可能性があります。

重度の腎臓および肝臓疾患
イオメプロールの使用は通常禁忌です。肝不全と腎不全が重なると造影剤の排泄が遅れ、その結果副作用が起こりやすくなる可能性があることを考慮する必要があります。
重度の心血管疾患
副作用のリスクは、重度の心臓病患者、特に心不全や冠状動脈疾患を患っている患者で高くなります。造影剤の静脈内投与は、顕著な心不全または初期の心不全の患者に肺水腫を引き起こす可能性があり、一方、肺高血圧症および心臓弁膜症の患者に造影剤を投与すると、血行動態の変化を誘発する可能性があります。心電図上に虚血の兆候や重度の不整脈が現れることは、高齢の患者や以前に心臓病を患った患者でより一般的であり、その頻度と重症度は心不全の程度と関連しているようです。重度の慢性高血圧は、造影剤投与の結果として腎損傷のリスクを高めるだけでなく、カテーテル治療に関連するリスクも高める可能性があります。
中枢神経系疾患
血液脳関門の変化、脳浮腫または急性脱髄を呈する急性脳梗塞、急性頭蓋内出血の患者に造影剤を静脈内投与する場合は、特別な予防措置を講じる必要があります。腫瘍または頭蓋内転移の存在、およびてんかんの病歴があると、発作が起こる可能性が高まるようです。変性性、炎症性、腫瘍性の脳血管の病状によって引き起こされる神経症状は悪化する可能性があります。造影剤の静脈内投与は、血管けいれんや脳虚血エピソードによるけいれんを引き起こす可能性があります。一過性の神経合併症のリスクは、症候性の脳血管疾患、最近心筋梗塞を起こした患者、または頻繁に起こる一過性虚血発作のある患者では高くなります。
フェノチアジン系の鎮痛薬や制吐薬など、発作閾値を下げる薬剤による治療は、検査の 48 時間前に中止する必要があります。治療は検査後 24 時間以内にのみ再度開始してください。
抗けいれん療法は中断すべきではなく、通常の用量で投与する必要があります。
アルコール依存症
急性および慢性のアルコール依存症が血液脳関門の透過性を高めることが実験的および臨床的に証明されています。この事実は、ヨウ素化物質の脳組織への通過を促進し、中枢神経系の変化を引き起こす可能性があります。アルコール患者に避妊薬を投与する場合は、けいれん閾値が低下する可能性があるため、特別な予防措置を講じる必要があります。薬物中毒:薬物中毒患者に造影剤を投与する場合、けいれん閾値が低下する可能性があるため、特別な予防措置を講じる必要があります。
患者関連の警告と予防措置:
水分補給
液体と電解質のバランスにおける重大な変化はすべて修正する必要があります。検査前には、特に多発性骨髄腫、糖尿病、多尿症、乏尿、高尿酸血症の患者、授乳中の母親、子供、高齢の患者では、十分な水分補給を確保する必要があります。
食事に関する推奨事項
特別な医学的推奨がない場合は、十分な水分摂取を確保しながら、検査当日は通常の食事を維持してください。ただし、患者は検査前の 2 時間は食事をとるべきではありません。
前投薬
褐色細胞腫の患者では、高血圧発症のリスクがあるため、β受容体拮抗薬による前投薬の投与が推奨されます。
過敏症
アトピーの可能性、ヨード造影剤に対する過敏症の病歴、および喘息の病歴がある患者では、アナフィラキシー様反応の可能性を回避するために、抗ヒスタミン薬および/またはコルチコステロイドの前投薬の投与が考慮される場合があります。
不安
興奮、不安、痛みの状態は、造影剤に関連した副作用の発生や反応の激化の原因となる可能性があります。このような場合、患者には鎮静剤が投与されることがあります。
併用薬
神経弛緩薬や抗うつ薬はけいれん閾値を下げるため、検査の 48 時間前までに投与を中止する必要があります。治療は検査後 24 時間以内にのみ再度開始してください。抗けいれん療法は中断すべきではなく、通常の用量で投与する必要があります。
手順に関する警告と注意事項:
カテーテルの凝固と洗浄
非イオン性造影剤の特性の 1 つは、正常な生理学的機能への干渉が最小限に抑えられることです。その結果、非イオン性造影剤は、インビトロではイオン性造影剤よりも抗凝固活性が低くなります。血管カテーテル治療を行う医療専門家は、この事実について知らされなければならず、この手術に関連する血栓症や塞栓症のリスクを最小限に抑えるために、血管造影手術やカテーテルの洗浄に関して特別な注意を払う必要があります。
感度試験
患者の病歴や感度検査に基づいて造影剤による重篤または致命的な反応の発生を予測することはできないため、感度検査は推奨されません。
患者の観察
可能な限り、造影剤の静脈内投与は患者を臥位にして行う必要があります。この薬を投与した後は、少なくとも 30 分間は患者を観察してください。
妊娠と授乳
動物実験では、イオメプロールの投与による催奇形性や胎児毒性の影響は明らかにされていません。他の非イオン性造影剤と同様に、妊婦に対する使用の安全性を確認できる対照研究はありません。
妊娠中の放射線被曝は可能な限り避けるべきです。そのため、造影剤の使用の有無にかかわらず、放射線検査のリスク/ベネフィット比を慎重に評価する必要があります。
造影剤の排泄は母乳中では大幅に減少します。これまでに得られた経験から、イオメプロールの投与後に授乳中の母親が害を受ける可能性は低いと結論付けることができます。
妊娠リスクカテゴリー:B.
この薬は、医師または歯科外科医のアドバイスなしに妊娠中の女性が使用すべきではありません。
車両の運転や機械の操作能力への影響
車の運転や機械の操作能力への影響は研究されていませんが、造影剤を使用した検査後 24 時間以内にこれらの活動を行うことはお勧めできません。これは、まれではありますが、造影剤の投与後に遅延反応が発生する可能性があるためです。 . ヨウ素化されたコントラスト。
イオメロンの副作用
他の薬と同様に、この薬も副作用を引き起こす可能性があります。
ヨウ素化化合物の使用は、通常は軽度から中等度の副作用だけでなく、死に至る可能性のあるアナフィラキシー様反応などのより重篤な副作用も引き起こす可能性があります。
軽度から中等度の反応には、熱感と痛み (注射部位および/または胸部の前部および後部)、悪寒、発熱、無力症、めまい、意識喪失、吐き気、嘔吐、発汗などがあります。 、顔面蒼白、呼吸困難、中等度の低血圧、全身性紅斑および浮腫。さらに、興奮、頭痛、喉頭浮腫、鼻づまりのケースも報告されています。皮膚反応は、さまざまな種類の発疹や丘疹のびまん性形成の形で発生し、場合によってはかゆみを伴う場合もあります。最も重篤な反応は心血管系に関与する可能性があり、顕著な低血圧、高血圧、頻脈または徐脈、チアノーゼ、呼吸困難、循環虚脱を伴う末梢血管拡張を引き起こします。
造影剤の静脈内または動脈内投与は、振戦、筋けいれん、精神錯乱、意識喪失、視覚障害、筋麻痺、失語症、けいれん、昏睡など、中枢神経系の変化に関連する反応を引き起こす可能性があります。
ただし、反応は本質的に穏やかで、持続時間は短く、自己限定的です。最も重篤な神経学的後遺症は、既存の病状の合併症によって生じる場合があります。乏尿およびタンパク尿を伴う一過性の腎不全、および血清クレアチニンの増加が、特に既存の腎不全を患っている患者で発生することがあります。注射部位に痛み、出血、腫れが生じる場合があります。血管外漏出の場合、たとえその発生がまれであっても、組織反応が発生する可能性があります。
|
非常に一般的な反応 |
くも膜下腔内投与: 頭痛。 |
|
一般的な反応 (gt; 1/100 および lt; 1/10) |
血管内投与:熱感。くも膜下腔内投与:めまい、高血圧、吐き気、嘔吐、背中の痛み、四肢の痛み、注射部位の反応。 |
|
異常な反応 |
血管内投与:めまい、頭痛、高血圧、呼吸困難、嘔吐、吐き気、紅斑、蕁麻疹、そう痒症、胸痛、注射部位の熱感と痛み。 |
|
まれな反応 |
血管内投与:失神前、徐脈、頻脈、期外収縮、低血圧、発疹、無力症、脱力感、悪寒、発熱、血清クレアチニンレベルの上昇。血小板減少症、アナフィラキシー様反応、不安、精神錯乱、昏睡、一過性虚血、麻痺、失神、けいれん、意識喪失、構音障害、感覚異常、健忘、眠気、味覚の変化、一過性失明、視覚障害、結膜炎、涙の増加、光視症、心停止、心筋梗塞、心不全、狭心症、不整脈、心室細動または心房細動、房室ブロック、チアノーゼ、循環虚脱またはショック、紅潮、顔面蒼白、呼吸停止、急性呼吸窮迫症候群(ARDS)、肺水腫、喉頭浮腫、咽頭浮腫、気管支けいれん、喘息、咳、咽頭不快感、喉頭不快感、鼻炎、発声困難、下痢、腹痛、唾液分泌過多、嚥下障害、唾液腺肥大、血管浮腫、発汗増加、腎不全、注射部位反応、倦怠感、心電図上昇ST セグメントと異常な心電図。 |
カテーテル処置後の冠動脈塞栓症および冠動脈血栓症の症例が処置の合併症として報告されています。
注意: この製品は新薬であり、研究により許容できる有効性と安全性が示されていますが、たとえ正しく指示され使用されたとしても、予測できないまたは未知の有害事象が発生する可能性があります。この場合、有害事象は健康監視通知システム NOTIVISA (http://www.anvisa.gov.br/hotsite/notivisa/index.htm) を通じて、または州または地方自治体の健康監視機関に報告してください。
イオメロンの薬物相互作用
昇圧剤はイオメプロールの前に投与すべきではありません。
糖尿病患者における腎障害の存在は、造影剤投与後の腎障害の素因の 1 つです。これにより、メトホルミンを投与されている患者では乳酸アシドーシスが促進される可能性があります。
コルチコステロイドはクモ膜炎の徴候や症状を促進し、影響を与える可能性があるため、ヨード造影剤を使用する場合は、硬膜外コルチコステロイドとくも膜下腔内コルチコステロイドを決して併用してはなりません。
以下の薬剤はこの薬と相互作用する可能性があります。
- 鎮痛剤;
- 制吐薬;
- 抗てんかん薬。
甲状腺機能検査
イオメプロールの使用は、甲状腺機能検査に干渉する可能性があります。
ヨウ素化造影剤の投与後、甲状腺の病状を診断するために放射性同位元素を取り込む甲状腺組織の能力は、最大 2 週間、場合によってはそれ以上の期間低下したままになります。
臨床検査
血漿および尿中に高濃度の造影剤が存在すると、ビリルビン、タンパク質、無機物質(鉄、銅、カルシウム、リン酸塩など)の検査結果に影響を及ぼす可能性があります。
胆嚢造影に使用される経口造影剤との相互作用
文献調査では、腎排泄造影剤と胆嚢造影に使用される経口造影剤との相互作用の証拠は明らかになりませんでした。
イオメロンという物質の作用
有効性の結果
血管内およびくも膜下腔内使用におけるイオメプロールの臨床的有効性は、心臓血管造影、脳血管造影、内臓および末梢血管造影、静脈内尿路造影、身体コンピュータ断層撮影および脊髄造影検査を受けている成人および小児患者を対象に実施された15件の研究で実証されました。
成人患者における有効性
心臓血管造影
合計 237 人の患者にイオメプロール 300 mgI/mL が投与されました (59 人)。イオメプロール 400mgI/mL (59 人の患者)。 4件の心臓血管造影研究では、イオベルソル320 mgI/mL(患者61人)またはイオパミドール370 mgI/mL(患者58人)。各心臓血管造影研究のすべての患者は、「良好」から「優秀」までの全体的な視覚診断の適切性評価を有しました。イオメプロール群の患者と対照薬の間で統計的に同等の結果が見られました。各研究では、各グループの患者の大多数 (70% 以上) が全体的な視覚診断の妥当性率を「優れた」としていました。全体的な視覚診断適合率が「悪い」画像を持った患者はいなかった。脳血管造影
2件の脳血管造影研究では、合計120人の患者がイオメプロール300mgI/mL(患者61人)またはイオベルソル320mgI/mL(患者59人)の投与を受けた。両方の研究および調査対象の両方の製品に参加したすべての患者は、脳の左側と右側の両方について全体的に「良好」または「優れた」視覚診断適合率を示しました。イオメプロール群とイオベルソル群の患者間で統計的に同等の結果が見られました。調査した各製品グループの患者の大多数 (71% 以上) は、左脳と右脳の両方について全体的な視覚診断の適合率が「優れた」ものでした。全体的な視覚診断適合率が「悪い」患者はいませんでした。
内臓/末梢血管造影
2件の内臓/末梢研究において、合計121人の患者がイオメプロール300mgI/mL(患者62人)またはイオパミドール300mgI/mL(患者59人)の投与を受けた。調査した各製品グループの患者の大多数 (96.6% 以上) は、全体的に「良好」または「優れた」視覚診断適合率を示しました。調査した各製品グループから 1 人の患者の全体的な視覚診断の適合率が「低かった」。イオメプロールは、イオパミドールと統計的に同等の全体的な診断適合率を有することが示されています。
体のコンピューター断層撮影
2件のコンピューター断層撮影研究で、合計114人の患者がイオメプロール400mgI/mL(患者59人)またはイオパミドール370mgI/mL(患者55人)を受けた。調査した両方の製品グループの患者の大部分 (96.4% 以上) で、視覚化は「良好」または「優れた」でした。これらの研究では、イオメプロールはイオパミドールと統計的に同等の全体的な診断適合性を有することが示されました。
脊髄造影検査
第 III 相試験では、合計 110 人の患者がイオメプロール 300 mgI/mL (患者 53 人) またはイオパミドール 300 mgI/mL (患者 57 人) の投与を受けました。ほとんどの患者の全体的な造影効率は「良好」または「優れた」でした。イオメプロールは、イオパミドールと同等の一般的な造影効果があることが示されています。
小児患者における有効性
10歳から15歳までの小児患者臨床研究では、1 か月と 18 年間にイオメプロールが投与されました。 4 つの主要な研究の結果を以下に要約します。
静脈泌尿器造影検査
対照研究では、生後1か月から12歳までの小児患者を対象に、イオメプロール 300 mgI/mL とイオパミドール 300 mgI/mL が比較されました。診断目的で尿路造影が必要な合計 69 人の小児が単一施設研究に参加した。患者は処置中に平均 29 mL (1.6 mL/kg) のイオメプロールまたは 27 mL (1.7 mL/kg) のイオパミドールを投与されました。平均投与速度は0.8mL/kg/秒であった。イオメプロールとイオパミドールは、評価したすべての腎臓および泌尿器領域で同様の視覚化を提供しました。どちらの造影剤でも、骨盤と尿管の最大混濁スコアはそれぞれ 1.2 ~ 2.3 (2 = 良好) と 0.4 ~ 0.7 (1 = 十分) の範囲でした。心臓血管造影
43 歳の小児患者を対象に非対照研究が実施されました。先天性心疾患のため心臓血管造影を受けた7歳。イオメプロール 400 mgI/mL は、患者の年齢と心臓の病状に応じて、総量 6 mL から最大 89 mL まで投与されました。一般的な用量は最大 6.8 mL/kg のイオメプロール 400 mgI/mL が投与されました。造影効率は 100% の症例で良好または優れていると測定され、臨床診断は一貫していました。
コンピュータ断層撮影法
非盲検試験では、中枢神経系病変の診断のためにコンピューター断層撮影を受けている生後2か月から13歳までの小児患者60人にイオメプロール300mgI/mLが投与されました。イオメプロール投与の平均速度は 0.9 mL/秒、平均総量は 27.0 mL、つまり体重 1 kg あたり約 1.1 mL でした。評価した X 線写真の 98% で良好または優れたコントラストが見られ、症例の 3% で十分なコントラストが見られました。
中枢神経系病変の診断のために脳のコンピューター断層撮影を必要とした1歳から15歳までの小児患者30人が、単一施設の非盲検研究に登録された。イオメプロール 300 mgI/mL の静脈内注射が 30 人の患者全員に投与されました。投与されたイオメプロールの平均速度および体積(体重に基づく)は、それぞれ0.5 mL/秒および1.4 mL/kgでした。イオメプロールは常に非常に効果的な造影剤であると考えられていました。平均不透明化率は 4 (4 = 優れた) でした。
薬理学的特徴
薬力学特性
薬物療法グループ: 低浸透圧、水溶性および腎栄養性 X 線検査用の造影剤。
ATCコード:V08AB10
イオメプロールは、X 線検査に適応される三ヨウ化非イオン性造影剤です。イオメプロール製剤は、他の非イオン性造影剤と比較した場合、特に低い浸透圧と粘度を特徴としています。
以下に示す濃度における本剤の注射液の物理化学的性質は次のとおりです。
|
ヨウ素濃度 mg I/mL |
密度§ (g/mL) |
浸透圧 mOsm/kg 水 |
粘度 mPa.s |
||
|
20℃ |
37℃ |
37℃ |
20℃ |
37℃ |
|
| 300 |
1,334 |
521 |
521 |
8.1 |
4.5 |
|
400 |
1,445 |
726 |
726 |
27.5 |
12.6 |
§ = Eur J Radiol Vol 18、suppl 1、1994: S1-S2。
薬物動態学的特性
イオメプロールの薬物動態、耐性、診断効果は、健康なボランティアと、尿路造影検査、血管造影検査、コンピューター断層撮影検査、体腔検査を必要とする患者を対象に、1 mL あたり最大 400 mg のヨウ素を含む溶液中で測定されました。
臨床検査値やバイタルサインに臨床的に重大な変化は記録されませんでした。
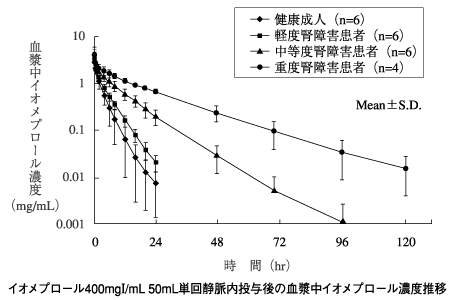
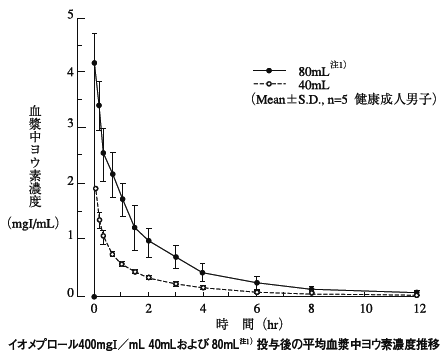
2 コンパートメント モデルで記述された静脈内投与によるイオメプロールの薬物動態は、急速な分布段階 (血漿および細胞外空間内) と同様に急速な薬物排出段階を明らかにしています。 18人の健康なボランティアにおいて、イオメプロール分布期と排出期の半減期はそれぞれ23分+14秒と109分+20秒で、投与後の最初の2時間で50%の尿中排泄を記録した。
前臨床安全性データ
ラット、マウス、およびイヌにおける研究データは、イオメプロールの単回静脈内または動脈内投与後のイオメプロールの急性毒性が他の非イオン性造影剤の急性毒性と同様であり、ラットにおける複数回の静脈内投与後にイオメプロールが良好な全身性耐性を有することを実証している。そして犬。
ラットに静脈内投与した後、イオメプロールは血漿および血管外空間全体に分布し、血漿タンパク質に結合しないか代謝され、ほぼ独占的に腎臓から排泄されます。ラットでは、投与量の 94% が最初の 8 時間で尿中に変化せずに検出されます。
動物へのさまざまな投与経路におけるイオメプロールの LD50 (g (ヨウ素)/kg、95% 信頼限界) は次のとおりです。
|
投与経路 |
ねずみ |
ねずみ |
犬 |
|
静脈内 |
19.9 (19.2 – 20.5) |
14.5 (13.2 – 16.0) |
gt; 12.5 |
|
腹腔内 |
26.1 (23.3 – 29.2) |
10 (8.9 – 11.3) |
|
|
脳内 |
1.3 (1.2 – 1.5) |
||
|
槽内 |
gt; 1.2 |
||
|
頸動脈内 |
5.8 (4.64 – 7.25) |


.jpg?ssl=1)







