- 閉経後の女性に対する最初の内分泌療法としてレトロゾールを使用。
- 以前に治療を受けた女性に対するフルベストラントの併用。
レトロゾールとフルベストラントに関する情報は、製品リーフレットに記載されています。医師もこの情報を提供してくれるでしょう。

イブランスはどのように機能しますか?
Palbociclib は、細胞の成長と増殖の過程で重要な役割を果たすサイクリン依存性キナーゼ (CDK) 4 および 6 の阻害剤です。臨床研究では、パルボシクリブをレトロゾールやフルベストラントなどの抗エストロゲン薬と組み合わせて投与すると、ホルモン受容体が陽性の乳がんの場合、腫瘍の増殖が抑制されることが示されています。
イブランス カプセルを摂取すると、薬は吸収され、6 ~ 12 時間以内に血中の最大量に達します。 8日間使用すると、血中の薬の量がバランスのとれた状態に達します。
イブランスの禁忌
イブランスの使用は、パルボシクリブまたは配合成分のいずれかに対して既知のアレルギーがある患者には禁忌です。
イブランスの使い方
Ibrance は、乳がんの治療経験のある医療専門家によって推奨されるはずです。常に医師の推奨に従って Ibrance を使用してください。医師が処方した量を超えて Ibrance を服用しないでください。
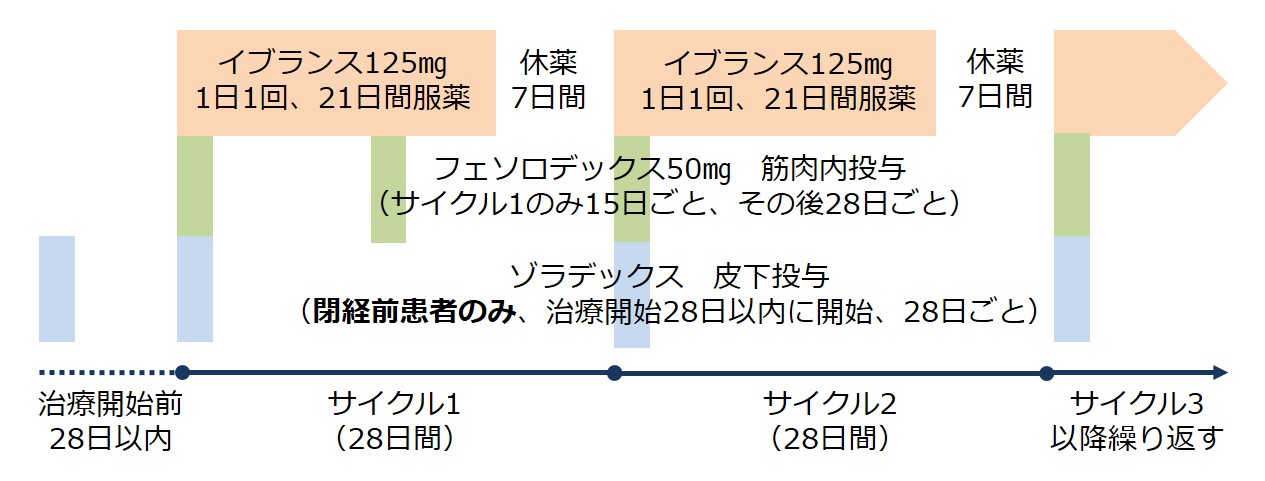
イブランスの推奨用量は、125 mg カプセル 1 錠を 1 日 1 回、連続 21 日間経口投与し、その後 7 日間治療なしで (3/1 スケジュール)、完全な 28 日サイクルを構成します。
パルボシクリブをレトロゾールと組み合わせて投与する場合、レトロゾールの推奨用量は、28 日サイクルで毎日 1 日 1 回 2.5 mg を経口投与します。
パルボシクリブをフルベストラントと組み合わせて投与する場合、フルベストラントの推奨用量は、1、15、29日目に500 mgを筋肉内投与し、その後は月に1回です。
イブランスは、毎日食事と一緒に、できれば同時に摂取する必要があります。イブランスをグレープフルーツまたはグレープフルーツジュースと一緒に投与しないでください。
Ibrance による治療中に自分がどのように感じているかを医師に伝えることが重要です。
治療に対するあなたの反応に応じて、医師はイブランスの用量を変更したり、治療を中止するよう求めたりする場合があります。
肝不全
軽度または中等度の肝障害(肝不全)の患者には用量調整は必要ありません。重度の肝障害がある場合、医師はイブランスの用量を減らして処方することがあります。
腎不全

軽度、中等度、重度の腎臓障害(腎不全)の患者には用量調整は必要ありません。 Ibrance は血液透析を受けている患者では評価されていません。
小児患者
小児におけるパルボシクリブの安全性と有効性は確立されていません。
高齢の患者さん
初回投与量を調整する必要はありません。
治療の時間、用量、期間を常に遵守し、医師の指示に従ってください。
医師の知識なしに治療を中止しないでください。
この薬は割ったり、開けたり、噛んだりしないでください。
Ibrance の使用を忘れた場合はどうすればよいですか?
患者が嘔吐したり、イブランスを飲み忘れた場合は、追加の用量を服用しないでください。次の処方量は通常の時間に服用する必要があります。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
イブランスの注意事項
この薬はあなたのために処方されました。たとえ相手があなたと似た症状を持っていたとしても、Ibrance を他の人と共有しないでください。
好中球減少症(血液中の防御細胞の一種である好中球の減少)
好中球として知られる血液中の防御細胞の減少は、イブランスの臨床研究に参加した患者が最も頻繁に経験する有害事象でした。血液中の好中球 (防御細胞) の数の減少は、平均して治療の 15 日目から起こります。イブランス臨床研究に参加した患者による、発熱に伴う血液中の好中球の減少(発熱性好中球減少症として知られている)の報告はまれ(~1%)でした。
イブランスによる治療を開始する前と各サイクルの開始時、および最初の 2 サイクルの 15 日目に医師の指示に従って血球数 (血液検査) をモニタリングする必要があります。

提示された好中球減少症の程度に応じて、医師は血中の好中球レベルが回復するまで治療サイクルの開始を中断または減量するか、延期することを選択する場合があります。
感染症
イブランスは血液防御細胞(白血球、好中球)の減少を引き起こす可能性があるため、この薬を使用する患者は感染症にかかりやすい可能性があります。
したがって、Ibrance を使用している患者は、発熱の症状があればすぐに医師に報告する必要があります。
閉経前/閉経周辺期の女性における卵巣切除(摘出)/抑制
アロマターゼ阻害剤の作用機序により、閉経前/閉経周辺期の女性がアロマターゼ阻害剤と組み合わせてイブランスを服用する場合、卵巣切除(摘出)または薬剤(LHRH受容体アゴニストとして知られる)を使用したその抑制が必須となります。閉経前/閉経周辺期の女性におけるパルボシクリブとフルベストラントの併用は、LHRH受容体アゴニストなどの卵巣抑制薬との併用でのみ研究されている。
受胎能力、妊娠、授乳
臨床研究では、女性の生殖能力に対するイブランスの影響に関するデータは得られませんでした。動物実験(前臨床)の結果によると、イブランスによる治療により男性の生殖能力が損なわれる可能性があります。男性は、イブランスによる治療を開始する前に、精子の保存(凍結)を検討する必要があります。
あなたが男性でイブランスを使用している場合は、治療中および投与中断中、およびイブランス治療の中止後少なくとも 97 日間は、性交中に(精管切除術が成功した場合でも)コンドームを使用する必要があります。
妊婦に対するイブランスの使用については、十分に管理された適切な研究はありません。動物実験の結果と薬の作用機序に基づいて、パルボシクリブを妊婦に投与すると胎児に害を及ぼす可能性があります。
この薬の投与を受けている妊娠の可能性のある女性、またはこの薬の投与を受けている妊娠の可能性のある女性のパートナーは、治療中、適切な避妊法(例:コンドームやペッサリーなどの二重バリア避妊法)を、最低21日間(女性)または97日間使用する必要があります。 (男性)治療終了後。あなたに合った効果的な避妊方法について医師と相談してください。
妊娠の可能性のある女性は、Ibrance による治療を開始する前に妊娠検査を受ける必要があります。
この薬は医師のアドバイスなしに妊婦が使用しないでください。妊娠が疑われる場合は、すぐに医師に知らせてください。
母乳中のイブランスの存在とその赤ちゃんへの影響については情報がありません。イブランスは乳児に重篤な副作用を引き起こす可能性があるため、イブランスによる治療中および最後の投与後 3 週間は授乳を中止する必要があります。治療における重要性を考慮して、授乳をやめるか、Ibrance の使用を中止するかについて医師と相談する必要があります。
機械の運転および操作能力への影響
車両の運転や機械の操作能力に対するイブランスの影響に関する研究は行われていない。
ただし、イブランスの使用により倦怠感(倦怠感)を感じる患者さんは、運転や機械の操作には注意が必要です。
注意:
この薬には乳糖が含まれています。ガラクトースや他の糖類に対する不耐症、ラップラクターゼ欠損症、またはグルコース-ガラクトース吸収不良などの遺伝性の問題がある患者さんは、この薬を服用する前に医師に相談してください。
イブランスに対する副作用
次のような症状がある場合は、すぐに医師に相談してください。
発熱、悪寒、脱力感、息切れ、出血、あざ。これらは重篤な血液疾患の兆候である可能性があります。
イブランスに対する副作用は以下のとおりです。
非常に一般的な反応 (この薬を使用している患者の 10% 以上で発生します):
感染症、好中球減少症(血液中の防御細胞の一種:好中球の減少)、白血球減少症(血液中の防御細胞:白血球の減少)、貧血(赤血球の数:赤血球の減少)、血小板減少症(血小板減少症)血液凝固の原因:血小板)、食欲減退、口内炎(口粘膜の炎症)、吐き気(気分が悪さ)、下痢、嘔吐、発疹(発疹)、脱毛症(脱毛)、倦怠感(倦怠感)、無力症(脱力感) 、発熱(発熱)。
一般的な反応 (この薬を使用している患者の 1% ~ 10% に発生します):
発熱性好中球減少症(発熱を伴う好中球の減少)、かすみ目、涙の増加、ドライアイ、味覚障害(味覚の変化)、鼻血(鼻血)、皮膚の乾燥、肝機能検査の異常(アラニンアミノトランスフェラーゼや肝酵素などの既知の肝酵素の増加)アスパラギン酸アミノトランスフェラーゼ)。
パルボシクリブとレトロゾールの併用療法を受けた患者で最も頻繁に報告された最も重篤な副作用(?1%)は次のとおりです。
感染症(4.6%)および発熱を伴う好中球減少症(血液中の防御細胞の一種である好中球の減少)(2.1%)。
パルボシクリブとフルベストラントの併用療法を受けた患者で最も頻繁に報告された最も重篤な副作用(?1%)は次のとおりでした。

感染症(4.1%)、発熱状態(1.4%)、好中球減少症(1.2%)、発熱を伴う好中球減少症(血液中の防御細胞の一種である好中球の減少)(0.9%)。
注意:
この製品は新薬であり、研究により許容できる有効性と安全性が示されていますが、たとえ正しく指示され使用されたとしても、予測できないまたは未知の有害事象が発生する可能性があります。この場合は医師または歯科医師に知らせてください。
イブランスの構成
プレゼンテーション
Ibrance 75 mg、100 mg、または 125 mg のパックに 21 個のハード カプセルが含まれています。
投与経路: 経口使用。
大人用。
構成
Ibrance 75 mg、100 mg、または 125 mg の各ハード カプセルには次のものが含まれています。
それぞれパルボシクリブ 75 mg、100 mg、または 125 mg。
賦形剤:
微結晶セルロース、乳糖一水和物、デンプングリコール酸ナトリウム、コロイド状二酸化ケイ素、ステアリン酸マグネシウム、およびハードゼラチンカプセル(ゼラチン、二酸化チタン、黄色酸化鉄および赤色酸化鉄)。
イブランスの過剰摂取
パルボシクリブに対する既知の解毒剤はありません。イブランスの過剰摂取に対する治療は、一般的な支持措置で構成する必要があります。

推奨される治療用量を超える用量を摂取した患者の多くは、誤って摂取したものです。
過剰摂取の場合に最も一般的に報告される有害事象は、好中球の減少や貧血など、骨髄内に存在する細胞の減少に関連するもので、悪化または長期化する可能性があります。場合によっては、胃腸症状(吐き気や嘔吐など)も報告されています。
誤って医師の処方量を超えてイブランスを服用した場合は、すぐに医師または病院に相談してください。 Ibrance ボックスを提示する必要があります。医師の治療が必要な場合があります。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
イブランスの薬物相互作用
服用しているすべての処方薬と市販薬のリストを書面で保管しておくことが重要です。ビタミン、ミネラル、その他の栄養補助食品などの製品も同様です。医師の診察を受けるとき、または病院に入院するときは、このリストを必ず持参してください。このリストは、緊急時に備えて持っていくべき重要な情報でもあります。
イブランスはレトロゾールまたはフルベストラントと併用できるため、これらの薬を服用する際には避けるべき他の薬についても医師に相談する必要があります。
イブランスは他の薬の作用に影響を与える可能性があります。
特に、以下の製品は、Ibrance による副作用のリスクを高める可能性があります。
- アンプレナビル、アタザナビル、デラビルジン、ホスアンプレナビル、インジナビル、ロピナビル、ネルフィナビル、リトナビル、サキナビル、テラプレビルは、HIV/AIDS ウイルス感染症の治療に使用されます。
- C型肝炎ウイルス感染症の治療に使用されるボセプレビルとテラプレビル。
- 抗菌薬のクラリスロマイシン、エリスロマイシン、テリスロマイシンは、細菌によって引き起こされる感染症の治療に使用されます。
- イトラコナゾール、ケトコナゾール、ミコナゾール、ポサコナゾール、ボリコナゾールは、真菌(真菌症など)によって引き起こされる感染症の治療に使用されます。
- ジルチアゼムとミベフラジルは高血圧と慢性狭心症の治療に使用されます。
- ネファゾドンはうつ病の治療に使用されていました。
- コニバプタンは、特定の血液電解質障害(例:低ナトリウム血症 – 血液中のナトリウム濃度の低下)の治療に使用されます。
- グレープフルーツ(グレープフルーツ)とグレープフルーツジュース。
Ibrance は、以下の製品に関連する副作用のリスクを高める可能性があります。
- キニジンは通常、心拍リズムの問題の治療に使用されます。
- 痛風の治療に使用されるコルヒチン。
- ジゴキシンは心不全や心拍リズムの問題の治療に使用されます。
- プラバスタチンとロスバスタチンは、高コレステロール値の治療に使用されます。
- スルファサラジンは関節リウマチの治療に使用されます。
- アルフェンタニルは手術の麻酔に使用されます。フェンタニルは、麻酔薬だけでなく痛み止めとしても前処置で使用されます。
- シクロスポリン、エベロリムス、タクロリムスおよびシロリムスは、臓器移植における拒絶反応を防ぐために使用されます。
- ジヒドロエルゴタミンとエルゴタミンは片頭痛の治療に使用されます。
- ピモジドは、統合失調症および慢性精神病の治療に使用されます。
- 糖尿病を治療するメトホルミン。
以下の製品は、Ibrance の有効性を低下させる可能性があります。
- カルバマゼピン、フェルバメート、フェノバルビタール、フェニトイン、およびプリミドンは、けいれんや発作を止めるために使用されます。
- リファブチン、リファンピン、リファペンチンは結核の治療に使用されます。
- ネビラピンは HIV/AIDS ウイルス感染症の治療に使用されます。
- エンザルタミドは、特定の種類のがんの治療に使用されます。
- セントジョーンズワート、軽度のうつ病や不安症の治療に使用されます。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
イブランスという物質の働き
有効性の結果
研究 1 – パルボシクリブ (活性物質) とレトロゾール (PALOMA-1) の併用の第1/2相ランダム化試験
パルボシクリブの有効性は、進行性疾患に対する全身治療を受けていないER陽性、HER2陰性進行乳がんの閉経後女性を対象とした、パルボシクリブとレトロゾールの併用療法とレトロゾール単独療法の無作為化非盲検多施設共同研究で評価された(PALOMA- 1)。
この研究は、パルボシクリブとレトロゾールの併用の安全性と忍容性を確認するために設計された限定された第 1 相パート (N = 12) と、それに続く有効性と安全性を評価するために設計された無作為化第 2 相パート (N = 165) で構成されました。 ER陽性、HER2陰性の進行乳がんを患う閉経後女性の第一選択治療における、レトロゾール単独と比較したパルボシクリブ(活性物質)とレトロゾールの併用試験。
無作為化は、疾患部位(内臓、骨のみ、その他)および無病期間(術後補助療法終了から疾患再発まで>12ヶ月対補助療法終了から疾患再発または進行疾患まで~12ヶ月)に従って層別化された。また)。

ベースライン時の患者の臨床的および人口統計的特徴は、年齢、人種、疾患部位、ステージ、および以前の治療法に関して研究群間で概してバランスがとれていた。以下の表 1 は、初期評価時の臨床的および人口統計的特徴の詳細な概要を示しています。
表 1. 治療の種類別の初期評価時の臨床的および人口統計的特徴の概要 – 研究 1 (治療意図のある集団)
|
パラメータ |
パルボシクリブ(活性物質)とレトロゾール(N = 84) |
レトロゾール (N = 81) |
|
年齢(歳) |
||
|
中央値 (最小、最大) |
62.5(41、89) |
64.0 (38, 84) |
|
lt;65 [n (%)] |
47(56.0) |
42(51.9) |
|
?65 [n (%)] |
37(44.0) |
39 (48.1) |
|
ECOG パフォーマンス ステータス [n (%)] |
||
| 0 | 46(54.8) |
45(55.6) |
| 1 | 38(45.2) |
36(44.4) |
|
疾患部位* [n (%)] |
||
|
内臓 |
39(46.4) |
40(49.4) |
|
骨のみ |
17 (20.2) |
14 (17.3) |
|
その他 |
28(33.3) |
27(33.3) |
|
無病期間* [n (%)] |
||
|
gt;補助療法終了から疾患再発まで12か月 |
37 (44.1) |
36(44.4) |
|
?術後補助療法の終了から疾患の再発または新たな進行疾患が発生するまでの12か月 |
47(56.0) |
45(55.6) |
|
以前の全身療法[n (%)] |
||
|
いいえ |
44(52.4) |
37(45.7) |
| はい | 40(47.6) |
44(54.3) |
|
化学療法 [n (%)] |
34(40.5) |
37(45.7) |
|
アントラサイクリン |
26(31.0) |
25(30.9) |
|
タキサン |
12(14.3) |
14 (17.3) |
|
その他 |
34(40.5) |
37(45.7) |
|
抗ホルモン療法 [n (%)] |
27(32.1) |
28(34.6) |
|
タモキシフェン |
24(28.6) |
24(29.6) |
|
アロマターゼ阻害剤 |
14 (16.7) |
12(14.8) |
|
アナストロゾール |
8(9.5) |
11(13.6) |
|
エキセメスタン |
4 (4.8) |
2(2.5) |
|
レトロゾール |
2 (2.4) |
1 (1,2) |
|
その他 |
2 (2.4) | 0 |
*ランダム化に基づいています。
略語:
ECOG (Eastern Cooperative Oncology Group) = 東部腫瘍学研究グループ。最大 = 最大値。 Min = 最小値。 N/n = 患者数。
研究の主要評価項目である無増悪生存期間(PFS)は、固形腫瘍における反応評価基準(RECIST – 固形腫瘍における反応評価基準)バージョン 1.0 に従って研究者によって評価されました。
パルボシクリブ+レトロゾール群の患者のPFS中央値(mPFS)は20.2カ月(95%信頼区間[CI]:13.8、-27.5)、レトロゾール単独群の患者では10.2カ月(95%信頼区間:5.7、-12.6)であった。アーム。観察されたハザード比 (HR – ハザード比) は、p 値 = 0 の層別片側ログランク検定で、パルボシクリブ (有効成分) とレトロゾールの併用療法が有利で 0.488 (95% CI: 0.319; -0.748) でした。 0004。
一次有効性結果は、研究 1 にランダム化された全患者の最終 PFS 分析で得られました (以下の図 1 を参照)。
図 1. 無増悪生存率に関するカプラン マイヤー曲線 (フェーズ 2、医師による評価、治療意図のある集団)
CI = 信頼区間。 LET = レトロゾール; N = 患者数。 PAL = パルボシクリブ (活性物質); PFS = 無増悪生存期間。
研究 2 – パルボシクリブ(活性物質)とレトロゾール(PALOMA-2)の併用のランダム化第 3 相試験5,6
パルボシクリブ(活性物質)とレトロゾールの併用の有効性と、プラセボとレトロゾールの併用の有効性が、進行性乳がんまたは転移性ERの女性を対象に実施された国際無作為化二重盲検プラセボ対照多施設並行群間試験で評価された。 -進行性疾患に対してこれまでに全身治療を受けていない陽性、HER2陰性(PALOMA-2)患者。
合計666人の閉経後女性が、パルボシクリブ+レトロゾール群またはプラセボ+レトロゾール群のいずれかに2:1で無作為に割り付けられ、疾患部位(内臓、非内臓)に応じて(ネオの終了からの無病期間で)層別化された。 )疾患再発までの補助治療(新規転移、補助治療終了から疾患再発まで12か月、gt;補助治療終了から疾患再発まで12か月)および(ネオ)補助抗悪性腫瘍剤の種類治療(以前のホルモン療法、以前のホルモン療法なし)。致死性の短期合併症のリスクがある進行性の症候性播種性内臓疾患患者(制御不能な胸水[胸水、心膜、腹膜]、肺リンパ管炎、肝臓病変が50%を超える患者を含む)は、対象に含める資格がなかった。研究。
患者は、客観的な疾患の進行、症状の悪化、耐えられない毒性、死亡、または同意の撤回のいずれかが先に起こるまで、割り当てられた治療を受け続けました。治療アーム間のクロスオーバーは許可されませんでした。
患者は、初期評価時の人口統計および疾患の臨床的特徴に従って、パルボシクリブ(有効成分)+レトロゾール群とプラセボ+レトロゾール群の間でマッチングされました。この研究に登録された患者の年齢中央値は62歳(範囲28~89歳)であった。進行乳がんと診断される前に、患者の48.3%が化学療法を受けており、56.3%がネオ(ネオ)補助療法設定で事前に抗ホルモン療法を受けていたのに対し、患者の37.2%は(ネオ)補助療法設定で事前に全身療法を受けていなかった。患者の大多数 (97.4%) は、初期評価時に転移性疾患を患っていました。患者の22.7%は骨疾患のみを有し、患者の49.2%は内臓疾患を有していた。
研究の主要評価項目(PFS)は、RECIST バージョン 1.1 に従って研究者によって評価されました。二次有効性エンドポイントには、客観的奏効率(ORR)、奏効率期間(DR)、臨床利益率(CBR)、全生存期間(OS)、安全性、EQ-5Dスコア、健康関連の生活の質(QoL)の変化が含まれていました。評価は、FACT-B アンケートを使用して評価されました。
この研究は、PFS を改善するという主な目的を達成しました。推定HRは0.576(95%CI:0.463;0.718)で、p値<0.000001の層別片側ログランク検定でパルボシクリブ(活性物質)とレトロゾールの併用療法が有利でした。 mPFSは、パルボシクリブ+レトロゾール群の患者では24.8カ月(95%CI:22.1;推定不能[NE])、プラセボ+レトロゾール群では14.5カ月(95%CI:12.9;17.1)だった。 PFSに対する併用治療の効果は、独立したX線写真解析によっても裏付けられ、推定HRは0.653(95%CI:0.505、0.844)でした。
PALOMA-2 研究の有効性データを表 2 にまとめ、PFS のカプラン マイヤー曲線を図 2 に示します。
表 2. PALOMA-2 研究の有効性結果 (治療意図のある集団)
|
締め切り日: 2016 年 1 月 26 日 |
||
|
パルボシクリブ (活性物質) とレトロゾール (N=444) |
プラセボとレトロゾール (N=222) |
|
|
無増悪生存期間 |
||
|
調査員の評価、イベント数 (%) |
194 (43.7%) |
137 (61.7%) |
|
中央値 [月 (95% CI) |
24.8 (22.1; 北東) |
14.5 (12.9; 17.1) |
|
ハザード比 (95% CI) と片側 p 値 |
0.576 (0.46; 0.72)、plt;0.000001 |
|
|
独立した X 線撮影分析、イベント数 (%) |
152 (34.2%) |
96 (43.2%) |
|
中央値 [月 (95% CI) |
30.5 (27.4; 北東) |
19.3 (16.4; 30.6) |
|
ハザード比 (95% CI) と片側 p 値 |
0.653 (0.505; 0.84)、p=0.000532 |
|
|
二次有効性エンドポイント (治験責任医師による評価) |
||
|
ORR (95% CI) |
46.4 (41.7; 51.2) |
38.3 (31.9; 45.0) |
|
ORR (測定可能な疾患) [% (95% CI)] |
60.7 (55.2; 65.9) |
49.1 (41.4; 56.9) |
|
CBR [% (95% CI)] |
85.8 (82.2; 88.9) |
71.2 (64.7; 77.0) |
N = 患者数。 CI = 信頼区間。 NE = 推定できない。 TORR = 客観的な応答率。 CBR = 臨床利益率。
副次エンドポイントの結果は、RECIST 1.1 に従って確認された応答と未確認の応答に基づいています。
図 2. 無増悪生存期間に関するカプラン マイヤー プロット (医師の評価、治療意図のある集団) – Paloma-2 研究
PAL=パルボシクリブ(活性物質); LET=レトロゾール; PCB=プラセボ。
表 3: PALOMA-2 研究による内臓疾患および非内臓疾患における有効性結果 (治療意図のある集団)
N = 患者数。 CI = 信頼区間。 ORR = RECIST 1.1 基準に基づく確認済みおよび未確認の応答に基づく客観的な応答率。 TTR = 最初の腫瘍反応までの時間。
治療効果の内部一貫性を調査するために、ベースライン時の人口統計および臨床疾患の特徴に基づいて、サブグループごとに事前に指定された一連の PFS 分析が実行されました。層別化因子とベースライン特性によって定義されるすべての個々の患者サブグループにおいて、パルボシクリブとレトロゾールの併用療法で疾患の進行または死亡のリスクの低下が観察されました。これは、内臓転移のある患者(HR 0.67 [95% CI: 0.50、0.89]、mPFS: 19.2 vs 12.9 か月)または内臓転移のない患者(HR 0.48 [95% CI: 0.34; 0.67]、mPFS: not)で明らかでした。 [NR]に達した患者(HR 0.36 [95% CI: 0.22; 0.59]、mPFS: NR対11.2か月)または骨のみの疾患がない患者(HR 0.65 [95% CI: 0.51、 0.84]、mPFS: 22.2対14.5 か月)。同様に、免疫組織化学 (IHC) で腫瘍が Rb タンパク質発現陽性であった 512 人の患者において、パルボシクリブとレトロゾールの併用療法で疾患の進行または死亡のリスクの低下が観察されました (HR 0.531 [95% CI: 0.42, 0.68]、 mPFS は 13.7 か月と比較して 24.2 か月)。 IHCによる腫瘍のRbタンパク質発現が陰性だった51人の患者において、パルボシクリブ+レトロゾール併用療法による疾患進行または死亡のリスクの減少は統計的に有意ではなかった(HR 0.675 [95% CI : 0.31, 1.48]、mPFS) NR の 18.5 か月と比較)。
がん治療乳房機能評価(FACT-B)アンケートにおける複合エンドポイント悪化までの時間(TTD)の分析。ベースライン評価から最初にFACTスコアが7ポイント低下するまでの時間として定義 -B 、Cox 比例ハザード モデルとロングランク テストを使用した生存分析手法に基づいて実施されました。パルボシクリブ+レトロゾール群とプラセボ+レトロゾール群の間のFACT-B合計スコアにおいて、TTDにおける統計的に有意な差は観察されなかった(HR 1.042 [95% CI: 0.838, 1.295];片側値 p = 0.663。
研究 3: パルボシクリブ (活性物質) とフルベストラントの併用のランダム化第 3 相試験
パルボシクリブとフルベストラントの併用とプラセボとフルベストラントの併用の有効性が、閉経期に関係なく、HR陽性、HER2陰性の進行乳がんの女性を対象に実施された国際無作為化二重盲検多施設並行群間試験で評価された。以前の内分泌療法後に病気が進行した状態。
補助内分泌療法終了後12ヶ月以内、または進行性疾患に対する内分泌療法終了後1ヶ月以内に疾患が進行した閉経前/閉経後の女性計521人を、パルボシクリブ(活性型)投与群:2:1に無作為に割り付けた。物質)+フルベストラント群、またはプラセボ+フルベストラント群で、以前の治療で記録されたホルモン療法に対する感受性、研究登録時の閉経状態(閉経前/閉経後と閉経後)および内臓転移の有無に従って層別化した。閉経前/閉経周辺期の女性には、LHRHアゴニストであるゴセレリンが投与されました。症候性および進行性/転移性の播種性播種性内臓疾患を有し、致死的な短期合併症のリスクがある患者(制御不能な胸水[胸水、心膜、腹膜]、肺リンパ管炎、および50%を超える肝臓病変を有する患者を含む)は、対象外であった。研究への登録。
患者は、客観的な疾患の進行、症状の悪化、耐えられない毒性、死亡、または同意の撤回のいずれかが先に起こるまで、割り当てられた治療を受け続けました。治療アーム間のクロスオーバーは許可されませんでした。
患者は、パルボシクリブ+フルベストラント群とプラセボ+フルベストラント群の間で、ベースライン時の予後および人口統計学的特徴のバランスがとれていた。各治療群の患者の大部分は白人で、平均年齢は57歳(範囲は29~88歳)で、以前のホルモン療法に対する感受性が記録されており、閉経後であった。
約20%は閉経前/閉経周辺期でした。すべての患者は以前に全身療法を受けており、各治療群の大多数は以前に化学療法を受けていました。半数以上(62%)は東部腫瘍学共同研究グループ(ECOG)のパフォーマンスステータスが0で、60%が内臓転移を有し、60%が一次診断で以前に1回以上の内分泌療法を受けていた。
研究の主要評価項目(PFS)は、RECIST バージョン 1.1 基準に従って研究者によって評価されました。補足的な PFS 分析は、独立した中央放射線検査に基づいていました。副次評価項目には、ORR、DOR、CBR、OS の安全性、QoL の変化、TTD が含まれていました。全体的な QoL と痛みを含む患者報告の転帰は、がん研究治療機構 (EORTC) の生活の質質問票 (QLQ-C30) および乳がんモジュール質問票 (BR23) を使用して測定されました。
この研究は、最終解析で計画されたPFSイベントの82%に基づいて、中間解析で研究者が評価したPFS延長を評価するという主要評価項目を達成した。結果は、事前に指定されたHaybittle-Peto有効性閾値 (? = 0.00135) を超え、統計的に有意な PFS の延長と臨床的に関連した治療効果を示しました。
層別解析からの推定HRは、パルボシクリブ(活性物質)とフルベストラントの併用が有利で、0.422(95%CI:0.318; 0.560; plt;0.000001片側)でした。
mPFSは、パルボシクリブ+フルベストラント群では9.2カ月(95%CI:7.5)、プラセボ+フルベストラント群では3.8カ月(95%CI:3.5;-5.5)だった。
表 4: 有効性の結果 – 主要評価項目(治験責任医師の評価、治療意図のある集団)
CI = 信頼区間。 PFS = 無増悪生存期間。
表 5: 有効性の結果 – 副次評価項目(治験責任医師の評価、治療意図のある集団)
結果は、確認された応答と未確認の応答に基づいています。
CBR = 臨床利益率。 CI = 信頼区間。 N = 患者数。 NE = 推定できない。 ORR = 客観的な応答率。
図 3. 無増悪生存期間に関するカプラン・マイヤープロット(医師の評価、治療意向集団) – PALOMA-3 研究(カットオフ日 2015 年 10 月 23 日)
FUL = フルベストラント。 PAL = パルボシクリブ (活性物質); PCB = プラセボ。
表 6. PALOMA-3 研究による内臓疾患および非内臓疾患における有効性結果(治療意図のある集団)
N = 患者数。 CI = 信頼区間。 ORR = RECIST 1.1 に基づく確認済みおよび未確認の応答に基づく客観的な応答率。 TTR = 最初の腫瘍反応までの時間。
パルボシクリブとフルベストラントの併用療法における PFS の延長は、個々の患者サブグループでも実証されており、この研究の PFS 利益に関する知見の内部一貫性が裏付けられ、独立した中央審査監査分析と 40.5% で実施された盲検 (BICR) ランダムサンプリングによって裏付けられました。ランダム化された 521 人の患者のうち (N = 211)。
閉経前/閉経周辺期の女性が研究に登録され、研究 2 の少なくとも 4 週間前と研究 2 の全期間にわたって LHRH ゴセレリナ拮抗薬の投与を受けました。
よりフレーバーの多いパロシクリベ群(活性物質)は、閉経前/閉経周辺期の集団(HR = 0.435 [95%: 0.228-0.831]および閉経後の集団(HR = 0.409 [95%: 0.298-0.560]))において同様の臨床利益を示しました。同様に、最も風味豊かなパロサイクライブ群(活性物質)の MPFS は、閉経前/閉経周辺期では 9.5 か月(95%CI: 7.2-n)であったのに対し、閉経後シナリオでは 9.2 か月(95%CI: 7.5-in)でした。最も風味豊かなプラセボ群の MPFS は、閉経前/閉経周辺期では 5.6 か月 (95%CI: 1.8; NE) であったのに対し、閉経後シナリオでは 3.7 か月 (95%CI: 3.5; -5; 、5) でした。患者から報告された症状は、EORTC QLQ-C30 および EORTC QLQ-BR23 を使用して評価されました。より風味豊かなパロサイクライブ群(活性物質)の合計 335 人の患者と、最も風味豊かなプラセボ群の 166 人の患者が、最初の評価来院時および少なくとも最初の評価後の来院時にアンケートに回答しました。
よりフレーバーを加えたパルボシクリブ(活性物質)群とフルベストスタントラ プラセボを加えた群の間で全体的な健康/QOLを比較した結果、パロシクリブ(活性物質)をより多く含んだフルベストスタント群を支持する統計的に有意な差が示されました。腕 (それぞれ -0.9 [95%CI: -2.5; 0.7]対-4.0 [95%IC: -6.3; 1.7]; 両側の値 p = 0.0313)。さらに、感情機能との比較でも、最も効果的なプラセボ群と比較して、より風味豊かなパルボサイクリブ群を支持する統計的に有意な差が示されました(2.7 [95%CI: 1.1; 4.3]対-1.9 [95%IC: -4.2]) ; 0.5]、それぞれ。
悪化時間(TTD)は、最初の評価と最初の痛み症状スコアの 10 ポイントの増加の間の時間として事前に定義されました。パルボシクリブ(有効成分)フルベストラントラの追加により、症状の改善がもたらされ、最も風味豊かなプラセボと比較して疼痛症状スコアのTTDが有意に遅延しました(中央値8か月対2.8か月、HR 0.64 [95%IC: 0.49;
薬理学的特徴
薬力学特性
Palocyclibe (活性物質) は経口投与され、サイクリン依存性ジョーク (CDK) 4 および 6 の可逆性が高く選択性の高い小さな分子の阻害剤です。サイクリナ D1 および CDK4/6 は、細胞増殖につながる複数の下流シグナル伝達経路です。 CDK4/6 の阻害により、パルボシクリベ (活性物質) は細胞増殖を減少させ、G1 細胞の細胞周期期への進行を阻止しました。癌細胞株パネルでのパロサイクライブ(活性物質)試験











