クロミッドは、このリーフレットに記載されている症状では排卵しない患者、およびクエン酸クロミフェンが禁忌ではない患者にのみ適応されます。治療の前に、他の不妊原因を除外するか、適切に治療する必要があります。

この薬はどのように作用するのでしょうか?
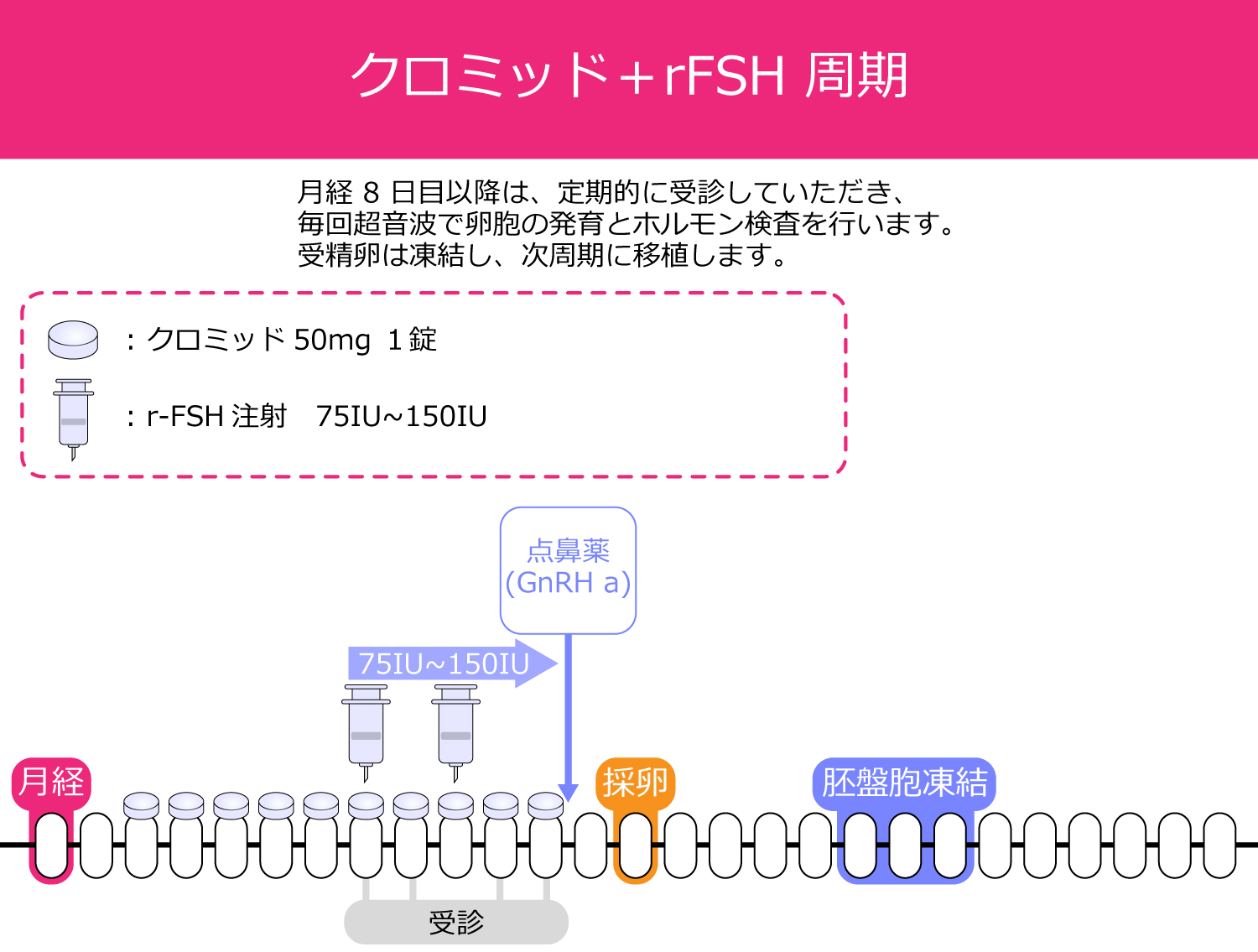
この薬は卵子の成長を助け、受精のために卵子が卵巣から放出されるようにします。排卵は通常、クロミッド服用後6〜12日で起こります。
クロミッドの禁忌
この薬は、クエン酸クロミフェンまたはその成分のいずれかに対して過敏症 (アレルギー) のある患者には禁忌です。
妊娠中および授乳中の使用
妊娠中はクロミッドを投与しないでください。
妊娠初期における不用意なクロミッドの投与を避けるために、各治療周期中に適切な検査を使用して排卵が起こったかどうかを判断する必要があります。たとえば、各治療周期を通して基礎体温を測定し、患者を注意深く観察して排卵の兆候があるかどうかを判断する必要があります。排卵。患者は、次のクロミッド治療サイクルを開始する前に妊娠検査を受ける必要があります。
その他の禁忌
クロミッドによる治療は、肝疾患または肝機能障害の病歴のある患者、ホルモン依存性腫瘍のある患者、または原因不明の異常子宮出血(子宮出血)、卵巣嚢腫(多嚢胞性卵巣を除く)のある患者には禁忌です。嚢胞が発生する可能性があります。
治療中に妊娠した場合は、投薬を中止し、医師に相談してください。授乳中の場合は医師に伝えてください。
この薬は、妊娠している女性、または治療中に妊娠する可能性のある女性は使用しないでください。
この製品にはタートラジンイエロー染料が含まれており、特にアセチルサリチル酸にアレルギーのある人に、気管支喘息などのアレルギー反応を引き起こす可能性があります。
糖尿病の方は注意してください:
砂糖が含まれています。
クロミッドの使い方
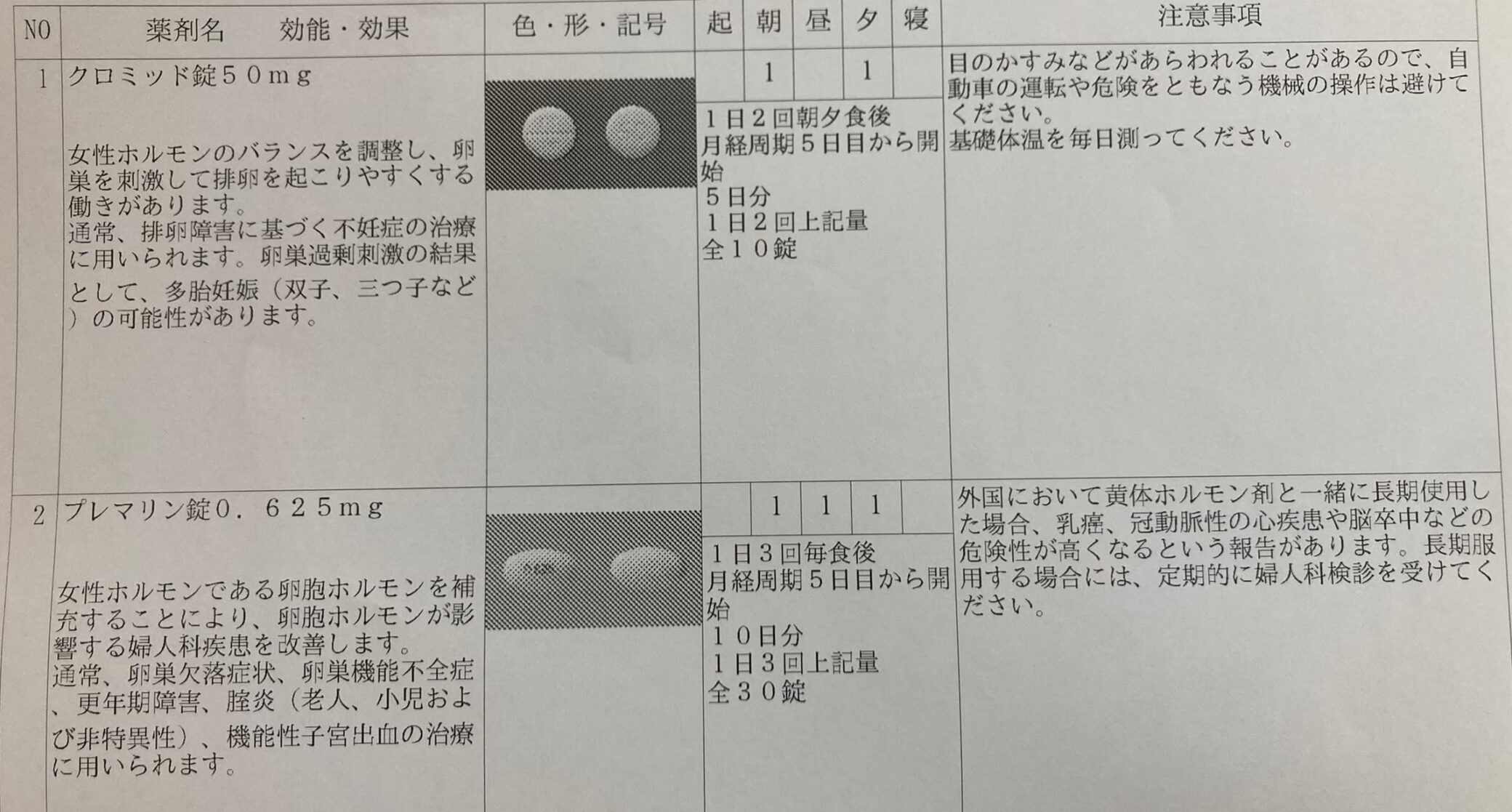
治療は 3 サイクルで構成され、医師の裁量により連続または交互に行うことができます。治療後は妊娠に努めるべきです。ただし、治療中に妊娠した場合は、薬の服用を中止する必要があります。治療の最初のサイクルで推奨される用量は、1 日あたり 50 mg (1 錠) を 5 日間です。月経のない患者さんでは、月経周期のどの時期でも治療を開始できます。プロゲステロンを使用して月経を誘発する予定がある場合、または自然月経が発生した場合は、周期の5日目からクロミッドを投与する必要があります。この用量で排卵が起こった場合、次の 2 サイクルで用量を増やす利点はありません。最初の治療サイクル後に排卵が起こらない場合は、前回の治療から 30 日後に 1 日あたり 100 mg を 5 日間投与する 2 番目のサイクルを開始する必要があります。
用量の増加は、5 日間 100 mg/日の用量および期間を超えてはなりません。クロミッドに反応する患者の大多数は、治療の最初のサイクルと 3 サイクル後に排卵します。この治療法を評価するには十分です。この期間内に排卵性月経が起こらない場合は、診断を再検討する必要があります。排卵の証拠が見られない患者には、3 サイクル後に治療を継続することはお勧めできません。
長期間の周期的治療の安全性は証明されていないため、6 周期(3 排卵周期を含む)後に治療を継続することはお勧めできません。
特別な集団
多嚢胞性卵巣症候群の患者など、下垂体ゴナドトロピンに対する異常な感受性が疑われる場合には、低用量または低治療サイクル期間での特別なケアが特に推奨されます。

クロミッドを長期間投与すると、コレステロール合成を妨げる可能性があります。長期治療を受けている患者は、コレステロールの前駆体であるデスモステロールの血中濃度が高い場合があります。
治療の時間、用量、期間を常に尊重し、医師のアドバイスに従ってください。
医師の知識なしに治療を中止しないでください。
この薬は割ったり、開けたり、噛んだりしないでください。
この薬を使い忘れた場合はどうすればよいですか?
飲み忘れた錠剤を補うために、同時に 2 錠服用しないでください。投与を忘れると、治療や排卵周期に支障をきたす可能性があります。さらなる指導を受けるために、できるだけ早く医師に知らせてください。
疑問がある場合は、薬剤師、医師、歯科医師に相談してください。
クロミッドの予防措置
卵巣過剰刺激症候群 (OHS)
卵巣過剰刺激症候群(OHS)は、クロミッド単独またはゴナドトロピンと組み合わせて治療を受けている患者で報告されています。重度のOHSSのまれなケースが報告されており、次の症状が発生します – 心膜液貯留(心臓周囲の過剰な体液)、アナサルカ(全身性の浮腫または腫れ)、水胸(胸腔内の過剰な体液)、急性腹症、心不全腎臓(腎機能の低下)、肺水腫(肺内の体液の蓄積)、卵巣出血(卵巣内の出血)、深部静脈血栓症(静脈内での血栓の形成または存在)、卵巣捻転、急性呼吸ストレス。妊娠の結果、重度の症候群が急速に進行する可能性があります。
クロミッド療法に伴う異常な卵巣肥大の可能性を最小限に抑えるために、良好な結果が予測される最低用量を使用することが推奨されます。クロミッドによる治療中または治療後に、腹部または骨盤の痛み、体重増加、不快感、および/または腹部容積の増加が発生した場合には、患者に医師に相談するようアドバイスしてください。クロミッド治療の中止後、数日間は卵巣の最大拡張が起こらない場合があります。ゴナドトロピンに対して異常に敏感な多嚢胞性卵巣症候群の患者の中には、通常の用量のクロミッドに対して過剰な反応を示す場合があります。
クロミッドの使用中に何らかの異常がある場合は、医師が診察し、骨盤の婦人科検査で卵巣嚢腫が出現していないかどうかを評価する必要があります。このようなことが起こった場合、治療前のサイズに完全に戻るまで治療は医師によって一時停止されます。クロミッドの使用に伴う卵巣の肥大または嚢胞形成は、通常、治療を中止してから数日または数週間後に自然に解消します。これらの患者のほとんどは保守的に観察する必要があります。次の治療サイクルの用量および/または期間を減らす必要があります。
視覚症状
クロミッドによる治療中または治療直後に、かすみ目や点や閃光(閃光暗点)などのその他の視覚症状が発生することがあります。これらの視覚障害は通常、可逆的です。しかし、クロミッド治療を中止した後でも、視覚障害が長引くケースが報告されています。視覚障害は、特に治療の用量と期間が増加すると、回復不能になる場合があります。これらの視覚症状の重要性はまだ解明されていません。視覚的な異常が発生した場合は、治療を中断し、詳細な眼科検査を実施する必要があります。
その他の注意事項
子宮筋腫患者にクロミッドを使用する場合は、子宮筋腫がさらに大きくなる可能性があるため注意が必要です。
クロミッドの市販後の経験において、高トリグリセリド血症(トリグリセリド値の上昇)の症例が報告されています。高脂血症の家族または既往歴、推奨量よりも高い用量の使用、および/またはクロミッドによる治療期間の延長は、高トリグリセリド血症のリスクと関連しています。このような患者では、血漿トリグリセリドを定期的にモニタリングすることが示唆される可能性があります。
妊娠
妊娠中はクロミッドを使用しないでください。

子宮外妊娠(子宮腔外で起こる妊娠)
クロミッド治療後に妊娠した女性では、子宮外妊娠(卵管および卵巣を含む)の可能性が高くなります。
催奇形性/非催奇形性の影響
臨床研究中にクロミッドによる治療によって誘発された妊娠における先天異常の報告の一般的な発生率は、一般集団で観察される範囲内です。
妊娠喪失
クロミッドの臨床研究中のすべての診断を受けた患者の経験では、妊娠喪失(単数または複数)または胎児喪失率が 21.4% であることが実証されました。
不妊への影響: 多胎妊娠
クロミッド治療に関連して多胎妊娠の可能性が高くなります。この薬を服用する前に、多胎妊娠から生じる潜在的な合併症やリスクについて患者と話し合う必要があります。臨床研究中に、結果が報告された妊娠患者の多胎妊娠の発生率は7.9%(2,369人中186人)でした。
この薬は、妊娠している女性、または治療中に妊娠する可能性のある女性は使用しないでください。
授乳中
クロミッドが母乳中に排泄されるかどうかは不明です。クロミッドは授乳を減らす可能性があります。
車両の運転や機械の操作能力の変化
車の運転や機械の操作などの活動は、特に照明条件が悪い場合に危険を伴う可能性があります。これらの症状の原因は不明です。
この製品にはタートラジンイエロー染料が含まれており、特にアセチルサリチル酸にアレルギーのある人に、気管支喘息などのアレルギー反応を引き起こす可能性があります。
糖尿病の方は注意してください:
砂糖が含まれています。
クロミッドの副作用
この薬は望ましくない反応を引き起こす可能性があります。アレルギー反応がある場合は、薬の使用を中止し、望ましくない反応がある場合は医師に知らせてください。
非常に一般的な反応(この薬を使用している患者の 10% 以上で発生します)
卵巣のサイズの増加、血管運動性のフラッシュ。
一般的な反応 (この薬を使用している患者の 1% ~ 10% で発生)
視覚症状、腹部不快感、吐き気と嘔吐、頭痛、子宮からの異常出血、排尿痛。
まれな反応(この薬を使用している患者の 0.01% ~ 0.1% で発生します)
白内障、視神経炎、発作。
その他の考えられる反応
一時的な感覚異常、めまい、不安、うつ病、気分障害、神経過敏、不眠症、皮膚炎、蕁麻疹、脱毛症、頻脈、動悸、膵炎、トランスアミナーゼの増加、子宮内膜厚の減少、高トリグリセリド血症。内分泌依存性の新生物/腫瘍の発生またはそれらの悪化に関する個別の報告が受けられています。
高トリグリセリド血症(場合によっては膵炎)は、既存の高トリグリセリド血症や家族歴がある患者、および/または説明書に記載されている用量推奨を超える用量および治療期間を持つ患者で観察されています。クロミッド治療中に子宮内膜症の新たな症例や、既存の子宮内膜症が悪化した症例が報告されています。
子宮内および子宮外の同時妊娠を含む複数の妊娠が報告されています。クロミッド治療中に妊娠した女性では、子宮外妊娠(卵管および卵巣を含む)の可能性が高くなります。
一般に、かすみ目、点や閃光(視覚暗点)として説明される視覚症状は、総線量の増加とともに発生率が増加します。これらの症状は、画像検査後の増強または長期化によるものと考えられており、これも報告されています。症状は多くの場合、初めて現れるか、過度の光/明るさの環境にさらされると悪化します。眼科的に定義された暗点、フォスフェン、および視力の低下が報告されています。これらの視覚障害は通常、可逆的です。しかし、クロミッド治療を中止した後に視覚障害が長引くケースが報告されています。
視覚障害は、特に治療の用量と期間が増加すると、回復不能になる場合があります。
薬の使用により望ましくない反応が現れた場合は、医師、歯科医師、または薬剤師に知らせてください。
また、顧客サービスを通じて会社に通知してください。
クロミッドの成分
プレゼンテーション
50mgの錠剤。 10錠入りパック。
大人用。
経口使用。
構成
各タブレットには次のものが含まれています。
|
クエン酸クロミフェン |
50mg |
|
賦形剤* 適量 |
1錠 |
*デンプン、タートラジンイエロー染料、ステアリン酸マグネシウム、乳糖一水和物、スクロース。
クロミッドの過剰摂取
クロミッドの急性中毒の症例は報告されていませんが、過剰摂取の記録された症例の数は少数です。過剰摂取の場合は、適切な補助措置を講じる必要があります。
この薬を大量に使用する場合は、すぐに医師の診察を受け、可能であれば薬のパッケージまたは説明書を持参してください。さらに詳しいガイダンスが必要な場合は、0800 722 6001 までお電話ください。
クロミッドの薬物相互作用
他の薬剤との相互作用についての具体的な報告はありませんが、医師は併用されている他の薬剤、特にコレステロール合成に作用する薬剤について患者から知らされる必要があります。
他の薬を服用している場合は、医師または歯科医に伝えてください。
医師の知識なしに薬を使用しないでください。健康に危険を及ぼす可能性があります。
クロミッドという物質の作用
有効性の結果
1964年から1978年までの11件の出版物をレビューしたところ、クエン酸クロミフェン(活性物質)を投与された排卵障害患者5,154人のうち35%で妊娠が起こったことが示されました。ニューイングランド・ジャーナル・オブ・メディシン誌に掲載された研究では、クロミフェンは女性の不妊症の治療においてメトホルミンよりも効果的であることが示された。多嚢胞性卵巣症候群は、米国の女性の 7% ~ 8% が罹患しており、女性の不妊症の主な原因である可能性があります。多嚢胞性卵巣症候群の不妊女性626人を追跡調査した。
このうち、208人はメトホルミンとプラセボで、209人はクエン酸クロミフェン(活性物質)とプラセボで、209人はクロミフェンとメトホルミンの併用で6カ月以上治療を受けた。妊娠が確認されるとすぐに投薬は中止され、赤ちゃんが生まれるまで女性の経過観察が行われた。クロミフェン群の出生率は22.5%(209人中47人)であったのに対し、メトホルミン群では7.2%(208人中15人)であった。 2つの薬剤を組み合わせて投与されたグループでは、26.8%(209人中56人)でした。多胎妊娠率はクロミフェン投与群で6%、メトホルミン投与群で0%、2剤併用群で3.1%だった。
妊娠第 1 期の胎児喪失は 3 つのグループで有意な差はありませんでした。しかし、排卵した女性の受胎率は、クロミフェン群(39.5%)と併用群(46%)で有意に高く、メトホルミン群(21.7%)では低かった。妊娠合併症を除いて、副作用はすべてのグループで同様でしたが、メトホルミンを投与されたグループでは胃腸の副作用がより頻繁に発生し、血管運動神経症状と排卵障害の症状はあまり頻繁ではありませんでした。
研究者らは、女性不妊症の治療に使用される部分エストロゲン受容体アゴニストであるクロミフェンが、妊娠を促進すると考えられている糖尿病の治療薬であるメトホルミンよりも効果的であると結論付けた。
プラセボ対照のランダム化クロスオーバー臨床試験では、原因不明の不妊症に悩む女性 118 人にクロミフェンまたはプラセボが 3 か月間投与されました。 3か月の受胎率が最も大きく上昇したのは、不妊症の女性にクロミフェンを3年以上投与した場合でした(クロミフェン14%、プラセボ3%)。著者らは、原因不明の不妊症期間が3年未満のカップルは本質的に正常であるが、不妊症期間が3年を超える患者では、クロミフェン療法によって微妙な排卵障害が修正されることが多いと示唆した。
別のランダム化研究では、原因不明の不妊症または子宮内膜症を外科的に矯正した67組のカップルを対象に、クエン酸クロミフェン(活性物質)と子宮内授精(IUI)による治療が排卵周囲性交と比較して生殖能力の増加をもたらすかどうかを評価した。 148 回の治療周期で 14 回の妊娠が発生しましたが、これは未治療の 150 周期での 5 回の妊娠よりも有意に多かったです。

クロミフェンは、原因不明の不妊症における経験的治療法として使用されるだけでなく、生殖補助医療と併用されても使用されています。排卵中の女性に投与すると複数の卵胞の発育を促進し、複数の排卵をもたらし、黄体期のプロゲステロンレベルを上昇させます。単独で使用することも、生殖補助医療の準備として過剰排卵を制御するために投与されるゴナドトロピンの量を減らすために使用することもできます。
不十分な黄体期におけるクロミフェン治療とプロゲステロンを比較した2つのランダム化臨床試験では、各治療で同様の妊娠率(20%~30%)が示されました(5,6)。クロミフェンは、外因性プロゲステロンとは異なり、黄体期を延長させないため、不妊カップルの不安や妊娠に関する不確実性の期間を軽減します。
薬理学的特性
薬力学特性
クエン酸クロミフェン (活性物質) (クエン酸クロミフェン (活性物質)) は、エストロゲン作用および抗エストロゲン作用を有する非ステロイド性薬剤であり、排卵しない特定の女性に排卵を誘発する可能性があります。
視床下部のエストロゲン受容体で内因性エストロゲンと競合します。クエン酸クロミフェン(活性物質)による周期的治療に対する排卵反応は、下垂体の性腺刺激ホルモンの産生増加によって媒介され、GnRH(性腺刺激ホルモン放出ホルモン)の分泌と、LH(黄体形成ホルモン)およびFSH(卵胞刺激ホルモン)のレベルの増加によって媒介されるようです。 )、これにより卵巣が刺激され、その結果として卵胞が成熟し、黄体が発達します。ゴナドトロピンとエストロゲンの尿中排泄の増加は、下垂体の関与を示唆しています。排卵は通常、一連のクエン酸クロミフェン(活性物質)の投与後 6 ~ 12 日後に起こります。
薬物動態学的特性
クエン酸クロミフェン(有効成分)の薬物動態に関して入手可能なデータはほとんどありません。
14Cで標識されたクエン酸クロミフェン(活性物質)をヒトに投与した研究では、その吸収が速いことが実証されています。
したがって、クエン酸クロミフェン(活性物質)とその代謝産物(14Cの形で測定)の一部は、クエン酸クロミフェン(活性物質)による治療サイクルの月経周期中に妊娠した女性の妊娠初期に体内に残る可能性があります。 )。
尿および糞便中の14C標識薬剤の平均累積排泄量は、6 人の被験者において 5 日後に投与された経口投与量の約 50% であり、平均尿中排泄量は 7.8%、平均糞便排泄量は 42.4% でした。 14 C で標識されたクエン酸クロミフェン (活性物質) の投与後 31 日目から 53 日目までに採取された糞便および尿サンプル中に排泄された量は、1 日あたり 1% 未満でした。
前臨床安全性データ
発がん性
クエン酸クロミフェン(活性物質)を長期間使用すると、境界領域または浸潤性卵巣腫瘍を発症するリスクが増加する可能性があります。
クエン酸クロミフェン(活性物質)の発がん性の可能性を評価するために、動物における長期毒性研究は行われていません。
変異原性
クエン酸クロミフェン (活性物質) の変異原性の可能性は評価されていません。
クロミッドの保管ケア
クロミッドは室温 (15 ~ 30°C) で保管する必要があります。光や湿気から守ります。
使用期限を過ぎた薬は使用しないでください。
元のパッケージに入れて保管してください。
バッチ番号と製造日および有効期限: パッケージを参照してください。
薬の特徴
この薬は円形の黄色の錠剤の形で提供され、端が面取りされており、一方の側には溝があり、もう一方の側にはメドレーの彫刻が施されています。
使用前に薬剤の外観を観察してください。使用期限を過ぎた場合、外観に変化があった場合は、使用してもよいか薬剤師に相談してください。
すべての薬は子供の手の届かないところに保管してください。
クロミッドの法律上の格言
MS – 1.8326.0245
農場。答え:
タチアナ・デ・カンポス博士
CRF-SP番号 29,482
メドレー・ファーマシューティカ株式会社。
Rua Macedo Costa、55 – カンピナス – SP
CNPJ 10.588.595/0007-97
ブラジルの産業
サノフィ・アベンティス・ファーマセウティカ社のブランド。











